Osteobion 200 Ui Solucion Para Pulverizacion Nasal
Información obsoleta, busque otroDE SANIDAD, POLÍTICA SOCIAL E IGUALDAD
|
1 | |
|
Oí |
k agencia española de 1 medicamentos y I productos sanitarios |
Lea todo el prospecto detenidamente antes de empezar a usar el medicamento.
- Conserve este prospecto. Puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado a Vd. personalmente y no debe darlo a otras personas. Puede
_perjudicarles, aun cuando sus síntomas sean los mismos que los suyos._
En este prospecto:
1. Qué es Osteobion® 200 UI solución para pulverización nasal y para qué se utiliza
2. Antes de usar Osteobion® 200 UI solución para pulverización nasal
3. Cómo usar Osteobion® 200 UI solución para pulverización nasal
4. Posibles efectos adversos
5. Conservación de Osteobion® 200 UI solución para pulverización nasal
OSTEOBION® 200 UI solución para pulverización nasal
Calcitonina sintética de salmón.
- El principio activo es calcitonina sintética de salmón.
Una pulverización equivale a 200 UI de calcitonina sintética de salmón.
- Los excipientes son: cloruro sódico, ácido clorhídrico, ácido cítrico monohidratado, citrato sódico dihidrato y agua purificada.
Titular y responsable de la Fabricación
Centrum, S.A.
Sagitario, 14
03006 Alicante (España)
1. QUÉ ES OSTEOBION® 200 UI solución para pulverización nasal Y PARA QUÉ SE UTILIZA
Osteobion® 200 UI se presenta en forma de solución para pulverización nasal.
Osteobion® 200 UI solución para pulverización nasal está disponible en dos formatos:
- 1 envase de 2,1 ml, conteniendo 14 pulverizaciones.
- 1 envase de 3,5 ml, conteniendo 28 pulverizaciones.
Osteobion® 200 UI solución para pulverización nasal pertenece al grupo de medicamentos denominado hormona antiparatiroidea.
Osteobion® se utiliza para:
- El tratamiento de la osteoporosis (desmineralización de los huesos) que aparece en la menopausia, para reducir el riesgo de fracturas de las vértebras.
2. ANTES DE USAR OSTEOBION® 200 UI solución para pulverización nasal
No utilice Osteobion® 200 UI solución para pulverización nasal si:
- Es alérgico a la calcitonina o a cualquiera de los excipientes de este medicamento,
- Tiene hipocalcemia (bajo nivel de calcio en la sangre).
Correo electrúnicoI
C / CAMPEZO, 1 - EDIFICIO 8 28022 MADRID
Tenga especial cuidado con Osteobion® 200 UI solución para pulverización nasal
Antes de empezar el tratamiento, su médico realizará una exploración nasal, para comprobar que no existe una afectación de la mucosa nasal.
Se interrumpirá el tratamiento si aparecen úlceras graves en la mucosa nasal; si son úlceras no muy importantes, se interrumpirá el tratamiento hasta que se curen.
Pueden aparecer reacciones de tipo alérgico al medicamento, incluyendo casos de reacciones graves. En caso de sospecha de alergia a la calcitonina, su médico puede decidir realizar una prueba de sensibilidad antes de iniciar el tratamiento.
Osteobion Solución para pulverización nasal contiene cloruro de benzalconio como excipiente. Este excipiente puede ser irritante para la mucosa nasal.
Embarazo
Consulte a su médico o farmacéutico antes de tomar cualquier medicamento.
No utilice Osteobion® 200 UI solución para pulverización nasal si está embarazada.
Lactancia
Consulte a su médico o farmacéutico antes de tomar cualquier medicamento.
No utilice Osteobion® 200 UI solución para pulverización nasal si se encuentra en periodo de lactancia.
Efectos sobre la capacidad de conducir y utilizar maquinaria
Osteobion® 200 UI solución para pulverización nasal puede provocar vértigo de forma transitoria. En caso de sufrir esta reacción adversa no deberá conducir ni utilizar máquinas.
Uso de otros medicamentos
No se han descrito interacciones de Osteobion® 200 UI solución para pulverización nasal con otros medicamentos.
3. CÓMO USAR OSTEOBION® 200 UI Solución para pulverización nasal
Siga estas instrucciones a menos que su médico le haya dado otras indicaciones distintas.
Recuerde utilizar su medicamento.
Su médico le indicará la dosis y la duración del tratamiento con Osteobion® 200 UI solución para pulverización nasal.
- Cada envase de 2,1 ml de Osteobion contiene 4.200 UI de calcitonina sintética de salmón, que garantizan 14 pulverizaciones de uso terapéutico y pulverizaciones adicionales necesarias para el correcto funcionamiento del dispositivo de administración.
- Cada envase de 3,5 ml de Osteobion contiene 7.000 UI de calcitonina sintética de salmón, que garantizan 28 pulverizaciones de uso terapéutico y pulverizaciones adicionales necesarias para el correcto funcionamiento del dispositivo de administración.
La dosis recomendada es de 1 pulverización al día (200 UI/día).
Se recomienda ir alternando las aplicaciones en las dos fosas nasales.
MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD
Instrucciones para la correcta administración
La bomba debe cebarse antes de su primera administración. 1. Sacar la
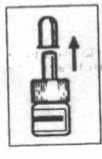
protección
del
pulverizador teniendo el pulverizador en posición vertical

2. Si se utiliza por 1a vez el pulverizador realizar dos pulverizacion es al aire manteniendo el
pulverizador en posición vertical
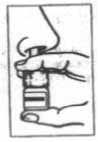
3.Introducir
el
pulverizador en una fosa nasal y realizar una pulverizació
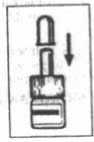
4. Cerrar de nuevo el pulverizador con la protección.
n
Si Vd. usa más Osteobion® 200 UI solución para pulverización nasal del que debiera
Contacte inmediatamente con su médico o farmacéutico. Las reacciones que cabe esperar en caso de sobredosis son náuseas, vómitos, enrojecimiento y vértigo.
En caso de sobredosis o ingestión accidental, consulte al Servicio de Información toxicológica. Teléfono 91.562.04.20.
Si olvidó tomar Osteobion® 200 UI solución para pulverización nasal
Si olvida tomar una dosis, administre el envase pulverizador cuando se acuerde. Si faltan pocas horas para la siguiente administración, espere y administre la dosis cuando tocaba.
No tome una dosis doble para compensar las dosis olvidadas.
4. POSIBLES EFECTOS ADVERSOS
Al igual que todos los medicamentos, Osteobion® 200 UI solución para pulverización nasal puede tener efectos adversos. Informe a su médico si sufre alguno de los siguientes efectos adversos.
Las reacciones adversas observadas más frecuentemente (en más de uno de cada 10 pacientes) incluyen reacciones locales como rinitis (inflamación de la membrana mucosa del interior de la nariz), incluyendo sequedad nasal, edema nasal, congestión nasal, estornudos, rinitis alérgica, síntomas nasales como irritación del conducto nasal, enrojecimiento, abrasión, alteración del olfato y rash papular (sarpullido).
Reacciones frecuentes (aparecen en 1 a 10 de cada 100 pacientes) son: náuseas, diarrea, dolor abdominal, rubor, rinitis ulcerativa, sinusitis, epistaxis (sangrado nasal), faringitis, vértigos, dolor de cabeza, dificultad para tragar (disgeusia), dolor musculoesquelético y fatiga.
Las reacciones adversas poco frecuentes (aparecen en 1 a 10 de cada 1000 pacientes) son: vómitos, tensión arterial alta, tos, alteración de la visión, edema (acumulación de líquido debajo la piel) en la cara y extremidades o en todo el cuerpo, dolor en las articulaciones, reacciones alérgicas de la piel, rubor, picor y enfermedad parecida a la gripe.
Reacciones adversas raras o muy raras son: desarrollo de anticuerpos contra calcitonina, reacciones alérgicas y de tipo anafilactoide tales como taquicardia (pulso acelerado), hipotensión, colapso circulatorio y shock anafiláctico.
MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD
Si se observa cualquier otra reacción adversa no descrita en este prospecto, consulte a su médico o farmacéutico.
5. CONSERVACIÓN DE OSTEOBION® 200 UI solución para pulverización nasal
Antes de su uso, Osteobion® 200 UI solución para pulverización nasal puede mantenerse en frigorífico (2-8°C). No congelar.
Cuando se esté utilizando Osteobion® 200 UI solución para pulverización nasal, puede conservarse a una temperatura no superior a 22°C hasta un máximo de 4 semanas.
Caducidad
No utilizar Osteobion® 200 UI solución para pulverización nasal después de la fecha de caducidad indicada en el envase.
Mantener fuera del alcance y de la vista de los niños Este prospecto ha sido aprobado en Julio de 2006
MINISTERIO DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD
Agencia española de
medicamentos y
productos sanitarios