Acido Zoledronico Mylan 4 Mg/100 Ml Solucion Para Perfusion Efg
Información obsoleta, busque otroFICHA TÉCNICA
1. NOMBRE DEL MEDICAMENTO
Ácido zoledrónico Mylan 4 mg/100 ml solución para perfusión EFG
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Un vial contiene 4 mg de ácido zoledrónico, equivalentes a 4,26 mg de ácido zoledrónico monohidrato.
Este medicamento contiene menos de 1 mmol (23 mg) de sodio por infusión, por lo que se considera esencialmente “exento de sodio”.
Para consultar la lista completa de excipientes, ver sección 6.1.
3. FORMA FARMACÉUTICA
Solución para perfusión Solución transparente e incolora
pH: 5,5-7,0
Osmolaridad: 0,27-0,33 osmol/kg
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
• Prevención de eventos relacionados con el esqueleto (fracturas patológicas, compresión medular, radiación o cirugía ósea, o hipercalcemia inducida por tumor) en pacientes adultos con neoplasias avanzadas con afectación ósea.
Tratamiento de pacientes adultos con hipercalcemia inducida por tumor (HIT)
4.2 Posología y forma de administración
Ácido zoledrónico Mylan sólo debe ser prescrito y administrado a los pacientes por profesionales sanitarios con experiencia en la administración de bisfosfonatos intravenosos.
Posología
Prevención de eventos relacionados con el esqueleto en pacientes con neoplasias avanzadas con afectación ósea
Adultos y personas de edad avanzada
La dosis recomendada en la prevención de eventos relacionados con el esqueleto en pacientes con neoplasias maligna avanzadas con afectación ósea es de 4 mg de ácido zoledrónico cada 3 o 4 semanas.
Deberá administrarse a los pacientes diariamente un suplemento oral de calcio de 500 mg y 400 UI de vitamina D.
La decisión de tratar a pacientes con metástasis óseas para la prevención de eventos relacionados con el esqueleto debe tener en cuenta que el inicio del efecto del tratamiento aparece a los 2-3 meses.
Tratamiento de la HIT
Adultos y personas de edad avanzada
La dosis recomendada en hipercalcemia (concentración corregida de calcio sérico respecto a la albúmina >
12.0 mg/dl o 3,0 mmol/l) es una dosis única de 4 mg de ácido zoledrónico.
Insuficiencia renal HIT:
En los pacientes con HIT que también sufran insuficiencia renal grave el tratamiento con Ácido zoledrónico Mylan deberá considerarse solamente tras la evaluación de los riesgos y los beneficios del tratamiento. En los ensayos clínicos, se excluyó a los pacientes con creatinina sérica > 400 pmol/l o > 4,5 mg/dl. No se requiere un ajuste de la dosis en los pacientes con HIT con una creatinina sérica < 400 pmol/l o < 4,5 mg/dl (ver sección 4.4).
Prevención de eventos relacionados con el esqueleto en pacientes con neoplasias maligna avanzadas con afectación ósea.
Cuando se inicia el tratamiento con Ácido zoledrónico Mylan en pacientes con mieloma múltiple o con lesiones metastásicas óseas de tumores sólidos, se deberá determinar la creatinina sérica y el aclaramiento de creatinina (CLcr). El CLcr se calcula a partir de la creatinina sérica utilizando la fórmula de Cockcroft-Gault. No se recomienda Ácido zoledrónico Mylan en los pacientes que presenten insuficiencia renal grave, definida para esta población como CLcr < 30 ml/min, antes del inicio del tratamiento. En los ensayos clínicos con ácido zoledrónico se excluyeron los pacientes con creatinina sérica > 265 pmol/l o >
3.0 mg/dl.
En pacientes con actividad renal normal (definida como CLcr > 60 ml/min), puede administrarse ácido zoledrónico 4 mg/100 ml solución para perfusión directamente sin ninguna preparación adicional. En pacientes con metástasis óseas que presentaban insuficiencia renal de leve a moderada, definida para esta población como CLcr 30-60 ml/min, antes del inicio del tratamiento, se recomiendan dosis reducidas de Ácido zoledrónico Mylan (ver también sección 4.4).
|
Aclaramiento de creatinina basal (ml/min) |
Dosis recomendada de ácido zoledrónico* |
|
> 60 |
4,0 mg |
|
50-60 |
3,5 mg* |
|
40-49 |
3,3 mg* |
|
30-39 |
3,0 mg* |
* Las dosis se han calculado asumiendo un AUC objetivo de 0,66 (mgh/l) (CLcr = 75 ml/min). Se espera que en los pacientes con insuficiencia renal las dosis reducidas alcancen la misma AUC que la observada en los pacientes con aclaramiento de creatinina de 75 ml/min.
Una vez iniciado el tratamiento deberá medirse la creatinina sérica antes de cada dosis de Ácido zoledrónico Mylan y el tratamiento deberá interrumpirse si se ha deteriorado la función renal. En los ensayos clínicos, el deterioro renal se definió como se indica a continuación:
• Para pacientes con creatinina sérica basal normal (< 1,4 mg/dl o < 124 pmol/l), un aumento de 0,5 mg/dl o 44 pmol/l;
• Para pacientes con creatinina basal anómala (> 1,4 mg/dl o > 124 pmol/l), un aumento de 1,0 mg/dl o 88 pmol/l.
En los ensayos clínicos, el tratamiento con ácido zoledrónico se reanudó únicamente cuando la concentración de creatinina volvió a hallarse dentro de un 10% del valor basal (ver sección 4.4). El tratamiento con Ácido zoledrónico Mylan deberá reanudarse a la misma dosis administrada antes de la interrupción del tratamiento.
Población pediátrica
No se ha establecido la seguridad y eficacia de ácido zoledrónico en niños de 1 año a 17 años. Los datos actualmente disponibles están descritos en la sección 5.1; sin embargo, no se puede hacer una recomendación posológica.
Forma de administración
Vía intravenosa.
Ácido zoledrónico Mylan 4 mg/100 ml para solución para perfusión EFG se debe administrar como una perfusión intravenosa única durante, como mínimo, 15 minutos.
En pacientes con actividad renal normal, definida como CLcr > 60 ml/min, la solución para perfusión de ácido zoledrónico 4 mg/100 ml no debe diluirse.
En pacientes con insuficiencia renal de leve a moderada, se recomiendan dosis reducidas de ácido zoledrónico (ver sección 6.3).
Para preparar dosis reducidas para pacientes con un valor basal de CLcr = 60 ml/min, consultar la Tabla 1 a continuación. Extraer del vial el volumen indicado de solución de ácido zoledrónico y sustituirlo por un volumen igual de solución inyectable estéril de cloruro de sodio 9 mg/ml (0,9%) o de solución inyectable de glucosa al 5%.
Tabla 1: Preparación de dosis reducidas de ácido zoledrónico 4 mg/100 ml solución para perfusión
|
Aclaramiento de creatinina basal (ml/min) |
Extraer la siguiente cantidad de solución de ácido zoledrónico para perfusión (ml) |
Sustituir con el siguiente volumen de solución inyectable estéril de cloruro de sodio 9 mg/ml (0,9%) o solución inyectable de glucosa al 5% (ml) |
Dosis ajustada (mg de ácido zoledrónico en 100 ml) |
|
50-60 |
12,0 |
12,0 |
3,5 |
|
40-49 |
18,0 |
18,0 |
3,3 |
|
30-39 |
25,0 |
25,0 |
3,0 |
Ácido zoledrónico Mylan 4 mg/100 ml para solución para perfusión EFG no se debe mezclar con otras soluciones para perfusión y se debe administrar como solución intravenosa única en una vía de perfusión separada.
Los pacientes se deben mantener bien hidratados antes y después de la administración de Ácido zoledrónico Mylan.
4.3 Contraindicaciones
• Hipersensibilidad al principio activo, a otros bisfosfonatos, o a alguno de los excipientes incluidos en la sección 6.1.
• Lactancia (ver sección 4.6)
4.4 Advertencias y precauciones especiales de empleo
General
Los pacientes deben ser evaluados antes de la administración de Ácido zoledrónico Mylan para asegurar que están adecuadamente hidratados.
Debe evitarse la sobrehidratación en pacientes con riesgo de insuficiencia cardíaca.
Los parámetros metabólicos habituales relacionados con la hipercalcemia, como las concentraciones séricas de calcio, fosfato y magnesio, deben vigilarse cuidadosamente después de iniciar el tratamiento con ácido zoledrónico. Puede ser necesario un tratamiento adicional a corto plazo si se produce hipocalcemia, hipofosfatemia o hipomagnesemia. Los pacientes con hipercalcemia no tratada presentan generalmente algún grado de alteración de la función renal, por lo tanto, deberá considerarse la monitorización cuidadosa de la actividad renal.
Se han notificado casos de hipocalcemia grave que requieren hospitalización. En algunos casos, puede aparecer hipocalcemia con riesgo vital.
Ácido zoledrónico Mylan contiene el mismo principio activo que ácido zoledrónico 5 mg/100 ml. Los pacientes que están siendo tratados con Ácido zoledrónico Mylan no deberán recibir tratamiento con ácido zoledrónico 5 mg/100 ml ni con ningún otro bisfosfonato de forma concomitante, puesto que se desconocen los efectos combinados de estos agentes.
Insuficiencia renal
Deberá evaluarse apropiadamente a los pacientes con HIT y signos de deterioro de la función renal, teniendo en consideración si el beneficio potencial del tratamiento con Ácido zoledrónico Mylan supera el posible riesgo.
La decisión de tratar a pacientes con metástasis óseas para la prevención de eventos relacionados con el esqueleto debe tener en cuenta que el inicio del efecto del tratamiento aparece a los 2-3 meses.
Ácido zoledrónico se ha asociado con descripciones de disfunción renal. Los factores que pueden aumentar el riesgo de deterioro de la función renal incluyen deshidratación, insuficiencia renal preexistente, ciclos múltiples de ácido zoledrónico y otros bisfosfonatos y también el uso de otros medicamentos nefrotóxicos. A pesar de que el riesgo se reduce con una dosis de 4 mg de ácido zoledrónico administrada durante 15 minutos, puede presentarse todavía deterioro de la función renal. Se han notificado casos de deterioro de la función renal con progresión a insuficiencia renal y diálisis después de la administración de la dosis inicial o de una dosis única de 4 mg de ácido zoledrónico. En algunos pacientes con administración crónica de ácido zoledrónico a las dosis recomendadas para prevención de eventos relacionados con el esqueleto también se presentan aumentos de creatinina sérica, aunque con menor frecuencia.
Antes de cada dosis de Ácido zoledrónico Mylan deberán valorarse las concentraciones de creatinina sérica de los pacientes. Al inicio del tratamiento de pacientes con metástasis óseas con insuficiencia renal de leve a moderada, se recomiendan dosis más bajas de ácido zoledrónico. En pacientes que muestren evidencia de deterioro renal durante el tratamiento, deberá interrumpirse la administración de Ácido zoledrónico Mylan. Solamente deberá reanudarse el tratamiento con Ácido zoledrónico Mylan cuando la creatinina sérica vuelva a hallarse dentro de un 10% del valor basal. El tratamiento con Ácido zoledrónico Mylan se debe reanudar a la misma dosis administrada antes de la interrupción del tratamiento.
En vista del impacto potencial de ácido zoledrónico sobre la actividad renal, la ausencia de datos clínicos de seguridad en pacientes con insuficiencia renal grave (definida en los ensayos clínicos como creatinina sérica > 400 pmol/l o > 4,5 mg/dl para pacientes con HIT y > 265 pmol/l o > 3,0 mg/dl para pacientes con cáncer y metástasis óseas, respectivamente) a nivel basal y los limitados datos de farmacocinética en pacientes con insuficiencia renal grave a nivel basal (aclaramiento de creatinina < 30 ml/min), no se recomienda el uso de ácido zoledrónico en pacientes con insuficiencia renal grave.
Insuficiencia hepática
Dado que solo se dispone de datos clínicos limitados en pacientes con insuficiencia hepática grave, no pueden darse recomendaciones específicas para esta población de pacientes.
Osteonecrosis de mandíbula.
Se ha observado osteonecrosis de mandíbula (ONM) predominantemente en pacientes con cáncer, tratados con medicamentos que inhiben la resorción ósea, como ácido zoledrónico. Muchos de estos pacientes también recibían quimioterapia y corticosteroides. La mayoría de los casos descritos se han asociado con procesos dentales, tales como una extracción dental. Muchos mostraron signos de infección local, incluyendo osteomielitis.
Se deben considerar los siguientes factores de riesgo al evaluar el riesgo individual de aparición de ONM:
• Potencia del bisfosfonato (mayor riesgo para los compuestos más potentes), vía de administración (mayor riesgo para la administración parenteral) y dosis acumulada
• Cáncer, quimioterapia, radioterapia, corticosteroides, tabaquismo.
• Antecedentes de enfermedad dental, higiene bucal deficiente, enfermedad periodontal, procedimientos dentales invasivos y dentaduras postizas mal ajustadas
En aquellos pacientes con factores de riesgo concomitante deberá considerarse un examen dental con una apropiada odontología preventiva, antes de iniciar el tratamiento con bisfosfonatos.
Durante el tratamiento, si es posible, estos pacientes deben evitar procesos dentales invasivos. La cirugía dental puede agravar la situación en pacientes que desarrollen osteonecrosis de mandíbula durante la terapia con bisfosfonatos. No hay datos disponibles que indiquen si la interrupción del tratamiento con bisfosfonatos reduce el riesgo de osteonecrosis de mandíbula en pacientes que precisen cirugía dental. La valoración clínica del médico debe orientar sobre cómo proceder con cada paciente según la valoración individual de la relación beneficio-riesgo
Dolor musculoesquelético
En la experiencia post-comercialización, se han notificado casos de dolor óseo, articular y muscular grave y ocasionalmente incapacitante, en pacientes que toman ácido zoledrónico. Sin embargo, estos informes han sido infrecuentes. El tiempo hasta la aparición de los síntomas varió desde un día hasta varios meses tras el inicio del tratamiento. La mayor parte de los pacientes mejoró al suspender el tratamiento. Un subgrupo presentó recurrencia de los síntomas al administrar otra vez ácido zoledrónico u otro bisfosfonato.
Fracturas atípicas de fémur
Se han notificado casos de fracturas de fémur atípicas, subtrocantéreas y diafisarias durante el tratamiento con bisfosfonatos, principalmente en pacientes en tratamiento prolongado para la osteoporosis. Estas fracturas transversales u oblicuas cortas pueden ocurrir en cualquier parte a lo largo del fémur, desde justo debajo del trocánter menor hasta justo por encima de la cresta supracondílea. Estas fracturas se producen después de un traumatismo mínimo o en ausencia de él y algunos pacientes tienen dolor en el muslo o en la ingle, a menudo asociado con imágenes características de fracturas por sobrecarga, semanas a meses antes de que se presente la fractura femoral completa. Las fracturas son generalmente bilaterales; por lo tanto, el fémur del lado opuesto debe ser examinado en los pacientes tratados con bisfosfonatos que hayan tenido una fractura de la diáfisis femoral. También se ha notificado un bajo índice de consolidación de estas fracturas. Debe considerarse la interrupción del tratamiento con bisfosfonatos, valorando de forma individualizada la relación beneficio-riesgo, en aquellos pacientes en los que exista sospecha de fractura atípica de fémur pendiente de evaluación.
Durante el tratamiento con bisfosfonatos debe advertirse a los pacientes que notifiquen cualquier dolor en el muslo, cadera o ingle. En cualquier paciente que presente dichos síntomas deberá valorarse si existe una fractura de fémur incompleta.
Este medicamento contiene menos de 1 mmol (23 mg) de sodio por infusión, por lo que se considera esencialmente “exento de sodio”.
4.5 Interacción con otros medicamentos y otras formas de interacción
En ensayos clínicos, ácido zoledrónico se ha administrado simultáneamente con agentes anticancerosos, diuréticos, antibióticos y analgésicos utilizados comúnmente sin que ocurrieran interacciones clínicamente evidentes. In vitro, ácido zoledrónico no se une considerablemente a proteínas plasmáticas y no inhibe las enzimas humanas del citocromo P450 (ver sección 5.2), aunque no se han realizado estudios clínicos estrictos de interacciones.
Se recomienda precaución cuando se administran bisfosfonatos con aminoglucósidos, dado que ambos agentes pueden ejercer un efecto aditivo, dando como resultado una menor concentración sérica de calcio durante periodos más largos de los necesarios.
otros medicamentos de que se desarrolle
aumentado cuando se
Se recomienda precaución cuando se utilice ácido zoledrónico junto con potencialmente nefrotóxicos. También debe prestarse atención a la posibilidad hipomagnesemia durante el tratamiento.
En los pacientes con mieloma múltiple, el riesgo de disfunción renal puede verse administra ácido zoledrónico en combinación con talidomida.
Se han recibido notificaciones de ONM en pacientes tratados con ácido zoledrónico y medicamentos antiangiogénicos de forma concomitante.
4.6 Fertilidad, embarazo y lactancia
Embarazo
No existen datos suficientes sobre la utilización de ácido zoledrónico en mujeres embarazadas. Estudios de reproducción en animales con ácido zoledrónico han mostrado toxicidad reproductiva (ver sección 5.3). Se desconoce el riesgo en seres humanos. Ácido zoledrónico no debe utilizarse durante el embarazo.
Lactancia
Se desconoce si ácido zoledrónico se excreta en la leche materna. Ácido zoledrónico está contraindicado en mujeres en periodo de lactancia (ver sección 4.3).
Fertilidad
Se estudió ácido zoledrónico en ratas para evaluar los potenciales efectos adversos sobre la fertilidad de la generación parental y la F1. Esto provocó unos efectos farmacológicos exagerados que se consideraron relacionados con la inhibición del metabolismo cálcico óseo debida al producto, que dio lugar a hipocalcemia periparturienta, un efecto de clase de los bisfosfonatos, distocia y finalización temprana del estudio. Por lo tanto, estos resultados impiden determinar un efecto claro de ácido zoledrónico sobre la fertilidad en humanos.
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
Las reacciones adversas como mareo y somnolencia pueden tener influencia sobre la capacidad para conducir o utilizar máquinas; por lo tanto, se debe tener precaución con el uso de ácido zoledrónico en la conducción y utilización de máquinas.
4.8 Reacciones adversas
Resumen del perfil de seguridad
En los tres días posteriores a la administración de ácido zoledrónico se ha notificado de forma frecuente una reacción de fase aguda, con síntomas que incluyen dolor óseo, fiebre, fatiga, artralgia, mialgia y escalofríos; estos síntomas habitualmente se resuelven en pocos días (ver descripción de las reacciones adversas seleccionadas).
Los siguientes riesgos importantes son los que se han identificado con ácido zoledrónico en las indicaciones autorizadas:
Alteración de la función renal, osteonecrosis de la mandíbula, reacción de fase aguda, hipocalcemia, efectos adversos oculares, fibrilación auricular, anafilaxia. En la Tabla 2 se muestran las frecuencias para cada uno de estos riesgos identificados.
Tabla de reacciones adversas
Las siguientes reacciones adversas, relacionadas en la Tabla 2, se han recopilado de los ensayos clínicos y de las notificaciones post-comercialización, principalmente tras el tratamiento crónico con 4 mg de ácido zoledrónico:
Tabla 2
Las reacciones adversas están agrupadas por frecuencias, las más frecuentes primero, utilizando la siguiente convención: Muy frecuentes (> 1/10); frecuentes (> 1/100 a < 1/10); poco frecuentes (> 1/1.000 a < 1/100); raras (> 1/10.000 a < 1/1.000); muy raras (< 1/10.000); frecuencia no conocida (no puede estimarse a partir de los datos disponibles).
Trastornos de la sangre y del sistema linfático
Frecuentes: Anemia
Poco frecuentes: Trombocitopenia, leucopenia
Raras: Pancitopenia
Trastornos del sistema inmunológico
Poco frecuentes:
Raras:
Trastornos psiquiátricos Poco frecuentes:
Raras:
Trastornos del sistema nervioso Frecuentes:
Poco frecuentes:
Trastornos oculares Frecuentes:
Poco frecuentes:
Reacciones de hipersensibilidad Edema angioneurótico
Ansiedad, alteraciones de sueño Confusión
Cefalea
Mareo, parestesia, alteración del gusto, hipoestesia, hiperestesia, temblores, somnolencia
Conjuntivitis
Visión borrosa, escleritis e inflamación orbital
Muy raras: Uveítis, episcleritis
Trastornos cardíacos
Poco frecuentes: Hipertensión, hipotensión, fibrilación auricular, hipotensión que
provoca síncope o colapso circulatorio
Raras: Bradicardia
Trastornos respiratorios, torácicos y mediastínicos
Poco frecuentes: Disnea, tos, broncoconstricción
|
Raras: |
Enfermedad pulmonar intersticial |
|
Trastornos gastrointestinales: | |
|
Frecuentes: |
Náuseas, vómitos y anorexia |
|
Poco frecuentes: |
Diarrea, estreñimiento, dolor abdominal, dispepsia, estomatitis, sequedad de boca |
|
Trastornos de la piel y del tejido subcutáneo | |
|
Poco frecuentes: |
Prurito, erupción (incluyendo erupción eritematosa y macular), aumento de la sudoración |
|
Trastornos musculoesqueléticos y del tejido conjuntivo | |
|
Frecuentes: |
Dolor óseo, mialgia, artralgia, dolor generalizado |
|
Poco frecuentes: |
Calambres musculares, osteonecrosis de la mandíbula* |
|
Trastornos renales y urinarios | |
|
Frecuentes: |
Insuficiencia renal |
|
Poco frecuentes: |
Insuficiencia renal aguda, hematuria, proteinuria |
|
Trastornos generales y alteraciones en |
el lugar de administración |
|
Frecuentes: |
Fiebre, síndrome similar a la gripe (incluyendo fatiga, escalofríos, malestar y sofocos) |
|
Poco frecuentes: |
Astenia, edema periférico, reacciones en el lugar de la inyección (incluyendo dolor, irritación, tumefacción, induración), dolor torácico, aumento de peso, reacción o choque anafiláctico, urticaria |
|
Exploraciones complementarias | |
|
Muy frecuentes: |
Hipofosfatemia |
|
Frecuentes: |
Aumento de la creatinina y urea sanguíneas, hipocalcemia |
|
Poco frecuentes: |
Hipomagnesemia, hipopotasemia |
|
Raras: |
Hiperpotasemia, hipernatremia |
Descripción de reacciones adversas seleccionadas
Alteración de la función renal
Ácido zoledrónico se ha asociado con notificaciones de alteración renal. En un análisis combinado de los datos de seguridad de los ensayos de registro de ácido zoledrónico para la prevención de eventos relacionados con el esqueleto en pacientes con neoplasias malignas avanzadas con afectación ósea, la frecuencia de acontecimientos adversos de insuficiencia renal que se sospechó que estaban relacionados con ácido zoledrónico (reacciones adversas) fue la siguiente: mieloma múltiple (3,2%), cáncer de próstata (3,1%), cáncer de mama (4,3%), pulmón y otros tumores sólidos (3,2%). El potencial deterioro de la función renal puede aumentar por factores tales como deshidratación, insuficiencia renal preexistente, ciclos múltiples de ácido zoledrónico u otros bisfosfonatos, así como un uso concomitante de medicamentos nefrotóxicos o un tiempo de perfusión más corto del actualmente recomendado. Se han notificado casos de deterioro de la función renal con progresión a insuficiencia renal y diálisis después de la administración de la dosis inicial o de una dosis única de 4 mg de ácido zoledrónico (ver sección 4.4).
Osteonecrosis de mandíbula.
Se han descrito casos de osteonecrosis (especialmente de las mandíbulas) predominantemente en pacientes con cáncer tratados con medicamentos que inhiben la resorción ósea, como ácido zoledrónico. Muchos de estos pacientes presentaron signos de infección local incluyendo osteomielitis, y la mayoría de los informes hacen referencia a pacientes con cáncer tras una extracción dentaria u otras cirugías dentales. La osteonecrosis de la mandíbula tiene múltiples factores de riesgo documentados, tales como cáncer diagnosticado, tratamientos concomitantes (p.ej. quimioterapia, radioterapia, corticosteroides) y enfermedades concomitantes (p.ej. anemia, coagulopatías, infección, afección oral preexistente). Aunque no se ha determinado la causalidad, se recomienda evitar la cirugía dental ya que la recuperación puede ser larga (ver sección 4.4).
Fibrilación auricular
En un ensayo clínico controlado, doble ciego, aleatorizado y de 3 años de duración que evaluó la eficacia y la seguridad de 5 mg de ácido zoledrónico administrados una vez al año respecto a un placebo en el tratamiento de la osteoporosis postmenopáusica (OPM), la incidencia global de fibrilación auricular en pacientes que recibieron 5 mg de ácido zoledrónico fue de un 2,5% (96 de 3.862), y de un 1,9% (75 de 3.852) en los tratados con un placebo. La proporción de reacciones adversas graves de fibrilación auricular fue de 1,3% (51 de 3.862) y de 0,6% (22 de 3.852) en pacientes que recibieron 5 mg de ácido zoledrónico y placebo, respectivamente. La diferencia observada en este ensayo no se ha observado en otros ensayos con ácido zoledrónico, incluyendo los ensayos con 4 mg de ácido zoledrónico administrado cada 3-4 semanas en pacientes oncológicos. Se desconoce el mecanismo causante del aumento de la incidencia de fibrilación auricular en este ensayo clínico en particular.
Reacción de fase aguda
Esta reacción adversa al fármaco consiste en un grupo de síntomas tales como fiebre, mialgia, cefalea, dolor en las extremidades, náuseas, vómitos, diarrea y artralgia. El tiempo de inicio es = 3 días tras la perfusión de ácido zoledrónico, y la reacción también se describe con los términos de síntomas “similares a la gripe” o “post-administración”.
Fracturas atípicas de fémur
Durante la experiencia postcomercialización se han notificado las siguientes reacciones adversas (frecuencia rara):
Fracturas atípicas subtrocantéreas y diafisarias del fémur (reacción adversa de clase de los bisfosfonatos)
Notificación de presuntas reacciones adversas
Es importante notificar las sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los
profesionales sanitarios a notificar las sospechas de reacciones adversas a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano, www.notificaRAM.es
4.9 Sobredosis
La experiencia clínica en relación con la sobredosis con ácido zoledrónico es limitada. Se ha notificado la administración de dosis de hasta 48 mg de ácido zoledrónico por error. Los pacientes que han recibido dosis superiores a las recomendadas (ver sección 4.2) deben someterse a una monitorización estrecha, dado que se ha observado alteración de la función renal (incluyendo insuficiencia renal) y valores anómalos de los electrolitos séricos (incluido calcio, fósforo y magnesio). Si se produce hipocalcemia deben administrarse perfusiones de gluconato cálcico según criterio clínico.
5. PROPIEDADES FARMACOLÓGICAS
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: Fármacos para el tratamiento de enfermedades óseas, bisfosfonatos, código ATC: M05BA08
Ácido zoledrónico pertenece a la clase de los bisfosfonatos y actúa principalmente en el hueso. Es un inhibidor de la resorción ósea osteoclástica.
La acción ósea selectiva de los bisfosfonatos se basa en su gran afinidad por el hueso mineralizado, pero el mecanismo molecular preciso que da lugar a la inhibición de la actividad osteoclástica aún no está claro. En estudios de larga duración en animales, ácido zoledrónico inhibe la resorción ósea sin perjudicar la formación, mineralización ni las propiedades mecánicas del hueso.
Además de ser un potente inhibidor de la resorción ósea, ácido zoledrónico también posee varias propiedades antitumorales que pueden contribuir a su eficacia general en el tratamiento de la metástasis ósea. Se han demostrado las siguientes propiedades en ensayos preclínicos:
• In vivo: Inhibición de la resorción ósea osteoclástica, lo que altera el microentorno de la médula ósea haciéndolo menos favorable al crecimiento de la célula tumoral, actividad antiangiogénica y actividad analgésica.
• In vi tro: Inhibición de la proliferación osteoblástica, actividad citostática directa y proapoptótica sobre las células tumorales, efecto citostático sinérgico con otros fármacos anticancerígenos, actividad antiadhesiva/invasiva.
Resultados de los ensayos clínicos en la prevención de eventos relacionados con el esqueleto en pacientes con neoplasias avanzadas con afectación ósea
El primer estudio aleatorizado, doble ciego, controlado con placebo comparó 4 mg de ácido zoledrónico respecto a un placebo para la prevención de eventos relacionados con el esqueleto (ERE) en pacientes con cáncer de próstata. La administración de 4 mg de ácido zoledrónico disminuyó significativamente la proporción de pacientes que experimentaron al menos un evento relacionado con el esqueleto (ERE), retrasó la mediana de tiempo hasta el primer ERE en más de 5 meses y redujo la incidencia anual de eventos por paciente (tasa de morbididad esquelética). El análisis de eventos múltiples mostró una reducción del riesgo del 36% en la aparición de ERE en el grupo de 4 mg de ácido zoledrónico en comparación con placebo. Los pacientes que recibieron 4 mg de ácido zoledrónico registraron un menor incremento del dolor que los que recibieron placebo, alcanzando diferencias significativas en los meses 3, 9, 21 y 24. Un menor número de pacientes tratados con 4 mg de ácido zoledrónico sufrió fracturas patológicas. Los efectos del tratamiento fueron menos pronunciados en pacientes con lesiones blásticas. Los resultados de eficacia se muestran en la Tabla 3.
En un segundo estudio, que incluía tumores sólidos diferentes del cáncer de mama y de próstata, 4 mg de ácido zoledrónico redujeron significativamente la proporción de pacientes con un ERE, retrasó la mediana de tiempo hasta el primer ERE en más de 2 meses y redujo la tasa de morbilidad esquelética. El análisis de eventos múltiples mostró una reducción del riesgo del 30,7% en la aparición de ERE en el grupo de 4 mg de ácido zoledrónico en comparación con placebo. Los resultados de eficacia se muestran en la Tabla 4.
Tabla 3: Resultados de eficacia (pacientes con cáncer de próstata que recibían terapia hormonal)
|
Algún ERE (+HIT) |
Fracturas* |
Radioterapia en hueso | ||||
|
ácido zoledrónico |
Placebo |
ácido zoledrónico |
Placebo |
ácido zoledrónico |
Placebo | |
|
4 mg |
4 mg |
4 mg | ||||
|
N |
214 |
208 |
214 |
208 |
214 |
208 |
|
Proporción de pacientes con ERE (%) |
38 |
49 |
17 |
25 |
26 |
33 |
|
Valor de p |
0,028 |
0,052 |
0,119 | |||
|
Mediana de tiempo hasta ERE (días) |
488 |
321 |
NA |
NA |
NA |
640 |
|
Valor de p |
0,009 |
0,020 |
0,055 | |||
|
Tasa de morbilidad esquelética |
0,77 |
1,47 |
0,20 |
0,45 |
0,42 |
0,89 |
|
Valor de p |
0,005 |
0,023 |
0,060 | |||
|
Reducción del riesgo de sufrir eventos múltiples** (%) |
36 |
- |
NAp |
NAp |
NAp |
NAp |
|
Valor de p |
0,002 |
NAp |
NAp | |||
|
* Incluye fracturas vertebrales y no vertebrales ** Tiene en cuenta todos los eventos esqueléticos, el número total así como durante el ensayo NA No alcanzado NAp No aplicable Tabla 4 : Resultados de eficacia (tumores sólidos distintos de cáncer de mama Algún ERE (+HIT) Fracturas* |
el tiempo hasta cada evento o próstata) Radioterapia en hueso | |||||
|
ácido zoledrónico |
Placebo |
ácido zoledrónico |
Placebo |
ácido zoledrónico |
Placebo | |
|
4 mg |
4 mg |
4 mg | ||||
|
N |
257 |
250 |
257 |
250 |
257 |
250 |
|
Proporción de pacientes con ERE (%) |
39 |
48 |
16 |
22 |
29 |
34 |
|
Valor de p |
0,039 |
0,064 |
0,173 | |||
|
Mediana de tiempo hasta |
236 |
155 |
NA |
NA |
424 |
307 |
|
¿i*. ím | |||||||
|
¡m | |||||||
|
ERE (días) | |||||||
|
Valor de p |
0,009 |
0,020 |
0,079 | ||||
|
Tasa de morbilidad esquelética |
1,74 |
2,71 |
0,39 |
0,63 |
1,24 |
1,89 | |
|
Valor de p |
0,012 |
0,066 |
0,099 | ||||
|
Reducción del riesgo de sufrir eventos múltiples** (%) |
30,7 |
- |
NAp |
NAp |
NAp |
NAp | |
|
Valor de p |
0,003 |
NAp |
NAp |
* Incluye fracturas vertebrales y no vertebrales
** Tiene en cuenta todos los eventos esqueléticos, el número total así como el tiempo hasta cada evento durante el ensayo NA No alcanzado NAp No aplicable
En un tercer ensayo de fase III aleatorizado, doble ciego, se comparó 4 mg de ácido zoledrónico con pamidronato 90 mg cada 3 o 4 semanas en pacientes con mieloma múltiple o cáncer de mama con al menos una lesión ósea. Los resultados demostraron que 4 mg de ácido zoledrónico mostraban una eficacia comparable a pamidronato 90 mg en la prevención de ERE. El análisis de eventos múltiples reveló una reducción significativa del riesgo del 16% en pacientes tratados con 4 mg de ácido zoledrónico en comparación con los pacientes que recibieron pamidronato. Los resultados de eficacia se muestran en la Tabla 5.
Tabla 5: Resultados de eficacia (pacientes con cáncer de mama o mieloma múltiple)
|
Aleún ERE (+HIT) |
Fracturas* |
Radioterapia en hueso | ||||
|
ácido zoledrónico |
Pam 90 mg |
ácido zoledrónico |
Pam 90 mg |
ácido zoledrónico |
Pam 90 mg | |
|
4 mg |
4 mg |
4 mg | ||||
|
N |
561 |
555 |
561 |
555 |
561 |
555 |
|
Proporción de pacientes con ERE (%) |
48 |
52 |
37 |
39 |
19 |
24 |
|
Valor de p |
0,198 |
0,653 |
0,037 | |||
|
Mediana de tiempo hasta ERE (días) |
376 |
356 |
NA |
714 |
NA |
NA |
|
Valor de p |
0,151 |
0,672 |
0,026 | |||
|
Tasa de morbilidad esquelética |
1,04 |
1,39 |
0,53 |
0,60 |
0,47 |
0,71 |
Valor de p
|
Valor de p Reducción del riesgo de |
0,084 16 - |
0,614 NAp |
NAp |
0,015 NAp |
.-ítp ¿mí» ¡m NAp |
|
sufrir eventos múltiples1 (%) Valor de p |
0,030 |
NAp |
NAp |
ÜE
Resultados de los ensayos clínicos en el tratamiento de la HIT
Los ensayos clínicos en hipercalcemia inducida por tumor (HIT) demostraron que ácido zoledrónico se caracteriza por disminuir el calcio sérico y la excreción urinaria de calcio. En los estudios de Fase I de búsqueda de dosis en pacientes con hipercalcemia inducida por tumor (HIT) de leve a moderada, las dosis efectivas ensayadas estuvieron en el intervalo de aproximadamente 1,2-2,5 mg.
Para valorar los efectos de 4 mg de ácido zoledrónico frente a 90 mg de pamidronato, se combinaron los resultados de dos ensayos multicéntricos pivotales en pacientes con HIT en un análisis previamente planificado. Hubo una normalización más rápida de las concentraciones corregidas de calcio sérico en el día 4 para 8 mg de ácido zoledrónico, y en el día 7 para 4 mg y 8 mg de ácido zoledrónico. Se observaron las proporciones de respuesta siguientes:
Tabla 6: Proporción de individuos con respuesta completa por día en estudios combinados de HIT
|
Día 4 |
Día 7 |
Día 10 | |
|
Ácido zoledrónico 4 mg (N=86) |
45,3% (p=0,104) |
82,6% (p=0,005)* |
88,4% (p=0,002)* |
|
Ácido zoledrónico 8 mg (N=90) |
55,6% (p=0,021)* |
83,3% (p=0,010)* |
86,7% (p=0,015)* |
|
Pamidronato 90 mg (N=99) |
33,3% |
63,6% |
69,7% |
|
*valores de p comparados |
con pamidronato |
La mediana de tiempo hasta la normocalcemia fue de 4 días. La mediana de tiempo hasta la recaída (reelevación de los valores de calcio sérico corregidos respecto a la albúmina = 2,9 mmol/l) fue de 30 a 40 días para los pacientes tratados con ácido zoledrónico frente a 17 días para los tratados con 90 mg de pamidronato (valores de p: 0,001 para 4 mg y 0,007 para 8 mg de ácido zoledrónico). No hubo diferencias estadísticamente significativas entre las dos dosis de ácido zoledrónico.
En los ensayos clínicos, a 69 pacientes que recayeron o que no respondieron al tratamiento inicial (ácido zoledrónico 4 mg, 8 mg o pamidronato 90 mg) se les repitió el tratamiento con 8 mg de ácido zoledrónico. La tasa de respuesta en estos pacientes fue de aproximadamente el 52%. Dado que a estos pacientes se les repitió el tratamiento solo con la dosis de 8 mg, no se dispone de datos que permitan la comparación con la dosis de 4 mg de ácido zoledrónico.
En los ensayos clínicos realizados en pacientes con hipercalcemia inducida por tumor (HIT), el perfil de seguridad global de los tres grupos de tratamiento (4 mg y 8 mg de ácido zoledrónico y 90 mg de pamidronato) fue similar en cuanto a tipo y gravedad.
Población pediátrica
Resultados del ensayo clínico en el tratamiento de osteogénesis imperfecta grave en pacientes pediátricos de 1 a 17 años de edad
Se compararon los efectos de ácido zoledrónico intravenoso en el tratamiento de la población pediátrica (de 1 a 17 años) con osteogénesis imperfecta grave (tipos I, III y IV) con los efectos de pamidronato intravenoso, en un ensayo abierto, internacional, multicéntrico, aleatorizado con 74 y 76 pacientes en cada grupo de tratamiento, respectivamente. El periodo de tratamiento del estudio fue de 12 meses precedidos por un periodo de selección de 4 a 9 semanas durante el cual se tomaron suplementos de vitamina D y calcio elemental durante al menos 2 semanas. En el programa clínico los pacientes de 1 a < 3 años recibieron 0,025 mg/kg de ácido zoledrónico (hasta una dosis única máxima de 0,35 mg) cada 3 meses y los pacientes de 3 a 17 años recibieron 0,05 mg/kg de ácido zoledrónico (hasta una dosis única máxima de 0,83 mg) cada 3 meses. Se llevó a cabo un ensayo de extensión para examinar la seguridad general y renal a largo plazo de la administración de ácido zoledrónico una vez al año o dos veces al año durante el periodo de tratamiento de la extensión de 12 meses en niños que habían completado un año de tratamiento con ácido zoledrónico o pamidronato en el estudio principal.
La variable principal del estudio fue el porcentaje de cambio en la densidad mineral ósea (DMO) de la columna lumbar desde el inicio hasta después de 12 meses de tratamiento. Los efectos del tratamiento sobre la DMO estimados fueron similares, pero el diseño del ensayo no fue suficientemente consistente para establecer la no inferioridad de eficacia para ácido zoledrónico. En particular, no se observó una evidencia clara de eficacia sobre la incidencia de fracturas o de dolor. Se notificaron efectos adversos de fracturas de los huesos largos en las extremidades inferiores en aproximadamente un 24% (fémur) y 14% (tibia) de los pacientes tratados con ácido zoledrónico frente a un 12% y 5% de pacientes tratados con pamidronato con osteogénesis imperfecta grave, independientemente del tipo de enfermedad y de la causalidad, pero la incidencia global de fracturas fue comparable para los pacientes tratados con ácido zoledrónico y con pamidronato: 43% (32/74) frente a 41% (31/76). La interpretación del riesgo de fractura se confunde con el hecho de que las fracturas son acontecimientos frecuentes en pacientes con osteogénesis imperfecta grave, como parte del proceso de la enfermedad.
El tipo de reacciones adversas observadas en esta población fue similar a las observadas anteriormente en adultos con neoplasias avanzadas con afectación ósea (ver sección 4.8). Las reacciones adversas, agrupadas por frecuencia, se presentan en la Tabla 7. Se utiliza la siguiente clasificación convencional: muy frecuentes (>1/10), frecuentes (>1/100 a <1/10), poco frecuentes (>1/1.000 a <1/100), raras (>1/10.000 a <1/1.000), muy raras (<1/10.000), frecuencia no conocida (no puede estimarse a partir de los datos disponibles).
Tabla 7: Reacciones adversas observadas en la población pediátrica con osteogénesis imperfecta2
Trastornos del sistema nervioso
Frecuentes: Cefalea
Trastornos cardíacos
Frecuentes: Taquicardia
Trastornos respiratorios, torácicos y mediastínicos Frecuentes: Nasofaringitis
Trastornos gastrointestinales
Muy frecuentes: Vómitos; náuseas
Frecuentes:
Dolor abdominal
Trastornos musculoesqueléticos y del tejido conjuntivo
Frecuentes: Dolor en las extremidades, artralgia, dolor musculoesquelético
Trastornos generales y alteraciones en el lugar de administración
Muy frecuentes: Pirexia, fatiga
Frecuentes: Reacción de fase aguda, dolor
Exploraciones complementarias
Muy frecuentes: Hipocalcemia
Frecuentes: Hipofosfatemia 2
La variabilidad entre pacientes de los parámetros farmacocinéticos para ácido zoledrónico fue alta, tal como se ha visto con otros bisfosfonatos.
No se dispone de datos farmacocinéticos de ácido zoledrónico en pacientes con hipercalcemia ni en pacientes con insuficiencia hepática. Ácido zoledrónico no inhibe las enzimas del citocromo P450 humano in vitro, no acusa biotransformación, y en estudios con animales, menos del 3% de la dosis administrada se recuperó en heces, lo cual indica que el hígado no desempeña una función importante en la farmacocinética de ácido zoledrónico.
El aclaramiento renal de ácido zoledrónico se correlacionó significativamente de forma positiva con el aclaramiento de creatinina, representando el aclaramiento renal el 75 ± 33% del aclaramiento de creatinina, que mostró una media de 84 ± 29 ml/min (intervalo de 22 a 143 ml/min) en los 64 pacientes con cáncer estudiados. El análisis de la población mostró que para un paciente con un aclaramiento de creatinina de 20 ml/min (insuficiencia renal grave), o 50 ml/min (insuficiencia moderada), el correspondiente aclaramiento esperado de ácido zoledrónico sería de 37% o 72%, respectivamente, del de un paciente con un aclaramiento de creatinina de 84 ml/min. Solo se dispone de datos farmacocinéticos limitados en pacientes con insuficiencia renal grave (aclaramiento de creatinina < 30 ml/min).
Ácido zoledrónico carece de afinidad por los componentes celulares de la sangre; su unión a proteínas plasmáticas es baja (aproximadamente 56%) e independiente de la concentración de ácido zoledrónico.
Poblaciones especiales
Población pediátrica
Datos farmacocinéticos limitados en niños con osteogénesis imperfecta grave sugieren que la farmacocinética de ácido zoledrónico en niños de 3 a 17 años es similar a la de los adultos a niveles de dosis mg/kg similares. Parece que la edad, el peso, el sexo y el aclaramiento de creatinina no tienen ningún efecto sobre la exposición sistémica a ácido zoledrónico.
5.3 Datos preclínicos sobre seguridad
Toxicidad aguda
La dosis única intravenosa máxima no letal fue de 10 mg/kg de peso corporal en ratones y 0,6 mg/kg en ratas.
Toxicidad crónica y subcrónica
Ácido zoledrónico fue bien tolerado cuando se administró por vía subcutánea a ratas y por vía intravenosa a perros en dosis de hasta 0,02 mg/kg diarios durante 4 semanas. La administración de 0,001 mg/kg/día por vía subcutánea a ratas y 0,005 mg/kg por vía intravenosa una vez cada 2-3 días a perros durante 52 semanas inclusive también fue bien tolerada.
El resultado más frecuente en estudios de dosis repetidas consistió en un aumento de la sustancia esponjosa primaria en las metáfisis de huesos largos de animales en crecimiento a prácticamente todas las dosis, hecho que refleja la actividad farmacológica antiresortiva del compuesto.
Los márgenes de seguridad relativos a los efectos renales fueron estrechos en estudios a largo plazo en animales con dosis parenterales repetidas, pero los niveles sin efectos adversos observados (NOAELs) acumulados en estudios de dosis única (1,6 mg/kg) y dosis múltiples durante un mes (0,06-0,6 mg/kg/día) no indicaron efectos renales a dosis equivalentes o superiores a la dosis terapéutica más alta recomendada en humanos. La administración a más largo plazo de dosis repetidas próximas a la dosis terapéutica más alta de ácido zoledrónico recomendada en humanos produjo efectos tóxicos en otros órganos tales como el tubo gastrointestinal, hígado, bazo y pulmones y en los lugares de inyección intravenosa.
Toxicidad en la reproducción
Ácido zoledrónico fue teratógeno en ratas en dosis subcutáneas > 0,2 mg/kg. No se observó teratogenicidad o fetotoxicidad en los conejos, pero sí toxicidad materna. Se observó distocia con la dosis mínima ensayada en ratas (0,01 mg/kg de peso corporal).
Mutagenicidad y potencial carcinogénico
Ácido zoledrónico no fue mutagénico en los ensayos de mutagenicidad realizados y los ensayos de carcinogénesis no revelaron signo alguno de potencial carcinogénico.
6 . DATOS FARMACÉUTICOS
6.1 Lista de excipientes
• Manitol (E421)
• Citrato de sodio (E331)
Agua para preparaciones inyectables
6.2 Incompatibilidades
Este medicamento no debe entrar en contacto con otras soluciones que contengan calcio, y no se debe mezclar ni administrar por vía intravenosa con ningún otro medicamento en la misma vía de perfusión.
6.3 Periodo de validez
Vial no abierto: 2 años.
Después de la primera apertura:
Se ha demostrado la estabilidad química y física durante 24 horas a 2oC-8oC y a 25oC.
Desde el punto de vista microbiológico, la solución para perfusión se debe utilizar inmediatamente. Si no se usa inmediatamente, el tiempo y las condiciones de almacenamiento durante su uso son responsabilidad del usuario y no deberían superar en condiciones normales las 24 horas a 2°C-8°C. La solución conservada en nevera debe alcanzar la temperatura ambiente antes de la administración.
6.4 Precauciones especiales de conservación
Este medicamento no requiere condiciones especiales de conservación.
Para las condiciones de conservación del medicamento después de la primera apertura, ver sección 6.3.
6.5 Naturaleza y contenido del envase
100 ml de solución se envasan en viales de vidrio transparente tipo I, recubiertos internamente con dióxido de silicio, cerrados con un tapón de goma (bromobutilo) tipo I y sellados con una cápsula desprendible flip-off de polipropileno de aluminio.
Ácido zoledrónico Mylan 4mg/100ml para solución para perfusión EFG se comercializa en envases que contienen:
1 vial
4 viales
5 viales 10 viales
Puede que solamente estén comercializados algunos tamaños de envases.
6.6 Precauciones especiales de eliminación y otras manipulaciones
En la sección 4.2 se adjunta información adicional sobre la manipulación de ácido zoledrónico, incluyendo instrucciones para la preparación de dosis reducidas utilizando el vial de ácido zoledrónico preparado para su uso.
Durante la preparación de la perfusión se deben utilizar técnicas asépticas.
Para un solo uso.
Solo se deben utilizar soluciones transparentes, sin partículas e incoloras.
Se advierte a los profesionales sanitarios que no eliminen la porción no utilizada de ácido zoledrónico mediante el sistema de desagüe doméstico.
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Mylan Pharmaceuticals, S.L.
C/ Plom, 2-4, 5a planta.
08038 Barcelona.
España
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
9. FECHA DE LA PRIMERA AUTORIZACIÓN/ RENOVACIÓN DE LA AUTORIZACIÓN
Septiembre 2014
10. FECHA DE LA REVISIÓN DEL TEXTO
Junio 2013
19 de 19
Tiene en cuenta todos los eventos esqueléticos, el número total así como el tiempo hasta cada evento durante el ensayo NA No alcanzado NAp No aplicable
Se estudiaron también 4 mg de ácido zoledrónico en un ensayo controlado con placebo, aleatorizado y doble ciego en 228 pacientes con metástasis óseas documentadas a partir de cáncer de mama, para evaluar el efecto de 4 mg de ácido zoledrónico sobre la tasa de eventos relacionados con el esqueleto (ERE), calculada como el número total de eventos ERE (excluyendo hipercalcemia y ajustado para fractura previa), dividido por el periodo total de riesgo. Los pacientes recibieron 4 mg de ácido zoledrónico o un placebo cada cuatro semanas durante un año. Los pacientes se distribuyeron a partes iguales entre los grupos tratados con ácido zoledrónico y con un placebo.
La tasa de ERE (eventos/persona año) fue 0,628 para ácido zoledrónico y 1,096 para el placebo. La proporción de pacientes con al menos un ERE (excluyendo hipercalcemia) fue de 29,8% en el grupo tratado con ácido zoledrónico frente a 49,6% en el grupo con placebo (p=0,003). La mediana de tiempo hasta el inicio del primer ERE no se alcanzó en el grupo tratado con ácido zoledrónico al final del ensayo y fue significativamente prolongada en comparación con un placebo (p=0,007). En un análisis de evento múltiple, 4 mg de ácido zoledrónico redujeron el riesgo de ERE en un 41% (RR=0,59, p=0,019) comparado con un placebo.
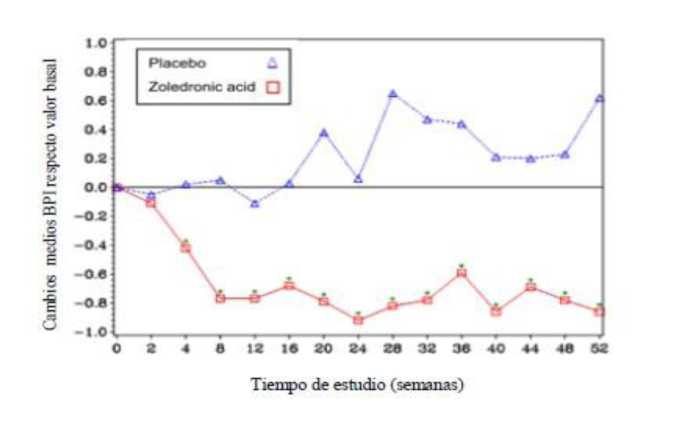
En el grupo tratado con ácido zoledrónico, se observó una mejoría estadísticamente significativa en la puntuación de medida del dolor (utilizando el “Brief Pain Inventory”, BPI) a las 4 semanas y en cada punto de tiempo posterior durante el estudio, en comparación con un placebo (Figura 1). La puntuación en la escala de dolor obtenida con ácido zoledrónico fue consistentemente inferior a la basal y la reducción de dolor se acompañó de una tendencia decreciente en las puntuaciones obtenidas en la escala de uso de analgésicos.
Figura 1: Cambios medios en la puntuación de BPI respecto al valor basal. Las diferencias estadísticamente significativas están marcadas (3p<0,05) para las comparaciones entre tratamientos (4 mg de ácido zoledrónico respecto a un placebo)
Las reacciones adversas que aparecieron con frecuencias inferiores al 5% se evaluaron médicamente y se demostró que estos casos eran consistentes con el perfil de seguridad bien establecido de ácido zoledrónico (ver sección 4.8).
En la población pediátrica con osteogénesis imperfecta grave, ácido zoledrónico parece que está asociado con riesgos más pronunciados de reacción de fase aguda, hipocalcemia y taquicardia no explicada, comparado con el pamidronato, pero esta diferencia disminuyó tras las perfusiones posteriores.
La Agencia Europea de Medicamentos ha eximido al titular de la obligación de presentar los resultados de los ensayos realizados con el medicamento de referencia que contiene ácido zoledrónico en los diferentes grupos de la población pediátrica para el tratamiento de la hipercalcemia inducida por tumor y la prevención de eventos relacionados con el esqueleto en pacientes con neoplasias avanzadas con afectación ósea (ver sección 4.2 para consultar la información sobre el uso en población pediátrica).
5.2 Propiedades farmacocinéticas
Perfusiones únicas y múltiples durante 5 y 15 minutos de 2, 4, 8 y 16 mg de ácido zoledrónico en 64 pacientes con metástasis ósea dieron como resultado los datos farmacocinéticos siguientes, observándose que son independientes de la dosis.
Después de iniciar la perfusión de ácido zoledrónico, las concentraciones plasmáticas de ácido zoledrónico aumentaron rápidamente, alcanzando el pico al final del periodo de perfusión, seguido de un rápido descenso hasta < 10% del pico después de 4 horas y < 1% del pico después de 24 horas, con un periodo subsiguiente prolongado de concentraciones muy bajas que no superan el 0,1% del pico antes de la segunda perfusión de ácido zoledrónico el día 28.
Ácido zoledrónico administrado por vía intravenosa se elimina por un proceso trifásico: eliminación bifásica rápida de la circulación sistémica, con semividas de t1/2a 0,24 y t1/2B 1,87 horas, seguida por una fase de eliminación prolongada con una semivida de eliminación terminal de t1/2? 146 horas. Después de dosis múltiples cada 28 días no hubo acumulación de ácido zoledrónico en plasma. Ácido zoledrónico no se metaboliza y se excreta inalterado por vía renal. Durante las primeras 24 horas, el 39 ± 16% de la dosis administrada se recupera en la orina, mientras que la restante se une principalmente al tejido óseo. Del tejido óseo se libera muy lentamente volviendo a la circulación sistémica y se elimina por vía renal. El aclaramiento corporal total es 5,04 ± 2,5 l/h, independiente de la dosis, y no está afectado por el sexo, edad, raza ni peso corporal. Incrementando el tiempo de perfusión de 5 a 15 minutos se produjo un descenso del 30% en la concentración de ácido zoledrónico al final de la perfusión, sin afectar al área bajo la curva de la concentración plasmática frente al tiempo.
Incluye fracturas vertebrales y no vertebrales