Ventilastin Novolizer 100 Microgramos/Dosis Polvo Para Inhalacion
Información obsoleta, busque otrofjljp
fjljp
STTÍ
RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
1. NOMBRE DEL MEDICAMENTO
Ventilastin Novolizer 100 microgramos / dosis polvo para inhalación
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada dosis suministrada contiene 100 microgramos de salbutamol equivalente a 120 microgramos de sulfato de salbutamol.
La dosis suministrada es la dosis disponible para el paciente después de pasar por la boquilla. Excipiente:
11,42 miligramos de lactosa monohidrato/dosis suministrada.
3. FORMA FARMACÉUTICA
Polvo para inhalación Polvo blanco.
4. DATOS CLÍNICOS
4.1. Indicaciones terapéuticas
Ventilastin Novolizer está indicado en adultos, adolescentes y niños de 6 a 12 años.
Tratamiento sintomático de trastornos asociados con obstrucción reversible de las vías respiratorias, por ejemplo, asma o enfermedad pulmonar obstructiva crónica con un importante componente de reversibilidad.
Prevención de los ataques de asma inducidos por el ejercicio o la exposición a alergenos.
4.2 Posología y forma de administración
Posología
La dosis depende del tipo, gravedad y evolución del trastorno.
Asma
Adultos (incluidas las personas de edad avanzada y adolescentes)
Para el alivio de los síntomas agudos, incluido broncoespasmo, en adultos se recomienda una dosis inicial de una inhalación (100 microgramos).
Para la prevención de los síntomas inducidos por el ejercicio o los alergenos se deberán realizar dos inhalaciones (200 microgramos) 10-15 minutos antes del estímulo.
La dosis máxima, según demanda, en 24 horas no debe superar las 8 inhalaciones (equivalentes a 800 microgramos).
Niños (de 6 a 12 años)
Para el alivio de los síntomas agudos, incluido el broncoespasmo, en niños de 6 o más años de edad se recomienda una dosis inicial de una inhalación (100 microgramos).
Para la prevención de síntomas inducidos por el ejercicio o los alergenos se deberá realizar una inhalación (100 microgramos) 10-15 minutos antes del estímulo y una inhalación adicional (hasta un total de 200 microgramos), si fuese necesario.
La dosis máxima, según demanda, en 24 horas no debe ser superior a 4 inhalaciones (equivalentes a 400 microgramos).
Niños menores de 6 años
Salbutamol Novolizer no está recomendado en niños menores de 6 años debido a que no hay datos suficientes sobre su seguridad y eficacia.
EPOC
Adultos (incluidas las personas de edad avanzada y adolescentes)
Para el alivio de los síntomas agudos, incluido el broncoespasmo, se recomienda una dosis inicial de una inhalación (100 microgramos) en adultos.
La dosis máxima, a demanda, en 24 horas no debe superar las 8 inhalaciones (equivalentes a 800 microgramos).
Para todos los pacientes
Cuando Ventilastin Novolizer 100 microgramos polvo para inhalación sustituye a otros inhaladores de Salbutamol, la cantidad de salbutamol suministrada a los pulmones puede variar entre diferentes inhaladores y, por consiguiente, se debe ajustar la posología.
Método de administración
Deberá haber un intervalo de al menos 1 minuto entre 2 inhalaciones.
Uso por inhalación
Uso y manejo del dispositivo Novolizer
Cartucho

Tapa deslizante

Recambio
1. Presione ligeramente las superficies onduladas a ambos lados de la tapa deslizante, desplácela hacia delante y levántela.
2. Retire la lámina protectora de aluminio de la caja del cartucho y extraiga el cartucho nuevo.
3. Inserte el cartucho en el dispositivo Novolizer con el contador de dosis orientado hacia la boquilla.
4. Vuelva a colocar la tapa entre las guías laterales desde arriba y presione hacia abajo, hacia el botón dosificador, hasta que encaje en su sitio. El cartucho se puede dejar en el dispositivo Novolizer hasta que su consumo total, o hasta 6 meses después de su inserción.
Nota: los cartuchos de Ventilastin Novolizer 100 microgramos solamente se pueden utilizar en el
inhalador de polvo Novolizer.
Utilización
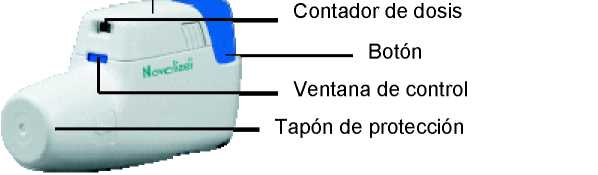
1. Cuando utilice el Novolizer manténgalo siempre en posición horizontal. En primer lugar retire el tapón protector.
2. Presione por completo el botón de dosificación coloreado. Se oirá un sonoro doble “clic” y el color de la ventana de control (abajo) cambiará de rojo a verde. Entonces suelte el botón coloreado. El color verde en la ventana indica que el Novolizer está listo para ser utilizado.
3. Exhale (pero no en el inhalador de polvo).
4. Coloque los labios alrededor de la boquilla. Inhale el polvo con una profunda inspiración. Durante esta inspiración se deberá oír un sonoro “clic”, que indica una inhalación correcta. Contenga la respiración durante algunos segundos y, a continuación, siga respirando normalmente.
Nota: Si el paciente necesita recibir más de una inhalación cada vez, se deberán repetir los pasos 2-4.
5. Vuelva a colocar el tapón de protección en la boquilla - el procedimiento de administración ha finalizado.
6. El número que aparece en la ventana superior indica el número de inhalaciones que quedan.
Nota: El botón de dosificación coloreado sólo se debe presionar inmediatamente antes de la inhalación.
Con el dispositivo Novolizer no es posible que se produzca una doble inhalación por error. El sonido del “clic” y el cambio de color en la ventana de control indican que la inhalación se ha realizado correctamente. Si el color de la ventana de control no cambia, se deberá repetir la inhalación. Si la inhalación no se realiza correctamente después de varios intentos, el paciente deberá consultar a su médico.
Limpieza
El dispositivo Novolizer se debe limpiar a intervalos regulares, pero al menos cada vez que se cambie el cartucho. En el prospecto se encuentran las “Instrucciones de Uso” donde se incluyen las instrucciones de limpieza del dispositivo.
Nota: Con el fin de garantizar el uso correcto del inhalador, los pacientes deben recibir instrucciones detalladas sobre la forma de utilizar el dispositivo. Los niños deberían utilizar este producto bajo supervisión de un adulto.
4.3 Contraindicaciones
Hipersensibilidad al principio activo, salbutamol, o al excipiente lactosa monohidrato (que contiene pequeñas cantidades de proteínas de la leche).
4.4 Advertencias y precauciones especiales de empleo
El tratamiento debe llevarse a cabo gradualmente, según la gravedad.
Los broncodilatadores no deben ser el único o principal tratamiento en pacientes con asma persistente.
El asma grave requiere evaluación médica regular, dado que los pacientes presentan el riesgo de ataques severos o, incluso, muerte.
Para pacientes con asma, el uso de Ventilastin Novolizer 100 microgramos polvo para inhalación no debe retrasar la introducción y el uso regular de la terapia con corticosteroides inhalados.
Salbutamol debe utilizarse con precaución, y sólo si está estrictamente indicado, en los casos siguientes:
- trastornos cardiacos graves, en particular infarto de miocardio reciente;
MINISTB?K)DE SANIDAD, POLIT1C A SOCIAL E IGUALDAD Agenc a es pariera de mercártenos y productos sanitarios
- enfermedad cardíaca coronaria, cardiomiopatía hipertrófica obstructiva y taqui-arritmia;
am
- hipertensión grave y no tratada;
- aneurisma;
- hipertiroidismo;
- diabetes de difícil control;
- feocromocitoma.
Existen evidencias, procedentes de los datos post-marketing y de la literatura publicada, de raros casos de isquemia miocárdica asociada con salbutamol. Se debe advertir a los pacientes con enfermedad cardíaca grave subyacente (ej. Enfermedad cardíaca isquémica, taquiarritmia o fallo cardíaco grave) que están recibiendo salbutamol para una enfermedad respiratoria, que informen a su médico si experimentan dolor de pecho o cualquier síntoma de empeoramiento de la enfermedad cardíaca.
Se debe tener cuidado en el tratamiento de ataques agudos de asma o exacerbaciones de asma grave ya que se han notificado casos de aumento de los niveles séricos de lactato, y rara vez, acidosis láctica después del uso de altas dosis de salbutamol. Estos síntomas son reversibles al reducir la dosis de salbutamol.
Es importante la auto-evaluación diaria del control del asma, siguiendo las instrucciones relativas al uso de Ventilastin Novolizer 100 microgramos y a cualquier otro medicamento necesario para el tratamiento del asma para poder realizar un seguimiento de la evolución de la enfermedad, monitorizando el éxito del tratamiento tanto broncodilatador como antiinflamatorio. El paciente debe aprender a medir regularmente la tasa máxima de flujo espiratorio (PEFR), empleando un espirómetro portátil.
Si el control de la enfermedad no mejora de forma satisfactoria o se deteriora, o si el tratamiento de alivio con broncodilatadores de corta acción pierde eficacia, o se requieren más inhalaciones de las habituales, se debe buscar consejo médico para volver a evaluar la situación clínica, revisándose el tratamiento farmacológico. En este caso, para pacientes con asma puede ser necesaria la terapia antiinflamatoria, puede precisarse incrementar la dosis de terapia antiinflamatoria o se puede necesitar un breve ciclo de glucocorticoides orales. En pacientes con enfermedad pulmonar obstructiva crónica, puede ser necesario el tratamiento regular con uno o más brocodilatadores de larga acción, rehabilitación, uso de corticoides inhalados u oxígeno a largo plazo.
El aumento en el uso de broncodilatadores y, en particular, de agonistas beta2-adrenérgicos inhalados de corta acción, para el alivio de los síntomas indica un deterioro del control de la enfermedad. Un deterioro súbito y creciente de los síntomas pueden amenazar la vida. Por consiguiente, se debe buscar de inmediato ayuda médica.
La dosis y frecuencia de inhalación de los agonistas beta2 de corta duración de acción sólo se deben aumentar por consejo médico, y si una dosis anteriormente eficaz fracasa en proporcionar el alivio esperado, el paciente deberá consultar con su médico. El uso de dosis superiores a las prescritas puede ser peligroso (ver sección 4.9). Si no se alivian los síntomas del asma agudo o incluso empeoran tras una segunda inhalación, o si los pacientes no son capaces de hacer funcionar el inhalador de polvo (= Novolizer) durante un ataque agudo de asma, deben pedir inmediatamente ayuda médica.
La terapia con beta2-agonistas puede tener como consecuencia una hipopotasemia potencialmente grave, en especial por administración parenteral o nebulizada. Se aconseja especial precaución en el asma agudo grave, ya que sus efectos pueden verse potenciados por la hipoxia.
Las preparaciones de salbutamol inhalado no son adecuadas para el tratamiento del parto prematuro y no se deben utilizar con amenaza de aborto.
La lactosa puede contener proteínas de la leche. Puede provocar reacciones alérgicas en pacientes con alergia a la proteína de la leche de vaca.
Los pacientes con intolerancia hereditaria a galactosa, insuficiencia de lactasa de Lapp (insuficiencia observada en ciertas poblaciones de Laponia) o malabsorción de glucosa o galactosa no deben usar esta medicamento.
Se debe instruir a los pacientes en el uso adecuado del dispositivo Novolizer. Es necesario comprobar la técnica de inhalación de los pacientes para garantizar que éste es capaz de utilizar correctamente el dispositivo Novolizer.
4.5 Interacción con otros medicamentos y otras formas de interacción
Salbutamol y los fármacos bloqueantes de receptores beta no selectivos normalmente no deben prescribirse conjuntamente. En pacientes con asma, la administración de bloqueantes de los receptores beta se asocia con un riesgo de broncoconstricción grave.
Cuando se administran anestésicos halogenados, por ejemplo, halotano, metoxiflurano o enflurano, a pacientes tratados con salbutamol, puede esperarse un aumento del riesgo de disritmias e hipotensión graves. Si se prevé una anestesia con anestésicos halogenados, se debe tener la precaución de asegurar que salbutamol no se utilice durante al menos 6 horas antes de iniciar la anestesia.
El tratamiento con salbutamol puede provocar hipopotasemia (ver secciones 4.4. y 4.8.). Este efecto puede verse potenciado por la administración simultánea de otros fármacos, en especial derivados de xantina, glucocorticoides, diuréticos y glucósidos cardiacos (digoxina). En estas situaciones se deberán vigilar los niveles de potasio en suero.
Los inhibidores de la monoamino-oxidasa y los antidepresivos tricíclicos pueden incrementar el riesgo de efectos secundarios cardiovasculares.
4.6 Fertilidad, embarazo y lactancia
Los estudios preclínicos y la experiencia clínica a largo plazo no han demostrado que salbutamol tenga efecto teratogénico alguno. Si la madre utiliza salbutamol durante la gestación, puede aumentar la frecuencia del pulso del feto. Dado que salbutamol se excreta de forma pasiva en la leche materna, dosis elevadas pueden inducir efectos farmacológicos en el lactante.
Aunque se considera que salbutamol es el tratamiento de primera línea para el alivio del broncoespasmo en mujeres asmáticas gestantes, su uso durante la gestación, especialmente durante el primer trimestre, y durante la lactancia sólo se deberá considerar después de haber valorado cuidadosamente los beneficios frente a los riesgos (ver sección 5.3).
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
No se han realizado estudios sobre los efectos en la capacidad para conducir y utilizar máquinas.
4.8 Reacciones adversas
Cabe esperar que hasta aproximadamente un 10% de los pacientes experimenten reacciones adversas.
Éstas dependen de la dosis y de la susceptibilidad individual. Las reacciones comunicadas con más frecuencia son: alteración del gusto (mal sabor, desagradable e inusual) y reacciones en el punto de administración (irritación de boca y garganta, sensación de ardor en la lengua), ligeros temblores (habitualmente de las manos), náuseas, sudación, inquietud, cefaleas y mareo. Estas reacciones adversas pueden desaparecer, en el plazo de 1-2 semanas, si se continúa con el tratamiento.
Al igual que con otras terapias de inhalación, en raros casos se puede producir un broncoespasmo paradójico, evidenciado por un incremento inmediato del jadeo tras la administración. El
broncoespasmo paradójico se debe tratar de inmediato con una presentación alternativa o con un broncodilatador inhalado diferente, de acción rápida. La administración de Ventilastin Novolizer 100 microgramos se debe interrumpir de inmediato, el paciente debe ser evaluado y, en caso necesario, instaurar un tratamiento alternativo.
am
MINISTERIO DE SANIDAD, POLIT1C A SOCIAL E IGUALDAD Agenos espanta oe mescamemos y productos sanéanos
Se han notificado efectos estimulantes sobre el sistema nervioso central tras la inhalación de salbutamol, los cuales se manifiestan con hiperexcitabilidad, conducta hiperactiva, trastornos del sueño y alucinaciones. Estas observaciones se han descrito predominantemente en niños de hasta 12 años de edad.
Los efectos adversos se indican a continuación clasificados por órganos del sistema y frecuencia. Las frecuencias se definen como:
Muy frecuentes (> 1/10); Frecuentes (> 1/100, < 1/10); Poco frecuentes (> 1/1.000, < 1/100); Raras (> 1/10.000, < 1/1.000); Muy raras (< 1/10.000)
|
Sistema de órganos |
Frecuencia |
Reacción adversa al fármaco |
|
Trastornos de la sangre y del sistema linfático |
Muy raro |
Trombopenia |
|
Trastornos del sistema inmunológico |
Muy raro |
Reacción de hipersensibilidad |
|
Trastornos del metabolismo y de la nutrición |
Raro |
Hipopotasemia, hiperglucemia, aumento de la insulina, ácidos grasos libres, glicerol y cuerpos cetónicos |
|
Trastornos psiquiátricos |
Frecuente |
Inquietud |
|
Trastornos del sistema nervioso |
Frecuente |
Temblores leves, mareo |
|
Raro |
Conducta hiperactiva | |
|
Muy raro |
Hiperexcitabilidad, alteraciones del sueño, alucinaciones | |
|
Trastornos cardiacos |
Raro |
Taquicardia, arritmia cardiaca (fibrilación auricular, taquicardia supraventricular, extrasístoles), palpitaciones, angina de pecho, efectos sobre la tensión arterial (descenso o elevación) |
|
Muy raro |
Isquemia miocárdica | |
|
Trastornos vasculares |
Raro |
Vasodilatación periférica |
|
Muy raro |
Colapso | |
|
Trastornos respiratorios, torácicos y mediastínicos |
Raro |
Tos Broncoespasmo paradójico |
|
Trastornos gastrointestinales |
Frecuente |
Náuseas, alteración del gusto |
|
Trastornos de la piel y del tejido subcutáneo |
Frecuente |
Sudación |
|
Muy raro |
Prurito, rash, eritema, urticaria, angioedema | |
|
Trastornos musculoesqueléticos y del tejido conjuntivo |
Raro |
Calambres musculares |
|
Trastornos renales y urinarios |
Muy raro |
Nefritis |
|
Trastornos generales y en el punto de administración |
Frecuente |
Cefaleas, reacciones en el lugar de administración (irritación de boca y garganta, sensación de ardor en la lengua) |
Lactosa monohidrato contiene pequeñas cantidades de proteínas de la leche y, por tanto, puede producir reacciones alérgicas.
Notificación de sospechas de reacciones adversas:
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del Sistema Español de Farmacovigilancia de medicamentos de Uso Humano: https://www.notificaram.es.
4.9 Sobredosis
Síntomas de sobredosis
En caso de sobredosis, los efectos adversos mencionados anteriormente (ver sección 4.8) se producen con mucha rapidez y con gravedad aumentada. Los síntomas típicos son: taquicardia, palpitaciones, arritmia, inquietud, alteraciones del sueño, dolor torácico y temblor intenso, especialmente de manos, pero también de todo el cuerpo.
Ocasionalmente, se han observado reacciones psicóticas tras dosis excesivas de salbutamol. En el caso de sobredosis de salbutamol puede haber un desplazamiento progresivo de potasio hacia el espacio intracelular, dando lugar a hipopotasemia, así como hiperglucemia, hiperlipidemia e hipercetonemia.
Tratamiento de la sobredosis
El tratamiento tras una sobredosis de un beta-simpatomimético es principalmente sintomático. Se pueden considerar las siguientes medidas, dependiendo de las circunstancias individuales:
- Si se ingieren grandes cantidades del fármaco, se deberá considerar el lavado de estómago. El carbón activo y los laxantes pueden tener efectos favorables sobre la absorción no deseada del beta-simpatomimético.
- Para los síntomas cardiacos de sobredosis con salbutamol, se puede considerar la administración de un beta-bloqueante cardio-selectivo, pero los beta-bloqueantes sólo se deben utilizar con precaución, evitándolos en lo posible en pacientes con antecedentes de broncoespasmo. En estos pacientes, está indicada la monitorización por ECG.
- En caso de una reducción bastante pronunciada de la tensión arterial, se recomienda la sustitución de volumen (por ejemplo, expansores del plasma).
- Si se desarrolla hipopotasemia, se deberá controlar el equilibrio electrolítico y, en caso necesario, puede ser necesario administrar electrolitos.
5. PROPIEDADES FARMACOLÓGICAS
am
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: AGENTES CONTRA PADECIMIENTOS OBSTRUCTIVOS DE LAS VÍAS RESPIRATORIAS, ADRENÉRGICOS, INHALATORIOS: Agonistas selectivos de receptores beta-2 adrenérgicos. Código ATC: R03AC02
Salbutamol es un agonista beta-2 selectivo de los adrenoceptores que, a dosis terapéuticas, tiene una acción selectiva sobre los receptores beta-2 bronquiales y escaso efecto sobre los beta-1 receptores cardiacos. Tras la inhalación, salbutamol ejerce una acción estimulante sobre los beta-2 receptores del músculo liso bronquial, asegurando así una rápida broncodilatación, que alcanza importancia en el plazo de pocos minutos y persiste durante 4 a 6 horas. El medicamento causa asimismo vasodilatación que da lugar a un efecto cronotrópico reflejo y a efectos metabólicos, incluida la hipopotasemia.
5.2 Propiedades farmacocinéticas
La absorción y metabolismo de salbutamol en pulmones y tracto gastrointestinal son diferentes. Tras la inhalación, aproximadamente el 20-47% del principio activo, referido a la dosis administrada, pasa a las vías bronquiales más profundas, mientras que el resto se deposita en la boca y en la parte superior del tracto respiratorio y se traga posteriormente. La fracción que se deposita en las vías respiratorias se absorbe en los tejidos pulmonares y la circulación, pero no se metaboliza en el pulmón. Al alcanzar la circulación sistémica, resulta accesible para el metabolismo hepático y se excreta principalmente con la orina como fármaco inalterado y como sulfato fenólico.
La fracción deglutida de una dosis inhalada se absorbe desde el tractor gastrointestinal y sufre un considerable metabolismo de primer paso, hasta formar el sulfato fenólico. Tanto el fármaco inalterado como el conjugado se excretan principalmente con la orina. La mayor parte de la dosis de salbutamol administrada por vía intravenosa, oral o por inhalación, se excreta en un plazo de 72 horas. Salbutamol se une a las proteínas plasmáticas en un 10%.
5.3 Datos preclínicos sobre seguridad
Los datos preclínicos no revelan riesgos especiales para el ser humano en base a los estudios convencionales de farmacología de seguridad, toxicidad de dosis repetidas, genotoxicidad, potencial carcinogénico y toxicidad reproductiva. Los efectos registrados en estudios de toxicidad se relacionaron con la actividad beta-adrenérgica de salbutamol.
6. DATOS FARMACÉUTICOS
6.1 Lista de excipientes
Lactosa monohidrato.
6.2 Incompatibilidades
No aplicable.
6.3 Período de validez
• Medicamento (Ventilastin polvo para inhalación) en el envase Período de validez antes de la apertura del envase
3 años
Período de validez después de la primera apertura del envase 6 meses
• Dispositivo Novolizer
Período de validez antes de la primera utilización 3 años
Período de validez durante la utilización 1 año
¡m
Nota: Se ha demostrado el funcionamiento del dispositivo Novolizer en ensayos para 2.000 dosis. Por lo tanto, se puede utilizar un máximo de 10 cartuchos que contienen 200 dosis medidas con este dispositivo (durante un solo año), antes de sustituirlo.
6.4 Precauciones especiales de conservación
No conservar a temperatura superior a 30°C.
Conservar en su envase original.
Durante su uso, Ventilastin Novolizer 100 microgramos se debe conservar protegido de la humedad.
6.5 Naturaleza y contenido del envase
Envases originales de venta y muestras:
1 cartucho de 200 dosis (poliestireno/polipropileno) con al menos 2,308 g de polvo, envasado en un contenedor de polipropileno sellado con una lámina de aluminio y 1 inhalador para polvo (boquilla de policarbonato y dispositivo de copolímero de acrilnitrilbutadienoestirol, polioximetileno).
Envases de recambio:
1 cartucho de 200 dosis (poliestireno / polipropileno) con al menos 2,308 g de polvo, envasado en un contenedor de polipropileno sellado con lámina de aluminio.
2 cartuchos de 200 dosis, cada uno, (poliestireno / polipropileno) con al menos 2,308 g de polvo, envasado en contenedores de polipropileno sellados con lámina de aluminio.
Envase para el Hospital:
Envase con 10 envases originales de venta.
No todas las presentaciones se encuentran comercializadas.
6.6 Precauciones especiales de eliminación y otras manipulaciones
Ninguna especial.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Meda Pharma, SAU Av. Castilla, 2
Parque Empresarial San Fernando - Edif. Berlín 28830 San Fernando de Henares (Madrid)
8. NÚMERO(S) DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
66.408
9. FECHA DE LA PRIMERA AUTORIZACIÓN / RENOVACIÓN DE LA AUTORIZACIÓN
Fecha de la primera autorización: 26 /Octubre/ 2004.
Fecha de la última renovación: 13 /Mayo/ 2011
10. FECHA DE REVISIÓN DEL TEXTO
Octubre 2013
La información detallada y actualizada de este medicamento está disponi ble en la página Web de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) http://www.aemps.gob.es.