Nivador 125 Mg/5 Ml Granulado Para Suspension Oral En Frasco
Información obsoleta, busque otroDE SANIDAD, POLÍTICA SOCIAL E IGUALDAD
|
1 | |
|
Oí |
k agencia española de 1 medicamentos y I productos sanitarios |
PROSPECTO: INFORMACIÓN PARA EL USUARIO
NIVADOR 125 mg/5 ml granulado para suspensión oral en frasco
Cefuroxima axetilo
Lea todo el prospecto detenidamente antes de empezar a tomar el medicamento.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado a usted y no debe dárselo a otras personas aunque tengan los mismos síntomas, ya que puede perjudicarles.
- Si considera que alguno de los efectos adversos que sufre es grave o si aprecia cualquier efecto adverso no mencionado en este prospecto, informe a su médico o farmacéutico.
Contenido del prospecto:
1. Qué es NIVADOR y para qué se utiliza
2. Antes de tomar NIvAdOR
3. Cómo tomar NIVADOR
4. Posibles efectos adversos
5. Conservación de NIVADOR
6. Información adicional
1. QUÉ ES NIVADOR Y PARA QUÉ SE UTILIZA
NIVADOR 125 mg/5 ml granulado para suspensión oral en frasco, contiene cefuroxima axetilo, antibiótico que pertenece al grupo de las cefalosporinas.
Este medicamento está indicado para el tratamiento de diversas infecciones, de intensidad leve a moderada, causadas por gérmenes sensibles a cefuroxima tales como: sinusitis, otitis, amigdalitis, faringitis, bronquitis, neumonía, infecciones urinarias, infecciones de la piel y de los tejidos blandos.
2. ANTES DE TOMAR NIVADOR No tome NIVADOR
Si es alérgico (hipersensible) a las penicilinas, a las cefalosporinas o a cualquiera de los demás componentes de NIVADOR (ver apartado 6).
Tenga especial cuidado con NIVADOR
-Si después de tomar el medicamento se produjera alguna reacción alérgica, suspenda el tratamiento y acuda a su médico lo antes posible.
-Si padece alguna enfermedad del riñón, su médico puede modificar la dosis a tomar.
-Si padece alguna enfermedad del hígado, consulte con su médico antes de tomar este medicamento.
-Si durante el tratamiento con este medicamento tiene diarreas abundantes, debería informar a su médico tan pronto como sea posible.
El uso de antibióticos como NIVADOR puede dar lugar a otro tipo de infección (Candida). El uso prolongado también puede dar lugar a otro tipo de infecciones (microorganismos no sensibles al medicamento), lo cual puede requerir la suspensión del tratamiento.
Correo electrúnicoI
C / CAMPEZO, 1 - EDIFICIO 8 28022 MADRID
Informe a su médico si le van a realizar alguna prueba de análisis para la determinación de glucosa en sangre o en orina, puesto que este medicamento podría alterar los resultados.

Uso de otros medicamentos
Informe a su médico o farmacéutico si está utilizando o ha utilizado recientemente otros medicamentos, incluso los adquiridos sin receta, ya que puede ser necesario interrumpir el tratamiento o ajustar la dosis de alguno de ellos.
-Informe a su médico o farmacéutico si está utilizando anticonceptivos, ya que puede ser necesario utilizar otros métodos anticonceptivos adicionales.
-Informe a su médico o farmacéutico si está tomando estrógenos (hormonas sexuales femeninas), ya que la administración conjunta con NIVADOR puede reducir el efecto de los mismos.
-Este medicamento no debe administrarse junto a antibióticos bacteriostáticos (cloranfenicol, tetraciclinas, sulfamidas).
-Debe tenerse especial precaución si se recibe tratamiento conjunto con diuréticos potentes (como furosemida y ácido etacrínico), ya que aumentan el riesgo de alteraciones renales por las cefalosporinas.
-Algunos medicamentos pueden reducir el efecto de este medicamento. Haga saber a su médico si está tomando algún antiácido.
-La administración conjunta de NIVADOR y probenecid (medicamento para tratar la gota) puede aumentar los efectos beneficiosos y/o tóxicos de NIVADOR.
Toma de NIVADOR con los alimentos y bebidas
Este medicamento debe tomarse después de ingerir algún alimento.
Si se desea, la suspensión oral de NIVADOR se puede a su vez diluir en zumos de frutas fríos o leche fría y tomar inmediatamente. En ningún caso se debe mezclar con bebidas calientes.
Embarazo y Lactancia
Consulte a su médico o farmacéutico antes de utilizar cualquier medicamento.
NIVADOR deberá administrarse con precaución durante el embarazo. Su médico valorará la necesidad de emplear este medicamento.
NIVADOR pasa a la leche materna y, en consecuencia, se deberá tener precaución cuando se administre a madres en período de lactancia.
Conducción y uso de máquinas
La administración de NIVADOR puede producir mareos, por lo que antes de conducir o manejar maquinaria se debe establecer cómo puede afectar la toma de dicho medicamento a cada persona.
Información importante sobre algunos de los componentes de NIVADOR granulado para suspensión oral en frasco
Este medicamento contiene unos 3 gramos de sacarosa por cada 5 ml, lo que debe ser tenido en cuenta en pacientes con diabetes mellitus y con intolerancia a ciertos azúcares. Si su médico le ha indicado que padece una intolerancia a ciertos azúcares, consulte con él antes de tomar este medicamento.
Este medicamento puede ser perjudicial para personas con fenilcetonuria porque contiene aspartamo que es una fuente de fenilalanina. Cada 5 ml de suspensión reconstituida contienen 11,8 mg de fenilalanina. Si su médico le ha indicado que padece fenilcetonuria, consulte con él antes de tomar este medicamento.
COMO TOMAR NIVADOR
3.

Siga exactamente las instrucciones de administración de NIVADOR indicadas por su médico. Consulte a su médico o farmacéutico si tiene dudas.
Su médico le indicará la duración de su tratamiento con NIVADOR. La dosis normal es:
• Adultos y niños mayores de 12 años: la dosis habitual es de 2 jeringas de 5 ml (250 mg) por toma, por vía oral, cada 12 horas. (Se incluye una jeringa dosificadora en el estuche).
En algunas enfermedades como bronquitis aguda, exacerbación aguda de bronquitis crónica y neumonía, la dosis se puede incrementar a 4 jeringas de 5 ml (500 mg) por toma, vía oral, cada 12 horas siempre y cuando su médico lo considere necesario.
• Niños de 5 a 12 años: la dosis habitual es de 1 jeringa de 5 ml (125 mg) por vía oral cada 12 horas. En niños con otitis media y en aquellos casos que el médico considere necesario, puede incrementarse la dosis a dos jeringas de 5 ml (250 mg) por toma, por vía oral, cada 12 horas.
• Niños de 3 meses a 5 años: en general 0,6 ml (15 mg) por kilogramo de peso al día, divididos en dos tomas. En niños con otitis media y en aquellos casos que el médico considere necesario, puede incrementarse la dosis a 15 mg por kilogramo de peso, dos veces al día.
No hay experiencia en niños menores de 3 meses.
No suspenda el tratamiento, a menos que su médico se lo indique. La duración normal del tratamiento es de 5 a 10 días. Es recomendable no prolongar el tratamiento durante más de 10 días.
Instrucciones para la correcta administración del preparado Agitar siempre el frasco vigorosamente antes de tomar la medicación.
La suspensión reconstituida se debe refrigerar inmediatamente en nevera a 2-8°C hasta un máximo de 10 días y mantener siempre en nevera a 2-8°C. La suspensión reconstituida o el granulado no
deberán mezclarse con líquidos calientes. . %,
medicamento.
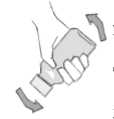
1. Agitar el frasco para desprender los gránulos. Retirar la tapa y la membrana termosellada. Si ésta última no está presente o está defectuosa el producto debe ser devuelto a la farmacia.
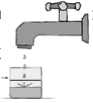
2. Llenar el vasito que se incluye en el estuche, con agua hasta la marca indicada (23 ml). Esa cantidad de agua es suficiente para reconstituir la suspensión de 60 ml.
3. Añadir el agua al frasco de una vez.
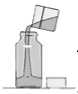
4. Introducir el adaptador de la jeringa dosificadora en el cuello del frasco. Presionar hacia abajo completamente hasta que el adaptador encaje perfectamente en el cuello del frasco.
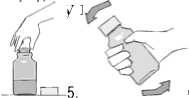
5. Volver a colocar la tapa. Invertir el frasco y agitar vigorosamente hasta obtener una suspensión homogénea.
Volver a poner el frasco en posición vertical y agitar vigorosamente.
6. Refrigerar inmediatamente en nevera a 2-8°C.
Mantener la suspensión reconstituida en nevera durante al menos una hora antes de tomar la primera dosis.
Instrucciones de uso para la jeringa dosificadora
1.
2.
3.

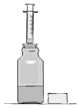
1. Quite la tapa del frasco e introduzca la jeringa dosificadora en el adaptador situado en el cuello del frasco.
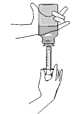
2. Invierta el frasco con la jeringa. Tire del émbolo hacia abajo hasta retirar la cantidad correcta. Coloque el frasco y jeringa en posición vertical. Asegúrese de que el émbolo no se mueve y retire y quite la jeringa del adaptador.
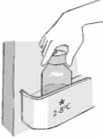
3. Con el paciente sentado en posición vertical, coloque la punta de la jeringa dentro de la boca del paciente, apuntando hacia el interior de la mejilla. Presione el émbolo de la jeringa lentamente para administrar el fármaco sin que el paciente se atragante. NO administre el fármaco a chorros.
Tras administrar la dosis vuelva a poner la tapa del frasco sin quitar el adaptador de plástico. Desmonte la jeringa y lávela con agua fría. Deje que el émbolo y el cuerpo de la jeringa se sequen al aire.
4. Vuelva a introducir el frasco inmediatamente en nevera a 2-8°C hasta la próxima dosis.
Si usted toma más NIVADOR del que debiera
Es poco probable que se produzca sobredosis con este medicamento. Si por alguna circunstancia ha
tomado más NIVADOR de lo que debe, consulte inmediatamente a su médico o farmacéutico o al
Servicio de Información Toxicológica, teléfono 91 562 04 20.
Si olvidó tomar NIVADOR
No tome una dosis doble para compensar las dosis olvidadas.
Si olvida tomar una dosis, tome la siguiente lo antes posible y continúe como hasta ese momento.
4. POSIBLES EFECTOS ADVERSOS
Al igual que todos los medicamentos, NIVADOR puede producir efectos adversos, aunque no todas las personas los sufran.
-Deje de tomar el medicamento y avise al médico inmeditamente:
Si experimentara respiración dificultosa, opresión en el pecho, hinchazón de párpados, cara o labios, o si apareciera urticaria o bultos en la piel.
-Deje de tomar el medicamento y comuníqueselo a su médico tan pronto como sea posible:
En caso de experimentar cualquiera de los siguientes síntomas: náuseas, diarrea importante, dolores severos de estómago, hemorragia del recto, heces con moco o pus o aparición de una tonalidad amarilla en la piel o los ojos.
-No deje de tomar el medicamento y avise a su médico:
En caso de experimentar alguno de los siguientes síntomas: picor, decoloración o escamosidad en la piel, dolores de cabeza, diarrea o náuseas leves, fácil aparición de magulladuras.

Los efectos adversos observados y asociados a la toma de NIVADOR son:
Efectos adversos frecuentes (pueden producirse en al menos 1 de cada 100 y menos de 1 de cada 10 personas)
• Dolores de cabeza, mareos
• Molestias gastrointestinales incluyendo diarreas, nauseas, dolor abdominal
• Eosinofilia (aumento del número de cierto tipo de leucocitos)
• Aumentos transitorios de los niveles de las enzimas del hígado
• Crecimiento de un hongo denominado Candida
Efectos adversos poco frecuentes (pueden producirse en al menos 1 de cada 1.000 y menos de 1 de cada 100 personas)
• Trombocitopenia (disminución del número de plaquetas)
• Leucopenia (disminución del número de leucocitos) en ocasiones profunda
• Erupción cutánea
• Vómitos
Efectos adversos raros (pueden producirse en al menos 1 de cada 10.000 y menos de 1 de cada 1.000 personas)
• Urticaria, prurito (picor)
• Colitis pseudomembranosa (diarrea mucosa sanguinolenta)
Efectos adversos muy raros (pueden producirse en menos de 1 de cada 10.000 personas)
• Anemia hemolítica (disminución del número de glóbulos rojos)
• Fiebre medicamentosa, enfermedad del suero (reacción alérgica de aparición tardía), anafilaxia (reacción de hipersensibilidad de aparición inmediata)
• Ictericia (coloración amarillenta de la piel y/o los ojos). Hepatitis
• Erupciones cutáneas graves
Si considera que alguno de los efectos adversos que sufre es grave o si aprecia cualquier efecto adverso no mencionado en este prospecto, informe a su médico o farmacéutico.
5. CONSERVACIÓN DE NIVADOR
Mantener fuera del alcance y de la vista de los niños.
No conservar a temperatura superior a 30°C.
Una vez reconstituida conservar inmediatamente en nevera entre 2°C y 8°C.
No utilice NIVADOR después de la fecha de caducidad que aparece en el envase, después de “CAD”. La fecha de caducidad es el último día del mes que se indica.
El plazo de validez de la suspensión oral una vez preparada es de 10 días en nevera, a temperatura entre 2°C y 8°C.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma ayudará a proteger el medio ambiente.


6. INFORMACIÓN ADICIONAL
Composición de NIVADOR 125 mg/5 ml granulado para suspensión oral en frasco
- El principio activo es: cefuroxima axetilo.
- Los demás componentes son: sacarosa, ácido esteárico, sabor tutti-frutti, povidona K30, aspartamo (E951), goma xantán y acesulfamo potásico.
Aspecto del producto y contenido del envase
Gránulos para suspensión oral. Cada frasco contiene gránulos para preparar una suspensión de 60 ml. El envase incluye una jeringa dosificadora de 5 ml dividida en unidades de 1 ml y un adaptador a presión, que encaja en el cuello de la botella y un vasito con una línea de enrase para adicionar el agua.
Titular de la autorización de comercialización y responsable de la fabricación
Titular de la autorización de comercialización:
Wellcome Farmacéutica, S.A.
Parque Tecnológico de Madrid
C/ Severo Ochoa, 2
28760 Tres Cantos (Madrid)
Teléfono: 902 202 700
Fax: 91 807 03 10
Correo electrónico: es-ci@gsk.com
Responsable de la fabricación:
Glaxo Wellcome Operations,
Barnard Castle, Reino Unido
OTRAS PRESENTACIONES
NIVADOR 125 mg comprimidos recubiertos con película, NIVADOR 250 mg comprimidos recubiertos con película y NIVADOR 500 mg comprimidos recubiertos con película: envases que contienen 12 comprimidos.
NIVADOR 125 mg granulado para suspensión oral en sobres, NIVADOR 250 mg granulado para suspensión oral en sobres y NIVADOR 500 mg granulado para suspensión oral en sobres: envases que contienen 12 sobres.
NIVADOR 250 mg/5 ml granulado para suspensión oral en frasco: envases conteniendo un frasco con gránulos para preparar 60 mililitros de suspensión oral.
Este prospecto ha sido aprobado en Mayo 2008
Agencia española de
medicamentos y
productos sanitarios