Meninvact Kit
Información obsoleta, busque otro
agencia española de medicamentos y productos sanitarios
MENINVACT Kit
Vacuna conjugada frente al meningocócico del grupo C (adsorbida) Polvo y disolvente para suspensión inyectable.
Lea todo el prospecto detenidamente antes de utilizar esta vacuna.
- Conserve este prospecto. Puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Esta vacuna se le ha recetado a usted./su hijo personalmente y no debe pasarla a otras personas.
Este prospecto contiene información sobre:
1. Qué es MENINVACT Kit y para qué se utiliza
2. Antes de usar MENINVACT Kit
3. Cómo usar MENINVACT Kit
4. Posibles efectos adversos
5. Conservación de MENINVACT Kit
MENINVACT Kit, es una vacuna conjugada frente al meningocócico del grupo C (adsorbida). Cada dosis de MENINVACT Kit se presenta en un envase que contiene un vial con polvo y una jeringa con disolvente para la preparación de una suspensión inyectable.
MENINVACT Kit se presenta en envases de 1, 5 y 10 dosis.
Cada dosis de 0,5 ml de vacuna reconstituida contiene 10 microgramos del principio activo, oligosacárido meningocócico del grupo C, conjugado (unido químicamente) a 12,5-25,0 microgramos de la proteína diftérica CRM197.
Los demás componentes del MENINVACT Kit son:
Vial de polvo: manitol, fosfato de sodio monobásico monohidrato, fosfato de sodio dibásico heptahidrato. Jeringa de disolvente: hidróxido de aluminio, cloruro de sodio y agua para inyectables.
Titular de la autorización de comercialización:
Sanofi Pasteur MSD, Ltd, Mallards Reach, Bridge Avenue, Maidenhead Berkshire, SL6 1QP Reino Unido
Responsable de la fabricación: Chiron S.r.l., Bellaria-Rosia, 53018 Sovicille (Siena), Italia.
1. QUÉ ES MENINVACT KIT Y PARA QUÉ SE UTILIZA
MENINVACT Kit es una vacuna que se utiliza para prevenir las enfermedades causadas por la bacteria Neisseria meningitidis serogrupo C. Actúa estimulando la producción de anticuerpos protectores frente al meningococo del serogrupo C.
La bacteria Neisseria meningitidis serogrupo C puede causar infecciones graves, a veces mortales, como la meningitis y la septicemia (infección de la sangre).
Grupo terapéutico: J07 (Vacunas) - Código ATC: J07A H (Vacunas antimenigococo)
Correo electrúnicoI
C / CAMPEZO, 1 - EDIFICIO 8 28022 MADRID
MENINVACT Kit está indicada en:
Vacunación frente a la enfermedad invasiva producida por Neisseria meningitidis serogrupo C en niños a partir de los 2 meses de edad, adolescentes y adultos.
El uso de MENINVACT Kit debe estar sujeto a las recomendaciones oficiales.
2. ANTES DE USAR MENINVACT Kit No debe administrarse MENINVACT Kit a personas:
- Que hayan presentado en el pasado una reacción alérgica a cualquier componente de la vacuna.
- Que presenten alguna enfermedad aguda con fiebre. En estos casos la vacunación deberá retrasarse.
Tenga especial cuidado con MENINVACT Kit:
El médico valorará si se debe administrar la vacuna en los siguientes casos:
- Si ha presentado reacciones alérgicas a otras vacunas.
- Si tiene problemas de coagulación de la sangre.
- Si tiene las defensas del organismo afectadas, ha recibido recientemente o está recibiendo un ciclo de tratamiento con corticosteroides u otros fármacos que alteran las defensas del organismo.
- Si usted sufre de una enfermedad de riñón llamada “síndrome nefrótico”.
Como medida de precaución, al igual que con todas las vacunas inyectables, la vacunación se debe realizar en un lugar que disponga del control médico y tratamiento apropiado para uso inmediato, en el caso poco probable de producirse una reacción anafiláctica (reacción alérgica grave) tras la administración de la vacuna.
No administrar por vía intravenosa subcutánea ni intradérmica.
Esta vacuna no protege frente a otros grupos de Neisseria meningitidis ni frente a otros organismos causantes de meningitis o septicemia que no sean Neisseria meningitidis serogrupo C. Además, aunque contiene la proteína diftérica CRM197, no protege frente a la difteria.
Embarazo:
No se ha establecido la seguridad de la vacuna en mujeres embarazadas por lo que debe evitarse su administración a menos que exista un riesgo definido de infección. El médico determinará si se debe administrar la vacuna.
Lactancia:
No hay información disponible sobre la seguridad de la vacuna durante el periodo de lactancia. El médico determinará si se debe administrar la vacuna.
Conducción y uso de máquinas:
Es poco probable que la vacuna produzca algún efecto sobre la capacidad de conducir o de utilizar máquinas. Se ha informado de la aparición poco frecuente de mareos después de la vacunación. Este efecto puede afectar temporalmente a la capacidad de conducir o utilizar maquinaria.
Uso con otros medicamentos:
Informe a su médico o farmacéutico si está tomando o ha tomado recientemente cualquier otro medicamento, incluso los adquiridos sin receta médica.
MENINVACT Kit se puede administrar al mismo tiempo que otras vacunas pediátricas (tales como, las vacunas orales o inyectables frente a la poliomielitis, vacunas de sarampión, rubéola y parotiditis (SRP), los toxoides de difteria y tétanos solos o combinados con vacuna de tos ferina, vacuna conjugada de Haemophilus influenzae tipo B (Hib) y vacuna de la Hepatitis B sola o al mismo tiempo que la Difteria, Tetanos, Hib, vacuna de la polio inactivada y pertussis acelular administradas como vacuna combinada, siguiendo las pautas habituales de vacunación, pero en diferente lugar de inyección.
MENINVACT Kit no se debe mezclar en la misma jeringa con otros medicamentos.
Información importante sobre algunos componentes de MENINVACT Kit
Este medicamento contiene menos de 23 mg de sodio por dosis (0,5 ml), esto es, esencialmente “exento de sodio”.
3. COMO UTILIZAR MENINVACT Kit
Siga estas instrucciones a menos que su médico le haya dado otras indicaciones distintas.
Recuerde realizar la vacunación en la fecha que le hayan recomendado.
Su médico le indicará el esquema de vacunación con MENINVACT Kit.
MENINVACT Kit se debe administrar mediante inyección intramuscular. En niños pequeños se administrará preferentemente en la zona anterolateral del muslo y en los niños mayores, adolescentes y adultos en la región deltoidea (músculo del hombro). Se debe prestar atención para no inyectar la vacuna en un vaso sanguíneo. Tampoco se debe inyectar vía subcutánea ni intradérmica.
La pauta de vacunación en la inmunización primaria en los niños menores de 12 meses es de dos dosis de MENINVACT Kit administradas a partir de los 2 meses de edad con un intervalo mínimo de dos meses.
En niños mayores de 12 meses, adolescentes y adultos: una dosis única de vacuna.
Si el niño se vacunó completamente en la infancia, se recomienda que reciba otra dosis de vacuna, llamada “dosis de recuerdo”, cuando él/ella sea mayor. Esta dosis extra es necesaria para reforzar la inmunidad del niño frente a Neisseria meningitidis grupo C.
Su medico le comunicará cuando se debe administrar esta dosis de recuerdo.
Todavía no se ha establecido la necesidad de administrar dosis de recuerdo posteriores en niños vacunados con una única dosis (es decir, a partir de 12 meses de edad al ser vacunados por primera vez).


La vacuna requiere preparación mediante reconstitución del vial que contiene el polvo con la jeringa de disolvente. Para ello, agitar suavemente la jeringa conteniendo el disolvente. Quitar la cápsula de la punta de la jeringa y adaptar un aguja apropiada. Utilizar el contenido total de la jeringa (0,6 ml de la suspensión) para reconstituir el vial con la vacuna Meningocócica C-CRM197 conjugada. Agitar suavemente el vial reconstituido hasta que la vacuna se disuelva completamente (esto asegurará que el antígeno está unido al adyuvante). Teniendo cuidado de no retirar totalmente el émbolo del cilindro de la jeringa, extraer el contenido total del vial dentro de la jeringa. Es normal que un pequeño residuo de líquido quede en el vial después de extraer la dosis.
Usted puede comparar la cantidad de vacuna reconstituida en su jeringa con la escala del dibujo siguiente para confirmar que ha retirado suficiente dosis de vacuna.
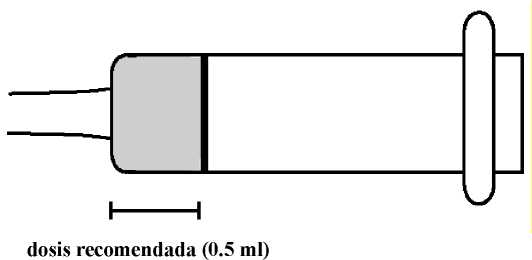
Asegúrese de que no haya burbujas de aire antes de inyectar la vacuna.
Después de la reconstitución, la vacuna es una suspensión homogénea ligeramente opaca e incolora o ligeramente amarillenta, sin partículas extrañas visibles. Si se observa alguna partícula extraña y/o algún cambio en su aspecto físico se deberá desechar la vacuna.
La vacuna se administrará inmediatamente después de la reconstitución.
Si se le administra más MENINVACT Kit del que debiera:
Es poco probable que se administre una sobredosificación de vacuna dado que cada inyección es una dosis única de 0,5 mililitros.
En caso de sobredosis o ingestión accidental consulte al Servicio de Información Toxicológica, teléfono: 91 562 04 20.
No hay experiencia de sobredosificación con MENINVACT Kit.
4. POSIBLES EFECTOS ADVERSOS
Como todos los medicamentos, MENINVACT Kit puede provocar efectos adversos en algunas personas.
Los efectos adversos se clasifican según su frecuencia en:
Muy frecuentes: mayor o igual a 1 de cada 10 pacientes Frecuentes: menos de 1 por cada 10, pero más de 1 por cada 100 pacientes Poco frecuentes: menos de 1 por cada 100 pero más de 1 por cada 1.000 pacientes Raros: menos de 1 por cada 1.000 pero más de 1 por cada 10.000 pacientes Muy raros: menos de 1 por cada 10.000 pacientes
Los efectos adversos fueron recogidos el día de la vacunación y en los días sucesivos durante al menos 3 y hasta 6 días tras la vacunación. La mayor parte de los efectos adversos se resolvieron durante el período de seguimiento.
A continuación se incluyen los efectos adversos recogidos en diferentes grupos de edad.
Trastornos generales Frecuentes: fiebre > 38°C
Reacciones en el lugar de inyección
Muy frecuentes: enrojecimiento, hinchazón y sensibilidad/dolor
Reacciones adicionales comunicadas en el primer y segundo año de vida
Trastornos generales
Muy frecuentes: irritabilidad, somnolencia y alteración del sueño Frecuentes: llanto
Trastornos del aparato digestivo
Muy frecuentes: diarrea y pérdida del apetito y vómitos (en menores de 1 año)
Frecuentes: vómitos (niños en el segundo año de vida)
Reacciones adicionales comunicadas en niños mayores y adultos
Trastornos generales
Muy frecuentes: malestar general y dolor de cabeza (en escolares de secundaria)
Frecuentes: dolor de cabeza (en escolares de primaria)
Trastornos de los músculos y los huesos
Muy frecuentes: dolor muscular y de las articulaciones
Trastornos digestivos
Muy frecuentes: náusea (adultos)
Efectos adversos que se han obtenido de la experiencia post-comercialización:
Trastornos generales
Frecuentes: mareos, aumento de la temperatura corporal, dolor de cabeza, nauseas, vómitos y desvanecimientos.
Trastornos del sistema inmunológico:
Muy raros: linfadenopatía, anafilaxia, reacciones de hipersensibilidad incluyendo broncoespasmos, edema facial y angioedema.
Trastornos del sistema nervioso:
Muy raras: mareos, convulsiones incluyendo las de tipo febril (sobre todo en niños menores de 1 año), desvanecimientos, disminución y alteración de la sensibilidad, debilidad muscular.
Trastornos oculares:

Muy raros: alteraciones visuales y sensibilidad a la luz.
Trastornos gastrointestinales:
Muy raros: vómitos, náuseas y diarrea
Trastornos de la piel y del tejido subcutáneo:
Muy raros: erupción, urticaria, prurito, púrpura, eritema multiforme y síndrome de Stevens-Johnson
Trastornos de los músculos y de los huesos:
Muy raros: dolor muscular y de las articulaciones
Trastornos del riñón y de las vías urinarias:
Se ha notificado recaída del síndrome nefrótico en asociación con las vacunas conjugadas de meningococo del grupo C.
Si se observa cualquier otra reacción adversa no descrita en este prospecto, consulte a su médico o farmacéutico.
5. CONSERVACIÓN DE MENINVACT Kit
Mantenga MENINVACT Kit fuera del alcance y de la vista de los niños.
Conservar en nevera (entre 2°C y 8°C).. No congelar. Guarde el vial y la jeringa en la caja de cartón para protegerlos de la luz.
Utilizar antes de la fecha de caducidad que figura en el envase.
Este prospecto ha sido aprobado en: Abril 2006
Agencia española de
medicamentos y
productos sanitarios