Mariona Diario 0,15 Mg/0,03 Mg Comprimidos Recubiertos Con Pelicula Efg
Información obsoleta, busque otroam
FICHA TECNICA
1. NOMBRE DEL MEDICAMENTO
Mariona Diario 0,15 mg/0,03 mg, comprimidos recubiertos con película EFG
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
21 comprimidos recubiertos con película de color blanco (comprimidos activos):
Cada comprimido recubierto contiene 0,15 mg de desogestrel y 0,03 mg de etinilestradiol. Excipiente con efecto conocido: lactosa monohidrato 55 mg, aceite de soja (máximo 0,026 mg)
7 comprimidos recubiertos con película de color verde, de placebo (inactivos):
Estos comprimidos no contienen sustancia activa.
Excipiente con efecto conocido: lactosa monohidrato 55 mg
Para consultar la lista completa de excipientes, ver apartado 6.1.
3. FORMA FARMACÉUTICA
Comprimido recubierto con película.
El comprimido activo es un comprimido recubierto de color blanco, redondo de 5,00 mmm de diámetro El comprimido placebo es un comprimido recubierto de color verde, redondo de 5,00 mmm de diámetro
4. DATOS CLÍNICOS
4.1. Indicaciones terapéuticas
Anticoncepción oral.
La decisión de prescribir Mariona Diario debe tener en cuenta los factores de riesgo actuales de cada mujer en particular, concretamente los de tromboembolismo venoso (TEV), y cómo se compara el riesgo de TEV con Mariona Diario con el de otros anticonceptivos hormonales combinados (AHCs) (ver secciones 4.3 y 4.4).
4.2. Posología y forma de administración
Vía de administración: vía oral.
Cómo tomar Mariona Diario
Los comprimidos deben tomarse todos los días aproximadamente a la misma hora, con un poco de líquido si es necesario y en el orden que se indica en el envase blíster. La toma de comprimidos es continua. Se tomará un comprimido diario durante 28 días consecutivos. Cada nuevo envase se empieza al día siguiente de terminar el último comprimido del envase anterior. La hemorragia por deprivación suele dar comienzo 2-3 días después de empezar a tomar los comprimidos placebo (última fila) y es posible que no haya cesado antes de empezar el siguiente envase.
1 de 16
Población pediátrica
No se ha establecido la seguridad y la eficacia de desogestrel en adolescentes menores de 18 años. No hay datos disponibles.
Cómo se debe empezar a tomar Mariona Diario
• Si no se ha usado ningún anticonceptivo hormonal anteriormente (en el mes anterior)
la hemorragia
Los comprimidos se empezarán a tomar el día 1 del ciclo natural de la mujer (es decir, el primer día de menstrual).
• Para sustituir a un anticonceptivo hormonal combinado (anticonceptivo hormonal combinado (AOC), anillo vaginal o parche transdérmico)
La mujer debe empezar a tomar Mariona preferiblemente el día después de tomar el último comprimido activo (el último comprimido que contiene principios activos) de su AOC, pero a más tardar al día siguiente de finalizar el intervalo habitual sin tomar comprimidos o la toma de los comprimidos de placebo de su AOC previo. En caso de uso de un anillo vaginal o parche transdérmico, la mujer debe empezar a tomar Mariona preferiblemente el día de la retirada, o a más tardar cuando se hubiera tenido que volver a aplicar.
• Para sustituir a un método basado exclusivamente en gestágenos (píldora de progestágeno solo, inyección, implante) o un sistema intrauterino de liberación de progestágenos (SIP)
La mujer puede sustituir la píldora de progestágeno sólo por la píldora de progestágeno cualquier día (si se trata de un implante o de un SIP, el mismo día de su retirada; si se trata de un inyectable, el día que corresponda la siguiente inyección), pero en todos estos casos se debe aconsejar que se utilice adicionalmente un método anticonceptivo de barrera durante los primeros siete días de toma de este medicamento.
• Tras un aborto en el primer trimestre
La mujer puede empezar a tomar este medicamento inmediatamente. En tal caso, no es necesario que tome medidas anticonceptivas adicionales.
• Tras el parto o un aborto en el segundo trimestre
Se recomienda a la mujer que empiece a tomar este medicamento tras 21-28 días del parto o del aborto en el segundo trimestre. Si lo hace más tarde, se debe aconsejar que utilice un método de barrera adicional durante los 7 primeros días. No obstante, si la relación sexual ya ha tenido lugar, hay que descartar que se haya producido un embarazo antes del inicio real del uso de AOC, o bien la mujer debe esperar a tener su primer período menstrual.
Para mujeres en periodo de lactancia, ver el apartado 4.6.
Conducta a seguir si se olvida la toma de algún comprimido
El olvido de la toma de los comprimidos placebos (4a y útlima fila) no tiene consecuencias. No obstante, éstos deber ser desechados para evitar prolongar de forma no intencionada la fase de comprimidos placebo. Los siguientes consejos se refieren sólo al olvido de comprimidos activos (filas 1-3)
La protección anticonceptiva no disminuye si la toma de un comprimido se retrasa menos de 12 horas . En tal caso, la mujer debe tomar el comprimido en cuanto se acuerde de ello y seguir tomando los siguientes comprimidos a la hora habitual .
Si la toma de un comprimido se retrasa más de 12 horas, la protección anticonceptiva puede verse reducida. La conducta a seguir en caso de olvido se rige por dos normas básicas:
1. Nunca se debe suspender la toma de comprimidos más de 7 días.
2. Es necesario tomar los comprimidos de forma ininterrumpida durante 7 días para conseguir una supresión adecuada del eje hipotálamo-hipófisis-ovario.
En consecuencia y siguiendo las indicaciones anteriores, en la práctica diaria se puede aconsejar lo siguiente:
• Semana 1
La mujer debe tomar el último comprimido olvidado tan pronto como se acuerde, aunque ello le obligue a tomar dos comprimidos a la vez. A partir de ahí seguirá tomando los comprimidos a su hora habitual. Además, durante los 7 días siguientes debe utilizar un método de barrera, como un preservativo. Si ha mantenido relaciones sexuales en los 7 días previos, debe considerar la posibilidad de haber quedado embarazada. Cuantos más comprimidos haya olvidado y cuánto más cerca esté de la fase de comprimidos placebo, mayor es el riesgo de embarazo .
• Semana 2
2 de 16
MINISTB?K)DE SANIDAD, POLIT1C A SOCIAL E IGUALDAD Ageticaesparicídóe medKarnentos y productos untarlos
La mujer debe tomar el último comprimido olvidado tan pronto como se acuerde, aunque ello le obligue a tomar dos comprimidos a la vez. A partir de ahí seguirá tomando los comprimidos a su hora habitual. Si en los 7 días anteriores al del comprimido olvidado ha tomado los comprimidos correctamente, no necesitará adoptar precauciones anticonceptivas adicionales. Sin embargo, si ha olvidado tomar más de 1 comprimido, debe aconsejarse la adopción de precauciones adicionales durante 7 días.
• Semana 3
El riesgo de reducción de la eficacia es inminente, debido a la cercanía de la fase de 7 días de comprimidos placebo . No obstante, ajustando el programa de toma de comprimidos, aún se puede impedir que disminuya la protección anticonceptiva. Por tanto, si sigue una de las dos opciones siguientes, no necesitará adoptar precauciones anticonceptivas adicionales, siempre que en los 7 días anteriores al primer olvido haya tomado todos los comprimidos correctamente. Si no es así, debe seguir la primera de las dos opciones que se indican a continuación y ha de adoptar precauciones anticonceptivas adicionales en los 7 días siguientes.
1. La mujer debe tomar el último comprimido olvidado tan pronto como se acuerde, aunque ello le obligue a tomar dos comprimidos a la vez. A partir de ahí seguirá tomando los comprimidos a su hora habitual hasta acabar los comprimidos activos. Los 7 comprimidos placebo de la última fila deben ser desechados. El siguiente envase se debe empezar inmediatamente. Es improbable que tenga una hemorragia por deprivación hasta que termine el segundo envase, pero puede presentar manchado o hemorragias por disrupción en los días de toma de comprimidos.
2. Suspender la toma de comprimidos activos del envase actual. Entonces, tomar los comprimidos placebos de la última fila durante 7 días como máximos, incluidos los días en que olvidó los comprimidos, y continuar con el siguiente envase.
Si la mujer olvida tomar varios comprimidos y posteriormente no presenta hemorragia por deprivación en la fase de comprimidos placebo, se debe considerar la posibilidad de embarazo.
Consejos en caso de trastornos gastrointestinales
En caso de trastornos gastrointestinales graves (p. ej.: vómitos o diarrea), puede que la absorción del AOC no sea completa siendo necesario tomar otras medidas anticonceptivas adicionales. Si aparecen vómitos en las 3 - 4 horas siguientes a la toma del comprimido activo, se debe tomar un nuevo comprimido (de reemplazo) lo antes posible. El nuevo comprimido se debería tomar, si fuera posible, dentro de las 12 horas de la toma habitual. Si transcurrieran más de 12 horas, se seguirían los mismos consejos que para el caso en que se olvida la toma de comprimidos, que se recogen en el apartado “Conducta a seguir si se olvida la toma de algún comprimido”. Si la mujer no desea cambiar su pauta normal de toma de comprimidos, tomará el/los comprimido/s extra de otro envase.
Cómo retrasar una hemorragia por deprivación
Para retrasar un período, la mujer debe continuar con otro envase de Mariona sin tomar los comprimidos placebo del envase actual. Puede mantener esta extensión tanto como desee hasta que se terminen los comprimidos activos del segundo envase. Durante la extensión, la mujer puede experimentar hemorragia por disrupción o manchado. Posteriormente, la toma regular de Mariona se reanuda tras la fase de comprimidos placebo.
Para cambiar sus períodos a otro día de la semana al que la mujer está acostumbrada, se le puede aconsejar que acorte la siguiente fase de comprimidos placebo tantos días como desee. Cuanto más corto sea, mayor es el riesgo de que no tenga hemorragia por deprivación, y de que experimente manchado y hemorragia por deprivación durante la toma del envase siguiente (igual que cuando se retrasa un período).
4.3. Contraindicaciones
No se deben utilizar anticonceptivos hormonales combinados (AHC) en presencia de las siguientes condiciones. Si alguna de ellas aparece por primera vez mientras se emplean AHC, la administración del preparado debe ser suspendida inmediatamente.
o Presencia o riesgo de tromboembolismo venoso (TEV).
o Tromboembolismo venoso: TEV actual (con anticoagulantes) o antecedentes del mismo (p. ej., trombosis venosa profunda (TVP) o embolia pulmonar (EP)).
o Predisposición hereditaria o adquirida conocida al tromboembolismo venoso, tal como resistencia a la PCA
3 de 16
(incluyendo el factor V Leiden), deficiencia de antitrombina III, deficiencia de proteína C, deficiencia de proteína S. o Cirugía mayor con inmovilización prolongada (ver sección 4.4).
o Riesgo elevado de tromboembolismo venoso debido a la presencia de varios factores de riesgo (ver sección 4.4). o Presencia o riesgo de tromboembolismo arterial (TEA).
o Tromboembolismo arterial: tromboembolismo arterial actual, antecedentes del mismo (p. ej. infarto de miocardio) o afección prodrómica (p. ej. angina de pecho).
o Enfermedad cerebrovascular: ictus actual, antecedentes de ictus o afección prodrómica (p. ej. accidente isquémico transitorio, AIT).
o Predisposición hereditaria o adquirida conocida al tromboembolismo arterial, tal como hiperhomocisteinemia y anticuerpos antifosfolípidos (anticuerpos anticardiolipina, anticoagulante del lupus).
o Antecedentes de migraña con síntomas neurológicos focales.
o Riesgo elevado de tromboembolismo arterial debido a múltiples factores de riesgo (ver sección 4.4) o a la presencia de un factor de riesgo grave como:
• diabetes mellitus con síntomas vasculares
• hipertensión grave
• dislipoproteinemia intensa
o Pancreatitis o antecedentes de pancreatitis si se asocia a hipertrigliceridemia grave.
o Presencia o antecedentes de enfermedad hepática grave, siempre que los valores de las pruebas de función hepática no se hayan normalizado
o Presencia o antecedentes de tumores hepáticos (benignos o malignos).
o Certeza o sospecha de afecciones malignas de los órganos genitales o de las mamas, si son dependientes de los esteroides sexuales.
o Hiperplasia endometrial. o Hemorragia vaginal no diagnosticada.
o Hipersensibilidad a cualquiera de los principios activos de Mariona Diario o a cualquiera de los excipientes enumerados en el apartado 6.1.
o Este medicamento contiene aceite de soja . No debe utilizarse en caso de alergia al cacahuete o a la soja.
4.4. Advertencias y precauciones especiales de empleo Advertencias
Si alguna de las afecciones o factores de riesgo que se mencionan a continuación está presente, se debe comentar con la mujer la idoneidad de Mariona Diario.
Si alguna de estas afecciones o de estos factores de riesgo se agrava o aparece por primera vez, se debe aconsejar a la mujer que consulte con su médico para determinar si se debe interrumpir el uso de Mariona Diario.
1. Trastornos circulatorios
Riesgo de tromboembolismo venoso (TEV)
4 de 16
MINISTB?K)DE SANIDAD, POLIT1C A SOCIAL E IGUALDAD Ageticaesparicídóe medKarnentos y productos untarlos
5füfi
am
El uso de cualquier anticonceptivo hormonal combinado (AHC) aumenta el riesgo de tromboembolismo venoso (TEV), comparado con la no utilización. Los medicamentos que contienen levonorgestrel, norgestimato o noretisterona se asocian con el riesgo más bajo de TEV. Otros medicamentos como Mariona Diario pueden tener hasta el doble de este nivel de riesgo. La decisión de utilizar cualquier medicamento diferente del que tiene el menor riesgo de TEV se debe tomar solamente después de comentarlo con la mujer para garantizar que comprende el riesgo de TEV con Mariona Diario, cómo afectan sus actuales factores de riesgo a este riesgo y que su riesgo de TEV es mayor durante el primer año de uso. También existen ciertas evidencias de que el riesgo aumenta cuando se reinicia el AHC después de una interrupción del uso de 4 semanas o más.
Entre las mujeres que no utilizan un AHC y que no están embarazadas, aproximadamente 2 de cada 10.000 presentarán un TEV en el plazo de un año. No obstante, el riesgo puede ser mucho mayor en cada mujer en particular, en función de sus factores de riesgo subyacentes (ver a continuación).
Se estima^ que de cada 10.000 mujeres que utilizan un AHC que contiene desogestrel, entre 9 y 12 presentarán TEV en un año, en comparación con unas 6^ mujeres que utilizan un AHC con levonorgestrel.
En ambos casos, el número de TEVs por año es inferior al número esperado en mujeres durante el embarazo o en el período de posparto.
El TEV puede ser mortal en el 1-2% de los casos
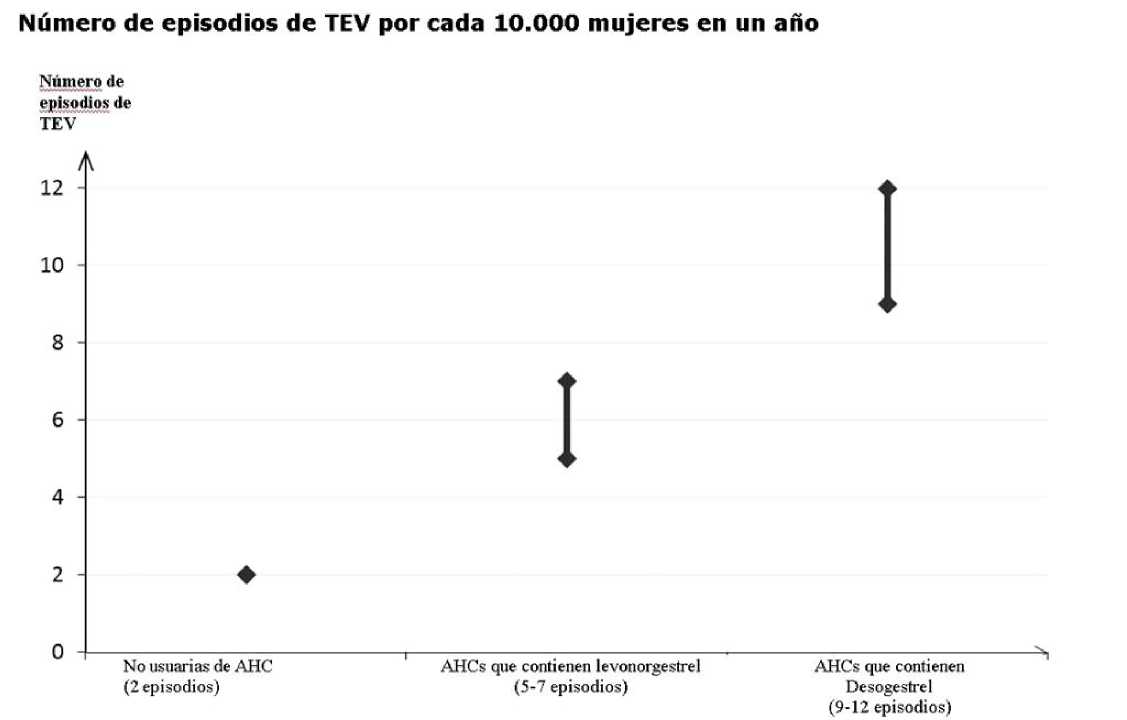
[ii_ Estas incidencias se estimaron a partir de la totalidad de los datos de estudios epidemiológicos, utilizando riesgos relativos para los diferentes productos comparados con los AHC que contienen levonorgestrel.
5 de 16
j2L Punto medio del intervalo 5-7 por cada 10.000 mujeres-año (MA), basado en un riesgo relativo para los AHCs que contienen levonorgestrel frente a la no utilización de aproximadamente 2,3 a 3,6.
De forma extremadamente rara, se han notificado casos de trombosis en otros vasos sanguíneos, p. ej., en venas y arterias hepáticas, mesentéricas, renales o retinianas, en usuarias de AHC.
Factores de riesgo de TEV
El riesgo de complicaciones tromboembólicas venosas en usuarias de AHC puede aumentar sustancialmente en una mujer con factores de riesgo adicionales, en particular si existen varios factores de riesgo (ver tabla).
Mariona Diaro está contraindicado si una mujer tiene varios factores de riesgo que la ponen en una situación de alto riesgo de trombosis venosa (ver sección 4.3). Si una mujer tiene más de un factor de riesgo, es posible que el aumento del riesgo sea mayor que la suma de los factores individuales; en este caso se debe tener en cuenta su riesgo total de TEV. Si se considera que la relación beneficio/riesgo es negativa, no se debe prescribir un AHC (ver sección 4.3).
|
Factor de Riesgo |
Comentario |
|
Obesidad (índice de masa corporal (IMC) superior a 30 kg/m2). |
El riesgo aumenta de forma sustancial con el aumento del IMC. |
|
Especialmente importante en mujeres con factores de riesgo adicionales. | |
|
Inmovilización prolongada, cirugía mayor, cualquier intervención quirúrgica de las piernas o pelvis, neurocirugía o traumatismo importante. Nota: La inmovilización temporal, incluyendo los viajes en avión >4 horas, también puede ser un factor de riesgo de TEV, en especial en mujeres con otros factores de riesgo. |
En estas circunstancias es aconsejable interrumpir el uso del parche/comprimido/anillo (en caso de intervención quirúrgica programada, al menos con cuatro semanas de antelación) y no reanudarlo hasta dos semanas después de que se recupere completamente la movilidad. Se debe utilizar otro método anticonceptivo para evitar un embarazo involuntario. |
|
Se debe considerar un tratamiento antitrombótico si no se ha interrumpido con antelación la toma de Mariona Diario. | |
|
Antecedentes familiares positivos (algún caso de tromboembolismo venoso en un hermano o en un progenitor, especialmente a una edad relativamente temprana, p. ej. antes de los 50 años). |
Si se sospecha que existe una predisposición hereditaria, la mujer debe ser derivada a un especialista antes de tomar la decisión de usar un AHC. |
|
Otras enfermedades asociadas al TEV. |
Cáncer, lupus eritematoso sistémico, síndrome urémico hemolítico, enfermedad intestinal, inflamatoria crónica (enfermedad de Crohn o colitis ulcerosa) y anemia de células falciformes. |
|
Aumento de la edad. |
En especial por encima de los 35 años. |
6 de 16
MINISTB?K)DE SANIDAD, POLIT1C A SOCIAL E IGUALDAD Ageticaesparicídóe medcamenios y productos sanearos
No hay consenso sobre el posible papel de las venas varicosas y la tromboflebitis superficial en la aparición o progresión de la trombosis venosa.
Es preciso tener en cuenta el aumento del riesgo de tromboembolismo en el embarazo, y en particular en el período de 6 semanas del puerperio (para obtener información sobre “Embarazo y lactancia”, ver sección 4.6).
Síntomas de TEV (trombosis venosa profunda y embolia pulmonar)
En el caso de que se produzcan síntomas, se debe aconsejar a la mujer que busque asistencia médica urgente y que informe al profesional sanitario de que está tomando un AHC.
Los síntomas de trombosis venosa profunda (TVP) pueden incluir:
- Hinchazón unilateral de la pierna y/o pie o a lo largo de una vena de la pierna.
- Dolor o sensibilidad en la pierna, que tal vez se advierta sólo al ponerse de pie o al caminar.
- Aumento de la temperatura en la pierna afectada; enrojecimiento o decoloración de la piel de la pierna.
Los síntomas de embolia pulmonar (EP) pueden incluir:
- Aparición repentina de falta de aliento o respiración rápida injustificadas.
- Tos repentina que puede estar asociada a hemoptisis.
- Dolor torácico agudo.
- Aturdimiento intenso o mareo.
- Latidos cardíacos acelerados o irregulares.
Algunos de estos síntomas (p. ej. “falta de aliento”, “tos”) son inespecíficos y se pueden confundir con acontecimientos más frecuentes o menos graves (p. ej. infecciones del tracto respiratorio).
Otros signos de oclusión vascular pueden incluir: dolor repentino, hinchazón y ligera coloración azul de una extremidad.
Si la oclusión se produce en el ojo, los síntomas pueden variar desde visión borrosa indolora, que puede evolucionar a pérdida de la visión. A veces la pérdida de la visión se puede producir casi de inmediato.
Riesgo de tromboembolismo arterial (TEA)
Estudios epidemiológicos han asociado el uso de los AHCs con un aumento del riesgo de tromboembolismo arterial (infarto de miocardio) o de accidente cerebrovascular (p. ej. accidente isquémico transitorio, ictus). Los episodios tromboembólicos arteriales pueden ser mortales.
Factores de riesgo de TEA
El riesgo de que se produzcan complicaciones tromboembólicas arteriales o un accidente cerebrovascular en las usuarias de AHC aumenta en mujeres con factores de riesgo (ver tabla). Mariona Diario está contraindicado si una mujer presenta varios factores de riesgo de TEA o uno grave que la ponen en una situación de alto riesgo de trombosis arterial (ver sección 4.3). Si una mujer tiene más de un factor de riesgo, es posible que el aumento del riesgo sea mayor que la suma de los factores individuales; en este caso se debe tener en cuenta su riesgo total. Si se considera que la relación beneficio/riesgo es negativa, no se debe prescribir un AHC (ver sección 4.3).
Tabla: Factores de riesgo TEA
|
Factor de Riesgo |
Comentario |
|
Aumento de la edad |
En especial por encima de los 35 años. |
|
Tabaquismo |
Se debe aconsejar a las mujeres que no |
|
fumen si desean utilizar un AHC. Se | |
|
debe aconsejar encarecidamente a las | |
|
mujeres de más de 35 años que |
7 de 16
|
continúan fumando que utilicen un método anticonceptivo diferente. | |
|
Hipertensión arterial | |
|
Obesidad (índice de masa corporal superior a 30 kg/m2). |
El riesgo aumenta de forma sustancial con el aumento del IMC. Especialmente importante en mujeres con factores de riesgo adicionales. |
|
Antecedentes familiares positivos (algún caso de tromboembolismo arterial en un hermano o en un progenitor, especialmente a una edad relativamente temprana, p. ej. menos de 50 años). |
Si se sospecha que existe una predisposición hereditaria, la mujer debe ser derivada a un especialista antes de tomar la decisión de usar un AHC. |
|
Migraña |
Un aumento de la frecuencia o la intensidad de las migrañas durante el uso de AHC (que puede ser prodrómico de un acontecimiento cerebrovascular) puede motivar su interrupción inmediata. |
|
Otras enfermedades asociadas a acontecimientos vasculares adversos |
Diabetes mellitus, hiperhomocisteinemia, valvulopatía y fibrilación auricular, dislipoproteinemia y lupus eritematoso sistémico. |
Síntomas de TEA
En el caso de que se produzcan síntomas, se debe aconsejar a la mujer que busque asistencia médica urgente y que informe al profesional sanitario de que está tomando un AHC.
Los síntomas de un accidente cerebrovascular pueden incluir:
- Entumecimiento o debilidad repentinos de la cara, brazo o pierna, especialmente en un lado del cuerpo.
- Dificultad repentina para caminar, mareo, pérdida del equilibrio o de la coordinación.
- Confusión repentina, dificultad para hablar o para comprender.
- Dificultad repentina de visión en un ojo o en ambos.
- Cefalea repentina, intensa o prolongada sin causa conocida.
- Pérdida del conocimiento o desmayo, con o sin convulsiones.
Los síntomas temporales sugieren que el episodio es un accidente isquémico transitorio (AIT).
Los síntomas de un infarto de miocardio (IM) pueden incluir:
- Dolor, molestias, presión, pesadez, sensación de opresión o plenitud en el toráx, brazo o debajo del esternón.
- Malestar que irradia a la espalda, la mandíbula, la garganta, el brazo o el estómago.
- Sensación de plenitud, indigestión o ahogo.
- Sudoración, náuseas, vómitos o mareo.
- Debilidad extrema, ansiedad o falta de aliento.
- Latidos cardíacos acelerados o irregulares.
8 de 16
Al considerar los riesgos/beneficios, el médico deberá tener en cuenta que el tratamiento adecuado de una condición puede reducir el riesgo asociado de trombosis y que el riesgo asociado con el embarazo es superior que el riesgo asociado con la utilización de anticonceptivos orales combinados.
2. Tumores
• En algunos estudios epidemiológicos se ha descrito un aumento del riesgo de cáncer cervical en usuarias de AOC infectadas con el virus del papiloma humano (VPH) durante largos periodos de tiempo. Sin embargo, sigue existiendo controversia acerca de hasta qué punto este hallazgo puede ser atribuido a factores de confusión (por ejemplo, diferencias en el número de parejas sexuales o en el uso de anticonceptivos de barrera).
• En un metaanálisis de 54 estudios epidemiológicos se observó que existe un ligero aumento del riesgo relativo (RR = 1,24) de que se diagnostique cáncer de mama en mujeres que están tomando AOC. Este aumento del riesgo desaparece gradualmente en los 10 años siguientes a la suspensión de los AOC. Dado que el cáncer de mama es raro en mujeres menores de 40 años, el aumento de diagnósticos de cáncer de mama en usuarias, que toman AOC en el momento actual o que los han tomado recientemente, es pequeño en relación con el riesgo total de cáncer de mama. Estos estudios no aportan evidencias sobre las causas. El patrón observado de aumento del riesgo puede deberse a que el diagnóstico de cáncer de mama es más precoz en usuarias de AOC, a los efectos biológicos de los AOC o a una combinación de ambos factores. Los cánceres de mama diagnosticados en mujeres que han utilizado un AOC en alguna ocasión suelen estar menos avanzados desde el punto de vista clínico que los diagnosticados en quienes nunca los han tomado.
• En raros casos, se han comunicado tumores hepáticos benignos, y aún más raramente malignos, en usuarias de AOC. En casos aislados, estos tumores han dado lugar a hemorragias intraabdominales con riesgo vital. Debe considerarse la posibilidad de que exista un tumor hepático en el diagnóstico diferencial de mujeres que toman AOC y que presentan dolor intenso en abdomen superior, aumento de tamaño del hígado o signos de hemorragia intraabdominal.
3. Otras afecciones
• Las mujeres con hipertrigliceridemia o con antecedentes familiares de dicho trastorno pueden tener mayor riesgo de pancreatitis cuando usan AOC.
• Aunque se ha comunicado la aparición de pequeños aumentos de la tensión arterial en mujeres que toman AOC, son raros los casos con relevancia clínica. No se ha establecido una relación entre la utilización de AOC y la hipertensión clínica. No obstante, durante el uso de un AOC, en caso de hipertensión preexistente, debe retirarse el AOC y tratar la hipertensión. Cuando se considere apropiado, puede reanudarse la toma del AOC si gracias al tratamiento antihipertensivo se alcanzan valores normales de tensión arterial.
• Aunque no se ha demostrado de forma concluyente que exista una asociación, se ha informado de que las siguientes afecciones se producen o empeoran con el embarazo y con el uso de AOC: ictericia y/o prurito relacionados con colestasis; cálculos biliares; porfiria; lupus eritematoso sistémico; síndrome hemolítico-urémico; corea de Sydenham; herpes gestacional; pérdida de la audición relacionada con otosclerosis; angiodema (hereditario).
• Los trastornos agudos o crónicos de la función hepática pueden obligar a suspender el uso de AOC hasta que los marcadores de función hepática recuperen valores normales. La recurrencia de una ictericia colestásica y/o de un prurito relacionado con colestasis que se hubieran presentado previamente durante el embarazo o durante un uso anterior de esteroides sexuales obliga a suspender los AOC.
• Aunque los AOC pueden tener un efecto sobre la resistencia periférica a la insulina y sobre la tolerancia a la glucosa, no existen evidencias que hagan necesario alterar el régimen terapéutico en diabéticas que tomen AOC. No obstante, las mujeres diabéticas deben ser observadas cuidadosamente, en especial durante la etapa inicial del uso de AOC.
• Durante la utilización de AOC, se han asociado la enfermedad de Crohn y la colitis ulcerosa.
• Puede producirse cloasma ocasionalmente, sobre todo en mujeres con antecedentes de cloasma gravídico. Las mujeres con tendencia al cloasma deben evitar la exposición al sol o a los rayos ultravioleta mientras tomen AOC.
• Los comprimidos de color blanco de este medicamento contienen 55 mg de lactosa por comprimido, y los comprimidos verdes contienen 55 mg. Las pacientes con intolerancia hereditaria a la galactosa, insuficiencia de lactasa de Lapp
9 de 16
MINISTB?K)DE SANIDAD, POLIT1C A SOCIAL E IGUALDAD Ageticaesparicídóe medKarnentos y productos untarlos
(insuficiencia observada en ciertas poblaciones de Laponia) o malabsorción de la glucosa o galactosa no deben tomar este medicamento.
Al elegir un método anticonceptivo, deberá tenerse en cuenta la información arriba indicada.
Exploración y consultas médicas
Antes de iniciar o reanudar el tratamiento con Mariona Diario, se debe realizar una anamnesis completa (incluidos los antecedentes familiares) y descartarse un posible embarazo. Se debe medir la tensión arterial y realizar una exploración física, guiada por las contraindicaciones (ver sección 4.3) y por las advertencias (ver sección 4.4). Es importante dirigir la atención de la mujer hacia la información sobre la trombosis venosa y arterial, incluido el riesgo de Mariona Diario en comparación con otros AHCs, los síntomas de TEV y TEA, los factores de riesgo conocidos y qué debe hacer en caso de una sospecha de trombosis.
También se debe indicar a la mujer que lea cuidadosamente el prospecto y siga las instrucciones que allí descritas La frecuencia y la naturaleza de las exploraciones deben basarse en las directrices clínicas establecidas y se adaptarán a cada mujer en particular.
Debe advertirse a las mujeres que los anticonceptivos hormonales no protegen frente a la infección por VIH (SIDA) ni frente a otras enfermedades de transmisión sexual.
Disminución de la eficacia
La eficacia de los AOC puede disminuir si la mujer olvida tomar los comprimidos (ver sección 4.2.3), o en caso de trastornos gastrointestinales (ver sección 4.2.4) o empleo de medicación concomitante (ver sección 4.5.1).
No deberán utilizarse preparaciones que contiene la Hierba de San Juan (Hypericumperforatum) durante la toma de Mariona Diario debido al riesgo del descenso de las concentraciones de plasma y la disminución de los efectos clínicos de Mariona Diario (ver sección 4.5 Interacciones).
Reducción del control de los ciclos
Todos los AOC pueden dar lugar a hemorragias irregulares (manchado o hemorragia por disrupción), especialmente durante los primeros meses de uso. Por consiguiente, la evaluación de cualquier hemorragia irregular sólo será significativa tras un intervalo de adaptación de unos tres ciclos.
Si las irregularidades hemorrágicas persisten o se producen tras ciclos que previamente eran regulares, habrá que tener en cuenta posibles causas no hormonales y está indicado tomar las medidas diagnósticas adecuadas para excluir procesos malignos o embarazos. Entre ellas se encontraría el legrado.
Es posible que en algunas mujeres no se produzca hemorragia por privación durante la semana de comprimidos placebo. Si ha tomado el AOC siguiendo las instrucciones que se describen en la sección 4.2, es improbable que la mujer esté embarazada. Sin embargo, si no ha tomado el AOC siguiendo estas instrucciones antes de la primera falta o si se produce una segunda falta hay que descartar un embarazo antes de seguir tomando el AOC.
Advertencias sobre excipientes
Este medicamento contiene lactosa. Los pacientes con intolerancia hereditaria a galactosa, insuficiencia de lactasa de Lapp (insuficiencia observada en ciertas poblaciones de Laponia) o malabsorción de glucosa o galactosa no deben tomar este medicamento.
4.5. Interacción con otros medicamentos y otras formas de interacción
Las interacciones entre los anticonceptivos orales y otros medicamentos pueden conducir a la aparición de hemorragia por disrupción o fallo de la anticoncepción. Las siguientes interacciones han sido notificadas y obtenidas de la literatura científica:
Metabolismo hepático: Pueden ocurrir interacciones con fármacos inductores de las enzimas hepáticas, lo que puede provocar
10 de 16
filial
an
un aumento del aclaramiento de las hormonas sexuales (p ej. hidantoína, barbitúricos, primidona, carbamazepina, rifampicina, bosentan, rifabutina y también posiblemente con oxcarbazepina, modafinilo, topiramato, felbamato, ritonavir , griseofulvina y productos que contienen la planta medicinal Hierba de San Juan). Asimismo, los inhibidores de la proteasa con un potencial de inducción (p.ej. ritonavir y nelfinavir) y los inhibidores no nucleosídicos de la transcriptasa inversa (p.ej. nevirapina y efavirenz) pueden afectar el metabolismo hepático. Habitualmente se observa una inducción enzimática máxima en unas 2-3 semanas, pero puede mantenerse al menos hasta 4 semanas después de la suspensión del tratamiento farmacológico.
También se han notificado fallos de los anticonceptivos con antibióticos como las penicilinas y tetraciclinas. No se ha dilucidado el mecanismo de este efecto.
Las mujeres tratadas con cualquiera de estos medicamentos deben utilizar un método de barrera además del AOC mientras o elegir otro método anticonceptivo. Con los medicamentos inductores de las enzimas microsomales, debe utilizarse el método de barrera durante el uso concomitante de estos medicamentos y hasta 28 días después de interrumpirlo. En mujeres sometidas a tratamiento de larga duración con principios activos inductores de las enzimas microsomales se recomienda usar otro método fiable de anticoncepción. Las mujeres tratadas con antibióticos (aparte de rifampicina y griseofulvina, que también actúan como medicamentos inductores de las enzimas microsomales) deben utilizar un método de barrera hasta 7 días después de suspender el tratamiento. Si la administración concomitante del medicamento dura más que los comprimidos activos del envase de AOC, los comprimidos placebo deben ser desechados y se debe iniciar inmediatamente el siguiente envase de AOC.
Los anticonceptivos orales pueden influir en el metabolismo de otros principios activos. En consecuencia, los niveles plasmáticos o tisulares pueden aumentar (ej. ciclosporina) o disminuir (ej. lamotrigina).
Nota: La información para recetar medicamentos concomitantes deberá consultarse para identificar las posibles interacciones.
El uso de anticonceptivos esteroidicos puede afectar a los resultados de ciertas pruebas de laboratorio, como los parámetros bioquímicos de función hepática, tiroidea, suprarrenal y renal, los niveles plasmáticos de proteínas (transportadoras), p. ej. la globulina transportadora de corticosteroides y las fracciones de lípidos/lipoproteínas, los parámetros del metabolismo de los hidratos de carbono y los parámetros de la coagulación y la fibrinólisis. Por lo general, los cambios permanecen dentro de los límites normales.
4.6. Fertilidad, embarazo y lactancia
Embarazo
Mariona Diario está contraindicado durante el embarazo. Si se produjera un embarazo durante el uso de Mariona, debe suspenderse su administración inmediatamente. No obstante, estudios epidemiológicos extensos no han revelado ni un aumento del riesgo de defectos congénitos en niños nacidos de madres usuarias de AOC antes del embarazo, ni un efecto teratogénico cuando los AOC fueron tomados de forma inadvertida durante un embarazo.
Se debe tener en cuenta el aumento de riesgo de TEV durante el periodo de posparto cuando se reinicia la administración con Mariona (ver sección 4.2 y 4.4)
Lactancia
La lactancia puede resultar afectada por los AOC, dado que éstos pueden reducir la cantidad de leche y alterar su composición. Por consiguiente, en general no debe recomendarse el empleo de AOC hasta que la madre haya cesado completamente la lactancia de su hijo. Durante el uso de AOC pueden eliminarse por la leche pequeñas cantidades de esteroides anticonceptivos y/o de sus metabolitos, pero no hay pruebas que estas cantidades puedan afectar al lactante.
4.7. Efectos sobre la capacidad para conducir y utilizar máquinas
Mariona no afecta a la capacidad de conducir y utilizar máquinas.
11 de 16
4.8. Reacciones adversas
Para los efectos adversos graves en usuarias de AHC ver el apartado 4.4.
Se han registrado las siguientes reacciones adversas durante el uso de Desogestrel/Etinilestradiol:
|
Sistema orgánico |
Frecuentes (>1/100 a <1/10) |
Poco frecuentes (>1/1.000 a <1/100) |
Raras (>1/10.000 a <1/1.000) |
|
Trastornos del sistema inmunológico |
Hipersensibilidad | ||
|
Trastornos del metabolismo y nutricionales |
Retención de líquidos | ||
|
Trastornos psiquiátricos |
Ánimo depresivo Ánimo alterado |
Disminución de la libido |
Aumento de la libido |
|
Trastornos del sistema nervioso |
Dolor de cabeza |
Migrañas | |
|
Trastornos oculares |
Intolerancia a las lente de contacto | ||
|
Trastornos vasculares |
Hipertensión |
Tromboembolismo venoso o arterial | |
|
Trastornos gastrointestinales |
Náuseas Dolor abdominal |
Vómitos Diarrea | |
|
Trastornos de la piel y del tejido subcutáneo |
Erupción Urticaria |
Eritema nudoso, eritema multiforme | |
|
Trastornos del aparato reproductor y de la mama |
Dolor mamario Mastalgia |
Aumento del tamaño de las mamas |
Secreción vaginal Secreción mamaria |
|
Trastornos generales y alteraciones en el lugar de administración |
Aumento de peso |
Disminución de peso |
Descripción de reacciones adversas seleccionadas
Se ha observado un aumento del riesgo de episodios trombóticos y tromboembólicos arteriales y venosos, entre ellos infarto de miocardio, accidente cerebrovascular, accidentes isquémicos transitorios, trombosis venosa y embolia pulmonar, en mujeres que utilizan AHCs, que se comentan con más detalle en la sección 4.4.
Se han registrado los siguientes efectos adversos graves en mujeres usuarias de AOC, que se discuten en la sección 4.4:
- Hipertensión;
- Tumores hepáticos;
- Aparición o deterioro de cuadros en los que la asociación con un AOC no resulta concluyente: Enfermedad de Crohn, colitis ulcerosa, epilepsia, mioma uterino, porfiria, lupus eritematoso sistémico, herpes gestacional, corea de Sydenham, síndrome
12 de 16
ÍTTÍ
hemolítico urémico; ictericia colestática;
- Cloasma;
- Los trastornos agudos o crónicos de la función hepática pueden necesitar el cese de la toma de AOC hasta que los marcadores de la función hepática retornen a la normalidad;
- En mujeres con angioedema hereditario, los estrógenos exógenos pueden inducir o exacerbar los síntomas del angioedema
La frecuencia del diagnóstico de cáncer de mama entre usuarias de AOC está aumentada de forma muy ligera. Dado que el cáncer de mama es raro en mujeres menores de 40 años, este aumento es pequeño con relación al riesgo global de cáncer de mama. Se desconoce la causalidad relacionada con el uso de AOC. Para más información ver las secciones 4.3. y 4.4.
Notificación de sospechas de reacciones adversas
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del Sistema Español de Farmacovigilancia de Medicamentos de Uso Humano: www.notificaRAM.es
4.9. Sobredosis
Hasta la fecha no ha habido ningún caso de sobredosis grave con este medicamento. Según la experiencia general con anticonceptivos orales combinados, los síntomas que posiblemente pueden producirse en este caso son: náuseas, vómitos y, en chicas jóvenes, sangrado vaginal leve. No existe antídoto y el tratamiento debe ser sintomático.
5. PROPIEDADES FARMACOLÓGICAS
5.1. Propiedades farmacodinámicas
Grupo farmacoterapéutico: Progestágenos y estrógenos, preparados de dosis fijas Código ATC: G03A A09.
El efecto anticonceptivo de los anticonceptivos orales combinados se basa en la interacción de diversos factores, de los cuales el más importante es la inhibición de la ovulación y los cambios en la secreción cervical.
Mariona es un anticonceptivo oral combinado con etinilestradiol y el progestágeno desogestrel.
Etinilestradiol es un estrógeno sintético muy conocido.
Desogestrel es un progestágeno sintético.
Tras la administración por vía oral, posee una fuerte actividad inhibidora de la ovulación.
En el mayor ensayo clínico multicéntrico (n=23 258 ciclos), el Índice de Pearl no corregido se estima en un 0,1 (95% intervalo de confianza 0,0-0,3). Asimismo, 4,5% de las mujeres manifestaron ausencia de sangrado de retirada y un 9,2% manifestaron la aparición de sangrado irregular tras 6 ciclos de tratamiento.
Población pediátrica
No existen datos clínicos sobre la seguridad y eficacia en adolescentes menores de 18 años.
5.2. Propiedades farmacocinéticas
Desogestrel
Absorción
La administración oral de desogestrel se absorbe completamente y se convierte con rapidez en etonogestrel. Las
13 de 16
concentraciones séricas máximas de 2 ng/ml se alcanzan 1,5 horas después de una sola toma. La biodisponibilidad es de 62-81 %.
Distribución
Etonogestrel se une a la albúmina sérica y a la globulina fijadora de esteroides sexuales (SHBG). De la concentración sérica total del medicamento solo está presente entre el 2-4% como esteroide libre. El 40-70% está específicamente unida a SHBG.
El incremento inducido por etinilestradiol en SHBG influye en la distribución de las proteínas séricas, causando un aumento de la fracción unida a SHBG y una disminución de la fracción unida a albúmina. El volumen de distribución aparente del desogestrel es de 1,5 l/kg.
Metabolismo
Etonogestrel se metaboliza por completo mediante las vías conocidas del metabolismo de esteroides . La velocidad de depuración metabólica a partir del suero es de aproximadamente 2 ml/min/kg. No se encontró ninguna interacción con el etinilestradiol que se administra concomitantemente.
Eliminación
Los niveles séricos de etonogestrel disminuyen en dos fases. La fase de eliminación final se caracteriza por una vida intermedia de aproximadamente 30 horas. El desogestrel y sus metabolitos se excretan en una relación urinaria/biliar de 6:4.
Condiciones de estado estacionario
La farmacocinética del etonogestrel depende de los niveles de SHBG, que se triplican por el etinilestradiol. Después de una toma diaria, las concentraciones séricas del etonogestrel aumentan de dos a tres veces, alcanzado las condiciones de estado estacionario durante la segunda mitad del ciclo de tratamiento.
Etinilestradiol
Absorción
El etinilestradiol se absorbe rápidamente y por completo después de la administración por vía oral. . Las concentraciones séricas máximas de aproximadamente 80 pg/ml se alcanzan dentro de las siguientes 1-2 horas . La biodisponibilidad absoluta, que es resultado de la conjugación presistémica y el metabolismo de primer paso, es aproximadamente de 60% .
Distribución
Etinilestradiol se une en un gran porcentaje a la albúmina sérica (aproximadamente 98,5%), aunque de manera inespecífica, e induce un aumento de las concentraciones séricas de SHBG . Se determinó un volumen aparente de distribución cercano a 5 l/kg.
Metabolismo
El e tinilestradiol es sujeto a conjugación presistémica en la mucosa del intestino grueso e hígado. Se metaboliza principalmente mediante hidroxilación aromática, y se forma una amplia variedad de metabolitos hidroxilados y metilados, los cuales están presentes como metabolitos libres y como conjugados con glucurónidos y sulfato. La velocidad de depuración metabólica es cercana a 5 ml/min/kg.
Eliminación
Los niveles séricos de etinilestradiol disminuyen en dos fases; la fase de eliminación terminal se caracteriza por una vida media de aproximadamente 24 horas. La porción del fármaco sin cambios no se excreta; los metabolitos del etinilestradiol se excretan en una relación urinaria/biliar de 4: 6. La vida media de excreción de los metabolitos es de alrededor de 1 día.
Condiciones de estado estacionario
Las concentraciones de estado estacionario se alcanzan después de 3 a 4 días cuando los niveles séricos del fármaco están 30 a 40% superiores, en comparación con una sola dosis.
5.3. Datos preclínicos sobre seguridad
Los datos no clínicos no revelan un riesgo especial para los humanos según los estudios convencionales sobre la seguridad, la
14 de 16
H*a
ÍTTÍ
farmacología, la toxicidad de dosis repetidas, la genotoxicidad, el potencial carcinogénico, la toxicidad para la reproducción y el desarrollo. No obstante, debe tenerse en cuenta que los esteroides sexuales pueden estimular los tejidos y la aparición de tumores dependientes de las hormonas.
6 . DATOS FARMACÉUTICOS 6.1. Lista de excipientes
Comprimidos activos (blancos):
• Núcleo:
Lactosa monohidrato Almidón de maíz Povidona K-30 (E1201) d-alfa-tocoferol (E307)
Aceite de soja
Sílice coloidal hidratada (E551) Sílice coloidal anhidra (E551)
Ácido esteárico (E570)
• Recubrimiento:
Hipromelosa 2910 (E464)
Triacetina (E1518)
Polisorbato
Dióxido de titanio (E171) Comprimidos placebo (verdes):
• Núcleo:
Lactosa monohidrato Almidón de maíz Povidona K-30 (E1201)
Sílice coloidal anhidra (E551) Estearato de magnesio (E572)
• Recubrimiento:
Hipromelosa 2910 (E464)
Triacetina (E1518)
Polisorbato
Dióxido de titanio (E171)
Laca aluminio FD & C Blue 2 (E132) Óxido de hierro amarillo (E172)
6.2. Incompatibilidades
No procede
6.3. Periodo de validez
2 años
15 de 16
6.4. Precauciones especiales de conservación
No conservar a una temperatura superior a 30°C. Conservar en el envase original para protegerlo de la luz.
6.5. Naturaleza y contenido del envase
Blísteres de hoja de aluminio de presión y película de PVC/PVCD de color claro ligeramente opaco.
Tamaños del envase:
1 x 28 comprimidos recubiertos con película (21 comprimidos activos y 7 comprimidos placebo)
3 x 28 comprimidos recubiertos con película (21 comprimidos activos y 7 comprimidos placebo)
6 x 28 comprimidos recubiertos con película (21 comprimidos activos y 7 comprimidos placebo)
Puede que solamente estén comercializados algunos tamaños de envases
6.6. Precauciones especiales de conservación
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Laboratorios León Farma, S.A.
Polígono Industrial Navatejera;
C/La Vallina s/n;
24008-Navatejera, León España
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
9. FECHA DE LA PRIMERA AUTORIZACIÓN/ RENOVACIÓN DE LA AUTORIZACIÓN
Marzo 2015
10. FECHA DE LA REVISIÓN DEL TEXTO
Junio 2014
16 de 16