Limifen 0,5 Mg/Ml Solucion Inyectable
FICHA TÉCNICA
1. NOMBRE DEL MEDICAMENTO
LIMIFEN 0,5 mg/ml solución inyectable
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada mililitro contiene una cantidad de clorhidrato de alfentanilo equivalente a 0,5 mg de alfentanilo. LIMIFEN (alfentanilo) se suministra en ampollas de 2 ml y 10 ml.
3. FORMA FARMACÉUTICA
LIMIFEN es una solución estéril acuosa, isotónica, sin conservantes, para uso intravenoso (I.V.).
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
LIMIFEN está indicado para su utilización en adultos como:
• agente inductor de la anestesia
• analgésico opioide en anestesia general así como adyuvante en anestesia regional y en intervenciones de corta duración (inyecciones en bolo) o de larga duración (en bolo suplementado con incrementos o por infusión).
Debido a su rápido inicio de acción y a su corta duración, LIMIFEN es particularmente adecuado como analgésico opiáceo para intervenciones cortas y cirugía ambulatoria, pero también como un suplemento analgésico para intervenciones de duración media y larga, dado que los períodos de estímulos muy dolorosos pueden superarse fácilmente con pequeños incrementos de LIMIFEN o adaptando la velocidad de la infusión.
LIMIFEN está indicado para uso en neonatos, lactantes y niños como:
• opioide en asociación con un hipnótico para inducir anestesia,
• como analgésico opioide en asociación con anestesia general y para intervenciones de corta y larga duración.
4.2 Posología y forma de administración
LIMIFEN debe usarse como inyecciones en bolo (en intervenciones de corta duración) o en bolos suplementarios o por perfusión continua (en intervenciones de larga duración)
La dosis de LIMIFEN debe individualizarse según la edad, peso corporal, estado físico, estado patológico subyacente, utilización de otros fármacos y tipo de intervención quirúrgica y de anestesia.
La dosis inicial deberá reducirse en pacientes geriátricos y en pacientes debilitados.
Adultos
Para evitar bradicardia, se recomienda administrar una pequeña dosis intravenosa de un fármaco anticolinérgico, justo antes de la inducción. Puede administrarse droperidol para prevenir las náuseas y los vómitos.
1. Utilización en intervenciones cortas y pacientes ambulatorios
Las dosis pequeñas de LIMIFEN son más útiles en intervenciones quirúrgicas menores y cortas, pero dolorosas, y en pacientes ambulatorios, siempre que se tenga disponible un buen equipo de monitorización. Una dosis intravenosa en bolo de 7 - 15 microgramos/kg (1 - 2 ml/70 kg) será suficiente para intervenciones que duren menos de 10 minutos. Si la duración de la intervención se
¡m
alarga más de 10 minutos, se administrarán incrementos adicionales de 7 - 15 microgramos/kg (1 -2 ml/70 kg) cada 10-15 minutos o según sea necesario.
En la mayoría de los casos deberá mantenerse la respiración espontánea con una dosis de 7 microgramos/kg (1 ml/70 kg) o inferior, inyectada lentamente; con esta técnica se recomiendan incrementos de 3,5 microgramos/kg (0,5 ml/70 kg).
Se recomienda no administrar droperidol o benzodiazepinas a pacientes ambulatorios dado que estos fármacos pueden prolongar el periodo de recuperación. En pacientes ambulatorios, la técnica preferible consiste en utilizar un fármaco anticolinérgico, un hipnótico de inducción de acción corta, LIMIFEN y N2O/O2.
Cuando se producen náuseas post-operatorias, éstas son de duración relativamente corta y fácilmente controlables con las medidas habituales.
2. Para intervenciones de duración media
La dosis intravenosa inicial en bolo debe adaptarse a la duración esperada de la intervención quirúrgica según se indica:
|
Duración de la |
Dosis IV de LIMIFEN en bolo | |
|
intervención(min.) |
microgramos/kg |
ml/70 kg |
|
10-30 |
20-40 |
3-6 |
|
30-60 |
40-80 |
6-12 |
|
>60 |
80-150 |
12-20 |
Cuando la intervención quirúrgica sea más prolongada o cruenta, la analgesia puede mantenerse por medio de:
- o bien incrementos de 15 microgramos/kg (2 ml/70 kg) de LIMIFEN cuando sea preciso (para evitar la depresión respiratoria post-operatoria no deberá administrarse LIMIFEN durante los últimos 10 minutos de intervención quirúrgica);
- o bien una infusión de LIMIFEN a un ritmo de 1 microgramos/kg/min (0,14 ml/70 kg/min) hasta 5 - 10 minutos antes de la finalización de la intervención.
Los períodos de estímulos muy dolorosos pueden superarse fácilmente por medio de pequeñas dosis adicionales o bien aumentando la velocidad de infusión.
Cuando se utiliza LIMIFEN sin N2O/O2 o sin otro anestésico inhalado, se precisa una dosis de mantenimiento de LIMIFEN más alta.
3. Para intervenciones quirúrgicas más largas
LIMIFEN puede utilizarse como el componente analgésico de la anestesia durante intervenciones quirúrgicas de larga duración, especialmente cuando se precisa una extubación rápida. Administrando una dosis intravenosa inicial adaptada de forma individual y ajustando el índice de infusión a la gravedad del estímulo quirúrgico y las reacciones de los pacientes, se mantendrá una analgesia óptima y una funcionalidad estable del sistema nervioso autónomo.
Población pediátrica
Debe haber un equipo de ventilación asistida disponible para el uso en niños de cualquier edad, incluso para intervenciones de corta duración en niños con respiración espontanea.
Los datos en niños de 1 mes a un año de edad son limitados (ver sección 5.2).
Neonatos (0-27 días): La farmacocinética es muy variable en neonatos, particularmente en los nacidos prematuramente. El aclaramiento y la unión a proteínas son más bajos y puede ser necesaria una dosis menor de alfentalino. Los neonatos deben ser estrechamente monitorizados y la dosis de alfentanilo se debe ajustar de acuerdo a la respuesta.
Lactantes y niños de 28 días a 23 meses de edad: El aclaramiento puede ser mayor en comparación con los adultos. Puede ser necesario aumentar la velocidad de perfusión para mantener la analgesia.
¡m
Niños de 2 a 11 años de edad: El aclaramiento podría ser ligeramente superior y puede ser necesario un aumento de la velocidad de perfusión.
Adolescentes: La farmacocinética de alfentanilo en adolescentes es similar a la de adultos y no se requieren recomendaciones específicas de dosificación.
Recomendaciones de dosificación para pacientes pediátricos
La amplia variabilidad de respuesta a alfentanilo dificulta proporcionar recomendaciones de dosificación para los niños de menor edad. Para niños mayores se considera apropiado una dosis en bolo de 10 a 20 pg/kg de alfentanilo para inducir anestesia (por ejemplo para suplementar propofol o anestesia por inhalación) o como analgésico. Se pueden administrar en bolos suplementarios de 5 a 10 pg/kg a intervalos apropiados.
Para mantener la anestesia en niños durante la intervención, puede administrarse LIMIFEN con una velocidad de perfusión de 0,5 a 2 pg/kg/min. La dosis debe ser ajustada en función de las necesidades de cada paciente. Cuando se combina con un anestésico intravenoso la dosis recomendada es aproximadamente 1pg/kg/min.
Puede existir un riesgo más elevado de complicaciones respiratorias y rigidez muscular cuando alfentanilo es administrado a neonatos y niños de menor edad (consultar sección 4.4 para ver las precauciones necesarias).
4.3 Contraindicaciones
Intolerancia conocida a alfentanilo o a cualquiera de sus componentes u otros morfinomiméticos.
4.4 Advertencias y precauciones especiales de empleo
Como ocurre con todos los opiáceos potentes, la depresión respiratoria es dosis-dependiente y puede revertirse con antagonistas específicos (naloxona), pero pueden ser necesarias dosis adicionales de estos últimos ya que la depresión respiratoria puede durar más que la acción del antagonista opiáceo. La analgesia profunda viene acompañada de depresión respiratoria importante y pérdida de conocimiento que puede persistir o recurrir durante el post-operatorio. Por ello los pacientes a los que se les administre LIMIFEN deben permanecer bajo vigilancia adecuada. Deben tenerse disponibles equipo de reanimación y antagonistas opiáceos. La hiperventilación durante la anestesia puede alterar la respuesta de los pacientes al CO2, afectando la respiración en el post-operatorio. Puede inducirse rigidez muscular, la cual podría incluir los músculos torácicos, pero ésta puede evitarse tomando las siguientes medidas: inyección i.v. lenta (generalmente suficiente para dosis bajas), premedicación con benzodiazepinas y utilización de relajantes musculares. Pueden ocurrir movimientos (mio)clónicos no epilépticos.
Si no se administran fármacos anticolinérgicos o si se utilizan relajantes musculares no vagolíticos se puede observar bradicardia e inclusoparo cardíaco. La bradicardia puede tratarse con atropina.
Los opiáceos pueden inducir hipotensión, especialmente en pacientes hipovolémicos. Deberán tomarse medidas adecuadas para mantener una presión arterial estable.
Alfentanilo se metaboliza fundamentalmente por vía enzimática del citocromo P450 3A4.
Los datos farmacocinéticos disponibles indican que el metabolismo de alfentanilo puede ser inhibido por algunos medicamentos (Ver Interacciones con otros medicamentos y otras formas de interacción). Esto podría aumentar el riesgo de una depresión respiratoria retardada o prolongada por lo que el uso concomitante de estos fármacos requiere una cuidadosa vigilancia del paciente, pudiendo ser necesario disminuir la dosis de LIMIFEN.
Deberá evitarse la utilización de inyecciones en bolo rápidas de opiáceos en pacientes con la distensibilidad intracerebral comprometida; en estos pacientes el descenso transitorio de la presión arterial media puede acompañarse, en ocasiones, por una reducción de corta duración de la presión de perfusión cerebral.
Los pacientes bajo tratamiento con opiáceos crónicos o con historial de dependencia a opiáceos pueden requerir dosis más altas.
¡m
Es recomendable reducir la posología en pacientes debilitados y ancianos. Los opiáceos deben administrarse con precaución en los siguientes estados: hipotiroidismo no controlado, enfermedades pulmonares, reservas respiratorias disminuidas, alcoholismo y función hepática o renal alteradas. Estos pacientes requieren además una monitorización post operatoria prolongada.
4.4.1 Población pediátrica
Puede existir un riesgo más elevado de complicaciones respiratorias y rigidez muscular cuando alfentanilo es administrado a neonatos y niños de menor edad que cuando es administrado a niños más mayores y adultos. Por esta razón los pacientes pediátricos de menor edad deben ser monitorizados inmediatamente después de la administración de alfentanilo. Debe haber un equipo de ventilación asistida disponible para el uso en niños de cualquier edad, incluso para intervenciones de corta duración en niños con respiración espontánea..
Si alfentanilo es usado en neonatos y lactantes se debe considerar el uso de un relajante muscular debido al riesgo de rigidez muscular. Todos los niños deben ser monitorizados durante un periodo de tiempo suficiente después de la finalización del tratamiento con alfentanilo para asegurar el retorno a respiración espontánea.
En neonatos puede ser necesaria una dosis menor de alfentanilo debido a las variaciones farmacocinéticas. Los neonatos deben ser estrechamente monitorizados y la dosis de alfentanilo se debe ajustar de acuerdo a la respuesta (ver sección 4.2)
4.5 Interacción con otros medicamentos y otras formas de interacción
Algunos fármacos como los barbitúricos, benzodiazepinas, neurolépticos, gases halogenados y otros depresores no selectivos del SNC (p.e. alcohol) pueden potenciar la depresión respiratoria que producen los opiáceos. Cuando se hayan administrado tales fármacos, la dosis necesaria de LIMIFEN será menor que la habitual; por el mismo motivo tras la administración de LIMIFEN deberán reducirse las dosis necesarias de los fármacos depresores del SNC.
Alfentanilo se metaboliza fundamentalmente por vía enzimática del citocromo P450 3A4. Datos in vitro sugieren que los inhibidores potentes de la enzima citocromo P450 3A4 (e.j. ketoconazol, itraconazol, ritonavir) podrían inhibir el metabolismo de alfentanilo.
Los datos farmacocinéticos disponibles indican que el metabolismo de alfentanilo es inhibido por conocidos inhibidores del citocromo P450 3A4 como: fluconazol, voriconazol, eritromicina, diltiazem y cimetidina.. Esto puede aumentar el riesgo de depresión respiratoria tardía o prolongada. El uso concomitante de estos fármacos requiere la observación y cuidados especiales del paciente; en particular, puede ser necesario disminuir la dosis de LIMIFEN.
Los inhibidores de la MAO potencian los efectos de los analgésicos opiáceos, por lo que se debe evitar el uso de LIMIFEN en aquellos pacientes que hayan recibido este tipo de fármacos durante las dos semanas previas a la intervención quirúrgica. Habitualmente, se recomienda interrumpir los IMAO al menos dos semanas antes de cualquier intervención quirúrgica o administración de anestesia.
Efecto del alfentanilo en el metabolismo de otros medicamentos
Las concentraciones sanguíneas de propofol son 17 veces más altas en combinación con LIMIFEN que en ausencia de LIMIFEN. El uso concomitante de alfentanilo y propofol podría requerir una dosis más baja de LIMIFEN.
4.6 Fertilidad, embarazo y lactancia Uso durante el embarazo
Aunque en la experimentación animal no se han observado teratogenicidad ni embriotoxicidad agudas, los datos de que se dispone no son suficientes para evaluar el potencial efecto dañino en el ser humano. Ver
¡m
Sección 5.3 (Datos preclínicos sobre seguridad). Consecuentemente se considerará la relación beneficio/riesgo antes de utilizar alfentanilo en mujeres embarazadas.
No se recomienda la administración de LIMIFEN en el parto (incluso en la cesárea) ya que el alfentanilo atraviesa la placenta y el centro respiratorio fetal es particularmente sensible a la acción de los opioides. En cualquier caso, si se utiliza LIMIFEN durante el parto, debe haber disponible de forma inmediata un equipo de ventilación asistida por si fuese necesario. Además siempre debe haber disponible un antagonista opioide . La vida media del antagonista opioide puede ser menor que la vida media de alfentanilo, por lo tanto, se debe considerar la administración repetida del antagonista opioide.
Uso durante la lactancia
LIMIFEN se puede excretar por la leche materna por lo cual no se recomienda la lactancia hasta después de transcurridas 24 horas desde la última administración.
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
La conducción de vehículos o el uso de maquinaria peligrosa se pueden reiniciar cuando ha pasado el tiempo suficiente desde la última administración de LIMIFEN. Aunque a este efecto la variación interindividual es grande, como media habrá que esperar entre 3 y 6 horas después de dosis de 1 a 3 ml y entre 12 y 24 horas después de dosis más altas o administración en infusión continua.
4.8 Reacciones adversas Datos del Ensayo clínico
Se evaluó la seguridad de LIMIFEN en 1157 sujetos que participaron en 18 ensayos clínicos. Se administró LIMIFEN como un agente inductor de la anestesia o como un adyuvante analgésico/anestésico para la anestesia general y local en procedimientos quirúrgicos cortos, medios y largos. Estos sujetos tomaron al menos una dosis de LIMIFEN y proporcionaron datos de seguridad. En la Tabla 1 se muestran las Reacciones Adversas al Fármaco que se comunicaron para el > 1% de los sujetos tratados con LIMIFEN en estos ensayos.
Tabla 1. Reacciones Adversas al fármaco comunicadas por el > 1% de los sujetos tratados con LIMIFEN en 18 Ensayos Clínicos de LIMIFEN
Clase de Órgano/Sistema
Reacción Adversa_
Trastornos psiquiátricos Estado de ánimo eufórico Trastornos del Sistema Nervioso
Trastorno del movimiento
Vértigo
Sedación
Discinesia
Trastornos oculares
Trastornos visuales
Trastornos cardíacos
Bradicardia
Taquicardia
Trastornos vasculares
Hipotensión
Hipertensión
Disminución de la presión sanguínea
Incremento de la presión sanguínea
Trastornos respiratorios, torácicos y mediastínicos
Apnea
Trastornos gastrointestinales
Náuseas
Vómitos
Trastornos
musculoesqueléticos y del tejido conjuntivo
Rigidez muscular
Trastornos generales y alteraciones en el lugar de administración
Fatiga Escalofríos Dolor en el lugar de inyección
Lesiones traumáticas, intoxicaciones y complicaciones de procedimientos terapéuticos
Dolor relacionado con el procedimiento
1,8
7,9
2.4
1.5
1.4
1,1
5.4 1,0
4.1
2.2
1,3
1,0
8,6
17.0
14.0
3,1
2,0
1,8
1,6
1,1
A continuación en la Tabla 2 se listan las Reacciones Adversas al fármaco adicionales que ocurrieron en el <1% de los sujetos tratados con LIMIFEN en los 18 ensayos clínicos.
Tabla 2. Reacciones Adversas al fármaco comunicadas por el < 1% de los sujetos tratados con LIMIFEN en 18 Ensayos Clínicos de LIMIFEN
¡m
Clase de Órgano/Sistema
Reacción Adversa_
Trastornos psiquiátricos
Agitación
Llanto
Trastornos del Sistema Nervioso
Dolor de cabeza Somnolencia Insensible al estímulo Trastornos cardíacos Arritmia
Disminución de la frecuencia cardiaca Trastornos vasculares Dolor venoso Trastornos respiratorios, torácicos y mediastínicos Broncoespasmo Hipo
Hipercapnia
Laringoespasmo
Epistaxis
Depresión respiratoria Trastornos de la piel y del tejido subcutáneo
Dermatitis alérgica
Hiperhidrosis
Prurito
Trastornos generales y alteraciones en el lugar de administración
Dolor
Lesiones traumáticas, intoxicaciones y complicaciones de procedimientos terapéuticos
Confusión postoperatoria Agitación postoperatoria Complicación de la anestesia en las vías respiratorias
Complicación neurológica anestésica
Complicación relacionado con el procedimiento Complicación en la intubación endotraqueal
Datos post-comercialización
Las primeras reacciones adversas al fármaco identificadas durante la experiencia post-comercialización con LIMIFEN están incluidas en las Tablas 3 y 4. En cada tabla, las frecuencias están suministradas de acuerdo a lo siguiente:
Muy frecuentes >1/10 Frecuentes > 1/100 y <1/10
Poco frecuentes >1/1000 y <1/100 Raras >1/10000, <1/1000
¡m
Muy raras <1/10000, incluyendo casos aislados
En la Tabla 3, se presentan las reacciones adversas al fármaco por categoría de frecuencia basado en la proporción de comunicaciones espontáneas, mientras que en la Tabla 4, se presentan las mismas reacciones adversas al fármaco por categoría de frecuencia basado en la incidencia cuando se conoce de los ensayos clínicos o estudios epidemiológicos. La categoría de frecuencia “no conocida” se usa para las reacciones adversas al fármaco para las cuales no se puede derivar de los ensayos clínicos una estimación válida de la proporción de incidencia.
Tabla 3. Reacciones adversas al fármaco identificadas durante la experiencia postcomercialización con LIMIFEN por categoría de frecuencias estimadas de la proporción de comunicaciones espontáneas.
Trastornos del Sistema Inmunológico
Muy raras Hipersensibilidad (incluyendo reacción anafiláctica, reacción anafilactoide y urticaria) Trastornos psiquiátricos Muy raras Desorientación
Trastornos del sistema nervioso
Muy raras Pérdida de conocimientoa, convulsión, mioclono
Trastornos oculares
Muy raras Miosis
Trastornos cardiacos
Muy raras Paro cardiaco
Trastornos respiratorios, torácicos y mediastínicos
Muy raras Parada respiratoria, depresión respiratoriab, tos
Trastornos de la piel y del tejido subcutáneo
Muy raras Eritema, rash
Trastornos generales y alteraciones en el lugar de administración Muy raras Pirexia
aperiodo postoperatorio b Incluyendo desenlace fatal
Tabla 4. Reacciones adversas al fármaco identificadas durante la experiencia postcomercialización con LIMIFEN por categoría de frecuencias estimadas de los ensayos clínicos o estudios epidemiológicos Trastornos del Sistema Inmunológico
¡m
No conocida Hipersensibilidad (incluyendo reacción anafiláctica, reacción anafilactoide y urticaria) Trastornos psiquiátricos No conocida Desorientación Trastornos del sistema nervioso
No conocida Pérdida de conocimientoa, convulsión, mioclono
Trastornos oculares
No conocida Miosis
Trastornos cardiacos
No conocida Paro cardiaco
Trastornos respiratorios, torácicos y mediastínicos
No conocida Parada respiratoria, tos
Poco frecuentes Depresión respiratoriab
Trastornos de la piel y del tejido subcutáneo
No conocida Eritema, rash
Trastornos generales y alteraciones en el lugar de administración No conocida Pirexia aperiodo postoperatorio b Incluyendo desenlace fatal
4.8.1 Población pediátrica
Es de esperar que la frecuencia, tipo y gravedad de reacciones adversas en niños sean las mismas que en adultos, con excepción de las siguientes:
En neonatos se ha visto frecuentemente rigidez muscular de leve a moderada, aunque el número de neonatos incluidos en el ensayo clínico fue bajo. Pueden ocurrir de manera menos frecuente casos de rigidez severa y sacudidas que pueden ir acompañadas de insuficiencia respiratoria transitoria especialmente con dosis altas de LIMIFEN o con una velocidad de inyección intravenosa rápida.
4.9 Sobredosis
Signos y Síntomas
Las manifestaciones de la sobredosis con LIMIFEN son una consecuencia de su acción farmacológica. Dependiendo de la sensibilidad individual, el cuadro clínico se determina principalmente por el grado de depresión respiratoria que puede variar desde bradipnea a apnea.
Tratamiento
Si se presentase hipoventilación o apnea se debe administrar oxígeno y utilizar ventilación asistida o controlada, según el caso.
Para controlar la depresión respiratoria se puede administrar un antagonista específico de los opiáceos tal como naloxona. Esto no excluye la utilización de contramedidas más inmediatas. La duración de la depresión respiratoria puede ser más larga que la del efecto del antagonista; consecuentemente, pueden ser necesarias dosis adicionales de estos últimos fármacos.
Si la depresión respiratoria está asociada a rigidez muscular, puede ser necesario un agente bloqueante neuromuscular intravenoso para facilitar la respiración asistida o controlada.
El paciente debe ser cuidadosamente observado; se mantendrá la temperatura corporal y se repondrán líquidos. Si se produjese hipotensión o si ésta persistiese se debe pensar en una posible hipovolemia y, por lo tanto, en la administración parenteral de fluidos.
5. PROPIEDADES FARMACOLÓGICAS
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: Anestésicos opioides, código ATC: N01AH02.
¡m
Alfentanilo es un potente analgésico opiáceo, relacionado con el fentanilo, que se caracteriza por tener un inicio de acción muy rápido y una duración muy breve. Tras su administración IV su acción se manifiesta de forma prácticamente instantánea. El inicio de la acción de alfentanilo es cuatro veces menor que una dosis equipotente de fentanilo. El máximo efecto anagésico y de depresión respiratoria tiene lugar en 1 ó 2 minutos (30 minutos con morfina).
La duración de acción de alfentanilo es tres veces más corta que una dosis equipotente de fentanilo y es claramente dosis dependiente. En los casos en que se requieran más de 60 minutos de analgesia se recomienda la administración en infusión continua. El efecto depresor de la frecuencia respiratoria y la ventilación alveolar es de menor duración que la que provoca el fentanilo y en la mayoría de los casos la duración del efecto analgésico excede a los efectos respiratorios. La duración y el grado de depresión respiratoria aumentan con la dosis.
La inducción que provoca es progresiva, indolora y carente de la respuesta cardiovascular u hormonal al stress que produce la intubación.
El alfentanilo tiene un amplio margen de seguridad. En ratas la relación DL50/DE50 en el nivel más bajo de analgesia, para alfentanilo es 1080, comparado con 4'6, 69'5 y 277 para petidina, morfina y fentanilo, respectivamente.
Como ocurre con otros analgésicos opiáceos, alfentanilo puede causar rigidez muscular, así como euforia, miosis y bradicardia, dependiendo de la dosis y de la velocidad de administración.
Alfentanilo en dosis de hasta 200 microgramos/kg, no produce un aumento significativo en los niveles histamínicos ni evidencia clínica de liberación de histamina.
La recuperación después de la administración de alfentanilo es rápida y suave con una baja incidencia de náusea y vómitos en el post-operatorio.
Todos los efectos de alfentanilo se pueden revertir, de forma completa e inmediata, con el uso de antagonistas específicos de los morfínicos como naloxona.
5.2 Propiedades farmacocinéticas
Alfentanilo es un opioide sintético con efectos farmacológicos p-agonista, usado solo intravenosamente. Distribución
La semivida de distribución secuencial es de 0,4 - 2,2 minutos y 8-32 minutos. El bajo grado de ionización (11% a pH=7,4) contribuye a una distribución rápida pero limitada en los tejidos.
Se ha informado que los volúmenes de distribución son de 1,27 - 4,81 L (volumen de distribución en el compartimento central) y 12,1 - 98,2 L (volumen de distribución en el estado de equilibrio). La unión de alfentanilo a proteínas plasmáticas es de aproximadamente 92%.
Metabolismo
Alfentanilo se metaboliza principalmente en el hígado. Solamente se encuentra el 1 % de alfentanilo inalterado en orina. Sus metabolitos son inactivos y el 70%-80% de ellos se eliminan vía urinaria.
Eliminación
Alfentanilo se elimina rápidamente después de la administración intravenosa. Se ha informado de una semivida de eliminación terminal de 83-223 minutos.
El aclaramiento plasmático en pacientes jóvenes es de 356 ml/minuto y disminuye con la edad.
Solamente se encuentra el 1 % de alfentanilo inalterado en orina.
Una vez que se alcanza el estado de equilibrio tras la infusión, la semivida de eliminación permanece estable.
Cuando la administración no es continua, el paciente despierta rápidamente sin los efectos típicos posteriores a la administración de opiáceos.
Poblaciones especiales
Población pediátrica
¡m
Los datos en niños son limitados. Los valores de parámetros farmacocinéticos se muestran en la siguiente tabla
|
Parámetros farmacocinéticos de alfentanilo en población pediátrica | |||
|
T1/2p (hr) |
AC (mL/kg/min) |
Vdss (L/kg) | |
|
Neonatos prematuros (0-27 días) Edad gestacional 25-40 semanas; n= 68 |
0,7-8,8 |
0,9-8,4 |
0,3-1,2 |
|
Neonatos (0-27 días) Edad gestacional: 3541 semanas; n= 18 |
4,1-5,5 |
1,7-3,2 |
0,5-0,8 |
|
Lactantes y niños de 28 días-23 meses de edad; n= 34 |
0,9-1,2 |
7,7-13,1 |
0,4-1,1 |
|
Niños de 2-11 años de edad; n= 32 |
0,7-1,3 |
4,7-10,2 |
0,2-1,0 |
|
Adolescentes 12-14 años; n= 3 |
1,1-1,9 |
5,5-7,4 |
0,3-0,6 |
Nota: Los datos para neonatos, lactantes y niños se expresan como rango de valores medios
AC = aclaramiento, Vdss = volumen de distribución en el estado de equilibrio, t1/2p = semivida de
eliminación
La unión a proteínas en recién nacidos es del 75 % y se incrementa en niños entre 4,5 y 7,75 años hasta el 85 %. La información farmacocinética del uso de alfentanilo en niños es limitada. Alfentanilo es metabolizado por CYP3A4. En neonatos la actividad de CYP3A4 es baja y aumenta después del nacimiento hasta alcanzar el 30-40% de los niveles del adulto al mes de edad.
Deterioro hepático
Después de la administración de una dosis intravenosa única de 50 pg/kg, la semivida terminal en pacientes cirróticos es significativamente más larga que en los controles. El volumen de distribución permanece inalterado. La fracción libre de alfentanilo aumenta en pacientes cirróticos hasta 18,5 % comparado con 11,5 % en los controles. Este incremento en la fracción libre junto con una reducción en el aclaramiento desde 3,06 ml/min/kg en los controles hasta 1,60 ml/min/kg en los pacientes cirróticos, tendrá como resultado un efecto más pronunciado y prolongado (ver sección 4.4).
Deterioro renal
El volumen de distribución y el aclaramiento de la fracción libre es similar en pacientes con fallo renal y controles sanos. La fracción libre de alfentanilo en pacientes con fallo renal está aumentada desde 12,4 a 19 % comparado con 10,3 a 11 % en los controles. Esto puede resultar en un incremento en el efecto clínico de alfentanilo (ver sección 4.4).
5.3 Datos preclínicos sobre seguridad
Los efectos preclínicos observados tan solo se vieron a exposiciones que excedieron considerablemente la exposición máxima en humanos, lo que indica una pequeña relevancia en el uso clínico.
Alfentanilo se ha probado en una batería de estudios de seguridad no clínicos incluyendo: toxicidad a dosis única después de la administración intravenosa (ratón, rata, cobaya, perro); toxicidad intravenosa a dosis repetida después de un mes en perros y ratas; estudios de reproducción en los que el fármaco se administró
i ¡Ti
intravenosamente y en los que se estudiaron la fertilidad y la reproducción en general en ratas, la teratogenicidad y la embriotoxicidad en ratas y conejos, y la reproducción perinatal/postnatal en ratas. Se evaluó la mutagenicidad tanto en estudios in vitro como in vivo que incluyeron: estudios de mutación genética y/o puntual in vitro en salmonella typhimurium y evaluaciones en ratas in vivo de los micronúcleos que se utilizaron en ensayos para aberraciones cromosómicas, y test letal dominante en ratones machos y hembras. Se llevaron a cabo algunos estudios especiales para evaluar la administración intra-arterial, la liberación de histamina y la hemólisis.
Los resultados obtenidos de los estudios de toxicidad a dosis única y repetida, de reproducción, de mutagenicidad y los estudios especiales indicaron que alfentanilo fue bien tolerado y tenía un amplio margen de seguridad cuando se comparó a los valores DE 50 en animales y a los distintos regímenes de dosificación clínica relevantes. La toxicidad y mortalidad observada en estos modelos de animales estuvo, en general, relacionada con dosis tóxicas altas más allá del intervalo terapéutico clínico propuesto (2,6 a 83 veces), o fue secundaria a la actividad farmacológica exagerada de este fármaco.
6 . DATOS FARMACEUTICOS
6.1 Lista de excipientes
Los ingredientes inactivos de la solución inyectable son cloruro sódico y agua para inyectable.
6.2 Incompatibilidades
La solución inyectable no se debe mezclar con otros productos.
Si se desea, LIMIFEN puede mezclarse con infusiones intravenosas de cloruro sódico o glucosa. Tales diluciones son compatibles con los juegos de infusión plástica. Éstos deberán utilizarse dentro de las 24 horas después de la preparación.
6.3 Periodo de validez
Cinco años
6.4 Precauciones especiales de conservación
Guárdese a temperatura ambiente.
Mantenga LIMIFEN fuera del alcance y de la vista de los niños.
6.5 Naturaleza y contenido del envase
Envases de 5 ampollas con 2 ó 10 ml.
6.6 Precauciones especiales de eliminación y otras manipulaciones
Si se desea, LIMIFEN puede mezclarse con infusiones intravenosas de cloruro sódico o glucosa. Tales diluciones son compatibles con los juegos de infusión plástica. Estos deberán utilizarse dentro de las 24 horas después de la preparación.
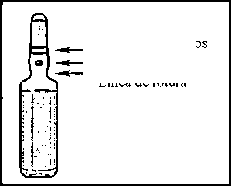
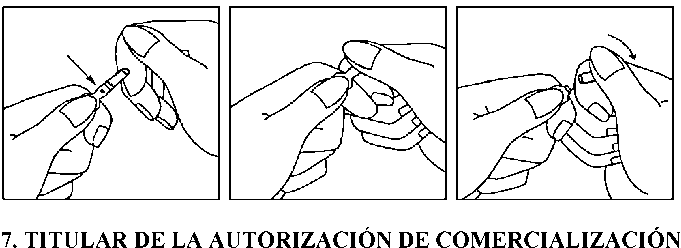
1. Mantener la ampolla entre los dedos índice y pulgar, dejando libre la punta de la ampolla
2. Con la otra mano, sujete la punta de la ampolla poniendo el dedo índice contra el cuello de la ampolla y el dedo pulgar en el punto coloreado en paralelo al (los) anillo(s) coloreado(s) de identificación.
3. Manteniendo el pulgar en ese punto, rompa la punta de la ampolla mientras sujeta firmemente la otra parte de la ampolla en la mano.
ÜE
JANSSEN-CILAG, S.A.
Paseo de Las Doce Estrellas, 5-7 28042 Madrid
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
LIMIFEN 0,5 mg/ml solución inyectable; N° Reg.: 57.471
9. FECHA DE LA PRIMERA AUTORIZACIÓN/ RENOVACIÓN DE LA AUTORIZACIÓN
12 de diciembre de 1988/30 de junio de 2008
10. FECHA DE LA REVISIÓN DEL TEXTO Julio 2016
13 de 13