Fosatur 40 U.i. Solucion Para Pulverizacion Nasal
Información obsoleta, busque otroFICHA TÉCNICA
1. DENOMINACIÓN DEL MEDICAMENTO
FOSATUR 40 UI Solución para pulverización nasal
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Elcatonina es un análogo de la calcitonina de anguila.
Una pulverización contiene 40 UI de elcatonina (DOE).
Lista de excipientes, en sección 6.1
3. FORMA FARMACÉUTICA Solución para pulverización nasal.
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
Tratamiento de osteoporosis postmenopáusica establecida para reducir el riesgo de fracturas vertebrales. No se ha demostrado una reducción en fracturas de cadera.
4.2 Posología y forma de administración
La dosis recomendada de calcitonina intranasal para el tratamiento de la osteoporosis postmenopáusica establecida es de 80 UI una vez al día. Se recomienda que el uso de calcitonina intranasal esté acompañado de una ingesta adecuada de calcio y vitamina D. El tratamiento debe ser administrado de forma prolongada, (ver sección 5.1., Propiedades farmacodinámicas).
Uso en pacientes ancianos, en alteración hepática y en insuficiencia renal
La experiencia obtenida con el uso de calcitonina intranasal en los pacientes con edad avanzada demuestra que no existe evidencia de una disminución de la tolerancia o de la necesidad de cambiar la pauta poso lógica. Esto mismo puede aplicarse a pacientes con la función renal o hepática alterada.
Uso en niños
Dado que la calcitonina intranasal está indicada para mujeres postmenopáusicas, no es adecuado su uso en niños.
Nota
Las instrucciones de uso completas para el paciente se hallan en el prospecto de paciente.
4.3 Contraindicaciones
Hipersensibilidad a la calcitonina (ver sección 4.8. Reacciones adversas) o a cualquiera de los excipientes del preparado (ver sección 6.1. Lista de excipientes).
La calcitonina también está contraindicada en pacientes con hipocalcemia.
4.4 Advertencias y precauciones especiales de empleo
Antes de iniciar el tratamiento deberá realizarse una exploración nasal y en caso de síntomas nasales no debe iniciarse el tratamiento. Si aparece ulceración grave de la mucosa nasal (p.ej. con afectación por debajo de la mucosa o asociación con sangrado importante), debe interrumpirse el tratamiento con calcitonina intranasal. En caso de ulceración moderada, deberá interrumpirse temporalmente el tratamiento hasta alcanzar la curación.
Debido a que la calcitonina es un péptido, existe la posibilidad de reacciones alérgicas sistémicas y se han descrito reacciones de tipo alérgico, incluyendo casos aislados de shock anafiláctico, en pacientes sometidos a un tratamiento con calcitonina intranasal. En pacientes en los que se sospecha que exista sensibilidad a la calcitonina, se debe considerar la realización de pruebas cutáneas de sensibilidad antes de iniciar el tratamiento.
4.5 Interacción con otros medicamentos y otras formas de interacción
No se han descrito interacciones de elcatonina intranasal con otros medicamentos.
4.6 Embarazo y lactancia
Dado que la calcitonina intranasal está indicada para mujeres postmenopáusicas, no se han realizado estudios en mujeres embarazadas o en periodo de lactancia. Por lo tanto, no debe administrarse calcitonina intranasal a estas pacientes. Sin embargo, estudios en animales no han demostrado potencial embriotóxico y teratogénico. Parece ser que elcatonina no atraviesa la barrera placentaria en animales.
No se sabe si elcatonina se excreta en la leche materna. Por lo tanto, no se recomienda la lactancia durante el tratamiento.
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
No existen datos acerca de los efectos de la calcitonina intranasal sobre la. capacidad para conducir y utilizar máquinas. La calcitonina intranasal puede causar vértigo de forma, transitoria (ver sección 4.8. Reacciones adversas) lo cual puede disminuir la capacidad de reacción del paciente. Por lo tanto, los pacientes deben ser advertidos de que pueden aparecer vértigos de forma transitoria , en cuyo caso no deberían conducir ni utilizar máquinas.
4.8 Reacciones adversas
Las reacciones adversas observadas durante el tratamiento con elcatonina son similares a las citadas tras la administración de la calcitonina de salmón.
Estimación de frecuencias:
Muy frecuentes (> 1/10); frecuentes (>l/100, <l/10); poco frecuentes (> 1/1.000, < 1/100); raras (>1/10.000, <l/1.000); muy raras (<1/10.000), casos aislados.
Trastornos gastrointestinales
Frecuente: náuseas, diarrea, dolor abdominal.
Poco frecuentes: vómitos.
Trastornos vasculares
Frecuentes: rubor.
Poco frecuentes: hipertensión.
Trastornos respiratorios
Muy frecuentes: rinitis (incluyendo sequedad nasal, edema nasal, congestión nasal, estornudos, rinitis alérgica), síntomas nasales inespecíficos (p.ej. irritación del conducto nasal, rash papular, parosmia, eritema, abrasión).
Frecuentes: rinitis ulcerativa, sinusitis, epistaxis, faringitis.
Poco frecuentes: tos.
Estos efectos son generalmente moderados (en aprox. 80% de los informes) y requieren la interrupción del tratamiento en menos del 5% de los casos.
Trastornos del sistema nervioso
Frecuentes: vértigos, cefalea, disgeusia.
Trastornos de los sentidos
Poco frecuentes: alteración de la visión.
Trastornos del tejido de la piel y subcutáneos
Poco frecuentes: edema (edema facial, edema periférico y anasarca).
Trastornos musculoesqueléticos
Frecuentes: dolor musculoesquelético.
Poco frecuentes: artralgia.
Trastornos del sistema inmunitario
Poco frecuentes: reacciones de hipersensibilidad tales como reacciones cutáneas generalizadas, rubor, edema (edema facial, edema periférico y anasarca), hipertensión, artralgia y prurito. Muy raras: reacciones alérgicas y reacciones de tipo anafilactoide tales como taquicardia, hipotensión, colapso circulatorio y shock anafiláctico.
Investigaciones
Raras: desarrollo de anticuerpos neutralizadores de la calcitonina. El desarrollo de estos anticuerpos no está, por lo general, relacionado con la pérdida de eficacia clínica, aunque su presencia en un pequeño porcentaje de pacientes tras una terapia a largo plazo con dosis altas de calcitonina podría dar como resultado una disminución en la respuesta al producto. La presencia de anticuerpos parece no tener relación con las reacciones alérgicas, que son raras. El descenso de regulación del receptor de calcitonina podría dar como resultado una respuesta clínica reducida en un pequeño porcentaje de pacientes tras una terapia a largo plazo con dosis altas.
Trastornos generales
Frecuentes: fatiga.
Poco frecuentes: enfermedad que se asemeja al síndrome gripal.
4.9 Sobredosis
Se sabe que las náuseas, vómitos, rubor y vértigo son reacciones dosis dependientes cuando se administra calcitonina por vía parenteral. Sin embargo, no se han citado casos de sobredosis. Si aparecen síntomas de sobredosificación, el tratamiento debe ser sintomático.
5.
PROPIEDADES FARMACOLÓGICAS
Grupo farmacoterapéutico: hormona antiparatiroidea, código ATC: H05B A04 (elcatonina).
5.1 Propiedades farmacodinámicas
La calcitonina es una hormona calciotrópica, que inhibe la resorción ósea por acción directa sobre los osteoclastos. Mediante la inhibición de la actividad de los osteoclastos, vía sus receptores específicos, elcatonina disminuye la resorción ósea.
La calcitonina reduce considerablemente el recambio óseo en situaciones en las que se produce una tasa elevada de resorción ósea, como en la osteoporosis.
Se ha demostrado la ausencia de defecto de mineralización con calcitonina mediante estudios histomorfométricos tanto en hombre como en animales.
En estudios farmacológicos, la calcitonina ha demostrado poseer actividad analgésica en modelos animales.
La calcitonina intranasal produce una respuesta biológica clínicamente relevante en humanos, como se demuestra por un incremento de la excreción urinaria de calcio, fósforo y sodio (reduciendo su reabsorción tubular) y por un descenso en la excreción urinaria de hidroxiprolina. La administración a largo plazo de calcitonina intranasal suprime significativamente los marcadores bioquímicos de recambio óseo, tales como los C-telopéptidos séricos (sCTX) e isoenzimas esqueléticos de la fosfatasa alcalina.
La calcitonina intranasal produjo un aumento estadísticamente significativo 1-2% de la Densidad Mineral Ósea (DMO) en la espina lumbar, el cual es evidente desde el primer año, manteniéndose hasta 5 años. Se mantiene la DMO de la cadera.
En un ensayo de 5 años con mujeres postmenopáusicas (estudio PROOF), la administración de 200 UI de calcitonina de salmón intranasal provocó una reducción del 33% en el riesgo relativo de desarrollar fracturas vertebrales. El riesgo relativo de desarrollar fracturas vertebrales, comparado con placebo (sólo tratamiento con vitamina D y calcio) en todas las pacientes tratadas con dosis diarias de 200 UI fue 0,67 (IC 95%: 0,47-0,97). El riesgo absoluto de desarrollar fracturas vertebrales durante 5 años se redujo de un 25,9% en el grupo placebo a un 17,8% en el grupo de 200 UI. No se ha demostrado una reducción de fracturas de cadera.
La dosis recomendada de elcatonina para el tratamiento de osteoporosis postmenopáusica establecida es de 80 UI una vez al día. Dosis más altas no fueron más efectivas.
5.2 Propiedades farmacocinéticas
Los parámetros farmacocinéticos de elcatonina administrada vía intranasal son difíciles de cuantificar debido a la sensibilidad inadecuada y a la especificidad incierta de los inmunoensayos disponibles, utilizados en los estudios realizados hasta la fecha. La biodisponibilidad de la dosis de 40 UI con respecto a la administración parenteral está entre el 45 y 53%. La calcitonina intranasal se absorbe rápidamente por la mucosa nasal y las concentraciones plasmáticas máximas aparecen dentro de la primera hora tras la administración. Dosis superiores a la recomendada conducen a niveles sanguíneos más elevados (tal y como se observa por un incremento en el AUC), sin embargo, la biodisponibilidad relativa no se incrementa. Como ocurre con otras hormonas polipeptídicas. la monitorización de los niveles plasmáticos de elcatonina tiene muy poco valor ya que no son directamente predictivos de la respuesta terapéutica. Por consiguiente, la actividad de calcitonina debería evaluarse utilizando parámetros clínicos de eficacia.
5.3 Datos preclínicos sobre seguridad
Se han realizado en animales de laboratorio estudios convencionales de toxicidad a largo plazo, de reproducción y de mutagenicidad. Además, se investigó la tolerancia nasal en perros y ratas.
Elcatonina carece de potencial embriotóxico, teratogénico y mutagénico. La administración intranasal diaria de dosis altas de una formulación de elcatonina conteniendo 2% de glicirricinato amónico durante 12 semanas fue bien tolerada por ratas y perros.
Elcatonina no atraviesa la barrera placentaria.
En animales en periodo de lactancia que recibieron calcitonina, se observó una supresión de la producción de leche. La calcitonina se excreta en la leche.
6. DATOS FARMACÉUTICOS
6.1 Lista de excipientes
Trometamina, meglumina, ácido cítrico anhidro, polivinilpirrolidona k30, parahidroxibenzoato de metilo, parahidroxibenzoato de propilo y agua para inyección.
6.2 Incompatibilidades
No se han descrito
6.3 Periodo de validez
2 años
6.4 Precauciones especiales de conservación
Antes de su uso FOSATUR 40 UI Solución para pulverización nasal debe mantenerse en frigorífico (2°C - 8°C). No congelar. Una vez abierto el envase, FOSATUR 40 UI Solución para pulverización nasal debe conservarse a temperatura ambiente (no por encima de 22°C) hasta un máximo de cuatro semanas.
6.5 Naturaleza y contenido del recipiente
El envase de FOSATUR 40 UI Solución para pulverización nasal es un frasco de vidrio transparente e incoloro y un dispositivo pulverizador.
Presentación: envase con una cantidad suficiente de solución para garantizar 24 aplicaciones útiles de 40 UI de Elcatonina cada una.
6. 6. Instrucciones de uso/manipulación
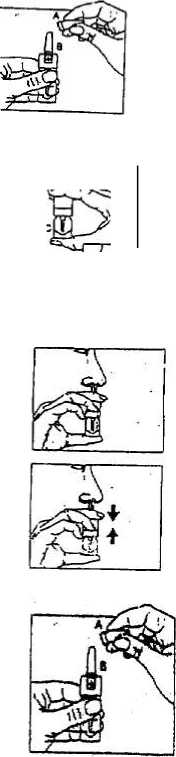
1. Separar el capuchón protector A del contador B.
Asegurarse de que aparece una flecha en el visor
del contador antes de proseguir con el paso n°
2.
2. Presionar con firmeza el contador B hacia el frasco C. Repetir el movimiento hasta que aparezca la letra P en la ventana indicadora del contador: en este punto el pulverizador está preparado para su utilización.
3. Introducir el pulverizador en las fosas nasales, manteniendo el frasco en posición vertical.
4. Sin inspirar, presionar con decisión, tal como se
indica en la figura, hasta sentir el disparo que señala la correcta administración. Después de la
primera pulverización la letra P de la ventana indicadora desaparecerá y no volverá a aparecer.
5. Perforar en el estuche el n° de la pulverización utilizada.
6. Cerrar de nuevo el pulverizador con el capuchón protector
7. Al perforar la última pulverización en el estuche, desechar el resto.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
CANTABRIA PHARMA, S.L.
C/ Ribera del Loira, 46 edificio 2 (Madrid) - 28042 - España
8. NÚMERO DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
63.061
9. FECHA DE LA PRIMERA AUTORIZACIÓN / RENOVACIÓN DE LA AUTORIZACIÓN
Mayo 2000
10. FECHA DE LA REVISION DEL TEXTO
Diciembre de 2003
Correo electrúnicoI
C / CAMPEZO, 1 - EDIFICIO 8 28022 MADRID
agencia española de medicamentos y productos sanitarios