Effentora 800 Microgramos Comprimidos Bucales
ANEXO I
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
1. NOMBRE DEL MEDICAMENTO
Effentora 100 microgramos comprimidos bucales
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada comprimido bucal contiene 100 microgramos de fentanilo (como citrato).
Excipiente(s) con efecto conocido: Cada comprimido contiene 10 mg de sodio. Para consultar la lista completa de excipientes, ver sección 6.1.
3. FORMA FARMACÉUTICA
Comprimido bucal.
Comprimido de caras planas, de color blanco, redondo y con bordes biselados, con una "C” grabado en una cara y en la otra con “1”
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
Effentora está indicado para el tratamiento del dolor irruptivo (DI) en pacientes adultos con cáncer que ya reciben tratamiento de mantenimiento con opioides para el dolor crónico asociado a cáncer.
El DI es una exacerbación transitoria del dolor que se produce sobre un fondo de dolor persistente controlado por otros medios.
Los pacientes que reciben tratamiento de mantenimiento con opioides son los que toman como mínimo 60 mg de morfina oral diarios, 25 microgramos de fentanilo transdérmico cada hora, 30 mg de oxicodona diarios, 8 mg de hidromorfona oral diarios o una dosis equianalgésica de otro opioide durante una semana o más.
4.2 Posología y forma de administración
El tratamiento debe ser instaurado y seguido bajo las directrices de un médico experimentado en la terapia con opioides en pacientes con cáncer. Los médicos deben considerar el riesgo del abuso del fentanilo. Se debe advertir al paciente que no debe utilizar dos concentraciones diferentes de fentanilo al mismo tiempo para el tratamiento del dolor irruptivo y que debe desechar cualquier producto de fentanilo prescrito para el dolor irruptivo cuando cambie a Effentora. Con objeto de prevenir confusiones y posibles sobredosis, los pacientes deben disponer en cada momento del mínimo número de concentraciones de los comprimidos.
Posología
Ajuste de la dosis
Effentora debe ajustarse de forma individual hasta obtener una dosis “eficaz” que proporcione la analgesia adecuada y minimice las reacciones adversas. En los ensayos clínicos, la dosis eficaz de Effentora para el DI no pudo predecirse a partir de la dosis diaria de mantenimiento de opioides.
Los pacientes deben monitorizarse cuidadosamente hasta que se establezca la dosis eficaz.
Ajuste de la dosis en pacientes que no cambian a Effentora desde otros medicamentos que contienen fentanilo
La dosis inicial de Effentora debe ser de 100 microgramos, que se incrementará según sea necesario dentro del rango de concentraciones de dosificación disponibles (100, 200, 400, 600 y 800 microgramos).
Ajuste de la dosis en pacientes que cambian a Effentora tras recibir otros medicamentos que contienen fentanilo
Debido a los diferentes perfiles de absorción, el cambio no debe hacerse en una proporción de 1:1. Si el cambio se hace desde otro medicamento de fentanilo como citrato oral, se precisa un ajuste de la dosis independiente con Effentora puesto que la biodisponibilidad difiere notablemente de un medicamento a otro. Sin embargo, en estos pacientes se puede considerar una dosis inicial mayor de 100 microgramos.
Proceso de ajuste de la dosis
Durante el ajuste de la dosis, si no se consigue una analgesia adecuada en los 30 minutos siguientes a la administración de un único comprimido, puede administrarse un segundo comprimido de Effentora de la misma concentración.
Si para tratar un episodio de DI se precisa más de un comprimido, para el tratamiento de futuros episodios de DI debe considerarse un aumento de la dosis hasta la siguiente concentración disponible.
Durante el proceso de ajuste de la dosis, se pueden combinar diferentes comprimidos. Se pueden utilizar hasta cuatro comprimidos de 100 microgramos o hasta cuatro comprimidos de 200 microgramos para tratar un episodio aislado de DI durante el proceso de ajuste de la dosis de acuerdo con el siguiente esquema:
• Si el comprimido inicial de 100 microgramos no es eficaz, se podrá prescribir al paciente dos comprimidos de 100 microgramos para tratar el siguiente episodio de DI. Se recomienda colocar un comprimido a cada lado de la boca. Si se establece que esa es la dosis eficaz, los futuros episodios de DI podrán seguir tratándose con un único comprimido de Effentora de
200 microgramos.
• Si un único comprimido de Effentora de 200 microgramos (o dos comprimidos de 100 microgramos) no resulta eficaz, podrá prescribirse al paciente dos comprimidos de
200 microgramos (o cuatro comprimidos de 100 microgramos) para tratar el siguiente episodio de DI. Se recomienda colocar dos comprimidos a cada lado de la boca. Si se considera que esa es la dosis eficaz, los futuros episodios de DI podrán seguir tratándose con un único comprimido de Effentora de 400 microgramos.
• Para el ajuste de la dosis con comprimidos de 600 microgramos y 800 microgramos, deben utilizarse comprimidos de 200 microgramos.
En los ensayos clínicos no se evaluaron dosis de más de 800 microgramos.
No deben utilizarse más de dos comprimidos para tratar un mismo episodio de DI, salvo cuando el ajuste de la dosis se realice utilizando cuatro comprimidos, como se ha explicado antes.
Durante el ajuste de la dosis, los pacientes deben esperar al menos 4 horas antes de tratar otro episodio de DI con Effentora.
Tratamiento de mantenimiento
Una vez determinada la dosis eficaz por medio del proceso de ajuste, los pacientes deben mantener esa dosis y limitar el consumo a un solo comprimido con la concentración que corresponda.
Los episodios de dolor irruptivo pueden variar en intensidad y la dosis de Effentora requerida puede aumentar con el tiempo debido a una progresión de la enfermedad oncológica subyacente. En estos casos se puede utilizar un segundo comprimido de Effentora de la misma concentración.
En caso de que se necesite un segundo comprimido de Effentora en diversas ocasiones consecutivas, se deberá reajustar la dosis de mantenimiento habitual (ver más abajo).
Durante el tratamiento de mantenimiento, los pacientes deben esperar al menos 4 horas antes de tratar otro episodio de DI con Effentora.
Reajuste de la dosis
La dosis de mantenimiento de Effentora debe aumentarse si el paciente necesita más de un comprimido por episodio de DI en varios episodios consecutivos de DI. Para el reajuste de la dosis se aplican los mismos principios descritos para Ajuste de la dosis (ver más arriba).
Si el paciente presenta con frecuencia más de cuatro episodios de DI en 24 horas, se debe volver a calcular la dosis del tratamiento de mantenimiento con opioides.
Interrupción del tratamiento
El tratamiento con Effentora se debe interrumpir inmediatamente si el paciente ya no presenta episodios de dolor irruptivo. El tratamiento del dolor de base persistente se debe mantener tal como estaba prescrito.
Si es necesario interrumpir la totalidad del tratamiento con opioides, el médico debe realizar un estrecho seguimiento del paciente con el fin de controlar el riesgo de efectos abruptos de abstinencia.
Pacientes con insuficiencia hepática o renal:
Effentora debe administrarse con precaución a pacientes con insuficiencia hepática o renal moderada o grave (ver sección 4.4).
Pacientes con xerostomía:
Se recomienda a los pacientes con xerostomía beber agua para humedecerse la cavidad bucal antes de la administración de Effentora. Si esta recomendación no basta para lograr una efervescencia suficiente, es posible que haya que cambiar de tratamiento.
Pacientes de edad avanzada (mayores de 65 años)
En los ensayos clínicos se ha observado que los pacientes mayores de 65 años necesitan dosis más bajas que los pacientes más jóvenes. Se recomienda especial precaución al ajustar la dosis de Effentora en pacientes de edad avanzada.
Población pediátrica:
No se ha establecido la seguridad y eficacia de Effentora en niños de 0 a 18 años. No se dispone de datos.
Forma de administración
Cuando el comprimido de Effentora se expone a la humedad, inicia una reacción efervescente en la que se libera el principio activo. Por ello debe advertirse a los pacientes que no abran el blister hasta el instante antes de colocarse el comprimido en la cavidad bucal.
Apertura del blister
Se debe explicar al paciente que NO trate de sacar el comprimido presionándolo contra el blister, porque eso puede dañar el comprimido bucal. La forma correcta de sacar el comprimido del blister es la siguiente:
Separar una de las unidades del blister del resto rasgándola por las perforaciones. Seguidamente, doblar la unidad del blister a lo largo de la línea impresa en la lámina posterior. Retirar la lámina posterior para dejar expuesto el comprimido.
También debe pedirse al paciente que no intente triturar ni partir el comprimido.
El comprimido no debe guardarse después de sacarlo del blister, pues no es posible garantizar su integridad ni evitar el riesgo de exposición accidental al medicamento.
Administración del comprimido
Los pacientes deben extraer el comprimido del alveolo blister e inmediatamente colocar el comprimido de Effentora entero en la cavidad bucal (cerca de un molar, entre la mejilla y la encía).
El comprimido de Effentora no debe chuparse, masticarse ni tragarse, ya que eso produciría unas concentraciones plasmáticas más bajas que cuando se disgrega en la boca.
Effentora debe colocarse y mantenerse dentro de la cavidad bucal durante el tiempo necesario para la disgregación del comprimido, que suele tardar unos 14-25 minutos.
Como alternativa el comprimido puede colocarse en el espacio sublingual (ver sección 5.2).
Si al cabo de 30 minutos siguen quedando restos del comprimido de Effentora, podrán tragarse con un vaso de agua.
El periodo de tiempo que tarda el comprimido en disgregarse completamente después de su administración bucal no parece que afecte a la exposición sistémica temprana al fentanilo.
Los pacientes no deben consumir ningún alimento ni bebida mientras tengan el comprimido en la cavidad bucal.
En caso de irritación de la mucosa bucal, se recomienda cambiar el lugar de colocación del comprimido dentro de la cavidad bucal.
4.3 Contraindicaciones
Hipersensibilidad al principio activo o a alguno de los excipientes incluidos en la sección 6.1.
Pacientes que no estén en tratamiento de mantenimiento con opioides, por el mayor riesgo de depresión respiratoria.
Depresión respiratoria grave o enfermedad pulmonar obstructiva grave.
Tratamiento del dolor agudo distinto al dolor irruptivo.
4.4 Advertencias y precauciones especiales de empleo
Debe advertirse a los pacientes y a sus cuidadores que Effentora contiene un principio activo en cantidades que pueden causar la muerte, especialmente a un niño. Por lo tanto todos los comprimidos deben mantenerse fuera de la vista y del alcance de los niños.
Con el fin de minimizar los riesgos de efectos adversos relacionados con los opioides y para establecer la dosis eficaz, es indispensable que los profesionales sanitarios monitoricen cuidadosamente a los pacientes durante el proceso de ajuste de la dosis.
Es importante que el tratamiento con opioides de acción prolongada utilizados para tratar el dolor persistente del paciente se haya estabilizado antes de iniciar el tratamiento con Effentora y que el paciente prosiga el tratamiento con el opioide de larga duración mientras esté tomando Effentora.
Depresión respiratoria
Como con todos los opioides, hay riesgo de depresión respiratoria clínicamente significativa asociada al uso de fentanilo. La selección inapropiada del paciente (ej. uso en pacientes que no reciben tratamiento de mantenimiento con opioides) y/o la dosis incorrecta, ha tenido desenlaces mortales con el uso de Effentora así como con otros productos a base de fentanilo.
Effentora sólo debe ser usado según las condiciones descritas en la sección 4.1.
Enfermedad pulmonar obstructiva crónica
Debe prestarse especial atención al ajuste de la dosis de Effentora en pacientes con enfermedad pulmonar obstructiva crónica no grave u otras afecciones que les predispongan a una depresión respiratoria, ya que incluso las dosis terapéuticas habituales de Effentora pueden reducir el impulso respiratorio hasta provocar insuficiencia respiratoria.
Aumento de la presión intracraneal, alteración del estado de conciencia
Effentora sólo debe administrarse con precaución extrema en pacientes que puedan ser especialmente sensibles a los efectos intracraneales de la retención de CO2, como aquellos con un aumento constatado de la presión intracraneal o con alteración del estado de conciencia. Los opioides pueden enmascarar la evolución clínica de un paciente con lesiones en la cabeza, y sólo deben utilizarse si están clínicamente justificados.
Enfermedad cardíaca
El fentanilo puede provocar bradicardia y debe administrarse con precaución en pacientes con bradiarritmias previas o ya existentes.
Insuficiencia renal o hepática
Además, Effentora debe administrarse con precaución a pacientes con insuficiencia hepática o renal. No se ha valorado la influencia de la insuficiencia hepática o renal sobre la farmacocinética del medicamento; sin embargo, cuando éste se administra por vía intravenosa, se ha comprobado que el aclaramiento del fentanilo está alterado en las enfermedades hepáticas y renales debido a la alteración del aclaramiento metabólico y de las proteínas plasmáticas. Tras la administración de Effentora, la insuficiencia hepática y la insuficiencia renal pueden ambas aumentar la biodisponibilidad del fentanilo ingerido y disminuir su aclaramiento sistémico, lo cual puede aumentar y prolongar los efectos opioides. Así pues, debe prestarse especial atención al ajuste de la dosis en pacientes con enfermedad hepática o renal moderada o grave.
Se deben tomar precauciones especiales en pacientes con hipovolemia e hipotensión.
Sindrome serotoninérgico
Se recomienda precaución cuando Effentora se administre de forma concomitante con fármacos que afecten a los sistemas de neurotransmisores serotoninérgicos.
El desarrollo de un síndrome serotoninérgico potencialmente mortal puede aparecer con el uso concomitante de fármacos serotoninérgicos, como los inhibidores selectivos de la recaptación de serotonina (ISRS) y los inhibidores de la recaptación de serotonina y noradrenalina (IRSN), y con los fármacos que afectan al metabolismo de la serotonina (incluidos los inhibidores de la monoamino oxidasa [IMAO]). Esto puede ocurrir con la dosis recomendada.
El síndrome serotoninérgico puede incluir cambios en el estado mental (p. ej., agitación, alucinaciones, coma), inestabilidad autonómica (p. ej., taquicardia, presión arterial lábil, hipertermia), anomalías neuromusculares (p. ej., hiperreflexia, descoordinación, rigidez) y/o síntomas gastrointestinales (p. ej., náuseas, vómitos, diarrea).
Si se sospecha de un síndrome serotoninérgico, debe suspenderse el tratamiento con Effentora. Tolerancia, dependencia
La administración repetida de opioides como el fentanilo puede inducir tolerancia y dependencia física y/o psicológica. Sin embargo, rara vez se produce adicción iatrogénica por el uso terapéutico de opioides.
Dietas pobres en sodio
Este medicamento contiene 10 mg de sodio por comprimido, lo que debe ser tenido en cuenta en pacientes con dietas pobres en sodio.
Anafilaxia e hipersensibilidad
Se han notificado anafilaxia e hipersensibilidad asociados al uso de medicamentos de fentanilo por vía oral transmucosa (ver sección 4.8)
4.5 Interacción con otros medicamentos y otras formas de interacción
El fentanilo se metaboliza por medio del sistema del isoenzima 3A4 del citocromo P450 (CYP3A4), por lo que pueden producirse interacciones cuando Effentora se administra concomitantemente con fármacos que afectan a la actividad de CYP3A4. La administración concomitante de fármacos que inducen la actividad 3A4 puede reducir la eficacia de Effentora. El uso concomitante de Effentora con inhibidores potentes del CYP3A4 (como ritonavir, ketoconazol, itraconazol, troleandomicina, claritromicina y nelfinavir) o inhibidores moderados del CYP3A4 (como aprenavir, aprepitant, diltiazem, eritromicina, fluconazol, fosamprenavir, zumo de pomelo y verapamilo) puede aumentar la concentración plasmática de fentanilo, causando en ocasiones reacciones adversas graves, incluida una depresión respiratoria mortal. Los pacientes que reciban Effentora e inhibidores moderados o potentes del CYP3A4 concomitantemente deben controlarse estrictamente durante un amplio período de tiempo. El aumento de la dosis debe realizarse con precaución.
El uso concomitante con otros depresores del sistema nervioso central, incluidos otros opioides, sedantes o hipnóticos, anestésicos generales, fenotiazinas, tranquilizantes, relajantes musculares, antihistamínicos sedantes y alcohol, puede producir efectos depresivos aditivos.
No se recomienda el uso de Effentora en pacientes que hayan recibido inhibidores de la monoamino oxidasa (MAO) en los 14 días anteriores, porque se ha descrito que los inhibidores de la MAO producen una potenciación grave e impredecible de los analgésicos opioides.
No se recomienda el uso concomitante de agonistas/antagonistas opioides parciales (p.ej. buprenorfina, nalbufina, pentazocina) ya que poseen una elevada afinidad por los receptores opioides con una actividad intrínseca relativamente baja y en consecuencia antagonizan parcialmente el efecto analgésico del fentanilo, pudiendo inducir síntomas de abstinencia en pacientes dependientes de opioides.
Fármacos serotoninérgicos
La administración concomitante de fentanilo con un fármaco serotoninérgico, como un inhibidor selectivo de la recaptación de serotonina (ISRS), un inhibidor de la recaptación de serotonina y noradrenalina (IRSN) o un inhibidor de la monoamino oxidasa (IMAO), puede aumentar el riesgo de síndrome serotoninérgico, un trastorno potencialmente mortal.
4.6 Fertilidad, embarazo y lactancia
Embarazo
No hay datos suficientes relativos al uso de de fentanilo en mujeres embarazadas. Los estudios realizados en animales han mostrado toxicidad para la reproducción (ver sección 5.3). Se desconoce el riesgo potencial en seres humanos. No debe utilizarse Effentora durante el embarazo a no ser que fuese absolutamente necesario.
El tratamiento prolongado durante el embarazo puede causar síntomas de abstinencia en el recién nacido.
Se aconseja no administrar fentanilo durante el parto (aunque sea por cesárea), ya que atraviesa la placenta y puede causar depresión respiratoria en el feto. Si se administra Effentora, debe disponerse fácilmente de un antídoto para el niño.
Lactancia
El fentanilo se excreta a través de la leche materna y puede causar sedación y depresión respiratoria en el lactante. El fentanilo no debe utilizarse durante la lactancia, no pudiendo reiniciarse la lactancia hasta transcurridos como mínimo 5 días de la última administración de fentanilo.
Fertilidad
No existen datos sobre la fertilidad en humanos. En los estudios realizados con animales, la fertilidad en machos se vio afectada (ver sección 5.3).
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
No se han realizado estudios de los efectos sobre la capacidad para conducir y utilizar máquinas. No obstante, los analgésicos opioides pueden disminuir la capacidad mental y/o física necesaria para realizar tareas potencialmente peligrosas (p. ej., conducir un coche o utilizar maquinaria). Debe advertirse a los pacientes de que no conduzcan ni utilicen maquinaria si sienten somnolencia, mareos o alteraciones visuales mientras toman Effentora, y de que no conduzcan ni utilicen maquinaria hasta que no sepan cómo van a reaccionar.
4.8 Reacciones adversas
Resumen del perfil de seguridad
Las reacciones adversas que pueden esperarse de Effentora son las típicas de los opioides. Frecuentemente, esos efectos adversos propios de los opioides cesan o disminuyen en intensidad con el uso continuado del medicamento, o con el ajuste de la dosis más adecuada para el paciente. No obstante, las reacciones adversas más graves son depresión respiratoria (que potencialmente puede culminar en apnea o parada respiratoria), depresión circulatoria, hipotensión y colapso, reacciones que deben vigilarse estrechamente en todos los pacientes.
Los ensayos clínicos con Effentora se diseñaron para valorar la seguridad y eficacia en el tratamiento del DI, y todos los pacientes tomaban ya opioides de forma concomitante, como morfina de liberación prolongada o fentanilo transdérmico, para su dolor persistente. Por consiguiente, no es posible distinguir con exactitud los efectos de Effentora solo.
Tabla de reacciones adversas
Se han notificado las siguientes reacciones adversas con Effentora y/u otros compuestos que contienen fentanilo provenientes de ensayos clínicos y de la experiencia postcomercialización . Las reacciones adversas se enumeran a continuación según el término preferente de MedDRA por el sistema de clasificación de órganos y frecuencia (frecuencias se definen como: muy frecuentes >1/10, frecuentes >1/100 a <1/10, poco frecuentes > 1/1.000 a < 1/100, raras >1/10.000 a <1/1.000, frecuencia no conocida (no puede estimarse a partir de los datos disponibles); las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada intervalo de frecuencia):
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Infecciones e infestaciones |
Candidiasis oral |
Faringitis |
Pústula oral | ||
|
Trastornos de la sangre y del sistema linfático |
Anemia Neutropenia |
Trombocito- penia | |||
|
Trastornos del sistema inmunológico |
Hipersensibili dad | ||||
|
Trastornos endocrinos |
Hipogonadismo | ||||
|
Trastornos del metabolismo y de la nutrición |
Anorexia |
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Trastornos psiquiátricos |
Depresión Ansiedad Estado confusional Insomnio |
Euforia Nerviosismo Alucinaciones Alucinaciones visuales Cambios del estado mental Drogodependen cia (adicción) Desorientación | |||
|
Trastornos del sistema nervioso |
Mareo Cefalea |
Disgeusia Somnolencia Letargia Temblores Sedación Hipoestesia Migraña |
Nivel de conciencia deprimido Trastornos de la atención Trastorno del equilibrio Disartria |
Trastorno cognitivo Disfunción motora |
Pérdida de consciencia Convulsión |
|
Trastornos oculares |
Alteraciones de la visión Hiperemia ocular Visión borrosa Disminución de la agudeza visual |
Sensación anómala en el ojo Fotopsia | |||
|
Trastornos del oído y del laberinto |
Vértigo Acúfenos Molestias en el oído | ||||
|
Trastornos cardiacos |
Taquicardia |
Bradicardia | |||
|
Trastornos vasculares |
Hipotensión Hipertensión |
Enrojecimiento Sofocos | |||
|
Trastornos respiratorios, torácicos y mediastínicos |
Disnea Dolor faringolaríng eo |
Depresión respiratoria Síndrome de apnea del sueño |
Paro respiratorio | ||
|
Trastornos gastrointestinales |
Náuseas Vómitos |
Estreñimient o Estomatitis Sequedad de boca Diarrea Dolor abdominal Enfermedad por reflujo gastroesofági co Molestias estomacales Dispepsia Dolor dental |
Íleo Ulceración de la boca Hipoestesia oral Molestias orales Decoloración de la mucosa oral Trastorno de los tejidos blandos de la boca Glosodinia Ampollas en la lengua Dolor gingival Ulceración de la lengua |
Ampollas en la mucosa oral Labios secos |
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Trastornos de la lengua Esofagitis Labios agrietados Trastornos dentales | |||||
|
Trastornos hepatobiliares |
Dilatación biliar | ||||
|
Trastornos de la piel y del tejido subcutáneo |
Prurito Hiperhidrosis Rash |
Sudor frío Edema facial Prurito generalizado Alopecia |
Onicorrexia | ||
|
Trastornos musculoesquelético s y del tejido conjuntivo |
Mialgia Dolor de espalda |
Calambres musculares Debilidad muscular | |||
|
Trastornos renales y urinarios |
Retención urinaria | ||||
|
Trastornos generales y alteraciones en el lugar de administración |
Reacciones en el lugar de la aplicación, como sangrado, dolor, úlcera, irritación, parestesia, anestesia, eritema, edema, hinchazón y vesículas |
Edema periférico Fatiga Astenia Síndrome de abstinencia Escalofríos |
Malestar general Pereza Molestias en el pecho Sensaciones anormales Sensación de inquietud Sed Sensación de frío Sensación de calor |
Pirexia | |
|
Exploraciones complementarias |
Disminución de peso |
Descenso del recuento de plaquetas Aumento de la frecuencia cardiaca Descenso del hematocrito Descenso de la hemoglobina | |||
|
Lesiones traumáticas, intoxicaciones y complicaciones de procedimientos terapéuticos |
Caídas |
Descripción de las reacciones adversas seleccionadas
Tras la administración repetida de opioides como fentanilo puede desarrollarse tolerancia, dependencia física y/o psicológica.
Con fentanilo por vía transmucosa se han observado síntomas de abstinencia de opioides tales como náuseas, vómitos, diarrea, ansiedad, escalofríos, temblor y sudoración.
Se han observado pérdida de consciencia y paro respiratorio en el contexto de una sobredosis.
Se han notificado reacciones de hipersensibilidad en la experiencia postcomercialización, incluidos prurito, eritema, edema labial y facial y urticaria.
Notificación de sospechas de reacciones adversas
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del. sistema nacional de notificación incluido en el Anexo V.
4.9 Sobredosis
Los síntomas de sobredosis con fentanilo son de naturaleza similar a los del fentanilo intravenoso y a los demás opioides, y son una prolongación de sus acciones farmacológicas, siendo los efectos graves más significativos la alteración del estado mental, pérdida de la consciencia, hipotensión, la depresión respiratoria, distrés respiratorio y el fallo respiratorio con resultado de muerte.
El tratamiento inmediato en caso de sobredosis de opioides consiste en retirar el comprimido bucal de Effentora, si el paciente todavía lo tiene en la boca, asegurando la apertura de las vías respiratorias; estimulación física y verbal del paciente; valoración del grado de conciencia, el estado ventilatorio y circulatorio; y respiración asistida (soporte ventilatorio) en caso necesario.
Para el tratamiento de una sobredosis (ingestión accidental) en una persona que no haya tomado nunca opioides, se debe colocar una vía intravenosa y utilizar naloxona u otros antagonistas de los opioides según esté indicado clínicamente. La depresión respiratoria causada por la sobredosis puede durar más que los efectos de la acción del antagonista de los opioides (así, la semivida de la naloxona varía de 30 a 81 minutos), por lo que puede ser necesaria la administración repetida. Consultar los detalles sobre este tipo de uso en la ficha técnica o resumen de las características del producto del antagonista de los opioides utilizado.
Para el tratamiento de una sobredosis en pacientes mantenidos con opioides, debe colocarse una vía intravenosa. El uso moderado de naloxona u otro antagonista opioide puede estar justificado en algunos casos, pero se asocia al riesgo de precipitar la aparición de un síndrome de abstinencia agudo.
Aunque no se ha observado rigidez muscular que interfiera con la respiración después del uso de Effentora, es una reacción que puede manifestarse con fentanilo y otros opioides. Si aparece, debe tratarse con respiración asistida, un antagonista de los opioides y, como último recurso, un agente bloqueante neuromuscular.
5. PROPIEDADES FARMACOLÓGICAS
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: analgésicos; opioides Código ATC: N02AB03.
El fentanilo es un analgésico opioide que actúa principalmente sobre los receptores de opioide p. Sus efectos terapéuticos principales son la analgesia y la sedación. Los efectos farmacológicos secundarios son depresión respiratoria, bradicardia, hipotermia, estreñimiento, miosis, dependencia física y euforia.
Los efectos analgésicos del fentanilo están relacionados con su concentración plasmática. En general, la concentración eficaz y la concentración a la que aparece toxicidad aumentan a medida que aumenta la tolerancia a los opioides. La velocidad de aparición de tolerancia varía mucho de una persona a otra. En consecuencia, la dosis de Effentora debe ajustarse individualmente para conseguir el efecto deseado (ver sección 4.2).
Todos los agonistas de los receptores de opioides p, entre ellos el fentanilo, producen depresión respiratoria dependiente de la dosis. El riesgo de depresión respiratoria es menor en pacientes que reciben tratamiento crónico con opioides, puesto que desarrollan tolerancia a los efectos de depresión respiratoria.
La seguridad y eficacia de Effentora se han evaluado en pacientes que recibieron el medicamento al inicio de un episodio de dolor irruptivo. El uso preventivo de Effentora para episodios de dolor predecibles no se ha investigado en ensayos clínicos. Se han realizado dos ensayos doble ciego, aleatorizados, controlados con placebo y cruzados en un total de 248 pacientes con DI y cáncer que experimentaron una media de 1-4 episodios de DI al día durante el tratamiento de mantenimiento con opioides. Durante una fase inicial abierta, se ajustó la dosis en cada paciente hasta establecer la dosis eficaz de Effentora. Los pacientes en los que se estableció una dosis eficaz entraron en la fase doble ciego del estudio. El criterio principal de eficacia fue la valoración por el propio paciente de la intensidad del dolor. Los pacientes valoraron la intensidad del dolor utilizando una escala de 11 puntos. En cada episodio de DI se evaluó la intensidad del dolor antes y en varias ocasiones después del tratamiento.
En el 67% de los pacientes se pudo establecer una dosis eficaz.
En el ensayo clínico pivotal (ensayo 1), el criterio de valoración principal fue la media de la suma de las diferencias en los valores de la intensidad del dolor desde el momento de administrar la dosis hasta 60 minutos después, inclusive (SPID60), que fue estadísticamente significativa respecto a placebo
(p<0,0001).
Ensayo 1: Media (+/- EEM) Diferencias en intensidad del dolor en cada valoración
(Sene completa de análisis)
SPID60 media (+/- DE)
EFFENTORA=9,7(5,58) p<0,0001 Placebo=4,9(4,38)
......I
120
Tiempo transcurndo desde la administración de la medicación del ensayo (minutos)
Grupo de tratamiento
EFFENTORA
Placebo
+ p<0,0001 Effentora frente a placebo, a favor de Effentora, mediante un análisis de la varianza
DID=diferencia en intensidad del dolor; KKY1 error estándar de la media
(Sene completa de análisis)
SPID30 media (+/- DE)
EFFENTORA=3,2(2,60) p<0,0001
Placebo=2,0(2,21)
O 5 10 15 30 45 60 90 120
Tiempo transcurrido desde la administración de la medicación del ensayo (minutos)
Grupo de tratamiento xxx EFFENTORA *** Placebo
* p<0,01 Effentora frente a placebo, a favor de Effentora, mediante una prueba de rangos con signo de Wilcoxon para una sola muestra
+ p<0,0001 Effentora frente a placebo, a favor de Effentora, mediante una prueba de rangos con signo de Wilcoxon para una sola muestra
DID=diferencia en intensidad del dolor: EEM=error estándar de la media
En el segundo estudio fundamental (ensayo 2), el criterio de valoración principal fue SPID30, que fue también estadísticamente significativo respecto a placebo (p<0,0001).
Se observó una mejora estadísticamente significativa en la diferencia de intensidad del dolor con Effentora frente a placebo ya a los 10 minutos en el Ensayo 1 y a los 15 minutos (primer punto temporal medido) en el Ensayo 2. En los dos ensayos, esas diferencias siguieron siendo significativas en todos los puntos temporales medidos.
5.2 Propiedades farmacocinéticas
Introducción general
El fentanilo es altamente lipofílico y puede ser absorbido muy rápidamente a través de la mucosa bucal y más lentamente por la vía gastrointestinal convencional. Está sujeto a un efecto de primer paso hepático e intestinal, y los metabolitos no contribuyen a los efectos terapéuticos del fentanilo.
La forma de liberación del principio activo se basa en una reacción efervescente que aumenta la velocidad y el grado de absorción del fentanilo a través de la mucosa bucal. Los cambios transitorios en el pH que acompañan a la reacción efervescente pueden optimizar la disolución (a un pH menor) y la permeabilidad de la membrana (a un pH mayor).
El tiempo de disolución (definido como el tiempo que tarda el comprimido en disgregarse totalmente tras su administración bucal) no afecta a la exposición sistémica temprana al fentanilo. El estudio comparativo entre la administración bucal (es decir entre la encía y la mejilla) y la administración sublingual de un comprimido de 400 mcg de Effentora cumplió los criterios de bioequivalencia.
No se han estudiado los efectos de la insuficiencia renal o hepática sobre la farmacocinética de Effentora.
Absorción:
Tras la administración bucal de Effentora, el fentanilo es absorbido rápidamente con una biodisponibilidad absoluta del 65%. El perfil de absorción de Effentora es, en su mayor parte, el resultado de una absorción rápida inicial a través de la mucosa bucal; las concentraciones plasmáticas máximas según las muestras de sangre venosa suelen alcanzarse generalmente en el transcurso de la hora siguiente a la administración bucal. Alrededor del 50% de la dosis total administrada se absorbe rápidamente por la mucosa bucal y pasa a la circulación sistémica. La otra mitad de la dosis total se traga y se absorbe lentamente en el tubo digestivo. Casi el 30% de la cantidad tragada (50% de la dosis total) escapa a la eliminación hepática e intestinal de primer paso y pasa a estar disponible sistémicamente.
En la siguiente tabla se indican los principales parámetros farmacocinéticos.
Parámetros_farmacocinéticos* en sujetos adultos tratados con Effentora
|
Parámetro farmacocinético (media) |
Effentora 400 microgramos |
|
Biodisponibilidad absoluta |
65% (±20%) |
|
Fracción absorbida por la mucosa |
48% (±31,8%) |
|
Tmax (minuto) ** |
46,8 (20-240) |
|
Cmax (ng/ml) |
1,02 (± 0,42) |
|
AUC0-tmax (ng.h/ml) |
0,40 (± 0,18) |
|
AUC0-inf (ng.h/ml) |
6,48 (± 2,98) |
* Basado en muestras de sangre venosa (plasma). Las concentraciones de citrato de fentanilo en suero fueron superiores a las obtenidas en plasma: La AUC y la Cmax séricas fueron superiores a la AUC y la Cmax plasmáticas aproximadamente en un 20% y un 30%, respectivamente. Se desconoce la razón de dicha diferencia.
** Datos de Tmax presentados como mediana (rango).
En estudios farmacocinéticos que compararon la biodisponibilidad absoluta y relativa de Effentora y del citrato de fentanilo bucal (CFB), la velocidad y el grado de absorción del fentanilo de Effentora demostraron que la exposición era un 30%-50% mayor que la obtenida con el citrato de fentanilo transmucosa. Si se cambia desde otro producto de citrato de fentanilo oral, se precisa un ajuste de la dosis independiente con Effentora puesto que la biodisponibilidad difiere notablemente de uno a otro producto. Sin embargo, en estos pacientes se puede considerar una dosis inicial mayor de 100 microgramos.
Concentración plasmática media frente a tiempo Perfiles tras la administración de dosis únicas de EFFENTORA y CFB en sujetos sanos
-©- 400 mcg EFFENTORA
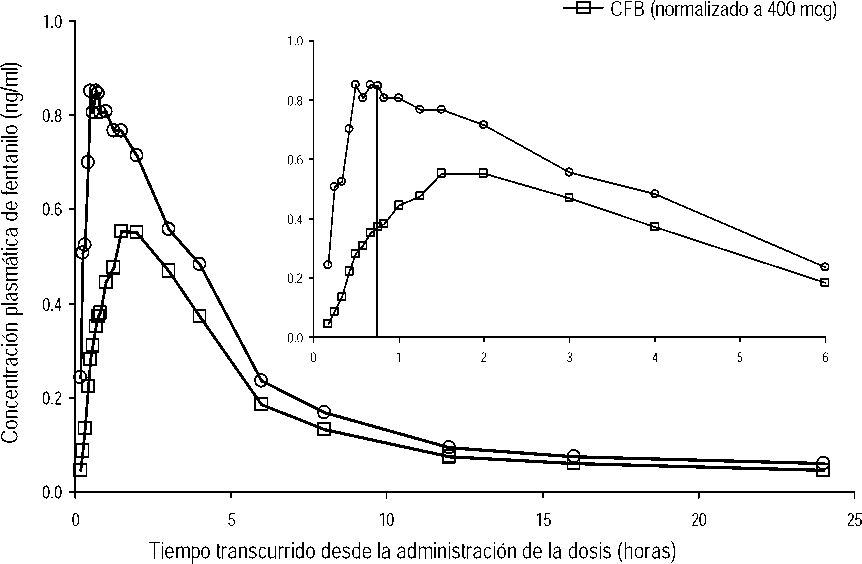
Los datos de CFB se presentan ajustados (de 800 mcg a 400 mcg).
En un ensayo clínico de pacientes con mucositis de grado 1, se observaron diferencias en la exposición con Effentora. La Cmax y la AUC0-8 fueron entre un 1% y un 25% mayores en los pacientes con mucositis que en los pacientes sin mucositis, respectivamente. Las diferencias observadas no fueron clínicamente significativas.
Distribución
El fentanilo es altamente lipofílico y se distribuye rápidamente fuera del sistema vascular, con un elevado volumen de distribución aparente. Tras la administración bucal de Effentora, el fentanilo experimenta una rápida distribución inicial que representa un equilibrio del fentanilo entre el plasma y los tejidos altamente perfundidos (cerebro, corazón y pulmones). Posteriormente, el fentanilo se redistribuye entre el compartimiento de los tejidos profundos (músculos y tejido adiposo) y el plasma.
La unión del fentanilo a las proteínas plasmáticas es del 80% al 85%. La principal proteína de unión es la alfa-1-ácido-glucoproteína, si bien tanto la albúmina como las lipoproteínas contribuyen en cierta medida. La fracción libre de fentanilo aumenta con la acidosis.
Biotransformación
En los ensayos clínicos no se han caracterizado las rutas metabólicas tras la administración bucal de Effentora. El fentanilo se metaboliza a norfentanilo en el hígado y en la mucosa intestinal por acción de la isoforma CYP3A4. El norfentanilo no es activo farmacológicamente en los estudios en animales. Más del 90% de la dosis administrada de fentanilo se elimina por biotransformación en metabolitos inactivos N-desalquilados e hidroxilados.
Eliminación
Tras la administración intravenosa de fentanilo, menos del 7% de la dosis administrada se elimina inalterada en la orina, y solamente un 1% se excreta inalterada en las heces. Los metabolitos se excretan principalmente en la orina, mientras que la excreción fecal es menos importante.
Tras la administración de Effentora, la fase de eliminación terminal de fentanilo es el resultado de la redistribución entre el plasma y el compartimiento de los tejidos profundos. Esta fase de eliminación es lenta, con una mediana de la semivida de eliminación terminal t1/2 de aproximadamente 22 horas tras la administración bucal de la formulación efervescente y de aproximadamente 18 horas tras la administración intravenosa. El aclaramiento en plasma total del fentanilo después de la administración intravenosa es aproximadamente de 42 l/h.
Linealidad/no linealidad
Se ha demostrado la proporcionalidad de la dosis desde 100 microgramos hasta 1.000 microgramos.
5.3 Datos preclínicos sobre seguridad
Los datos de los estudios no clínicos no muestran riesgos especiales para los seres humanos según los estudios convencionales de farmacología de seguridad, toxicidad a dosis repetidas, genotoxicidad y carcinogenicidad.
Los estudios de toxicidad del desarrollo embrionario y fetal llevados a cabo en ratas y conejos no evidenciaron malformaciones ni alteraciones del desarrollo inducidas por el fármaco, administrado durante el período de la organogénesis.
En un estudio de fertilidad y desarrollo embrionario temprano, en ratas, se observó un efecto asociado a los machos a altas dosis (300 mcg/kg/día s.c.) y se considera secundario a los efectos sedantes del fentanilo en estudios animales.
En estudios sobre el desarrollo pre y postnatal en ratas, la tasa de supervivencia de la progenie se redujo significativamente a dosis que causaban toxicidad materna severa. Los hallazgos adicionales en las crías de la generación F1, tras dosis maternales tóxicas, fueron retraso del desarrollo físico, de las funciones sensoriales, reflejos y comportamiento. Dichos efectos pueden ser indirectos debidos a una alteración de los cuidados maternos y/o disminución de la frecuencia de la lactancia o bien un efecto directo del fentanilo sobre las crías.
Los estudios de carcinogenicidad (bioensayo dérmico alternativo de 26 semanas en ratones transgénicos Tg.AC; estudio de carcinogenicidad subcutánea de 2 años en ratas) con fentanilo no pusieron de manifiesto ningún hallazgo indicativo de potencial oncogénico. La evaluación de los cortes laminares de cerebro del estudio de carcinogenicidad en ratas mostró lesiones cerebrales en los animales tratados con dosis altas de citrato de fentanilo. Se desconoce la relevancia de estos hallazgos para los seres humanos.
6. DATOS FARMACÉUTICOS
6.1 Lista de excipientes
Manitol
Carboximetilalmidón sódico tipo A Hidrogenocarbonato de sodio Carbonato de sodio anhidro Ácido cítrico anhidro Estearato de magnesio
6.2 Incompatibilidades
No procede.
6.3 Periodo de validez
3 años
6.4 Precauciones especiales de conservación
Conservar en el embalaje original para protegerlo de la humedad.
6.5 Naturaleza y contenido del envase
Blister laminado de PVC/lámina de aluminio/poliamida/PVC con cierre de papel/poliéster.
Los blister se presentan en cajas de 4 ó 28 comprimidos. Puede que solamente estén comercializados algunos tamaños de envases.
6.6 Precauciones especiales de eliminación
Hay que explicar a los pacientes y a sus cuidadores que desechen todos los comprimidos sin abrir que les sobren cuando ya no necesiten más el tratamiento.
La eliminación del medicamento utilizado o no utilizado pero que ya no se necesita y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V.
Swensweg 5 2031 GA Haarlem Países Bajos
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/08/441/001 -002
9. FECHA DE LA PRIMERA AUTORIZACIÓN/RENOVACIÓN DE LA
AUTORIZACIÓN
Fecha de la primera autorización: 20 febrero 2013
10. FECHA DE LA REVISIÓN DEL TEXTO
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos http://www.ema.europa.eu.
1. NOMBRE DEL MEDICAMENTO
Effentora 200 microgramos comprimidos bucales
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada comprimido bucal contiene 200 microgramos de fentanilo (como citrato).
Excipiente(s) con efecto conocido: Cada comprimido contiene 20 mg de sodio. Para consultar la lista completa de excipientes, ver sección 6.1.
3. FORMA FARMACÉUTICA
Comprimido bucal.
Comprimido de caras planas, de color blanco, redondo y con bordes biselados, con una "C” grabado en una cara y en la otra con “2”
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
Effentora está indicado para el tratamiento del dolor irruptivo (DI) en pacientes adultos con cáncer que ya reciben tratamiento de mantenimiento con opioides para el dolor crónico asociado a cáncer.
El DI es una exacerbación transitoria del dolor que se produce sobre un fondo de dolor persistente controlado por otros medios.
Los pacientes que reciben tratamiento de mantenimiento con opioides son los que toman como mínimo 60 mg de morfina oral diarios, 25 microgramos de fentanilo transdérmico cada hora, 30 mg de oxicodona diarios, 8 mg de hidromorfona oral diarios o una dosis equianalgésica de otro opioide durante una semana o más.
4.2 Posología y forma de administración
El tratamiento debe ser instaurado y seguido bajo las directrices de un médico experimentado en la terapia con opioides en pacientes con cáncer. Los médicos deben considerar el riesgo del abuso del fentanilo. Se debe advertir al paciente que no debe utilizar dos concentraciones diferentes de fentanilo al mismo tiempo para el tratamiento del dolor irruptivo y que debe desechar cualquier producto de fentanilo prescrito para el dolor irruptivo cuando cambie a Effentora. Con objeto de prevenir confusiones y posibles sobredosis, los pacientes deben disponer en cada momento del mínimo número de concentraciones de los comprimidos.
Posología
Ajuste de la dosis
Effentora debe ajustarse de forma individual hasta obtener una dosis “eficaz” que proporcione la analgesia adecuada y minimice las reacciones adversas. En los ensayos clínicos, la dosis eficaz de Effentora para el DI no pudo predecirse a partir de la dosis diaria de mantenimiento de opioides.
Los pacientes deben monitorizarse cuidadosamente hasta que se establezca la dosis eficaz.
Ajuste de la dosis en pacientes que no cambian a Effentora desde otros medicamentos que contienen fentanilo
La dosis inicial de Effentora debe ser de 100 microgramos, que se incrementará según sea necesario dentro del rango de concentraciones de dosificación disponibles (100, 200, 400, 600 y 800 microgramos).
Ajuste de la dosis en pacientes que cambian a Effentora tras recibir otros medicamentos que contienen fentanilo
Debido a los diferentes perfiles de absorción, el cambio no debe hacerse en una proporción de 1:1. Si el cambio se hace desde otro medicamento de fentanilo como citrato oral, se precisa un ajuste de la dosis independiente con Effentora puesto que la biodisponibilidad difiere notablemente de un medicamento a otro. Sin embargo, en estos pacientes se puede considerar una dosis inicial mayor de 100 microgramos.
Proceso de ajuste de la dosis
Durante el ajuste de la dosis, si no se consigue una analgesia adecuada en los 30 minutos siguientes a la administración de un único comprimido, puede administrarse un segundo comprimido de Effentora de la misma concentración.
Si para tratar un episodio de DI se precisa más de un comprimido, para el tratamiento de futuros episodios de DI debe considerarse un aumento de la dosis hasta la siguiente concentración disponible.
Durante el proceso de ajuste de la dosis, se pueden combinar diferentes comprimidos. Se pueden utilizar hasta cuatro comprimidos de 100 microgramos o hasta cuatro comprimidos de 200 microgramos para tratar un episodio aislado de DI durante el proceso de ajuste de la dosis de acuerdo con el siguiente esquema:
• Si el comprimido inicial de 100 microgramos no es eficaz, se podrá prescribir al paciente dos comprimidos de 100 microgramos para tratar el siguiente episodio de DI. Se recomienda colocar un comprimido a cada lado de la boca. Si se establece que esa es la dosis eficaz, los futuros episodios de DI podrán seguir tratándose con un único comprimido de Effentora de
200 microgramos.
• Si un único comprimido de Effentora de 200 microgramos (o dos comprimidos de 100 microgramos) no resulta eficaz, podrá prescribirse al paciente dos comprimidos de
200 microgramos (o cuatro comprimidos de 100 microgramos) para tratar el siguiente episodio de DI. Se recomienda colocar dos comprimidos a cada lado de la boca. Si se considera que esa es la dosis eficaz, los futuros episodios de DI podrán seguir tratándose con un único comprimido de Effentora de 400 microgramos.
• Para el ajuste de la dosis con comprimidos de 600 microgramos y 800 microgramos, deben utilizarse comprimidos de 200 microgramos.
En los ensayos clínicos no se evaluaron dosis de más de 800 microgramos.
No deben utilizarse más de dos comprimidos para tratar un mismo episodio de DI, salvo cuando el ajuste de la dosis se realice utilizando cuatro comprimidos, como se ha explicado antes.
Durante el ajuste de la dosis, los pacientes deben esperar al menos 4 horas antes de tratar otro episodio de DI con Effentora.
Tratamiento de mantenimiento
Una vez determinada la dosis eficaz por medio del proceso de ajuste, los pacientes deben mantener esa dosis y limitar el consumo a un solo comprimido con la concentración que corresponda.
Los episodios de dolor irruptivo pueden variar en intensidad y la dosis de Effentora requerida puede aumentar con el tiempo debido a una progresión de la enfermedad oncológica subyacente. En estos casos se puede utilizar un segundo comprimido de Effentora de la misma concentración.
En caso de que se necesite un segundo comprimido de Effentora en diversas ocasiones consecutivas, se deberá reajustar la dosis de mantenimiento habitual (ver más abajo).Durante el tratamiento de mantenimiento, los pacientes deben esperar al menos 4 horas antes de tratar otro episodio de DI con Effentora.
Reajuste de la dosis
La dosis de mantenimiento de Effentora debe aumentarse si el paciente necesita más de un comprimido por episodio de DI en varios episodios consecutivos de DI. Para el reajuste de la dosis se aplican los mismos principios descritos para Ajuste de la dosis (ver más arriba).
Si el paciente presenta con frecuencia más de cuatro episodios de DI en 24 horas, se debe volver a calcular la dosis del tratamiento de mantenimiento con opioides.
Interrupción del tratamiento
El tratamiento con Effentora se debe interrumpir inmediatamente si el paciente ya no presenta episodios de dolor irruptivo. El tratamiento del dolor de base persistente se debe mantener tal como estaba prescrito.
Si es necesario interrumpir la totalidad del tratamiento con opioides, el médico debe realizar un estrecho seguimiento del paciente con el fin de controlar el riesgo de efectos abruptos de abstinencia.
Pacientes con insuficiencia hepática o renal:
Effentora debe administrarse con precaución a pacientes con insuficiencia hepática o renal moderada o grave (ver sección 4.4).
Pacientes con xerostomía:
Se recomienda a los pacientes con xerostomía beber agua para humedecerse la cavidad bucal antes de la administración de Effentora. Si esta recomendación no basta para lograr una efervescencia suficiente, es posible que haya que cambiar de tratamiento.
Pacientes de edad avanzada (mayores de 65 años)
En los ensayos clínicos se ha observado que los pacientes mayores de 65 años necesitan dosis más bajas que los pacientes más jóvenes. Se recomienda especial precaución al ajustar la dosis de Effentora en pacientes de edad avanzada.
Población pediátrica:
No se ha establecido la seguridad y eficacia de Effentora en niños de 0 a 18 años. No se dispone de datos.
Forma de administración
Cuando el comprimido de Effentora se expone a la humedad, inicia una reacción efervescente en la que se libera el principio activo. Por ello debe advertirse a los pacientes que no abran el blister hasta el instante antes de colocarse el comprimido en la cavidad bucal.
Apertura del blister
Se debe explicar al paciente que NO trate de sacar el comprimido presionándolo contra el blister, porque eso puede dañar el comprimido bucal. La forma correcta de sacar el comprimido del blister es la siguiente:
Separar una de las unidades del blister del resto rasgándola por las perforaciones. Seguidamente, doblar la unidad del blister a lo largo de la línea impresa en la lámina posterior. Retirar la lámina posterior para dejar expuesto el comprimido.
También debe pedirse al paciente que no intente triturar ni partir el comprimido.
El comprimido no debe guardarse después de sacarlo del blister, pues no es posible garantizar su integridad ni evitar el riesgo de exposición accidental al medicamento.
Administración del comprimido
Los pacientes deben extraer el comprimido del alveolo blister e inmediatamente colocar el comprimido de Effentora entero en la cavidad bucal (cerca de un molar, entre la mejilla y la encía).
El comprimido de Effentora no debe chuparse, masticarse ni tragarse, ya que eso produciría unas concentraciones plasmáticas más bajas que cuando se disgrega en la boca.
Effentora debe colocarse y mantenerse dentro de la cavidad bucal durante el tiempo necesario para la disgregación del comprimido, que suele tardar unos 14-25 minutos.
Como alternativa el comprimido puede colocarse en el espacio sublingual (ver sección 5.2).
Si al cabo de 30 minutos siguen quedando restos del comprimido de Effentora, podrán tragarse con un vaso de agua.
El periodo de tiempo que tarda el comprimido en disgregarse completamente después de su administración bucal no parece que afecte a la exposición sistémica temprana al fentanilo.
Los pacientes no deben consumir ningún alimento ni bebida mientras tengan el comprimido en la cavidad bucal.
En caso de irritación de la mucosa bucal, se recomienda cambiar el lugar de colocación del comprimido dentro de la cavidad bucal.
4.3 Contraindicaciones
Hipersensibilidad al principio activo o a alguno de los excipientes incluidos en la sección 6.1.
Pacientes que no estén en tratamiento de mantenimiento con opioides, por el mayor riesgo de depresión respiratoria.
Depresión respiratoria grave o enfermedad pulmonar obstructiva grave.
Tratamiento del dolor agudo distinto al dolor irruptivo.
4.4 Advertencias y precauciones especiales de empleo
Debe advertirse a los pacientes y a sus cuidadores que Effentora contiene un principio activo en cantidades que pueden causar la muerte, especialmente a un niño. Por lo que todos los comprimidos deben mantenerse fuera de la vista y del alcance de los niños.
Con el fin de minimizar los riesgos de efectos adversos relacionados con los opioides y para establecer la dosis eficaz, es indispensable que los profesionales sanitarios monitoricen cuidadosamente a los pacientes durante el proceso de ajuste de la dosis.
Es importante que el tratamiento con opioides de acción prolongada utilizados para tratar el dolor persistente del paciente se haya estabilizado antes de iniciar el tratamiento con Effentora y que el paciente prosiga el tratamiento con el opioide de larga duración mientras esté tomando Effentora.
Depresión respiratoria
Como con todos los opioides, hay riesgo de depresión respiratoria clínicamente significativa asociada al uso de fentanilo. . La selección inapropiada del paciente (ej. uso en pacientes que no reciben tratamiento de mantenimiento con opioides) y/o la dosis incorrecta ha tenido desenlaces mortales con el uso de Effentora así como con otros productos a base de fentanilo.
Effentora sólo debe ser usado según las condiciones descritas en la sección 4.1.
Enfermedad pulmonar obstructiva crónica
Debe prestarse especial atención al ajuste de la dosis de Effentora en pacientes con enfermedad pulmonar obstructiva crónica no grave u otras afecciones que les predispongan a una depresión respiratoria, ya que incluso las dosis terapéuticas habituales de Effentora pueden reducir el impulso respiratorio hasta provocar insuficiencia respiratoria.
Aumento de la presión intracraneal, alteración del estado de conciencia
Effentora sólo debe administrarse con precaución extrema en pacientes que puedan ser especialmente sensibles a los efectos intracraneales de la retención de CO2, como aquellos con un aumento constatado de la presión intracraneal o con alteración del estado de conciencia. Los opioides pueden enmascarar la evolución clínica de un paciente con lesiones en la cabeza, y sólo deben utilizarse si están clínicamente justificados.
Enfermedad cardíaca
El fentanilo puede provocar bradicardia y debe administrarse con precaución en pacientes con bradiarritmias previas o ya existentes.
Insuficiencia renal o hepática
Además, Effentora debe administrarse con precaución a pacientes con insuficiencia hepática o renal. No se ha valorado la influencia de la insuficiencia hepática o renal sobre la farmacocinética del medicamento; sin embargo, cuando éste se administra por vía intravenosa, se ha comprobado que el aclaramiento del fentanilo está alterado en las enfermedades hepáticas y renales debido a la alteración del aclaramiento metabólico y de las proteínas plasmáticas. Tras la administración de Effentora. la insuficiencia hepática y la insuficiencia renal pueden ambas aumentar la biodisponibilidad del fentanilo ingerido y disminuir su aclaramiento sistémico, lo cual puede aumentar y prolongar los efectos opioides. Así pues, debe prestarse especial atención al ajuste de la dosis en pacientes con enfermedad hepática o renal moderada o grave.
Se deben tomar precauciones especiales en pacientes con hipovolemia e hipotensión.
Sindrome serotoninérgico
Se recomienda precaución cuando Effentora se administre de forma concomitante con fármacos que afecten a los sistemas de neurotransmisores serotoninérgicos.
El desarrollo de un síndrome serotoninérgico potencialmente mortal puede aparecer con el uso concomitante de fármacos serotoninérgicos, como los inhibidores selectivos de la recaptación de serotonina (ISRS) y los inhibidores de la recaptación de serotonina y noradrenalina (IRSN), y con los fármacos que afectan al metabolismo de la serotonina (incluidos los inhibidores de la monoamino oxidasa [IMAO]). Esto puede ocurrir con la dosis recomendada.
El síndrome serotoninérgico puede incluir cambios en el estado mental (p. ej., agitación, alucinaciones, coma), inestabilidad autonómica (p. ej., taquicardia, presión arterial lábil, hipertermia), anomalías neuromusculares (p. ej., hiperreflexia, descoordinación, rigidez) y/o síntomas gastrointestinales (p. ej., náuseas, vómitos, diarrea).
Si se sospecha de un síndrome serotoninérgico, debe suspenderse el tratamiento con Effentora. Tolerancia, dependencia
La administración repetida de opioides como el fentanilo puede inducir tolerancia y dependencia física y/o psicológica. Sin embargo, rara vez se produce adicción iatrogénica por el uso terapéutico de opioides.
Dietas pobres en sodio
Este medicamento contiene 20 mg de sodio por comprimido, lo que debe ser tenido en cuenta en pacientes con dietas pobres en sodio.
Anafilaxia e hipersensibilidad
Se han notificado anafilaxia e hipersensibilidad asociados al uso de medicamentos de fentanilo por vía oral transmucosa (ver sección 4.8).
4.5 Interacción con otros medicamentos y otras formas de interacción
El fentanilo se metaboliza por medio del sistema del isoenzima 3A4 del citocromo P450 (CYP3A4), por lo que pueden producirse interacciones cuando Effentora se administra concomitantemente con fármacos que afectan a la actividad de CYP3A4. La administración concomitante de fármacos que inducen la actividad 3A4 puede reducir la eficacia de Effentora. El uso concomitante de Effentora con inhibidores potentes del CYP3A4 (como ritonavir, ketoconazol, itraconazol, troleandomicina, claritromicina y nelfinavir) o inhibidores moderados del CYP3A4 (como aprenavir, aprepitant, diltiazem, eritromicina, fluconazol, fosamprenavir, zumo de pomelo y verapamilo) puede aumentar la concentración plasmática de fentanilo, causando en ocasiones reacciones adversas graves, incluida una depresión respiratoria mortal. Los pacientes que reciban Effentora e inhibidores moderados o potentes del CYP3A4 concomitantemente deben controlarse estrictamente durante un amplio período de tiempo. El aumento de la dosis debe realizarse con precaución.
El uso concomitante con otros depresores del sistema nervioso central, incluidos otros opioides, sedantes o hipnóticos, anestésicos generales, fenotiazinas, tranquilizantes, relajantes musculares, antihistamínicos sedantes y alcohol, puede producir efectos depresivos aditivos.
No se recomienda el uso de Effentora en pacientes que hayan recibido inhibidores de la monoamino oxidasa (MAO) en los 14 días anteriores, porque se ha descrito que los inhibidores de la MAO producen una potenciación grave e impredecible de los analgésicos opioides.
No se recomienda el uso concomitante de agonistas/antagonistas opioides parciales (p.ej. buprenorfina, nalbufina, pentazocina) ya que poseen una elevada afinidad por los receptores opioides con una actividad intrínseca relativamente baja y en consecuencia antagonizan parcialmente el efecto analgésico del fentanilo, pudiendo inducir síntomas de abstinencia en pacientes dependientes de opioides.
Fármacos serotoninérgicos
La administración concomitante de fentanilo con un fármaco serotoninérgico, como un inhibidor selectivo de la recaptación de serotonina (ISRS), un inhibidor de la recaptación de serotonina y noradrenalina (IRSN) o un inhibidor de la monoamino oxidasa (IMAO), puede aumentar el riesgo de síndrome serotoninérgico, un trastorno potencialmente mortal.
4.6 Fertilidad, embarazo y lactancia
Embarazo
No hay datos suficientes relativos al uso de de fentanilo en mujeres embarazadas. Los estudios realizados en animales han mostrado toxicidad para la reproducción (ver sección 5.3). Se desconoce el riesgo potencial en seres humanos. No debe utilizarse Effentora durante el embarazo a no ser que fuese absolutamente necesario.
El tratamiento prolongado durante el embarazo puede causar síntomas de abstinencia en el recién nacido.
Se aconseja no administrar fentanilo durante el parto (aunque sea por cesárea), ya que atraviesa la placenta y puede causar depresión respiratoria en el feto. Si se administra Effentora, debe disponerse fácilmente de un antídoto para el niño.
Lactancia
El fentanilo se excreta a través de la leche materna y puede causar sedación y depresión respiratoria en el lactante. El fentanilo no debe utilizarse durante la lactancia, no pudiendo reiniciarse la lactancia hasta transcurridos como mínimo 5 días de la última administración de fentanilo.
Fertilidad
No existen datos sobre la fertilidad en humanos. En los estudios realizados con animales, la fertilidad en machos se vio afectada (ver sección 5.3).
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
No se han realizado estudios de los efectos sobre la capacidad para conducir y utilizar máquinas. No obstante, los analgésicos opioides pueden disminuir la capacidad mental y/o física necesaria para realizar tareas potencialmente peligrosas (p. ej., conducir un coche o utilizar maquinaria). Debe advertirse a los pacientes de que no conduzcan ni utilicen maquinaria si sienten somnolencia, mareos o alteraciones visuales mientras toman Effentora, y de que no conduzcan ni utilicen maquinaria hasta que no sepan cómo van a reaccionar.
4.8 Reacciones adversas
Resumen del perfil de seguridad
Las reacciones adversas que pueden esperarse de Effentora son las típicas de los opioides. Frecuentemente, esos efectos adversos propios de los opioides cesan o disminuyen en intensidad con el uso continuado del medicamento, o con el ajuste de la dosis más adecuada para el paciente. No obstante, las reacciones adversas más graves son depresión respiratoria (que potencialmente puede culminar en apnea o parada respiratoria), depresión circulatoria, hipotensión y colapso, reacciones que deben vigilarse estrechamente en todos los pacientes.
Los ensayos clínicos con Effentora se diseñaron para valorar la seguridad y eficacia en el tratamiento del DI, y todos los pacientes tomaban ya opioides de forma concomitante, como morfina de liberación prolongada o fentanilo transdérmico, para su dolor persistente. Por consiguiente, no es posible distinguir con exactitud los efectos de Effentora solo.
Se han notificado las siguientes reacciones adversas con Effentora y/u otros compuestos que contienen fentanilo provenientes de ensayos clínicos y de la experiencia postcomercialización. Las reacciones adversas se enumeran a continuación según el término preferente de MedDRA por el sistema de clasificación de órganos y frecuencia (frecuencias se definen como: muy frecuentes >1/10, frecuentes >1/100 a <1/10, poco frecuentes > 1/1.000 a < 1/100, raras >1/10.000 a <1/1.000, frecuencia no conocida (no puede estimarse a partir de los datos disponibles); las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada intervalo de frecuencia):
Tabla de reacciones adversas
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Infecciones e infestaciones |
Candidiasis oral |
Faringitis |
Pústula oral | ||
|
Trastornos de la sangre y del sistema linfático |
Anemia Neutropenia |
Trombocito- penia | |||
|
Trastornos del sistema inmunológico |
Hipersensibili dad | ||||
|
Trastornos endocrinos |
Hipogonadismo | ||||
|
Trastornos del metabolismo y de la nutrición |
Anorexia |
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Trastornos psiquiátricos |
Depresión Ansiedad Estado confusional Insomnio |
Euforia Nerviosismo Alucinaciones Alucinaciones visuales Cambios del estado mental Drogodependen cia (adicción) Desorientación | |||
|
Trastornos del sistema nervioso |
Mareo Cefalea |
Disgeusia Somnolencia Letargia Temblores Sedación Hipoestesia Migraña |
Nivel de conciencia deprimido Trastornos de la atención Trastorno del equilibrio Disartria |
Trastorno cognitivo Disfunción motora |
Pérdida de consciencia Convulsión |
|
Trastornos oculares |
Alteraciones de la visión Hiperemia ocular Visión borrosa Disminución de la agudeza visual |
Sensación anómala en el ojo Fotopsia | |||
|
Trastornos del oído y del laberinto |
Vértigo Acúfenos Molestias en el oído | ||||
|
Trastornos cardiacos |
Taquicardia |
Bradicardia | |||
|
Trastornos vasculares |
Hipotensión Hipertensión |
Enrojecimiento Sofocos | |||
|
Trastornos respiratorios, torácicos y mediastínicos |
Disnea Dolor faringolaríng eo |
Depresión respiratoria Síndrome de apnea del sueño |
Paro respiratorio | ||
|
Trastornos gastrointestinales |
Náuseas Vómitos |
Estreñimient o Estomatitis Sequedad de boca Diarrea Dolor abdominal Enfermedad por reflujo gastroesofági co Molestias estomacales Dispepsia Dolor dental |
Íleo Ulceración de la boca Hipoestesia oral Molestias orales Decoloración de la mucosa oral Trastorno de los tejidos blandos de la boca Glosodinia Ampollas en la lengua Dolor gingival Ulceración de la lengua Trastornos de la |
Ampollas en la mucosa oral Labios secos |
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
lengua Esofagitis Labios agrietados Trastornos dentales | |||||
|
Trastornos hepatobiliares |
Dilatación biliar | ||||
|
Trastornos de la piel y del tejido subcutáneo |
Prurito Hiperhidrosis Rash |
Sudor frío Edema facial Prurito generalizado Alopecia |
Onicorrexia | ||
|
Trastornos musculoesquelético s y del tejido conjuntivo |
Mialgia Dolor de espalda |
Calambres musculares Debilidad muscular | |||
|
Trastornos renales y urinarios |
Retención urinaria | ||||
|
Trastornos generales y alteraciones en el lugar de administración |
Reacciones en el lugar de la aplicación, como sangrado, dolor, úlcera, irritación, parestesia, anestesia, eritema, edema, hinchazón y vesículas |
Edema periférico Fatiga Astenia Síndrome de abstinencia Escalofríos |
Malestar general Pereza Molestias en el pecho Sensaciones anormales Sensación de inquietud Sed Sensación de frío Sensación de calor |
Pirexia | |
|
Exploraciones complementarias |
Disminución de peso |
Descenso del recuento de plaquetas Aumento de la frecuencia cardiaca Descenso del hematocrito Descenso de la hemoglobina | |||
|
Lesiones traumáticas, intoxicaciones y complicaciones de procedimientos terapéuticos |
Caídas |
Descripción de las reacciones adversas seleccionadas
Tras la administración repetida de opioides como fentanilo puede desarrollarse tolerancia, dependencia física y/o psicológica.
Con fentanilo por vía transmucosa se han observado síntomas de abstinencia de opioides tales como náuseas, vómitos, diarrea, ansiedad, escalofríos, temblor y sudoración.
Se han observado pérdida de consciencia y paro respiratorio en el contexto de una sobredosis.
Se han notificado reacciones de hipersensibilidad en la experiencia postcomercialización, incluidos prurito, eritema, edema labial y facial y urticaria.
Notificación de sospechas de reacciones adversas
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del sistema nacional de notificación incluido en el Anexo V.
4.9 Sobredosis
Los síntomas de sobredosis con fentanilo son de naturaleza similar a los del fentanilo intravenoso y a los demás opioides, y son una prolongación de sus acciones farmacológicas, siendo los efectos graves más significativos la alteración del estado mental, pérdida de la consciencia, hipotensión, la depresión respiratoria, distrés respiratorio y el fallo respiratorio con resultado de muerte.
El tratamiento inmediato en caso de sobredosis de opioides consiste en retirar el comprimido bucal de Effentora, si el paciente todavía lo tiene en la boca, asegurando la apertura de las vías respiratorias; estimulación física y verbal del paciente; valoración del grado de conciencia, el estado ventilatorio y circulatorio; y respiración asistida (soporte ventilatorio) en caso necesario.
Para el tratamiento de una sobredosis (ingestión accidental) en una persona que no haya tomado nunca opioides, se debe colocar una vía intravenosa y utilizar naloxona u otros antagonistas de los opioides según esté indicado clínicamente. La depresión respiratoria causada por la sobredosis puede durar más que los efectos de la acción del antagonista de los opioides (así, la semivida de la naloxona varía de 30 a 81 minutos), por lo que puede ser necesaria la administración repetida. Consultar los detalles sobre este tipo de uso en la ficha técnica del antagonista de los opioides utilizado.
Para el tratamiento de una sobredosis en pacientes mantenidos con opioides, debe colocarse una vía intravenosa. El uso moderado de naloxona u otro antagonista opioide puede estar justificado en algunos casos, pero se asocia al riesgo de precipitar la aparición de un síndrome de abstinencia agudo.
Aunque no se ha observado rigidez muscular que interfiera con la respiración después del uso de Effentora, es una reacción que puede manifestarse con fentanilo y otros opioides. Si aparece, debe tratarse con respiración asistida, un antagonista de los opioides y, como último recurso, un agente bloqueante neuromuscular.
5. PROPIEDADES FARMACOLÓGICAS
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: analgésicos; opioides Código ATC: N02AB03.
El fentanilo es un analgésico opioide que actúa principalmente sobre los receptores de opioides p. Sus efectos terapéuticos principales son la analgesia y la sedación. Los efectos farmacológicos secundarios son depresión respiratoria, bradicardia, hipotermia, estreñimiento, miosis, dependencia física y euforia.
Los efectos analgésicos del fentanilo están relacionados con su concentración plasmática. En general, la concentración eficaz y la concentración a la que aparece toxicidad aumentan a medida que aumenta la tolerancia a los opioides. La velocidad de aparición de tolerancia varía mucho de una persona a otra.
En consecuencia, la dosis de Effentora debe ajustarse individualmente para conseguir el efecto deseado (ver sección 4.2).
Todos los agonistas de los receptores de opioides p, entre ellos el fentanilo, producen depresión respiratoria dependiente de la dosis. El riesgo de depresión respiratoria es menor en pacientes que reciben tratamiento crónico con opioides, puesto que desarrollan tolerancia a los efectos de depresión respiratoria.
La seguridad y eficacia de Effentora se han evaluado en pacientes que recibieron el medicamento al inicio de un episodio de dolor irruptivo. El uso preventivo de Effentora para episodios de dolor predecibles no se ha investigado en ensayos clínicos. Se han realizado dos ensayos doble ciego, aleatorizados, controlados con placebo y cruzados en un total de 248 pacientes con DI y cáncer que experimentaron una media de 1-4 episodios de DI al día durante el tratamiento de mantenimiento con opioides. Durante una fase inicial abierta, se ajustó la dosis en cada paciente hasta establecer la dosis eficaz de Effentora. Los pacientes en los que se estableció una dosis eficaz entraron en la fase doble ciego del estudio. El criterio principal de eficacia fue la valoración por el propio paciente de la intensidad del dolor. Los pacientes valoraron la intensidad del dolor utilizando una escala de 11 puntos. En cada episodio de DI se evaluó la intensidad del dolor antes y en varias ocasiones después del tratamiento.
En el 67% de los pacientes se pudo establecer una dosis eficaz.
En el ensayo clínico pivotal (ensayo 1), el criterio de valoración principal fue la media de la suma de las diferencias en los valores de la intensidad del dolor desde el momento de administrar la dosis hasta 60 minutos después, inclusive (SPID60), que fue estadísticamente significativa respecto a placebo
(p<0,0001).
Ensayo 1: Media (+/- EEM) Diferencias en intensidad del dolor en cada valoración
(Sene completa de análisis)
SPID60 media (+/- DE)
EFFENTORA=9,7(5,58) p<0,0001
Placebo=4,9(4,38)
. — -I
120
Tiempo transcurrido desde la administración de la medicación del ensayo (minutos)
Grupo de tratamiento
XXX
EFFENTORA
-kirie
Placebo
+ p<0?0001 Effentora trente a placebo, a tavor de Effentora, mediante un análisis de la varianza
DID=diterencia en intensidad del dolor; EEM=error estándar de la media
(Sene completa de análisis)
SPID30 media (+/- DE)
EFFENTORA=3,2(2,60) p<0,0001
Placebo=2,0(2,21)
O 5 10 15 30 45 60 90 120
Tiempo transcurrido desde la administración de la medicación del ensayo (minutos)
Grupo de tratamiento xxx EFFENTORA *** Placebo
* p<0,01 Effentora frente a placebo, a favor de Effentora, mediante una prueba de rangos con signo de Wilcoxon para una sola muestra
+ p<0,0001 Effentora frente a placebo, a favor de Effentora, mediante una prueba de rangos con signo de Wilcoxon para una sola muestra
DID=diferencia en intensidad del dolor: EEM=error estándar de la media
En el segundo estudio fundamental (ensayo 2), el criterio de valoración principal fue SPID30, que fue también estadísticamente significativo respecto a placebo (p<0,0001).
Se observó una mejora estadísticamente significativa en la diferencia de intensidad del dolor con Effentora frente a placebo ya a los 10 minutos en el Ensayo 1 y a los 15 minutos (primer punto temporal medido) en el Ensayo 2. En los dos ensayos, esas diferencias siguieron siendo significativas en todos los puntos temporales medidos.
5.2 Propiedades farmacocinéticas
Introducción general
El fentanilo es altamente lipofílico y puede ser absorbido muy rápidamente a través de la mucosa bucal y más lentamente por la vía gastrointestinal convencional. Está sujeto a un efecto de primer paso hepático e intestinal, y los metabolitos no contribuyen a los efectos terapéuticos del fentanilo.
La forma de liberación del principio activo se basa en una reacción efervescente que aumenta la velocidad y el grado de absorción del fentanilo a través de la mucosa bucal. Los cambios transitorios en el pH que acompañan a la reacción efervescente pueden optimizar la disolución (a un pH menor) y la permeabilidad de la membrana (a un pH mayor).
El tiempo de disolución (definido como el tiempo que tarda el comprimido en disgregarse totalmente tras su administración bucal) no afecta a la exposición sistémica temprana al fentanilo. El estudio comparativo entre la administración bucal (es decir entre la encía y la mejilla) y la administración sublingual de un comprimido de 400 mcg de Effentora cumplió los criterios de bioequivalencia.
No se han estudiado los efectos de la insuficiencia renal o hepática sobre la farmacocinética de Effentora.
Tras la administración bucal de Effentora, el fentanilo es absorbido rápidamente con una biodisponibilidad absoluta del 65%. El perfil de absorción de Effentora es, en su mayor parte, el resultado de una absorción rápida inicial a través de la mucosa bucal; las concentraciones plasmáticas máximas según las muestras de sangre venosa suelen alcanzarse generalmente en el transcurso de la hora siguiente a la administración bucal. Alrededor del 50% de la dosis total administrada se absorbe rápidamente por la mucosa bucal y pasa a la circulación sistémica. La otra mitad de la dosis total se traga y se absorbe lentamente en el tubo digestivo. Casi el 30% de la cantidad tragada (50% de la dosis total) escapa a la eliminación hepática e intestinal de primer paso y pasa a estar disponible sistémicamente.
En la siguiente tabla se indican los principales parámetros farmacocinéticos.
Parámetros_farmacocinéticos* en sujetos adultos tratados con Effentora
|
Parámetro farmacocinético (media) |
Effentora 400 microgramos |
|
Biodisponibilidad absoluta |
65% (±20%) |
|
Fracción absorbida por la mucosa |
48% (±31,8%) |
|
Tmax (minuto) ** |
46,8 (20-240) |
|
Cmax (ng/ml) |
1,02 (± 0,42) |
|
AUC0-tmax (ng.h/ml) |
0,40 (± 0,18) |
|
AUC0-inf (ng.h/ml) |
6,48 (± 2,98) |
* Basado en muestras de sangre venosa (plasma). ). Las concentraciones de citrato de fentanilo en suero fueron superiores a las obtenidas en plasma: La AUC y la Cmax séricas fueron superiores a la AUC y la Cmax plasmáticas aproximadamente en un 20% y un 30%, respectivamente. Se desconoce la razón de dicha diferencia.
** Datos de Tmax presentados como mediana (rango).
En estudios farmacocinéticos que compararon la biodisponibilidad absoluta y relativa de Effentora y del citrato de fentanilo bucal (CFB), la velocidad y el grado de absorción del fentanilo de Effentora demostraron que la exposición era un 30%-50% mayor que la obtenida con el citrato de fentanilo transmucosa. Si se cambia desde otro producto de citrato de fentanilo oral, se precisa un ajuste de la dosis independiente con Effentora puesto que la biodisponibilidad difiere notablemente de uno a otro producto. Sin embargo, en estos pacientes se puede considerar una dosis inicial mayor de 100 microgramos.
Concentración plasmática media frente a tiempo Perfiles tras la administración de dosis únicas de EFFENTORA y CFB en sujetos sanos
-©- 400 mcg EFFENTORA
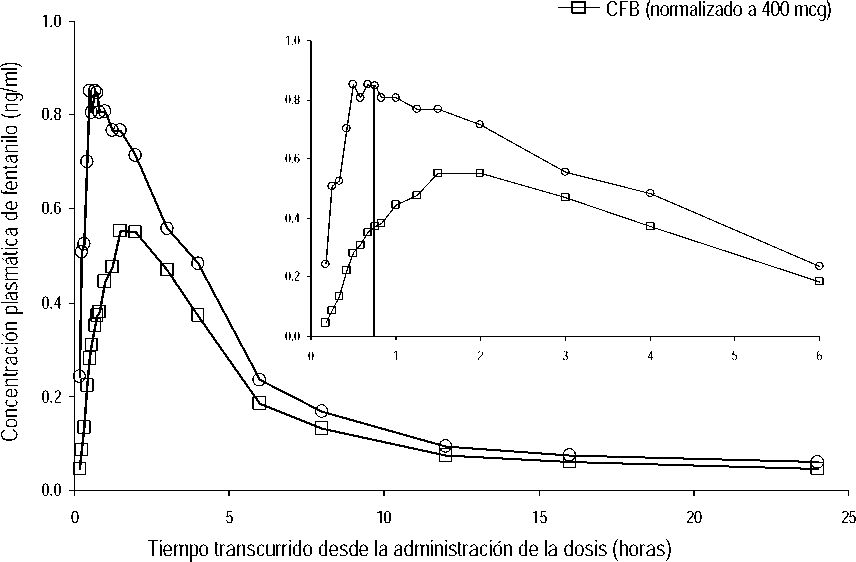
Los datos de CFB se presentan ajustados (de 800 mcg a 400 mcg).
En un ensayo clínico de pacientes con mucositis de grado 1, se observaron diferencias en la exposición con Effentora. La Cmax y la AUC0-8 fueron entre un 1% y un 25% mayores en los pacientes con mucositis que en los pacientes sin mucositis, respectivamente. Las diferencias observadas no fueron clínicamente significativas.
Distribución
El fentanilo es altamente lipofílico y se distribuye rápidamente fuera del sistema vascular, con un elevado volumen de distribución aparente. Tras la administración bucal de Effentora, el fentanilo experimenta una rápida distribución inicial que representa un equilibrio del fentanilo entre el plasma y los tejidos altamente perfundidos (cerebro, corazón y pulmones). Posteriormente, el fentanilo se redistribuye entre el compartimiento de los tejidos profundos (músculos y tejido adiposo) y el plasma.
La unión del fentanilo a las proteínas plasmáticas es del 80% al 85%. La principal proteína de unión es la alfa-1-ácido-glucoproteína, si bien tanto la albúmina como las lipoproteínas contribuyen en cierta medida. La fracción libre de fentanilo aumenta con la acidosis.
Biotransformación
En los ensayos clínicos no se han caracterizado las rutas metabólicas tras la administración bucal de Effentora. El fentanilo se metaboliza a norfentanilo en el hígado y en la mucosa intestinal por acción de la isoforma CYP3A4. El norfentanilo no es activo farmacológicamente en los estudios en animales. Más del 90% de la dosis administrada de fentanilo se elimina por biotransformación en metabolitos inactivos N-desalquilados e hidroxilados.
Eliminación
Tras la administración intravenosa de fentanilo, menos del 7% de la dosis administrada se elimina inalterada en la orina, y solamente un 1% se excreta inalterada en las heces. Los metabolitos se excretan principalmente en la orina, mientras que la excreción fecal es menos importante.
Tras la administración de Effentora, la fase de eliminación terminal de fentanilo es el resultado de la redistribución entre el plasma y el compartimiento de los tejidos profundos. Esta fase de eliminación es lenta, con una mediana de la semivida de eliminación terminal t1/2 de aproximadamente 22 horas tras la administración bucal de la formulación efervescente y de aproximadamente 18 horas tras la administración intravenosa. El aclaramiento en plasma total del fentanilo después de la administración intravenosa es aproximadamente de 42 l/h.
Linealidad/no linealidad
Se ha demostrado la proporcionalidad de la dosis desde 100 microgramos hasta 1.000 microgramos.
5.3 Datos preclínicos sobre seguridad
Los datos de los estudios no clínicos no muestran riesgos especiales para los seres humanos según los estudios convencionales de farmacología de seguridad, toxicidad a dosis repetidas, genotoxicidad y carcinogenicidad.
Los estudios de toxicidad del desarrollo embrionario y fetal llevados a cabo en ratas y conejos no evidenciaron malformaciones ni alteraciones del desarrollo inducidas por el fármaco, administrado durante el período de la organogénesis.
En un estudio de fertilidad y desarrollo embrionario temprano, en ratas, se observó un efecto asociado a los machos a altas dosis (300 mcg/kg/día s.c.) y se considera secundario a los efectos sedantes del fentanilo en estudios animales.
En estudios sobre el desarrollo pre y postnatal en ratas, la tasa de supervivencia de la progenie se redujo significativamente a dosis que causaban toxicidad materna severa. Los hallazgos adicionales en las crías de la generación F1, tras dosis maternales tóxicas, fueron retraso del desarrollo físico, de las funciones sensoriales, reflejos y comportamiento. Dichos efectos pueden ser indirectos debidos a una alteración de los cuidados maternos y/o disminución de la frecuencia de la lactancia o bien un efecto directo del fentanilo sobre las crías.
Los estudios de carcinogenicidad (bioensayo dérmico alternativo de 26 semanas en ratones transgénicos Tg.AC; estudio de carcinogenicidad subcutánea de 2 años en ratas) con fentanilo no pusieron de manifiesto ningún hallazgo indicativo de potencial oncogénico. La evaluación de los cortes laminares de cerebro del estudio de carcinogenicidad en ratas mostró lesiones cerebrales en los animales tratados con dosis altas de citrato de fentanilo. Se desconoce la relevancia de estos hallazgos para los seres humanos.
6. DATOS FARMACÉUTICOS
6.1 Lista de excipientes
Manitol
Carboximetilalmidón sódico tipo A Hidrogenocarbonato de sodio Carbonato de sodio anhidro Ácido cítrico anhidro Estearato de magnesio
6.2 Incompatibilidades
No procede.
6.3 Periodo de validez
3 años
6.4 Precauciones especiales de conservación
Conservar en el embalaje original para protegerlo de la humedad.
6.5 Naturaleza y contenido del envase
Blister laminado de PVC/lámina de aluminio/poliamida/PVC con cierre de papel/poliéster.
Los blister se presentan en cajas de 4 ó 28 comprimidos. Puede que solamente estén comercializados algunos tamaños de envases.
6.6 Precauciones especiales de eliminación
Hay que explicar a los pacientes y a sus cuidadores que desechen todos los comprimidos sin abrir que les sobren cuando ya no necesiten más el tratamiento.
La eliminación del medicamento utilizado o no utilizado pero que ya no se necesita y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V.
Swensweg 5 2031 GA Haarlem Países Bajos
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/08/441/003-004
9. FECHA DE LA PRIMERA AUTORIZACIÓN/RENOVACIÓN DE LA
AUTORIZACIÓN
Fecha de la primera autorización: 20 febrero 2013
10. FECHA DE LA REVISIÓN DEL TEXTO
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos http://www.ema.europa.eu.
1. NOMBRE DEL MEDICAMENTO
Effentora 400 microgramos comprimidos bucales
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada comprimido bucal contiene 400 microgramos de fentanilo (como citrato).
Excipiente(s) con efecto conocido: Cada comprimido contiene 20 mg de sodio. Para consultar la lista completa de excipientes, ver sección 6.1.
3. FORMA FARMACÉUTICA
Comprimido bucal.
Comprimido de caras planas, de color blanco, redondo y con bordes biselados, con una "C” grabado en una cara y en la otra con “4”
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
Effentora está indicado para el tratamiento del dolor irruptivo (DI) en pacientes adultos con cáncer que ya reciben tratamiento de mantenimiento con opioides para el dolor crónico asociado a cáncer.
El DI es una exacerbación transitoria del dolor que se produce sobre un fondo de dolor persistente controlado por otros medios.
Los pacientes que reciben tratamiento de mantenimiento con opioides son los que toman como mínimo 60 mg de morfina oral diarios, 25 microgramos de fentanilo transdérmico cada hora, 30 mg de oxicodona diarios, 8 mg de hidromorfona oral diarios o una dosis equianalgésica de otro opioide durante una semana o más.
4.2 Posología y forma de administración
El tratamiento debe ser instaurado y seguido bajo las directrices de un médico experimentado en la terapia con opioides en pacientes con cáncer. Los médicos deben considerar el riesgo del abuso del fentanilo. Se debe advertir al paciente que no debe utilizar dos concentraciones diferentes de fentanilo al mismo tiempo para el tratamiento del dolor irruptivo y que debe desechar cualquier producto de fentanilo prescrito para el dolor irruptivo cuando cambie a Effentora. Con objeto de prevenir confusiones y posibles sobredosis, los pacientes deben disponer en cada momento del mínimo número de concentraciones de los comprimidos.
Posología
Ajuste de la dosis
Effentora debe ajustarse de forma individual hasta obtener una dosis “eficaz” que proporcione la analgesia adecuada y minimice las reacciones adversas. En los ensayos clínicos, la dosis eficaz de Effentora para el DI no pudo predecirse a partir de la dosis diaria de mantenimiento de opioides.
Los pacientes deben monitorizarse cuidadosamente hasta que se establezca la dosis eficaz.
Ajuste de la dosis en pacientes que no cambian a Effentora desde otros medicamentos que contienen fentanilo
La dosis inicial de Effentora debe ser de 100 microgramos, que se incrementará según sea necesario dentro del rango de concentraciones de dosificación disponibles (100, 200, 400, 600 y 800 microgramos).
Ajuste de la dosis en pacientes que cambian a Effentora tras recibir otros medicamentos que contienen fentanilo
Debido a los diferentes perfiles de absorción, el cambio no debe hacerse en una proporción de 1:1. Si el cambio se hace desde otro medicamento de fentanilo como citrato oral, se precisa un ajuste de la dosis independiente con Effentora puesto que la biodisponibilidad difiere notablemente de un medicamento a otro. Sin embargo, en estos pacientes se puede considerar una dosis inicial mayor de 100 microgramos.
Proceso de ajuste de la dosis
Durante el ajuste de la dosis, si no se consigue una analgesia adecuada en los 30 minutos siguientes a la administración de un único comprimido, puede administrarse un segundo comprimido de Effentora de la misma concentración.
Si para tratar un episodio de DI se precisa más de un comprimido, para el tratamiento de futuros episodios de DI debe considerarse un aumento de la dosis hasta la siguiente concentración disponible.
Durante el proceso de ajuste de la dosis, se pueden combinar diferentes comprimidos. Se pueden utilizar hasta cuatro comprimidos de 100 microgramos o hasta cuatro comprimidos de 200 microgramos para tratar un episodio aislado de DI durante el proceso de ajuste de la dosis de acuerdo con el siguiente esquema:
• Si el comprimido inicial de 100 microgramos no es eficaz, se podrá prescribir al paciente dos comprimidos de 100 microgramos para tratar el siguiente episodio de DI. Se recomienda colocar un comprimido a cada lado de la boca. Si se establece que esa es la dosis eficaz, los futuros episodios de DI podrán seguir tratándose con un único comprimido de Effentora de
200 microgramos.
• Si un único comprimido de Effentora de 200 microgramos (o dos comprimidos de 100 microgramos) no resulta eficaz, podrá prescribirse al paciente dos comprimidos de
200 microgramos (o cuatro comprimidos de 100 microgramos) para tratar el siguiente episodio de DI. Se recomienda colocar dos comprimidos a cada lado de la boca. Si se considera que esa es la dosis eficaz, los futuros episodios de DI podrán seguir tratándose con un único comprimido de Effentora de 400 microgramos.
• Para el ajuste de la dosis con comprimidos de 600 microgramos y 800 microgramos, deben utilizarse comprimidos de 200 microgramos.
En los ensayos clínicos no se evaluaron dosis de más de 800 microgramos.
No deben utilizarse más de dos comprimidos para tratar un mismo episodio de DI, salvo cuando el ajuste de la dosis se realice utilizando cuatro comprimidos, como se ha explicado antes.
Durante el ajuste de la dosis, los pacientes deben esperar al menos 4 horas antes de tratar otro episodio de DI con Effentora.
Tratamiento de mantenimiento
Una vez determinada la dosis eficaz por medio del proceso de ajuste, los pacientes deben mantener esa dosis y limitar el consumo a un solo comprimido con la concentración que corresponda.
Los episodios de dolor irruptivo pueden variar en intensidad y la dosis de Effentora requerida puede aumentar con el tiempo debido a una progresión de la enfermedad oncológica subyacente. En estos casos se puede utilizar un segundo comprimido de Effentora de la misma concentración.
En caso de que se necesite un segundo comprimido de Effentora en diversas ocasiones consecutivas, se deberá reajustar la dosis de mantenimiento habitual (ver más abajo).
Durante el tratamiento de mantenimiento, los pacientes deben esperar al menos 4 horas antes de tratar otro episodio de DI con Effentora.
Reajuste de la dosis
La dosis de mantenimiento de Effentora debe aumentarse si el paciente necesita más de un comprimido por episodio de DI en varios episodios consecutivos de DI. Para el reajuste de la dosis se aplican los mismos principios descritos para Ajuste de la dosis (ver más arriba).
Si el paciente presenta con frecuencia más de cuatro episodios de DI en 24 horas, se debe volver a calcular la dosis del tratamiento de mantenimiento con opioides.
Interrupción del tratamiento
El tratamiento con Effentora se debe interrumpir inmediatamente si el paciente ya no presenta episodios de dolor irruptivo. El tratamiento del dolor de base persistente se debe mantener tal como estaba prescrito.
Si es necesario interrumpir la totalidad del tratamiento con opioides, el médico debe realizar un estrecho seguimiento del paciente con el fin de controlar el riesgo de efectos abruptos de abstinencia.
Pacientes con insuficiencia hepática o renal:
Effentora debe administrarse con precaución a pacientes con insuficiencia hepática o renal moderada o grave (ver sección 4.4).
Pacientes con xerostomía:
Se recomienda a los pacientes con xerostomía beber agua para humedecerse la cavidad bucal antes de la administración de Effentora. Si esta recomendación no basta para lograr una efervescencia suficiente, es posible que haya que cambiar de tratamiento.
Pacientes de edad avanzada (mayores de 65 años)
En los ensayos clínicos se ha observado que los pacientes mayores de 65 años necesitan dosis más bajas que los pacientes más jóvenes. Se recomienda especial precaución al ajustar la dosis de Effentora en pacientes de edad avanzada.
Población pediátrica:
No se ha establecido la seguridad y eficacia de Effentora en niños de 0 a 18 años. No se dispone de datos.
Forma de administración
Cuando el comprimido de Effentora se expone a la humedad, inicia una reacción efervescente en la que se libera el principio activo. Por ello debe advertirse a los pacientes que no abran el blister hasta el instante antes de colocarse el comprimido en la cavidad bucal.
Apertura del blister
Se debe explicar al paciente que NO trate de sacar el comprimido presionándolo contra el blister, porque eso puede dañar el comprimido bucal. La forma correcta de sacar el comprimido del blister es la siguiente:
Separar una de las unidades del blister del resto rasgándola por las perforaciones. Seguidamente, doblar la unidad del blister a lo largo de la línea impresa en la lámina posterior. Retirar la lámina posterior para dejar expuesto el comprimido.
También debe pedirse al paciente que no intente triturar ni partir el comprimido.
El comprimido no debe guardarse después de sacarlo del blister, pues no es posible garantizar su integridad ni evitar el riesgo de exposición accidental al medicamento.
Administración del comprimido
Los pacientes deben extraer el comprimido del alveolo blister e inmediatamente colocar el comprimido de Effentora entero en la cavidad bucal (cerca de un molar, entre la mejilla y la encía).
El comprimido de Effentora no debe chuparse, masticarse ni tragarse, ya que eso produciría unas concentraciones plasmáticas más bajas que cuando se disgrega en la boca.
Effentora debe colocarse y mantenerse dentro de la cavidad bucal durante el tiempo necesario para la disgregación del comprimido, que suele tardar unos 14-25 minutos.
Como alternativa el comprimido puede colocarse en el espacio sublingual (ver sección 5.2).
Si al cabo de 30 minutos siguen quedando restos del comprimido de Effentora, podrán tragarse con un vaso de agua.
El periodo de tiempo que tarda el comprimido en disgregarse completamente después de su administración bucal no parece que afecte a la exposición sistémica temprana al fentanilo.
Los pacientes no deben consumir ningún alimento ni bebida mientras tengan el comprimido en la cavidad bucal.
En caso de irritación de la mucosa bucal, se recomienda cambiar el lugar de colocación del comprimido dentro de la cavidad bucal.
4.3 Contraindicaciones
Hipersensibilidad al principio activo o a alguno de los excipientes incluidos en la sección 6.1.
Pacientes que no estén en tratamiento de mantenimiento con opioides, por el mayor riesgo de depresión respiratoria.
Depresión respiratoria grave o enfermedad pulmonar obstructiva grave.
Tratamiento del dolor agudo distinto al dolor irruptivo.
4.4 Advertencias y precauciones especiales de empleo
Debe advertirse a los pacientes y a sus cuidadores que Effentora contiene un principio activo en cantidades que pueden causar la muerte, especialmente a un niño . Por lo que todos los comprimidos deben mantenerse fuera de la vista y del alcance de los niños.
Con el fin de minimizar los riesgos de efectos adversos relacionados con los opioides y para establecer la dosis eficaz, es indispensable que los profesionales sanitarios monitoricen cuidadosamente a los pacientes durante el proceso de ajuste de la dosis.
Es importante que el tratamiento con opioides de acción prolongada utilizados para tratar el dolor persistente del paciente se haya estabilizado antes de iniciar el tratamiento con Effentora y que el paciente prosiga el tratamiento con el opioide de larga duración mientras esté tomando Effentora.
Depresión respiratoria
Como con todos los opioides, hay riesgo de depresión respiratoria clínicamente significativa asociada al uso de fentanilo. . La selección inapropiada del paciente (ej. uso en pacientes que no reciben tratamiento de mantenimiento con opioides) y/o la dosis incorrecta ha tenido desenlaces mortales con el uso de Effentora así como con otros productos a base de fentanilo.
Effentora sólo debe ser usado según las condiciones descritas en la sección 4.1
Enfermedad pulmonar obstructiva crónica
Debe prestarse especial atención al ajuste de la dosis de Effentora en pacientes con enfermedad pulmonar obstructiva crónica no grave u otras afecciones que les predispongan a una depresión respiratoria, ya que incluso las dosis terapéuticas habituales de Effentora pueden reducir el impulso respiratorio hasta provocar insuficiencia respiratoria.
Aumento de la presión intracraneal, alteración del estado de conciencia
Effentora sólo debe administrarse con precaución extrema en pacientes que puedan ser especialmente sensibles a los efectos intracraneales de la retención de CO2, como aquellos con un aumento constatado de la presión intracraneal o con alteración del estado de conciencia. Los opioides pueden enmascarar la evolución clínica de un paciente con lesiones en la cabeza, y sólo deben utilizarse si están clínicamente justificados.
Enfermedad cardíaca
El fentanilo puede provocar bradicardia y debe administrarse con precaución en pacientes con bradiarritmias previas o ya existentes.
Insuficiencia renal o hepática
Además, Effentora debe administrarse con precaución a pacientes con insuficiencia hepática o renal. No se ha valorado la influencia de la insuficiencia hepática o renal sobre la farmacocinética del medicamento; sin embargo, cuando éste se administra por vía intravenosa, se ha comprobado que el aclaramiento del fentanilo está alterado en las enfermedades hepáticas y renales debido a la alteración del aclaramiento metabólico y de las proteínas plasmáticas. Tras la administración de Effentora, la insuficiencia hepática y la insuficiencia renal pueden ambas aumentar la biodisponibilidad del fentanilo ingerido y disminuir su aclaramiento sistémico, lo cual puede aumentar y prolongar los efectos opioides. Así pues, debe prestarse especial atención al ajuste de la dosis en pacientes con enfermedad hepática o renal moderada o grave.
Se deben tomar precauciones especiales en pacientes con hipovolemia e hipotensión.
Sindrome serotoninérgico
Se recomienda precaución cuando Effentora se administre de forma concomitante con fármacos que afecten a los sistemas de neurotransmisores serotoninérgicos.
El desarrollo de un síndrome serotoninérgico potencialmente mortal puede aparecer con el uso concomitante de fármacos serotoninérgicos, como los inhibidores selectivos de la recaptación de serotonina (ISRS) y los inhibidores de la recaptación de serotonina y noradrenalina (IRSN), y con los fármacos que afectan al metabolismo de la serotonina (incluidos los inhibidores de la monoamino oxidasa [IMAO]). Esto puede ocurrir con la dosis recomendada.
El síndrome serotoninérgico puede incluir cambios en el estado mental (p. ej., agitación, alucinaciones, coma), inestabilidad autonómica (p. ej., taquicardia, presión arterial lábil, hipertermia), anomalías neuromusculares (p. ej., hiperreflexia, descoordinación, rigidez) y/o síntomas gastrointestinales (p. ej., náuseas, vómitos, diarrea).
Si se sospecha de un síndrome serotoninérgico, debe suspenderse el tratamiento con Effentora. Tolerancia, dependencia
La administración repetida de opioides como el fentanilo puede inducir tolerancia y dependencia física y/o psicológica. Sin embargo, rara vez se produce adicción iatrogénica por el uso terapéutico de opioides.
Dietas pobres en sodio
Este medicamento contiene 20 mg de sodio por comprimido, lo que debe ser tenido en cuenta en pacientes con dietas pobres en sodio.
Anafilaxia e hipersensibilidad
Se han notificado anafilaxia e hipersensibilidad asociados al uso de medicamentos de fentanilo por vía oral transmucosa (ver sección 4.8).
4.5 Interacción con otros medicamentos y otras formas de interacción
El fentanilo se metaboliza por medio del sistema del isoenzima 3A4 del citocromo P450 (CYP3A4), por lo que pueden producirse interacciones cuando Effentora se administra concomitantemente con fármacos que afectan a la actividad de CYP3A4. La administración concomitante de fármacos que inducen la actividad 3A4 puede reducir la eficacia de Effentora. El uso concomitante de Effentora con inhibidores potentes del CYP3A4 (como ritonavir, ketoconazol, itraconazol, troleandomicina, claritromicina y nelfinavir) o inhibidores moderados del CYP3A4 (como aprenavir, aprepitant, diltiazem, eritromicina, fluconazol, fosamprenavir, zumo de pomelo y verapamilo) puede aumentar la concentración plasmática de fentanilo, causando en ocasiones reacciones adversas graves, incluida una depresión respiratoria mortal. Los pacientes que reciban Effentora e inhibidores moderados o potentes del CYP3A4 concomitantemente deben controlarse estrictamente durante un amplio período de tiempo. El aumento de la dosis debe realizarse con precaución.
El uso concomitante con otros depresores del sistema nervioso central, incluidos otros opioides, sedantes o hipnóticos, anestésicos generales, fenotiazinas, tranquilizantes, relajantes musculares, antihistamínicos sedantes y alcohol, puede producir efectos depresivos aditivos.
No se recomienda el uso de Effentora en pacientes que hayan recibido inhibidores de la monoamino oxidasa (MAO) en los 14 días anteriores, porque se ha descrito que los inhibidores de la MAO producen una potenciación grave e impredecible de los analgésicos opioides.
No se recomienda el uso concomitante de agonistas/antagonistas opioides parciales (p.ej. buprenorfina, nalbufina, pentazocina) ya que poseen una elevada afinidad por los receptores opioides con una actividad intrínseca relativamente baja y en consecuencia antagonizan parcialmente el efecto analgésico del fentanilo, pudiendo inducir síntomas de abstinencia en pacientes dependientes de opioides.
Fármacos serotoninérgicos
La administración concomitante de fentanilo con un fármaco serotoninérgico, como un inhibidor selectivo de la recaptación de serotonina (ISRS), un inhibidor de la recaptación de serotonina y noradrenalina (IRSN) o un inhibidor de la monoamino oxidasa (IMAO), puede aumentar el riesgo de síndrome serotoninérgico, un trastorno potencialmente mortal.
4.6 Fertilidad, embarazo y lactancia
Embarazo
No hay datos suficientes relativos al uso de de fentanilo en mujeres embarazadas. Los estudios realizados en animales han mostrado toxicidad para la reproducción (ver sección 5.3). Se desconoce el riesgo potencial en seres humanos. No debe utilizarse Effentora durante el embarazo a no ser que fuese absolutamente necesario.
El tratamiento prolongado durante el embarazo puede causar síntomas de abstinencia en el recién nacido.
Se aconseja no administrar fentanilo durante el parto (aunque sea por cesárea), ya que atraviesa la placenta y puede causar depresión respiratoria en el feto. Si se administra Effentora, debe disponerse fácilmente de un antídoto para el niño.
Lactancia
El fentanilo se excreta a través de la leche materna y puede causar sedación y depresión respiratoria en el lactante. El fentanilo no debe utilizarse durante la lactancia, n o pudiendo reiniciarse la lactancia hasta transcurridos como mínimo 5 días de la última administración de fentanilo.
Fertilidad
No existen datos sobre la fertilidad en humanos. En los estudios realizados con animales, la fertilidad en machos se vio afectada (ver sección 5.3).
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
No se han realizado estudios de los efectos sobre la capacidad para conducir y utilizar máquinas. No obstante, los analgésicos opioides pueden disminuir la capacidad mental y/o física necesaria para realizar tareas potencialmente peligrosas (p. ej., conducir un coche o utilizar maquinaria). Debe advertirse a los pacientes de que no conduzcan ni utilicen maquinaria si sienten somnolencia, mareos o alteraciones visuales mientras toman Effentora, y de que no conduzcan ni utilicen maquinaria hasta que no sepan cómo van a reaccionar.
4.8 Reacciones adversas
Resumen del perfil de seguridad
Las reacciones adversas que pueden esperarse de Effentora son las típicas de los opioides. Frecuentemente, esos efectos adversos propios de los opioides cesan o disminuyen en intensidad con el uso continuado del medicamento, o con el ajuste de la dosis más adecuada para el paciente. No obstante, las reacciones adversas más graves son depresión respiratoria (que potencialmente puede culminar en apnea o parada respiratoria), depresión circulatoria, hipotensión y colapso, reacciones que deben vigilarse estrechamente en todos los pacientes.
Los ensayos clínicos con Effentora se diseñaron para valorar la seguridad y eficacia en el tratamiento del DI, y todos los pacientes tomaban ya opioides de forma concomitante, como morfina de liberación prolongada o fentanilo transdérmico, para su dolor persistente. Por consiguiente, no es posible distinguir con exactitud los efectos de Effentora solo.
Tabla de reacciones adversas
Se han notificado las siguientes reacciones adversas con Effentora y/u otros compuestos que contienen fentanilo provenientes de ensayos clínicos y de la experiencia postcomercialización. Las reacciones adversas se enumeran a continuación según el término preferente de MedDRA por el sistema de clasificación de órganos y frecuencia (frecuencias se definen como: muy frecuentes >1/10, frecuentes >1/100 a <1/10, poco frecuentes > 1/1.000 a < 1/100, raras >1/10.000 a <1/1.000, frecuencia no conocida (no puede estimarse a partir de los datos disponibles); las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada intervalo de frecuencia):
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Infecciones e infestaciones |
Candidiasis oral |
Faringitis |
Pústula oral | ||
|
Trastornos de la sangre y del sistema linfático |
Anemia Neutropenia |
Trombocito-penia | |||
|
Trastornos del sistema inmunológico |
Hipersensibil idad | ||||
|
Trastornos endocrinos |
Hipogonadism o | ||||
|
Trastornos del metabolismo y de la nutrición |
Anorexia |
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Trastornos psiquiátricos |
Depresión Ansiedad Estado confusional Insomnio |
Euforia Nerviosismo Alucinaciones Alucinaciones visuales Cambios del estado mental Drogodependencia (adicción) Desorientación | |||
|
Trastornos del sistema nervioso |
Mareo Cefalea |
Disgeusia Somnolencia Letargia Temblores Sedación Hipoestesia Migraña |
Nivel de conciencia deprimido Trastornos de la atención Trastorno del equilibrio Disartria |
Trastorno cognitivo Disfunción motora |
Pérdida de consciencia Convulsión |
|
Trastornos oculares |
Alteraciones de la visión Hiperemia ocular Visión borrosa Disminución de la agudeza visual |
Sensación anómala en el ojo Fotopsia | |||
|
Trastornos del oído y del laberinto |
Vértigo Acúfenos Molestias en el oído | ||||
|
Trastornos cardiacos |
Taquicardia |
Bradicardia | |||
|
Trastornos vasculares |
Hipotensión Hipertensión |
Enrojecimiento Sofocos | |||
|
Trastornos respiratorios, torácicos y mediastínicos |
Disnea Dolor faringolarínge o |
Depresión respiratoria Síndrome de apnea del sueño |
Paro respiratorio | ||
|
Trastornos gastrointestinales |
Náuseas Vómitos |
Estreñimiento Estomatitis Sequedad de boca Diarrea Dolor abdominal Enfermedad por reflujo gastroesofágic o Molestias estomacales Dispepsia Dolor dental |
Íleo Ulceración de la boca Hipoestesia oral Molestias orales Decoloración de la mucosa oral Trastorno de los tejidos blandos de la boca Glosodinia Ampollas en la lengua Dolor gingival Ulceración de la lengua Trastornos de la lengua Esofagitis Labios agrietados |
Ampollas en la mucosa oral Labios secos |
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Trastornos dentales | |||||
|
Trastornos hepatobiliares |
Dilatación biliar | ||||
|
Trastornos de la piel y del tejido subcutáneo |
Prurito Hiperhidrosis Rash |
Sudor frío Edema facial Prurito generalizado Alopecia |
Onicorrexia | ||
|
Trastornos musculoesquelético s y del tejido conjuntivo |
Mialgia Dolor de espalda |
Calambres musculares Debilidad muscular | |||
|
Trastornos renales y urinarios |
Retención urinaria | ||||
|
Trastornos generales y alteraciones en el lugar de administración |
Reacciones en el lugar de la aplicación, como sangrado, dolor, úlcera, irritación, parestesia, anestesia, eritema, edema, hinchazón y vesículas |
Edema periférico Fatiga Astenia Síndrome de abstinencia Escalofríos |
Malestar general Pereza Molestias en el pecho Sensaciones anormales Sensación de inquietud Sed Sensación de frío Sensación de calor |
Pirexia | |
|
Exploraciones complementarias |
Disminución de peso |
Descenso del recuento de plaquetas Aumento de la frecuencia cardiaca Descenso del hematocrito Descenso de la hemoglobina | |||
|
Lesiones traumáticas, intoxicaciones y complicaciones de procedimientos terapéuticos |
Caídas |
Descripción de las reacciones adversas seleccionadas
Tras la administración repetida de opioides como fentanilo puede desarrollarse tolerancia, dependencia física y/o psicológica.
Con fentanilo por vía transmucosa se han observado síntomas de abstinencia de opioides tales como náuseas, vómitos, diarrea, ansiedad, escalofríos, temblor y sudoración.
Se han observado pérdida de consciencia y paro respiratorio en el contexto de una sobredosis.
Se han notificado reacciones de hipersensibilidad en la experiencia postcomercialización, incluidos prurito, eritema, edema labial y facial y urticaria.
Notificación de sospechas de reacciones adversas
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del sistema nacional de notificación incluido en el Anexo V.
4.9 Sobredosis
Los síntomas de sobredosis con fentanilo son de naturaleza similar a los del fentanilo intravenoso y a los demás opioides, y son una prolongación de sus acciones farmacológicas, siendo los efectos graves más significativos la alteración del estado mental, pérdida de la consciencia, hipotensión, la depresión respiratoria, distrés respiratorio y el fallo respiratorio con resultado de muerte.
El tratamiento inmediato en caso de sobredosis de opioides consiste en retirar el comprimido bucal de Effentora, si el paciente todavía lo tiene en la boca, asegurando la apertura de las vías respiratorias; estimulación física y verbal del paciente; valoración del grado de conciencia, el estado ventilatorio y circulatorio; y respiración asistida (soporte ventilatorio) en caso necesario.
Para el tratamiento de una sobredosis (ingestión accidental) en una persona que no haya tomado nunca opioides, se debe colocar una vía intravenosa y utilizar naloxona u otros antagonistas de los opioides según esté indicado clínicamente. La depresión respiratoria causada por la sobredosis puede durar más que los efectos de la acción del antagonista de los opioides (así, la semivida de la naloxona varía de 30 a 81 minutos), por lo que puede ser necesaria la administración repetida. Consultar los detalles sobre este tipo de uso en la ficha técnica del antagonista de los opioides utilizado.
Para el tratamiento de una sobredosis en pacientes mantenidos con opioides, debe colocarse una vía intravenosa. El uso moderado de naloxona u otro antagonista opioide puede estar justificado en algunos casos, pero se asocia al riesgo de precipitar la aparición de un síndrome de abstinencia agudo.
Aunque no se ha observado rigidez muscular que interfiera con la respiración después del uso de Effentora, es una reacción que puede manifestarse con fentanilo y otros opioides. Si aparece, debe tratarse con respiración asistida, un antagonista de los opioides y, como último recurso, un agente bloqueante neuromuscular.
5. PROPIEDADES FARMACOLÓGICAS
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: analgésicos; opioides Código ATC: N02AB03.
El fentanilo es un analgésico opioide que actúa principalmente sobre los receptores de opioides p. Sus efectos terapéuticos principales son la analgesia y la sedación. Los efectos farmacológicos secundarios son depresión respiratoria, bradicardia, hipotermia, estreñimiento, miosis, dependencia física y euforia.
Los efectos analgésicos del fentanilo están relacionados con su concentración plasmática. En general, la concentración eficaz y la concentración a la que aparece toxicidad aumentan a medida que aumenta la tolerancia a los opioides. La velocidad de aparición de tolerancia varía mucho de una persona a otra. En consecuencia, la dosis de Effentora debe ajustarse individualmente para conseguir el efecto deseado (ver sección 4.2).
Todos los agonistas de los receptores de opioides p, entre ellos el fentanilo, producen depresión respiratoria dependiente de la dosis. El riesgo de depresión respiratoria es menor en pacientes que reciben tratamiento crónico con opioides, puesto que desarrollan tolerancia a los efectos de depresión respiratoria.
La seguridad y eficacia de Effentora se han evaluado en pacientes que recibieron el medicamento al inicio de un episodio de dolor irruptivo. El uso preventivo de Effentora para episodios de dolor predecibles no se ha investigado en ensayos clínicos. Se han realizado dos ensayos doble ciego, aleatorizados, controlados con placebo y cruzados en un total de 248 pacientes con DI y cáncer que experimentaron una media de 1-4 episodios de DI al día durante el tratamiento de mantenimiento con opioides. Durante una fase inicial abierta, se ajustó la dosis en cada paciente hasta establecer la dosis eficaz de Effentora. Los pacientes en los que se estableció una dosis eficaz entraron en la fase doble ciego del estudio. El criterio principal de eficacia fue la valoración por el propio paciente de la intensidad del dolor. Los pacientes valoraron la intensidad del dolor utilizando una escala de 11 puntos. En cada episodio de DI se evaluó la intensidad del dolor antes y en varias ocasiones después del tratamiento.
En el 67% de los pacientes se pudo establecer una dosis eficaz.
En el ensayo clínico pivotal (ensayo 1), el criterio de valoración principal fue la media de la suma de las diferencias en los valores de la intensidad del dolor desde el momento de administrar la dosis hasta 60 minutos después, inclusive (SPID60), que fue estadísticamente significativa respecto a placebo
(p<0,0001).
Ensayo 1: Media (+/- EEM) Diferencias en intensidad del dolor en cada valoración
(Serie completa de análisis)
SPID60 media (+/- DE)
EFFENTORA=9,7(5,58) p<0,0001 Placebo=4,9(4,38)
20
Tiempo transcurrido desde la administración de la medicación del ensayo (minutos)
Grupo de tratamiento
xxx EFFENTORA
★★★
Placebo
+ dmEOOOI Effentora trente a placebo, a tavor de Effentora, mediante un análisis de la varianza
DID=diterencia en intensidad del dolor; EEM=error estándar de la media
(Sene completa de análisis)
SPID30 media (+/- DE)
EFFENTORA=3,2(2,60) p<0,0001
Placebo=2,0(2,21)
O 5 10 15 30 45 60 90 120
Tiempo transcurrido desde la administración de la medicación del ensayo (minutos)
Grupo de tratamiento xxx EFFENTORA *** Placebo
* p<0,01 Effentora frente a placebo, a favor de Effentora, mediante una prueba de rangos con signo de Wilcoxon para una sola muestra
+ p<0,0001 Effentora frente a placebo, a favor de Effentora, mediante una prueba de rangos con signo de Wilcoxon para una sola muestra
DID=diferencia en intensidad del dolor: EEM=error estándar de la media
En el segundo estudio fundamental (ensayo 2), el criterio de valoración principal fue SPID30, que fue también estadísticamente significativo respecto a placebo (p<0,0001).
Se observó una mejora estadísticamente significativa en la diferencia de intensidad del dolor con Effentora frente a placebo ya a los 10 minutos en el Ensayo 1 y a los 15 minutos (primer punto temporal medido) en el Ensayo 2. En los dos ensayos, esas diferencias siguieron siendo significativas en todos los puntos temporales medidos.
5.2 Propiedades farmacocinéticas
Introducción general
El fentanilo es altamente lipofílico y puede ser absorbido muy rápidamente a través de la mucosa bucal y más lentamente por la vía gastrointestinal convencional. Está sujeto a un efecto de primer paso hepático e intestinal, y los metabolitos no contribuyen a los efectos terapéuticos del fentanilo.
La forma de liberación del principio activo se basa en una reacción efervescente que aumenta la velocidad y el grado de absorción del fentanilo a través de la mucosa bucal. Los cambios transitorios en el pH que acompañan a la reacción efervescente pueden optimizar la disolución (a un pH menor) y la permeabilidad de la membrana (a un pH mayor).
El tiempo de disolución (definido como el tiempo que tarda el comprimido en disgregarse totalmente tras su administración bucal) no afecta a la exposición sistémica temprana al fentanilo. El estudio comparativo entre la administración bucal (es decir entre la encía y la mejilla) y la administración sublingual de un comprimido de 400 mcg de Effentora cumplió los criterios de bioequivalencia.
No se han estudiado los efectos de la insuficiencia renal o hepática sobre la farmacocinética de Effentora.
Absorción:
Tras la administración bucal de Effentora, el fentanilo es absorbido rápidamente con una biodisponibilidad absoluta del 65%. El perfil de absorción de Effentora es, en su mayor parte, el resultado de una absorción rápida inicial a través de la mucosa bucal; las concentraciones plasmáticas máximas según las muestras de sangre venosa suelen alcanzarse generalmente en el transcurso de la hora siguiente a la administración bucal. Alrededor del 50% de la dosis total administrada se absorbe rápidamente por la mucosa bucal y pasa a la circulación sistémica. La otra mitad de la dosis total se traga y se absorbe lentamente en el tubo digestivo. Casi el 30% de la cantidad tragada (50% de la dosis total) escapa a la eliminación hepática e intestinal de primer paso y pasa a estar disponible sistémicamente.
En la siguiente tabla se indican los principales parámetros farmacocinéticos.
Parámetros_farmacocinéticos* en sujetos adultos tratados con Effentora
|
Parámetro farmacocinético (media) |
Effentora 400 microgramos |
|
Biodisponibilidad absoluta |
65% (±20%) |
|
Fracción absorbida por la mucosa |
48% (±31,8%) |
|
Tmax (minuto) ** |
46,8 (20-240) |
|
Cmax (ng/ml) |
1,02 (± 0,42) |
|
AUC0-tmax (ng.h/ml) |
0,40 (± 0,18) |
|
AUC0-inf (ng.h/ml) |
6,48 (± 2,98) |
* Basado en muestras de sangre venosa (plasma). Las concentraciones de citrato de fentanilo en suero fueron superiores a las obtenidas en plasma: La AUC y la Cmax séricas fueron superiores a la AUC y la Cmax plasmáticas aproximadamente en un 20% y un 30%, respectivamente. Se desconoce la razón de dicha diferencia.
** Datos de Tmax presentados como mediana (rango).
En estudios farmacocinéticos que compararon la biodisponibilidad absoluta y relativa de Effentora y del citrato de fentanilo bucal (CFB), la velocidad y el grado de absorción del fentanilo de Effentora demostraron que la exposición era un 30%-50% mayor que la obtenida con el citrato de fentanilo transmucosa. Si se cambia desde otro producto de citrato de fentanilo oral, se precisa un ajuste de la dosis independiente con Effentora puesto que la biodisponibilidad difiere notablemente de uno a otro producto. Sin embargo, en estos pacientes se puede considerar una dosis inicial mayor de 100 microgramos.
Concentración plasmática media frente a tiempo Perfiles tras la administración de dosis únicas de EFFENTORA y CFB en sujetos sanos
-©- 400 mcg EFFENTORA
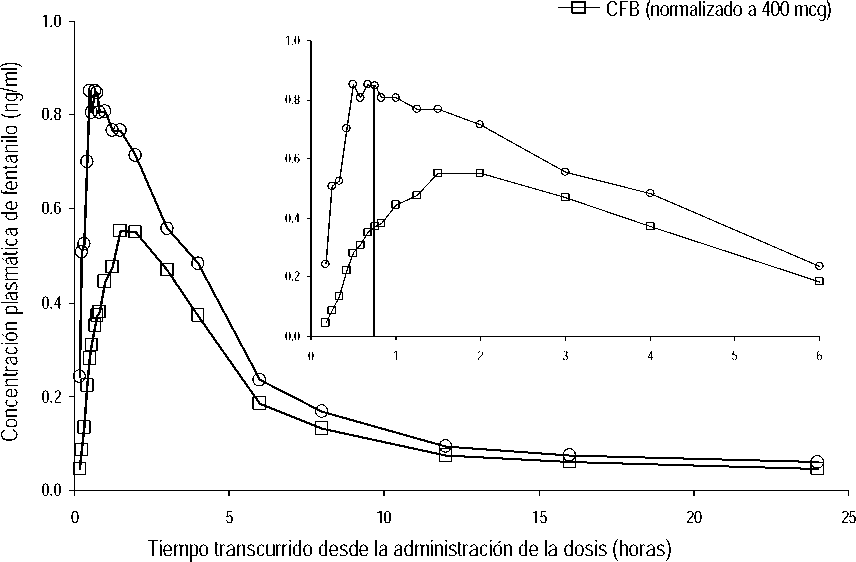
Los datos de CFB se presentan ajustados (de 800 mcg a 400 mcg).
En un ensayo clínico de pacientes con mucositis de grado 1, se observaron diferencias en la exposición con Effentora. La Cmax y la AUC0-8 fueron entre un 1% y un 25% mayores en los pacientes con mucositis que en los pacientes sin mucositis, respectivamente. Las diferencias observadas no fueron clínicamente significativas.
Distribución
El fentanilo es altamente lipofílico y se distribuye rápidamente fuera del sistema vascular, con un elevado volumen de distribución aparente. Tras la administración bucal de Effentora, el fentanilo experimenta una rápida distribución inicial que representa un equilibrio del fentanilo entre el plasma y los tejidos altamente perfundidos (cerebro, corazón y pulmones). Posteriormente, el fentanilo se redistribuye entre el compartimiento de los tejidos profundos (músculos y tejido adiposo) y el plasma.
La unión del fentanilo a las proteínas plasmáticas es del 80% al 85%. La principal proteína de unión es la alfa-1-ácido-glucoproteína, si bien tanto la albúmina como las lipoproteínas contribuyen en cierta medida. La fracción libre de fentanilo aumenta con la acidosis.
Biotransformación
En los ensayos clínicos no se han caracterizado las rutas metabólicas tras la administración bucal de Effentora. El fentanilo se metaboliza a norfentanilo en el hígado y en la mucosa intestinal por acción de la isoforma CYP3A4. El norfentanilo no es activo farmacológicamente en los estudios en animales. Más del 90% de la dosis administrada de fentanilo se elimina por biotransformación en metabolitos inactivos N-desalquilados e hidroxilados.
Eliminación
Tras la administración intravenosa de fentanilo, menos del 7% de la dosis administrada se elimina inalterada en la orina, y solamente un 1% se excreta inalterada en las heces. Los metabolitos se excretan principalmente en la orina, mientras que la excreción fecal es menos importante.
Tras la administración de Effentora, la fase de eliminación terminal de fentanilo es el resultado de la redistribución entre el plasma y el compartimiento de los tejidos profundos. Esta fase de eliminación es lenta, con una mediana de la semivida de eliminación terminal t1/2 de aproximadamente 22 horas tras la administración bucal de la formulación efervescente y de aproximadamente 18 horas tras la administración intravenosa. El aclaramiento en plasma total del fentanilo después de la administración intravenosa es aproximadamente de 42 l/h.
Linealidad/no linealidad
Se ha demostrado la proporcionalidad de la dosis desde 100 microgramos hasta 1.000 microgramos.
5.3 Datos preclínicos sobre seguridad
Los datos de los estudios no clínicos no muestran riesgos especiales para los seres humanos según los estudios convencionales de farmacología de seguridad, toxicidad a dosis repetidas, genotoxicidad y carcinogenicidad.
Los estudios de toxicidad del desarrollo embrionario y fetal llevados a cabo en ratas y conejos no evidenciaron malformaciones ni alteraciones del desarrollo inducidas por el fármaco, administrado durante el período de la organogénesis.
En un estudio de fertilidad y desarrollo embrionario temprano, en ratas, se observó un efecto asociado a los machos a altas dosis (300 mcg/kg/día s.c.) y se considera secundario a los efectos sedantes del fentanilo en estudios animales.
En estudios sobre el desarrollo pre y postnatal en ratas, la tasa de supervivencia de la progenie se redujo significativamente a dosis que causaban toxicidad materna severa. Los hallazgos adicionales en las crías de la generación F1, tras dosis maternales tóxicas, fueron retraso del desarrollo físico, de las funciones sensoriales, reflejos y comportamiento. Dichos efectos pueden ser indirectos debidos a una alteración de los cuidados maternos y/o disminución de la frecuencia de la lactancia o bien un efecto directo del fentanilo sobre las crías.
Los estudios de carcinogenicidad (bioensayo dérmico alternativo de 26 semanas en ratones transgénicos Tg.AC; estudio de carcinogenicidad subcutánea de 2 años en ratas) con fentanilo no pusieron de manifiesto ningún hallazgo indicativo de potencial oncogénico. La evaluación de los cortes laminares de cerebro del estudio de carcinogenicidad en ratas mostró lesiones cerebrales en los animales tratados con dosis altas de citrato de fentanilo. Se desconoce la relevancia de estos hallazgos para los seres humanos.
6. DATOS FARMACÉUTICOS
6.1 Lista de excipientes
Manitol
Carboximetilalmidón sódico tipo A Hidrogenocarbonato de sodio Carbonato de sodio anhidro Ácido cítrico anhidro Estearato de magnesio
6.2 Incompatibilidades
No procede.
6.3 Periodo de validez
3 años
6.4 Precauciones especiales de conservación
Conservar en el embalaje original para protegerlo de la humedad.
6.5 Naturaleza y contenido del envase
Blister laminado de PVC/lámina de aluminio/poliamida/PVC con cierre de papel/poliéster.
Los blister se presentan en cajas de 4 ó 28 comprimidos. Puede que solamente estén comercializados algunos tamaños de envases.
6.6 Precauciones especiales de eliminación
Hay que explicar a los pacientes y a sus cuidadores que desechen todos los comprimidos sin abrir que les sobren cuando ya no necesiten más el tratamiento.
La eliminación del medicamento utilizado o no utilizado pero que ya no se necesita y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V.
Swensweg 5 2031 GA Haarlem Países Bajos
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/08/441/005-006
9. FECHA DE LA PRIMERA AUTORIZACIÓN/RENOVACIÓN DE LA AUTORIZACIÓN
Fecha de la primera autorización: 20 febrero 2013
10. FECHA DE LA REVISIÓN DEL TEXTO
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos http://www.ema.europa.eu.
1. NOMBRE DEL MEDICAMENTO
Effentora 600 microgramos comprimidos bucales
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada comprimido bucal contiene 600 microgramos de fentanilo (como citrato).
Excipiente(s) con efecto conocido: Cada comprimido contiene 20 mg de sodio. Para consultar la lista completa de excipientes, ver sección 6.1.
3. FORMA FARMACÉUTICA
Comprimido bucal.
Comprimido de caras planas, de color blanco, redondo y con bordes biselados, con una "C” grabado en una cara y en la otra con “6”
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
Effentora está indicado para el tratamiento del dolor irruptivo (DI) en pacientes adultos con cáncer que ya reciben tratamiento de mantenimiento con opioides para el dolor crónico asociado a cáncer.
El DI es una exacerbación transitoria del dolor que se produce sobre un fondo de dolor persistente controlado por otros medios.
Los pacientes que reciben tratamiento de mantenimiento con opioides son los que toman como mínimo 60 mg de morfina oral diarios, 25 microgramos de fentanilo transdérmico cada hora, 30 mg de oxicodona diarios, 8 mg de hidromorfona oral diarios o una dosis equianalgésica de otro opioide durante una semana o más.
4.2 Posología y forma de administración
El tratamiento debe ser instaurado y seguido bajo las directrices de un médico experimentado en la terapia con opioides en pacientes con cáncer. Los médicos deben considerar el riesgo del abuso del fentanilo. Se debe advertir al paciente que no debe utilizar dos concentraciones diferentes de fentanilo al mismo tiempo para el tratamiento del dolor irruptivo y que debe desechar cualquier producto de fentanilo prescrito para el dolor irruptivo cuando cambie a Effentora. Con objeto de prevenir confusiones y posibles sobredosis, los pacientes deben disponer en cada momento del mínimo número de concentraciones de los comprimidos.
Posología
Ajuste de la dosis
Effentora debe ajustarse de forma individual hasta obtener una dosis “eficaz” que proporcione la analgesia adecuada y minimice las reacciones adversas. En los ensayos clínicos, la dosis eficaz de Effentora para el DI no pudo predecirse a partir de la dosis diaria de mantenimiento de opioides.
Los pacientes deben monitorizarse cuidadosamente hasta que se establezca la dosis eficaz.
Ajuste de la dosis en pacientes que no cambian a Effentora desde otros medicamentos que contienen fentanilo
La dosis inicial de Effentora debe ser de 100 microgramos, que se incrementará según sea necesario dentro del rango de concentraciones de dosificación disponibles (100, 200, 400, 600 y 800 microgramos).
Ajuste de la dosis en pacientes que cambian a Effentora tras recibir otros medicamentos que contienen fentanilo
Debido a los diferentes perfiles de absorción, el cambio no debe hacerse en una proporción de 1:1. Si el cambio se hace desde otro medicamento de fentanilo como citrato oral, se precisa un ajuste de la dosis independiente con Effentora puesto que la biodisponibilidad difiere notablemente de un medicamento a otro. Sin embargo, en estos pacientes se puede considerar una dosis inicial mayor de 100 microgramos.
Proceso de ajuste de la dosis
Durante el ajuste de la dosis, si no se consigue una analgesia adecuada en los 30 minutos siguientes a la administración de un único comprimido, puede administrarse un segundo comprimido de Effentora de la misma concentración.
Si para tratar un episodio de DI se precisa más de un comprimido, para el tratamiento de futuros episodios de DI debe considerarse un aumento de la dosis hasta la siguiente concentración disponible.
Durante el proceso de ajuste de la dosis, se pueden combinar diferentes comprimidos. Se pueden utilizar hasta cuatro comprimidos de 100 microgramos o hasta cuatro comprimidos de 200 microgramos para tratar un episodio aislado de DI durante el proceso de ajuste de la dosis de acuerdo con el siguiente esquema:
• Si el comprimido inicial de 100 microgramos no es eficaz, se podrá prescribir al paciente dos comprimidos de 100 microgramos para tratar el siguiente episodio de DI. Se recomienda colocar un comprimido a cada lado de la boca. Si se establece que esa es la dosis eficaz, los futuros episodios de DI podrán seguir tratándose con un único comprimido de Effentora de
200 microgramos.
• Si un único comprimido de Effentora de 200 microgramos (o dos comprimidos de 100 microgramos) no resulta eficaz, podrá prescribirse al paciente dos comprimidos de
200 microgramos (o cuatro comprimidos de 100 microgramos) para tratar el siguiente episodio de DI. Se recomienda colocar dos comprimidos a cada lado de la boca. Si se considera que esa es la dosis eficaz, los futuros episodios de DI podrán seguir tratándose con un único comprimido de Effentora de 400 microgramos.
• Para el ajuste de la dosis con comprimidos de 600 microgramos y 800 microgramos, deben utilizarse comprimidos de 200 microgramos.
En los ensayos clínicos no se evaluaron dosis de más de 800 microgramos.
No deben utilizarse más de dos comprimidos para tratar un mismo episodio de DI, salvo cuando el ajuste de la dosis se realice utilizando cuatro comprimidos, como se ha explicado antes.
Durante el ajuste de la dosis, los pacientes deben esperar al menos 4 horas antes de tratar otro episodio de DI con Effentora.
Tratamiento de mantenimiento
Una vez determinada la dosis eficaz por medio del proceso de ajuste, los pacientes deben mantener esa dosis y limitar el consumo a un solo comprimido con la concentración que corresponda.
Los episodios de dolor irruptivo pueden variar en intensidad y la dosis de Effentora requerida puede aumentar con el tiempo debido a una progresión de la enfermedad oncológica subyacente. En estos casos se puede utilizar un segundo comprimido de Effentora de la misma concentración.
En caso de que se necesite un segundo comprimido de Effentora en diversas ocasiones consecutivas, se deberá reajustar la dosis de mantenimiento habitual (ver más abajo).
Durante el tratamiento de mantenimiento, los pacientes deben esperar al menos 4 horas antes de tratar otro episodio de DI con Effentora.
Reajuste de la dosis
La dosis de mantenimiento de Effentora debe aumentarse si el paciente necesita más de un comprimido por episodio de DI en varios episodios consecutivos de DI. Para el reajuste de la dosis se aplican los mismos principios descritos para Ajuste de la dosis (ver más arriba).
Si el paciente presenta con frecuencia más de cuatro episodios de DI en 24 horas, se debe volver a calcular la dosis del tratamiento de mantenimiento con opioides.
Interrupción del tratamiento
El tratamiento con Effentora se debe interrumpir inmediatamente si el paciente ya no presenta episodios de dolor irruptivo. El tratamiento del dolor de base persistente se debe mantener tal como estaba prescrito.
Si es necesario interrumpir la totalidad del tratamiento con opioides, el médico debe realizar un estrecho seguimiento del paciente con el fin de controlar el riesgo de efectos abruptos de abstinencia.
Pacientes con insuficiencia hepática o renal:
Effentora debe utilizarse con precaución en pacientes con insuficiencia hepática o renal moderada o grave (ver sección 4.4).
Pacientes con xerostomía:
Se recomienda a los pacientes con xerostomía beber agua para humedecerse la cavidad bucal antes de la administración de Effentora. Si esta recomendación no basta para lograr una efervescencia suficiente, es posible que haya que cambiar de tratamiento.
Pacientes de edad avanzada (mayores de 65 años)
En los ensayos clínicos se ha observado que los pacientes mayores de 65 años necesitan dosis más bajas que los pacientes más jóvenes. Se recomienda especial precaución al ajustar la dosis de Effentora en pacientes de edad avanzada.
Población pediátrica:
No se ha establecido la seguridad y eficacia de Effentora en niños de 0 a 18 años. No se dispone de datos.
Forma de administración:
Cuando el comprimido de Effentora se expone a la humedad, inicia una reacción efervescente en la que se libera el principio activo. Por ello debe advertirse a los pacientes que no abran el blister hasta el instante antes de colocarse el comprimido en la cavidad bucal.
Apertura del blister
Se debe explicar al paciente que NO trate de sacar el comprimido presionándolo contra el blister, porque eso puede dañar el comprimido bucal. La forma correcta de sacar el comprimido del blister es la siguiente:
Separar una de las unidades del blister del resto rasgándola por las perforaciones. Seguidamente, doblar la unidad del blister a lo largo de la línea impresa en la lámina posterior. Retirar la lámina posterior para dejar expuesto el comprimido.
También debe pedirse al paciente que no intente triturar ni partir el comprimido.
El comprimido no debe guardarse después de sacarlo del blister, pues no es posible garantizar su integridad ni evitar el riesgo de exposición accidental al medicamento.
Administración del comprimido
Los pacientes deben extraer el comprimido del alveolo blister e inmediatamente colocar el comprimido de Effentora entero en la cavidad bucal (cerca de un molar, entre la mejilla y la encía).
El comprimido de Effentora no debe chuparse, masticarse ni tragarse, ya que eso produciría unas concentraciones plasmáticas más bajas que cuando se disgrega en la boca.
Effentora debe colocarse y mantenerse dentro de la cavidad bucal durante el tiempo necesario para la disgregación del comprimido, que suele tardar unos 14-25 minutos.
Como alternativa el comprimido puede colocarse en el espacio sublingual (ver sección 5.2).
Si al cabo de 30 minutos siguen quedando restos del comprimido de Effentora, podrán tragarse con un vaso de agua.
El periodo de tiempo que tarda el comprimido en disgregarse completamente después de su administración bucal no parece que afecte a la exposición sistémica temprana al fentanilo.
Los pacientes no deben consumir ningún alimento ni bebida mientras tengan el comprimido en la cavidad bucal.
En caso de irritación de la mucosa bucal, se recomienda cambiar el lugar de colocación del comprimido dentro de la cavidad bucal.
4.3 Contraindicaciones
Hipersensibilidad al principio activo o a alguno de los excipientes incluidos en la sección 6.1.
Pacientes que no estén en tratamiento de mantenimiento con opioides, por el mayor riesgo de depresión respiratoria.
Depresión respiratoria grave o enfermedad pulmonar obstructiva grave.
Tratamiento del dolor agudo distinto al dolor irruptivo.
4.4 Advertencias y precauciones especiales de empleo
Debe advertirse a los pacientes y a sus cuidadores que Effentora contiene un principio activo en cantidades que pueden causar la muerte, especialmente a un niño. Por lo que todos los comprimidos deben mantenerse fuera de la vista y del alcance de los niños.
Con el fin de minimizar los riesgos de efectos adversos relacionados con los opioides y para establecer la dosis eficaz, es indispensable que los profesionales sanitarios monitoricen cuidadosamente a los pacientes durante el proceso de ajuste de la dosis.
Es importante que el tratamiento con opioides de acción prolongada utilizados para tratar el dolor persistente del paciente se haya estabilizado antes de iniciar el tratamiento con Effentora y que el paciente prosiga el tratamiento con el opioide de larga duración mientras esté tomando Effentora.
Depresión respiratoria
Como con todos los opioides, hay riesgo de depresión respiratoria clínicamente significativa asociada al uso de fentanilo. . La selección inapropiada del paciente (ej. uso en pacientes que no reciben tratamiento de mantenimiento con opioides) y/o la dosis incorrecta ha tenido desenlace mortales con el uso de Effentora así como con otros productos a base de fentanilo.
Effentora sólo debe ser usado según las condiciones descritas en la sección 4.1
Enfermedad pulmonar obstructiva crónica
Debe prestarse especial atención al ajuste de la dosis de Effentora en pacientes con enfermedad pulmonar obstructiva crónica no grave u otras afecciones que les predispongan a una depresión respiratoria, ya que incluso las dosis terapéuticas habituales de Effentora pueden reducir el impulso respiratorio hasta provocar insuficiencia respiratoria.
Aumento de la presión intracraneal, alteración del estado de conciencia
Effentora sólo debe administrarse con precaución extrema en pacientes que puedan ser especialmente sensibles a los efectos intracraneales de la retención de CO2, como aquellos con un aumento constatado de la presión intracraneal o con alteración del estado de conciencia. Los opioides pueden enmascarar la evolución clínica de un paciente con lesiones en la cabeza, y sólo deben utilizarse si están clínicamente justificados.
Enfermedad cardíaca
El fentanilo puede provocar bradicardia y debe administrarse con precaución en pacientes con bradiarritmias previas o ya existentes.
Insuficiencia renal o hepática
Además, Effentora debe administrarse con precaución a pacientes con insuficiencia hepática o renal. No se ha valorado la influencia de la insuficiencia hepática o renal sobre la farmacocinética del medicamento; sin embargo, cuando éste se administra por vía intravenosa, se ha comprobado que el aclaramiento del fentanilo está alterado en las enfermedades hepáticas y renales debido a la alteración del aclaramiento metabólico y de las proteínas plasmáticas. Tras la administración de Effentora, la insuficiencia hepática y la insuficiencia renal pueden ambas aumentar la biodisponibilidad del fentanilo ingerido y disminuir su aclaramiento sistémico, lo cual puede aumentar y prolongar los efectos opioides. Así pues, debe prestarse especial atención al ajuste de la dosis en pacientes con enfermedad hepática o renal moderada o grave.
Se deben tomar precauciones especiales en pacientes con hipovolemia e hipotensión.
Sindrome serotoninérgico
Se recomienda precaución cuando Effentora se administre de forma concomitante con fármacos que afecten a los sistemas de neurotransmisores serotoninérgicos.
El desarrollo de un síndrome serotoninérgico potencialmente mortal puede aparecer con el uso concomitante de fármacos serotoninérgicos, como los inhibidores selectivos de la recaptación de serotonina (ISRS) y los inhibidores de la recaptación de serotonina y noradrenalina (IRSN), y con los fármacos que afectan al metabolismo de la serotonina (incluidos los inhibidores de la monoamino oxidasa [IMAO]). Esto puede ocurrir con la dosis recomendada.
El síndrome serotoninérgico puede incluir cambios en el estado mental (p. ej., agitación, alucinaciones, coma), inestabilidad autonómica (p. ej., taquicardia, presión arterial lábil, hipertermia), anomalías neuromusculares (p. ej., hiperreflexia, descoordinación, rigidez) y/o síntomas gastrointestinales (p. ej., náuseas, vómitos, diarrea).
Si se sospecha de un síndrome serotoninérgico, debe suspenderse el tratamiento con Effentora. Tolerancia, dependencia
La administración repetida de opioides como el fentanilo puede inducir tolerancia y dependencia física y/o psicológica. Sin embargo, rara vez se produce adicción iatrogénica por el uso terapéutico de opioides.
Dietas pobres en sodio
Este medicamento contiene 20 mg de sodio por comprimido, lo que debe ser tenido en cuenta en pacientes con dietas pobres en sodio.
Anafilaxia e hipersensibilidad
Se han notificado anafilaxia e hipersensibilidad asociados al uso de medicamentos de fentanilo por vía oral transmucosa (ver sección 4.8).
4.5 Interacción con otros medicamentos y otras formas de interacción
El fentanilo se metaboliza por medio del sistema del isoenzima 3A4 del citocromo P450 (CYP3A4), por lo que pueden producirse interacciones cuando Effentora se administra concomitantemente con fármacos que afectan a la actividad de CYP3A4. La administración concomitante de fármacos que inducen la actividad 3A4 puede reducir la eficacia de Effentora. El uso concomitante de Effentora con inhibidores potentes del CYP3A4 (como ritonavir, ketoconazol, itraconazol, troleandomicina, claritromicina y nelfinavir) o inhibidores moderados del CYP3A4 (como aprenavir, aprepitant, diltiazem, eritromicina, fluconazol, fosamprenavir, zumo de pomelo y verapamilo) puede aumentar la concentración plasmática de fentanilo, causando en ocasiones reacciones adversas graves, incluida una depresión respiratoria mortal. Los pacientes que reciban Effentora e inhibidores moderados o potentes del CYP3A4 concomitantemente deben controlarse estrictamente durante un amplio período de tiempo. El aumento de la dosis debe realizarse con precaución.
El uso concomitante con otros depresores del sistema nervioso central, incluidos otros opioides, sedantes o hipnóticos, anestésicos generales, fenotiazinas, tranquilizantes, relajantes musculares, antihistamínicos sedantes y alcohol, puede producir efectos depresivos aditivos.
No se recomienda el uso de Effentora en pacientes que hayan recibido inhibidores de la monoamino oxidasa (MAO) en los 14 días anteriores, porque se ha descrito que los inhibidores de la MAO producen una potenciación grave e impredecible de los analgésicos opioides.
No se recomienda el uso concomitante de agonistas/antagonistas opioides parciales (p.ej. buprenorfina, nalbufina, pentazocina) ya que poseen una elevada afinidad por los receptores opioides con una actividad intrínseca relativamente baja y en consecuencia antagonizan parcialmente el efecto analgésico del fentanilo, pudiendo inducir síntomas de abstinencia en pacientes dependientes de opioides.
Fármacos serotoninérgicos
La administración concomitante de fentanilo con un fármaco serotoninérgico, como un inhibidor selectivo de la recaptación de serotonina (ISRS), un inhibidor de la recaptación de serotonina y noradrenalina (IRSN) o un inhibidor de la monoamino oxidasa (IMAO), puede aumentar el riesgo de síndrome serotoninérgico, un trastorno potencialmente mortal.
4.6 Fertilidad, embarazo y lactancia
Embarazo
No hay datos suficientes relativos al uso de de fentanilo en mujeres embarazadas. Los estudios realizados en animales han mostrado toxicidad para la reproducción (ver sección 5.3). Se desconoce el riesgo potencial en seres humanos. No debe utilizarse Effentora durante el embarazo a no ser que fuese absolutamente necesario.
El tratamiento prolongado durante el embarazo puede causar síntomas de abstinencia en el recién nacido.
Se aconseja no administrar fentanilo durante el parto (aunque sea por cesárea), ya que atraviesa la placenta y puede causar depresión respiratoria en el feto. Si se administra Effentora, debe disponerse fácilmente de un antídoto para el niño.
Lactancia
El fentanilo se excreta a través de la leche materna y puede causar sedación y depresión respiratoria en el lactante. El fentanilo no debe utilizarse durante la lactancia, no pudiendo reiniciarse la lactancia hasta transcurridos como mínimo 5 días de la última administración de fentanilo.
Fertilidad
No existen datos sobre la fertilidad en humanos. En los estudios realizados con animales, la fertilidad en machos se vio afectada (ver sección 5.3).
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
No se han realizado estudios de los efectos sobre la capacidad para conducir y utilizar máquinas. No obstante, los analgésicos opioides pueden disminuir la capacidad mental y/o física necesaria para realizar tareas potencialmente peligrosas (p. ej., conducir un coche o utilizar maquinaria). Debe advertirse a los pacientes de que no conduzcan ni utilicen maquinaria si sienten somnolencia, mareos o alteraciones visuales mientras toman Effentora, y de que no conduzcan ni utilicen maquinaria hasta que no sepan cómo van a reaccionar.
4.8 Reacciones adversas
Resumen del perfil de seguridad
Las reacciones adversas que pueden esperarse de Effentora son las típicas de los opioides. Frecuentemente, esos efectos adversos propios de los opioides cesan o disminuyen en intensidad con el uso continuado del medicamento, o con el ajuste de la dosis más adecuada para el paciente. No obstante, las reacciones adversas más graves son depresión respiratoria (que potencialmente puede culminar en apnea o parada respiratoria), depresión circulatoria, hipotensión y colapso, reacciones que deben vigilarse estrechamente en todos los pacientes.
Los ensayos clínicos con Effentora se diseñaron para valorar la seguridad y eficacia en el tratamiento del DI, y todos los pacientes tomaban ya opioides de forma concomitante, como morfina de liberación prolongada o fentanilo transdérmico, para su dolor persistente. Por consiguiente, no es posible distinguir con exactitud los efectos de Effentora solo.
Tabla de reacciones adversas
Se han notificado las siguientes reacciones adversas con Effentora y/u otros compuestos que contienen fentanilo provenientes de ensayos clínicos y de la experiencia postcomercialización. Las reacciones adversas se enumeran a continuación según el término preferente de MedDRA por el sistema de clasificación de órganos y frecuencia (frecuencias se definen como: muy frecuentes >1/10, frecuentes >1/100 a <1/10, poco frecuentes > 1/1.000 a < 1/100, raras >1/10.000 a <1/1.000, frecuencia no conocida (no puede estimarse a partir de los datos disponibles); las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada intervalo de frecuencia):
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Infecciones e infestaciones |
Candidiasis oral |
Faringitis |
Pústula oral | ||
|
Trastornos de la sangre y del sistema linfático |
Anemia Neutropenia |
Trombocito-penia | |||
|
Trastornos del sistema inmunológico |
Hipersensib ilidad | ||||
|
Trastornos endocrinos |
Hipogonadis mo | ||||
|
Trastornos del metabolismo y de la nutrición |
Anorexia | ||||
|
Trastornos psiquiátricos |
Depresión Ansiedad Estado confusional Insomnio |
Euforia Nerviosismo Alucinaciones Alucinaciones visuales Cambios del estado mental Drogodependencia (adicción) Desorientación |
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Trastornos del sistema nervioso |
Mareo Cefalea |
Disgeusia Somnolencia Letargia Temblores Sedación Hipoestesia Migraña |
Nivel de conciencia deprimido Trastornos de la atención Trastorno del equilibrio Disartria |
Trastorno cognitivo Disfunción motora |
Pérdida de consciencia Convulsión |
|
Trastornos oculares |
Alteraciones de la visión Hiperemia ocular Visión borrosa Disminución de la agudeza visual |
Sensación anómala en el ojo Fotopsia | |||
|
Trastornos del oído y del laberinto |
Vértigo Acúfenos Molestias en el oído | ||||
|
Trastornos cardiacos |
Taquicardia |
Bradicardia | |||
|
Trastornos vasculares |
Hipotensión Hipertensión |
Enrojecimiento Sofocos | |||
|
Trastornos respiratorios, torácicos y mediastínicos |
Disnea Dolor faringolarínge o |
Depresión respiratoria Síndrome de apnea del sueño |
Paro respiratorio | ||
|
Trastornos gastrointestinales |
Náuseas Vómitos |
Estreñimiento Estomatitis Sequedad de boca Diarrea Dolor abdominal Enfermedad por reflujo gastroesofágic o Molestias estomacales Dispepsia Dolor dental |
Íleo Ulceración de la boca Hipoestesia oral Molestias orales Decoloración de la mucosa oral Trastorno de los tejidos blandos de la boca Glosodinia Ampollas en la lengua Dolor gingival Ulceración de la lengua Trastornos de la lengua Esofagitis Labios agrietados Trastornos dentales |
Ampollas en la mucosa oral Labios secos | |
|
Trastornos hepatobiliares |
Dilatación biliar | ||||
|
Trastornos de la piel y del tejido subcutáneo |
Prurito Hiperhidrosis Rash |
Sudor frío Edema facial Prurito generalizado Alopecia |
Onicorrexia |
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Trastornos musculoesqueléticos y del tejido conjuntivo |
Mialgia Dolor de espalda |
Calambres musculares Debilidad muscular | |||
|
Trastornos renales y urinarios |
Retención urinaria | ||||
|
Trastornos generales y alteraciones en el lugar de administración |
Reacciones en el lugar de la aplicación, como sangrado, dolor, úlcera, irritación, parestesia, anestesia, eritema, edema, hinchazón y vesículas |
Edema periférico Fatiga Astenia Síndrome de abstinencia Escalofríos |
Malestar general Pereza Molestias en el pecho Sensaciones anormales Sensación de inquietud Sed Sensación de frío Sensación de calor |
Pirexia | |
|
Exploraciones complementarias |
Disminución de peso |
Descenso del recuento de plaquetas Aumento de la frecuencia cardiaca Descenso del hematocrito Descenso de la hemoglobina | |||
|
Lesiones traumáticas, intoxicaciones y complicaciones de procedimientos terapéuticos |
Caídas |
Descripción de las reacciones adversas seleccionadas
Tras la administración repetida de opioides como fentanilo puede desarrollarse tolerancia, dependencia física y/o psicológica.
Con fentanilo por vía transmucosa se han observado síntomas de abstinencia de opioides tales como náuseas, vómitos, diarrea, ansiedad, escalofríos, temblor y sudoración.
Se han observado pérdida de consciencia y paro respiratorio en el contexto de una sobredosis.
Se han notificado reacciones de hipersensibilidad en la experiencia postcomercialización, incluidos prurito, eritema, edema labial y facial y urticaria.
Notificación de sospechas de reacciones adversas
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del sistema nacional de notificación incluido en el Anexo V.
4.9 Sobredosis
Los síntomas de sobredosis con fentanilo son de naturaleza similar a los del fentanilo intravenoso y a los demás opioides, y son una prolongación de sus acciones farmacológicas, siendo los efectos graves más significativos la alteración del estado mental, pérdida de la consciencia, hipotensión, la depresión respiratoria, distrés respiratorio y el fallo respiratorio con resultado de muerte.
El tratamiento inmediato en caso de sobredosis de opioides consiste en retirar el comprimido bucal de Effentora, si el paciente todavía lo tiene en la boca, asegurando la apertura de las vías respiratorias; estimulación física y verbal del paciente; valoración del grado de conciencia, el estado ventilatorio y circulatorio; y respiración asistida (soporte ventilatorio) en caso necesario.
Para el tratamiento de una sobredosis (ingestión accidental) en una persona que no haya tomado nunca opioides, se debe colocar una vía intravenosa y utilizar naloxona u otros antagonistas de los opioides según esté indicado clínicamente. La depresión respiratoria causada por la sobredosis puede durar más que los efectos de la acción del antagonista de los opioides (así, la semivida de la naloxona varía de 30 a 81 minutos), por lo que puede ser necesaria la administración repetida. Consultar los detalles sobre este tipo de uso en la ficha técnica del antagonista de los opioides utilizado.
Para el tratamiento de una sobredosis en pacientes mantenidos con opioides, debe colocarse una vía intravenosa. El uso moderado de naloxona u otro antagonista opioide puede estar justificado en algunos casos, pero se asocia al riesgo de precipitar la aparición de un síndrome de abstinencia agudo.
Aunque no se ha observado rigidez muscular que interfiera con la respiración después del uso de Effentora, es una reacción que puede manifestarse con fentanilo y otros opioides. Si aparece, debe tratarse con respiración asistida, un antagonista de los opioides y, como último recurso, un agente bloqueante neuromuscular.
5. PROPIEDADES FARMACOLÓGICAS
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: analgésicos; opioides Código ATC: N02AB03.
El fentanilo es un analgésico opioide que actúa principalmente sobre los receptores de opioides p. Sus efectos terapéuticos principales son la analgesia y la sedación. Los efectos farmacológicos secundarios son depresión respiratoria, bradicardia, hipotermia, estreñimiento, miosis, dependencia física y euforia.
Los efectos analgésicos del fentanilo están relacionados con su concentración plasmática. En general, la concentración eficaz y la concentración a la que aparece toxicidad aumentan a medida que aumenta la tolerancia a los opioides. La velocidad de aparición de tolerancia varía mucho de una persona a otra. En consecuencia, la dosis de Effentora debe ajustarse individualmente para conseguir el efecto deseado (ver sección 4.2).
Todos los agonistas de los receptores de opioides p, entre ellos el fentanilo, producen depresión respiratoria dependiente de la dosis. El riesgo de depresión respiratoria es menor en pacientes que reciben tratamiento crónico con opioides, puesto que desarrollan tolerancia a los efectos de depresión respiratoria.
La seguridad y eficacia de Effentora se han evaluado en pacientes que recibieron el medicamento al inicio de un episodio de dolor irruptivo. El uso preventivo de Effentora para episodios de dolor predecibles no se ha investigado en ensayos clínicos. Se han realizado dos ensayos doble ciego, aleatorizados, controlados con placebo y cruzados en un total de 248 pacientes con DI y cáncer que experimentaron una media de 1-4 episodios de DI al día durante el tratamiento de mantenimiento con opioides. Durante una fase inicial abierta, se ajustó la dosis en cada paciente hasta establecer la dosis eficaz de Effentora. Los pacientes en los que se estableció una dosis eficaz entraron en la fase doble ciego del estudio. El criterio principal de eficacia fue la valoración por el propio paciente de la
intensidad del dolor. Los pacientes valoraron la intensidad del dolor utilizando una escala de 11 puntos. En cada episodio de DI se evaluó la intensidad del dolor antes y en varias ocasiones después del tratamiento.
En el 67% de los pacientes se pudo establecer una dosis eficaz.
En el ensayo clínico pivotal (ensayo 1), el criterio de valoración principal fue la media de la suma de las diferencias en los valores de la intensidad del dolor desde el momento de administrar la dosis hasta 60 minutos después, inclusive (SPID60), que fue estadísticamente significativa respecto a placebo
(p<0,0001).
Ensayo 1: Media (+/- EEM) Diferencias en intensidad del dolor en cada valoración
(Serie completa de análisis)
SPID60 media (+/- DE)
EFFENTORA=9,7(5,58) p<0,0001 Placebo=4,9(4,38)
......I
20
Tiempo transcurrido desde la administración de la medicación del ensayo (minutos)
Grupo de tratamiento
x x x EFFENTORA
★★★
Placebo
-t p<0,0001 Effentora trente a placebo, a favor de Effentora, mediante un análisis de la varianza
DID=diferencia en intensidad del dolor; EEM=error estándar de la media
(Sene completa de análisis)
SPID30 media (+/- DE)
EFFENTORA=3,2(2,60) p<0,0001
Placebo=2,0(2,21)
O 5 10 15 30 45 60 90 120
Tiempo transcurrido desde la administración de la medicación del ensayo (minutos)
Grupo de tratamiento xxx EFFENTORA *** Placebo
* p<0,01 Effentora frente a placebo, a favor de Effentora, mediante una prueba de rangos con signo de Wilcoxon para una sola muestra
+ p<0,0001 Effentora frente a placebo, a favor de Effentora, mediante una prueba de rangos con signo de Wilcoxon para una sola muestra
DID=diferencia en intensidad del dolor: EEM=error estándar de la media
En el segundo estudio fundamental (ensayo 2), el criterio de valoración principal fue SPID30, que fue también estadísticamente significativo respecto a placebo (p<0,0001).
Se observó una mejora estadísticamente significativa en la diferencia de intensidad del dolor con Effentora frente a placebo ya a los 10 minutos en el Ensayo 1 y a los 15 minutos (primer punto temporal medido) en el Ensayo 2. En los dos ensayos, esas diferencias siguieron siendo significativas en todos los puntos temporales medidos.
5.2 Propiedades farmacocinéticas
Introducción general
El fentanilo es altamente lipofílico y puede ser absorbido muy rápidamente a través de la mucosa bucal y más lentamente por la vía gastrointestinal convencional. Está sujeto a un efecto de primer paso hepático e intestinal, y los metabolitos no contribuyen a los efectos terapéuticos del fentanilo.
La forma de liberación del principio activo se basa en una reacción efervescente que aumenta la velocidad y el grado de absorción del fentanilo a través de la mucosa bucal. Los cambios transitorios en el pH que acompañan a la reacción efervescente pueden optimizar la disolución (a un pH menor) y la permeabilidad de la membrana (a un pH mayor).
El tiempo de disolución (definido como el tiempo que tarda el comprimido en disgregarse totalmente tras su administración bucal) no afecta a la exposición sistémica temprana al fentanilo. El estudio comparativo entre la administración bucal (es decir entre la encía y la mejilla) y la administración sublingual de un comprimido de 400 mcg de Effentora cumplió los criterios de bioequivalencia.
No se han estudiado los efectos de la insuficiencia renal o hepática sobre la farmacocinética de Effentora.
Tras la administración bucal de Effentora, el fentanilo es absorbido rápidamente con una biodisponibilidad absoluta del 65%. El perfil de absorción de Effentora es, en su mayor parte, el resultado de una absorción rápida inicial a través de la mucosa bucal; las concentraciones plasmáticas máximas según las muestras de sangre venosa suelen alcanzarse generalmente en el transcurso de la hora siguiente a la administración bucal. Alrededor del 50% de la dosis total administrada se absorbe rápidamente por la mucosa bucal y pasa a la circulación sistémica. La otra mitad de la dosis total se traga y se absorbe lentamente en el tubo digestivo. Casi el 30% de la cantidad tragada (50% de la dosis total) escapa a la eliminación hepática e intestinal de primer paso y pasa a estar disponible sistémicamente.
En la siguiente tabla se indican los principales parámetros farmacocinéticos.
Parámetros_farmacocinéticos* en sujetos adultos tratados con Effentora
|
Parámetro farmacocinético (media) |
Effentora 400 microgramos |
|
Biodisponibilidad absoluta |
65% (±20%) |
|
Fracción absorbida por la mucosa |
48% (±31,8%) |
|
Tmax (minuto) ** |
46,8 (20-240) |
|
Cmax (ng/ml) |
1,02 (± 0,42) |
|
AUC0-tmax (ng.h/ml) |
0,40 (± 0,18) |
|
AUC0-inf (ng.h/ml) |
6,48 (± 2,98) |
* Basado en muestras de sangre venosa (plasma). Las concentraciones de citrato de fentanilo en suero fueron superiores a las obtenidas en plasma: La AUC y la Cmax séricas fueron superiores a la AUC y la Cmax plasmáticas aproximadamente en un 20% y un 30%, respectivamente. Se desconoce la razón de dicha diferencia.
** Datos de Tmax presentados como mediana (rango).
En estudios farmacocinéticos que compararon la biodisponibilidad absoluta y relativa de Effentora y del citrato de fentanilo bucal (CFB), la velocidad y el grado de absorción del fentanilo de Effentora demostraron que la exposición era un 30%-50% mayor que la obtenida con el citrato de fentanilo transmucosa. Si se cambia desde otro producto de citrato de fentanilo oral, se precisa un ajuste de la dosis independiente con Effentora puesto que la biodisponibilidad difiere notablemente de uno a otro producto. Sin embargo, en estos pacientes se puede considerar una dosis inicial mayor de 100 microgramos.
Concentración plasmática media frente a tiempo Perfiles tras la administración de dosis únicas de EFFENTORA y CFB en sujetos sanos
-©- 400 mcg EFFENTORA

Los datos de CFB se presentan ajustados (de 800 mcg a 400 mcg).
En un ensayo clínico de pacientes con mucositis de grado 1, se observaron diferencias en la exposición con Effentora. La Cmax y la AUC0-8 fueron entre un 1% y un 25% mayores en los pacientes con mucositis que en los pacientes sin mucositis, respectivamente. Las diferencias observadas no fueron clínicamente significativas.
Distribución
El fentanilo es altamente lipofílico y se distribuye rápidamente fuera del sistema vascular, con un elevado volumen de distribución aparente. Tras la administración bucal de Effentora, el fentanilo experimenta una rápida distribución inicial que representa un equilibrio del fentanilo entre el plasma y los tejidos altamente perfundidos (cerebro, corazón y pulmones). Posteriormente, el fentanilo se redistribuye entre el compartimiento de los tejidos profundos (músculos y tejido adiposo) y el plasma.
La unión del fentanilo a las proteínas plasmáticas es del 80% al 85%. La principal proteína de unión es la alfa-1-ácido-glucoproteína, si bien tanto la albúmina como las lipoproteínas contribuyen en cierta medida. La fracción libre de fentanilo aumenta con la acidosis.
Biotransformación
En los ensayos clínicos no se han caracterizado las rutas metabólicas tras la administración bucal de Effentora. El fentanilo se metaboliza a norfentanilo en el hígado y en la mucosa intestinal por acción de la isoforma CYP3A4. El norfentanilo no es activo farmacológicamente en los estudios en animales. Más del 90% de la dosis administrada de fentanilo se elimina por biotransformación en metabolitos inactivos N-desalquilados e hidroxilados.
Eliminación
Tras la administración intravenosa de fentanilo, menos del 7% de la dosis administrada se elimina inalterada en la orina, y solamente un 1% se excreta inalterada en las heces. Los metabolitos se excretan principalmente en la orina, mientras que la excreción fecal es menos importante.
Tras la administración de Effentora, la fase de eliminación terminal de fentanilo es el resultado de la redistribución entre el plasma y el compartimiento de los tejidos profundos. Esta fase de eliminación es lenta, con una mediana de la semivida de eliminación terminal t1/2 de aproximadamente 22 horas tras la administración bucal de la formulación efervescente y de aproximadamente 18 horas tras la administración intravenosa. El aclaramiento en plasma total del fentanilo después de la administración intravenosa es aproximadamente de 42 l/h.
Linealidad/no linealidad
Se ha demostrado la proporcionalidad de la dosis desde 100 microgramos hasta 1.000 microgramos.
5.3 Datos preclínicos sobre seguridad
Los datos de los estudios no clínicos no muestran riesgos especiales para los seres humanos según los estudios convencionales de farmacología de seguridad, toxicidad a dosis repetidas, genotoxicidad y carcinogenicidad.
Los estudios de toxicidad del desarrollo embrionario y fetal llevados a cabo en ratas y conejos no evidenciaron malformaciones ni alteraciones del desarrollo inducidas por el fármaco, administrado durante el período de la organogénesis.
En un estudio de fertilidad y desarrollo embrionario temprano, en ratas, se observó un efecto asociado a los machos a altas dosis (300 mcg/kg/día s.c.) y se considera secundario a los efectos sedantes del fentanilo en estudios animales.
En estudios sobre el desarrollo pre y postnatal en ratas, la tasa de supervivencia de la progenie se redujo significativamente a dosis que causaban toxicidad materna severa. Los hallazgos adicionales en las crías de la generación F1, tras dosis maternales tóxicas, fueron retraso del desarrollo físico, de las funciones sensoriales, reflejos y comportamiento. Dichos efectos pueden ser indirectos debidos a una alteración de los cuidados maternos y/o disminución de la frecuencia de la lactancia o bien un efecto directo del fentanilo sobre las crías.
Los estudios de carcinogenicidad (bioensayo dérmico alternativo de 26 semanas en ratones transgénicos Tg.AC; estudio de carcinogenicidad subcutánea de 2 años en ratas) con fentanilo no pusieron de manifiesto ningún hallazgo indicativo de potencial oncogénico. La evaluación de los cortes laminares de cerebro del estudio de carcinogenicidad en ratas mostró lesiones cerebrales en los animales tratados con dosis altas de citrato de fentanilo. Se desconoce la relevancia de estos hallazgos para los seres humanos.
6. DATOS FARMACÉUTICOS
6.1 Lista de excipientes
Manitol
Carboximetilalmidón sódico tipo A Hidrogenocarbonato de sodio Carbonato de sodio anhidro Ácido cítrico anhidro Estearato de magnesio
6.2 Incompatibilidades
No procede.
6.3 Periodo de validez
3 años
6.4 Precauciones especiales de conservación
Conservar en el embalaje original para protegerlo de la humedad.
6.5 Naturaleza y contenido del envase
Blister laminado de PVC/lámina de aluminio/poliamida/PVC con cierre de papel/poliéster.
Los blister se presentan en cajas de 4 ó 28 comprimidos. Puede que solamente estén comercializados algunos tamaños de envases.
6.6 Precauciones especiales de eliminación
Hay que explicar a los pacientes y a sus cuidadores que desechen todos los comprimidos sin abrir que les sobren cuando ya no necesiten más el tratamiento.
La eliminación del medicamento utilizado o no utilizado pero que ya no se necesita y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V.
Swensweg 5 2031 GA Haarlem Países Bajos
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/08/441/007-008
9. FECHA DE LA PRIMERA AUTORIZACIÓN/RENOVACIÓN DE LA
AUTORIZACIÓN
Fecha de la primera autorización: 20 febrero 2013
10. FECHA DE LA REVISIÓN DEL TEXTO
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos http://www.ema.europa.eu.
1. NOMBRE DEL MEDICAMENTO
Effentora 800 microgramos comprimidos bucales
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada comprimido bucal contiene 800 microgramos de fentanilo (como citrato).
Excipiente(s) con efecto conocido: Cada comprimido contiene 20 mg de sodio. Para consultar la lista completa de excipientes, ver sección 6.1.
3. FORMA FARMACÉUTICA
Comprimido bucal.
Comprimido de caras planas, de color blanco, redondo y con bordes biselados, con una "C” grabado en una cara y en la otra con “8”
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
Effentora está indicado para el tratamiento del dolor irruptivo (DI) en pacientes adultos con cáncer que ya reciben tratamiento de mantenimiento con opioides para el dolor crónico asociado a cáncer.
El DI es una exacerbación transitoria del dolor que se produce sobre un fondo de dolor persistente controlado por otros medios.
Los pacientes que reciben tratamiento de mantenimiento con opioides son los que toman como mínimo 60 mg de morfina oral diarios, 25 microgramos de fentanilo transdérmico cada hora, 30 mg de oxicodona diarios, 8 mg de hidromorfona oral diarios o una dosis equianalgésica de otro opioide durante una semana o más.
4.2 Posología y forma de administración
El tratamiento debe ser instaurado y seguido bajo las directrices de un médico experimentado en la terapia con opioides en pacientes con cáncer. Los médicos deben considerar el riesgo del abuso del fentanilo. Se debe advertir al paciente que no debe utilizar dos concentraciones diferentes de fentanilo al mismo tiempo para el tratamiento del dolor irruptivo y que debe desechar cualquier producto de fentanilo prescrito para el dolor irruptivo cuando cambie a Effentora. Con objeto de prevenir confusiones y posibles sobredosis, los pacientes deben disponer en cada momento del mínimo número de concentraciones de los comprimidos.
Posología
Ajuste de la dosis
Effentora debe ajustarse de forma individual hasta obtener una dosis “eficaz” que proporcione la analgesia adecuada y minimice las reacciones adversas. En los ensayos clínicos, la dosis eficaz de Effentora para el DI no pudo predecirse a partir de la dosis diaria de mantenimiento de opioides.
Los pacientes deben monitorizarse cuidadosamente hasta que se establezca la dosis eficaz.
Ajuste de la dosis en pacientes que no cambian a Effentora desde otros medicamentos que contienen fentanilo
La dosis inicial de Effentora debe ser de 100 microgramos, que se incrementará según sea necesario dentro del rango de concentraciones de dosificación disponibles (100, 200, 400, 600 y 800 microgramos).
Ajuste de la dosis en pacientes que cambian a Effentora tras recibir otros medicamentos que contienen fentanilo
Debido a los diferentes perfiles de absorción, el cambio no debe hacerse en una proporción de 1:1. Si el cambio se hace desde otro medicamento de fentanilo como citrato oral, se precisa un ajuste de la dosis independiente con Effentora puesto que la biodisponibilidad difiere notablemente de un medicamento a otro. Sin embargo, en estos pacientes se puede considerar una dosis inicial mayor de 100 microgramos.
Proceso de ajuste de la dosis
Durante el ajuste de la dosis, si no se consigue una analgesia adecuada en los 30 minutos siguientes a la administración de un único comprimido, puede administrarse un segundo comprimido de Effentora de la misma concentración.
Si para tratar un episodio de DI se precisa más de un comprimido, para el tratamiento de futuros episodios de DI debe considerarse un aumento de la dosis hasta la siguiente concentración disponible.
Durante el proceso de ajuste de la dosis, se pueden combinar diferentes comprimidos. Se pueden utilizar hasta cuatro comprimidos de 100 microgramos o hasta cuatro comprimidos de 200 microgramos para tratar un episodio aislado de DI durante el proceso de ajuste de la dosis de acuerdo con el siguiente esquema:
• Si el comprimido inicial de 100 microgramos no es eficaz, se podrá prescribir al paciente dos comprimidos de 100 microgramos para tratar el siguiente episodio de DI. Se recomienda colocar un comprimido a cada lado de la boca. Si se establece que esa es la dosis eficaz, los futuros episodios de DI podrán seguir tratándose con un único comprimido de Effentora de
200 microgramos.
• Si un único comprimido de Effentora de 200 microgramos (o dos comprimidos de 100 microgramos) no resulta eficaz, podrá prescribirse al paciente dos comprimidos de
200 microgramos (o cuatro comprimidos de 100 microgramos) para tratar el siguiente episodio de DI. Se recomienda colocar dos comprimidos a cada lado de la boca. Si se considera que esa es la dosis eficaz, los futuros episodios de DI podrán seguir tratándose con un único comprimido de Effentora de 400 microgramos.
• Para el ajuste de la dosis con comprimidos de 600 microgramos y 800 microgramos, deben utilizarse comprimidos de 200 microgramos.
En los ensayos clínicos no se evaluaron dosis de más de 800 microgramos.
No deben utilizarse más de dos comprimidos para tratar un mismo episodio de DI, salvo cuando el ajuste de la dosis se realice utilizando cuatro comprimidos, como se ha explicado antes.
Durante el ajuste de la dosis, los pacientes deben esperar al menos 4 horas antes de tratar otro episodio de DI con Effentora.
Tratamiento de mantenimiento
Una vez determinada la dosis eficaz por medio del proceso de ajuste, los pacientes deben mantener esa dosis y limitar el consumo a un solo comprimido con la concentración que corresponda.
Los episodios de dolor irruptivo pueden variar en intensidad y la dosis de Effentora requerida puede aumentar con el tiempo debido a una progresión de la enfermedad oncológica subyacente. En estos casos se puede utilizar un segundo comprimido de Effentora de la misma concentración.
En caso de que se necesite un segundo comprimido de Effentora en diversas ocasiones consecutivas, se deberá reajustar la dosis de mantenimiento habitual (ver más abajo).Durante el tratamiento de mantenimiento, los pacientes deben esperar al menos 4 horas antes de tratar otro episodio de DI con Effentora.
Reajuste de la dosis
La dosis de mantenimiento de Effentora debe aumentarse si el paciente necesita más de un comprimido por episodio de DI en varios episodios consecutivos de DI. Para el reajuste de la dosis se aplican los mismos principios descritos para Ajuste de la dosis (ver más arriba).
Si el paciente presenta con frecuencia más de cuatro episodios de DI en 24 horas, se debe volver a calcular la dosis del tratamiento de mantenimiento con opioides.
Interrupción del tratamiento
El tratamiento con Effentora se debe interrumpir inmediatamente si el paciente ya no presenta episodios de dolor irruptivo. El tratamiento del dolor de base persistente se debe mantener tal como estaba prescrito.
Si es necesario interrumpir la totalidad del tratamiento con opioides, el médico debe realizar un estrecho seguimiento del paciente con el fin de controlar el riesgo de efectos abruptos de abstinencia.
Pacientes con insuficiencia hepática o renal:
Effentora debe utilizarse con precaución en pacientes con insuficiencia hepática o renal moderada o grave (ver sección 4.4).
Pacientes con xerostomía:
Se recomienda a los pacientes con xerostomía beber agua para humedecerse la cavidad bucal antes de la administración de Effentora. Si esta recomendación no basta para lograr una efervescencia suficiente, es posible que haya que cambiar de tratamiento.
Pacientes de edad avanzada (mayores de 65 años)
En los ensayos clínicos se ha observado que los pacientes mayores de 65 años necesitan dosis más bajas que los pacientes más jóvenes. Se recomienda especial precaución al ajustar la dosis de Effentora en pacientes de edad avanzada.
Población pediátrica:
No se ha establecido la seguridad y eficacia de Effentora en niños de 0 a 18 años. No se dispone de datos.
Forma de administración:
Cuando el comprimido de Effentora se expone a la humedad, inicia una reacción efervescente en la que se libera el principio activo. Por ello debe advertirse a los pacientes que no abran el blister hasta el instante antes de colocarse el comprimido en la cavidad bucal.
Apertura del blister
Se debe explicar al paciente que NO trate de sacar el comprimido presionándolo contra el blister, porque eso puede dañar el comprimido bucal. La forma correcta de sacar el comprimido del blister es la siguiente:
Separar una de las unidades del blister del resto rasgándola por las perforaciones. Seguidamente, doblar la unidad del blister a lo largo de la línea impresa en la lámina posterior. Retirar la lámina posterior para dejar expuesto el comprimido.
También debe pedirse al paciente que no intente triturar ni partir el comprimido.
El comprimido no debe guardarse después de sacarlo del blister, pues no es posible garantizar su integridad ni evitar el riesgo de exposición accidental al medicamento.
Administración del comprimido
Los pacientes deben extraer el comprimido del alveolo blister e inmediatamente colocar el comprimido de Effentora entero en la cavidad bucal (cerca de un molar, entre la mejilla y la encía).
El comprimido de Effentora no debe chuparse, masticarse ni tragarse, ya que eso produciría unas concentraciones plasmáticas más bajas que cuando se disgrega en la boca.
Effentora debe colocarse y mantenerse dentro de la cavidad bucal durante el tiempo necesario para la disgregación del comprimido, que suele tardar unos 14-25 minutos.
Como alternativa el comprimido puede colocarse en el espacio sublingual (ver sección 5.2).
Si al cabo de 30 minutos siguen quedando restos del comprimido de Effentora, podrán tragarse con un vaso de agua.
El periodo de tiempo que tarda el comprimido en disgregarse completamente después de su administración bucal no parece que afecte a la exposición sistémica temprana al fentanilo.
Los pacientes no deben consumir ningún alimento ni bebida mientras tengan el comprimido en la cavidad bucal.
En caso de irritación de la mucosa bucal, se recomienda cambiar el lugar de colocación del comprimido dentro de la cavidad bucal.
4.3 Contraindicaciones
Hipersensibilidad al principio activo o a alguno de los excipientes incluidos en la sección 6.1.
Pacientes que no estén en tratamiento de mantenimiento con opioides, por el mayor riesgo de depresión respiratoria.
Depresión respiratoria grave o enfermedad pulmonar obstructiva grave.
Tratamiento del dolor agudo distinto al dolor irruptivo.
4.4 Advertencias y precauciones especiales de empleo
Debe advertirse a los pacientes y a sus cuidadores que Effentora contiene un principio activo en cantidades que pueden causar la muerte, especialmente a un niño . Por lo que todos los comprimidos deben mantenerse fuera de la vista y del alcance de los niños.
Con el fin de minimizar los riesgos de efectos adversos relacionados con los opioides y para establecer la dosis eficaz, es indispensable que los profesionales sanitarios monitoricen cuidadosamente a los pacientes durante el proceso de ajuste de la dosis.
Es importante que el tratamiento con opioides de acción prolongada utilizados para tratar el dolor persistente del paciente se haya estabilizado antes de iniciar el tratamiento con Effentora y que el paciente prosiga el tratamiento con el opioide de larga duración mientras esté tomando Effentora.
Depresión respiratoria
Como con todos los opioides, hay riesgo de depresión respiratoria clínicamente significativa asociada al uso de fentanilo. La selección inapropiada del paciente (ej. uso en pacientes que no reciben tratamiento de mantenimiento con opioides) y/o la dosis incorrecta ha desenlaces mortales con el uso de Effentora así como con otros productos a base de fentanilo.
Effentora sólo debe ser usado según las condiciones descritas en la sección 4.1
Enfermedad pulmonar obstructiva crónica
Debe prestarse especial atención al ajuste de la dosis de Effentora en pacientes con enfermedad pulmonar obstructiva crónica no grave u otras afecciones que les predispongan a una depresión respiratoria, ya que incluso las dosis terapéuticas habituales de Effentora pueden reducir el impulso respiratorio hasta provocar insuficiencia respiratoria.
Aumento de la presión intracraneal, alteración del estado de conciencia
Effentora sólo debe administrarse con precaución extrema en pacientes que puedan ser especialmente sensibles a los efectos intracraneales de la retención de CO2, como aquellos con un aumento constatado de la presión intracraneal o con alteración del estado de conciencia. Los opioides pueden enmascarar la evolución clínica de un paciente con lesiones en la cabeza, y sólo deben utilizarse si están clínicamente justificados.
Enfermedad cardíaca
El fentanilo puede provocar bradicardia y debe administrarse con precaución en pacientes con bradiarritmias previas o ya existentes.
Insuficiencia renal o hepática
Además, Effentora debe administrarse con precaución a pacientes con insuficiencia hepática o renal. No se ha valorado la influencia de la insuficiencia hepática o renal sobre la farmacocinética del medicamento; sin embargo, cuando éste se administra por vía intravenosa, se ha comprobado que el aclaramiento del fentanilo está alterado en las enfermedades hepáticas y renales debido a la alteración del aclaramiento metabólico y de las proteínas plasmáticas. Tras la administración de Effentora. la insuficiencia hepática y la insuficiencia renal pueden ambas aumentar la biodisponibilidad del fentanilo ingerido y disminuir su aclaramiento sistémico, lo cual puede aumentar y prolongar los efectos opioides. Así pues, debe prestarse especial atención al ajuste de la dosis en pacientes con enfermedad hepática o renal moderada o grave.
Se deben tomar precauciones especiales en pacientes con hipovolemia e hipotensión.
Sindrome serotoninérgico
Se recomienda precaución cuando Effentora se administre de forma concomitante con fármacos que afecten a los sistemas de neurotransmisores serotoninérgicos.
El desarrollo de un síndrome serotoninérgico potencialmente mortal puede aparecer con el uso concomitante de fármacos serotoninérgicos, como los inhibidores selectivos de la recaptación de serotonina (ISRS) y los inhibidores de la recaptación de serotonina y noradrenalina (IRSN), y con los fármacos que afectan al metabolismo de la serotonina (incluidos los inhibidores de la monoamino oxidasa [IMAO]). Esto puede ocurrir con la dosis recomendada.
El síndrome serotoninérgico puede incluir cambios en el estado mental (p. ej., agitación, alucinaciones, coma), inestabilidad autonómica (p. ej., taquicardia, presión arterial lábil, hipertermia), anomalías neuromusculares (p. ej., hiperreflexia, descoordinación, rigidez) y/o síntomas gastrointestinales (p. ej., náuseas, vómitos, diarrea).
Si se sospecha de un síndrome serotoninérgico, debe suspenderse el tratamiento con Effentora. Tolerancia, dependencia
La administración repetida de opioides como el fentanilo puede inducir tolerancia y dependencia física y/o psicológica. Sin embargo, rara vez se produce adicción iatrogénica por el uso terapéutico de opioides.
Dietas pobres en sodio
Este medicamento contiene 20 mg de sodio por comprimido, lo que debe ser tenido en cuenta en pacientes con dietas pobres en sodio.
Anafilaxia e hipersensibilidad
Se han notificado anafilaxia e hipersensibilidad asociados al uso de medicamentos de fentanilo por vía oral transmucosa (ver sección 4.8).
4.5 Interacción con otros medicamentos y otras formas de interacción
El fentanilo se metaboliza por medio del sistema del isoenzima 3A4 del citocromo P450 (CYP3A4), por lo que pueden producirse interacciones cuando Effentora se administra concomitantemente con fármacos que afectan a la actividad de CYP3A4. La administración concomitante de fármacos que inducen la actividad 3A4 puede reducir la eficacia de Effentora. El uso concomitante de Effentora con inhibidores potentes del CYP3A4 (como ritonavir, ketoconazol, itraconazol, troleandomicina, claritromicina y nelfinavir) o inhibidores moderados del CYP3A4 (como aprenavir, aprepitant, diltiazem, eritromicina, fluconazol, fosamprenavir, zumo de pomelo y verapamilo) puede aumentar la concentración plasmática de fentanilo, causando en ocasiones reacciones adversas graves, incluida una depresión respiratoria mortal. Los pacientes que reciban Effentora e inhibidores moderados o potentes del CYP3A4 concomitantemente deben controlarse estrictamente durante un amplio período de tiempo. El aumento de la dosis debe realizarse con precaución.
El uso concomitante con otros depresores del sistema nervioso central, incluidos otros opioides, sedantes o hipnóticos, anestésicos generales, fenotiazinas, tranquilizantes, relajantes musculares, antihistamínicos sedantes y alcohol, puede producir efectos depresivos aditivos.
No se recomienda el uso de Effentora en pacientes que hayan recibido inhibidores de la monoamino oxidasa (MAO) en los 14 días anteriores, porque se ha descrito que los inhibidores de la MAO producen una potenciación grave e impredecible de los analgésicos opioides.
No se recomienda el uso concomitante de agonistas/antagonistas opioides parciales (p.ej. buprenorfina, nalbufina, pentazocina) ya que poseen una elevada afinidad por los receptores opioides con una actividad intrínseca relativamente baja y en consecuencia antagonizan parcialmente el efecto analgésico del fentanilo, pudiendo inducir síntomas de abstinencia en pacientes dependientes de opioides.
Fármacos serotoninérgicos
La administración concomitante de fentanilo con un fármaco serotoninérgico, como un inhibidor selectivo de la recaptación de serotonina (ISRS), un inhibidor de la recaptación de serotonina y noradrenalina (IRSN) o un inhibidor de la monoamino oxidasa (IMAO), puede aumentar el riesgo de síndrome serotoninérgico, un trastorno potencialmente mortal.
4.6 Fertilidad, embarazo y lactancia
Embarazo
No hay datos suficientes relativos al uso de de fentanilo en mujeres embarazadas. Los estudios realizados en animales han mostrado toxicidad para la reproducción (ver sección 5.3). Se desconoce el riesgo potencial en seres humanos. No debe utilizarse Effentora durante el embarazo a no ser que fuese absolutamente necesario.
El tratamiento prolongado durante el embarazo puede causar síntomas de abstinencia en el recién nacido.
Se aconseja no administrar fentanilo durante el parto (aunque sea por cesárea), ya que atraviesa la placenta y puede causar depresión respiratoria en el feto. Si se administra Effentora, debe disponerse fácilmente de un antídoto para el niño.
Lactancia
El fentanilo se excreta a través de la leche materna y puede causar sedación y depresión respiratoria en el lactante. El fentanilo no debe utilizarse durante la lactancia, no pudiendo reiniciarse la lactancia hasta transcurridos como mínimo 5 días de la última administración de fentanilo.
Fertilidad
No existen datos sobre la fertilidad en humanos. En los estudios realizados con animales, la fertilidad en machos se vio afectada (ver sección 5.3).
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
No se han realizado estudios de los efectos sobre la capacidad para conducir y utilizar máquinas. No obstante, los analgésicos opioides pueden disminuir la capacidad mental y/o física necesaria para realizar tareas potencialmente peligrosas (p. ej., conducir un coche o utilizar maquinaria). Debe advertirse a los pacientes de que no conduzcan ni utilicen maquinaria si sienten somnolencia, mareos o alteraciones visuales mientras toman Effentora, y de que no conduzcan ni utilicen maquinaria hasta que no sepan cómo van a reaccionar.
4.8 Reacciones adversas
Resumen del perfil de seguridad
Las reacciones adversas que pueden esperarse de Effentora son las típicas de los opioides. Frecuentemente, esos efectos adversos propios de los opioides cesan o disminuyen en intensidad con el uso continuado del medicamento, o con el ajuste de la dosis más adecuada para el paciente. No obstante, las reacciones adversas más graves son depresión respiratoria (que potencialmente puede culminar en apnea o parada respiratoria), depresión circulatoria, hipotensión y colapso, reacciones que deben vigilarse estrechamente en todos los pacientes.
Los ensayos clínicos con Effentora se diseñaron para valorar la seguridad y eficacia en el tratamiento del DI, y todos los pacientes tomaban ya opioides de forma concomitante, como morfina de liberación prolongada o fentanilo transdérmico, para su dolor persistente. Por consiguiente, no es posible distinguir con exactitud los efectos de Effentora solo.
Tabla de reacciones adversas
Se han notificado las siguientes reacciones adversas con Effentora y/u otros compuestos que contienen fentanilo provenientes de ensayos clínicos y de la experiencia postcomercialización. Las reacciones adversas se enumeran a continuación según el término preferente de MedDRA por el sistema de clasificación de órganos y frecuencia (frecuencias se definen como: muy frecuentes >1/10, frecuentes>1/100 a <1/10, poco frecuentes > 1/1.000 a < 1/100, raras >1/10.000 a <1/1.000, frecuencia no conocida (no puede estimarse a partir de los datos disponibles); las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada intervalo de frecuencia):
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Infecciones e infestaciones |
Candidiasis oral |
Faringitis |
Pústula oral | ||
|
Trastornos de la sangre y del sistema linfático |
Anemia Neutropenia |
Trombocito-penia | |||
|
Trastornos del sistema inmunológico |
Hipersensibili dad | ||||
|
Trastornos endocrinos |
Hipogonadismo | ||||
|
Trastornos del metabolismo y de la nutrición |
Anorexia | ||||
|
Trastornos psiquiátricos |
Depresión Ansiedad Estado confusional Insomnio |
Euforia Nerviosismo Alucinaciones Alucinaciones visuales Cambios del estado mental Drogodependenci a (adicción) Desorientación |
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Trastornos del sistema nervioso |
Mareo Cefalea |
Disgeusia Somnolencia Letargia Temblores Sedación Hipoestesia Migraña |
Nivel de conciencia deprimido Trastornos de la atención Trastorno del equilibrio Disartria |
Trastorno cognitivo Disfunción motora |
Pérdida de consciencia Convulsión |
|
Trastornos oculares |
Alteraciones de la visión Hiperemia ocular Visión borrosa Disminución de la agudeza visual |
Sensación anómala en el ojo Fotopsia | |||
|
Trastornos del oído y del laberinto |
Vértigo Acúfenos Molestias en el oído | ||||
|
Trastornos cardiacos |
Taquicardia |
Bradicardia | |||
|
Trastornos vasculares |
Hipotensión Hipertensión |
Enrojecimiento Sofocos | |||
|
Trastornos respiratorios, torácicos y mediastínicos |
Disnea Dolor faringolaríng eo |
Depresión respiratoria Síndrome de apnea del sueño |
Paro respiratorio | ||
|
Trastornos gastrointestinales |
Náuseas Vómitos |
Estreñimient o Estomatitis Sequedad de boca Diarrea Dolor abdominal Enfermedad por reflujo gastroesofági co Molestias estomacales Dispepsia Dolor dental |
Íleo Ulceración de la boca Hipoestesia oral Molestias orales Decoloración de la mucosa oral Trastorno de los tejidos blandos de la boca Glosodinia Ampollas en la lengua Dolor gingival Ulceración de la lengua Trastornos de la lengua Esofagitis Labios agrietados Trastornos dentales |
Ampollas en la mucosa oral Labios secos | |
|
Trastornos hepatobiliares |
Dilatación biliar | ||||
|
Trastornos de la piel y del tejido subcutáneo |
Prurito Hiperhidrosis Rash |
Sudor frío Edema facial Prurito generalizado Alopecia |
Onicorrexia |
|
Muy frecuentes |
Frecuentes |
Poco frecuentes |
Raras |
Frecuencia no conocida | |
|
Trastornos musculoesquelético s y del tejido conjuntivo |
Mialgia Dolor de espalda |
Calambres musculares Debilidad muscular | |||
|
Trastornos renales y urinarios |
Retención urinaria | ||||
|
Trastornos generales y alteraciones en el lugar de administración |
Reacciones en el lugar de la aplicación, como sangrado, dolor, úlcera, irritación, parestesia, anestesia, eritema, edema, hinchazón y vesículas |
Edema periférico Fatiga Astenia Síndrome de abstinencia Escalofríos |
Malestar general Pereza Molestias en el pecho Sensaciones anormales Sensación de inquietud Sed Sensación de frío Sensación de calor |
Pirexia | |
|
Exploraciones complementarias |
Disminución de peso |
Descenso del recuento de plaquetas Aumento de la frecuencia cardiaca Descenso del hematocrito Descenso de la hemoglobina | |||
|
Lesiones traumáticas, intoxicaciones y complicaciones de procedimientos terapéuticos |
Caídas |
Descripción de las reacciones adversas seleccionadas
Tras la administración repetida de opioides como fentanilo puede desarrollarse tolerancia, dependencia física y/o psicológica.
Con fentanilo por vía transmucosa se han observado síntomas de abstinencia de opioides tales como náuseas, vómitos, diarrea, ansiedad, escalofríos, temblor y sudoración.
Se han observado pérdida de consciencia y paro respiratorio en el contexto de una sobredosis.
Se han notificado reacciones de hipersensibilidad en la experiencia postcomercialización, incluidos prurito, eritema, edema labial y facial y urticaria.
Notificación de sospechas de reacciones adversas
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del sistema nacional de notificación incluido en el Anexo V.
4.9 Sobredosis
Los síntomas de sobredosis con fentanilo son de naturaleza similar a los del fentanilo intravenoso y a los demás opioides, y son una prolongación de sus acciones farmacológicas, siendo los efectos graves más significativos la alteración del estado mental, pérdida de la consciencia, hipotensión, la depresión respiratoria, distrés respiratorio y el fallo respiratorio con resultado de muerte.
El tratamiento inmediato en caso de sobredosis de opioides consiste en retirar el comprimido bucal de Effentora, si el paciente todavía lo tiene en la boca, asegurando la apertura de las vías respiratorias; estimulación física y verbal del paciente; valoración del grado de conciencia, el estado ventilatorio y circulatorio; y respiración asistida (soporte ventilatorio) en caso necesario.
Para el tratamiento de una sobredosis (ingestión accidental) en una persona que no haya tomado nunca opioides, se debe colocar una vía intravenosa y utilizar naloxona u otros antagonistas de los opioides según esté indicado clínicamente. La depresión respiratoria causada por la sobredosis puede durar más que los efectos de la acción del antagonista de los opioides (así, la semivida de la naloxona varía de 30 a 81 minutos), por lo que puede ser necesaria la administración repetida. Consultar los detalles sobre este tipo de uso en la ficha técnica del antagonista de los opioides utilizado.
Para el tratamiento de una sobredosis en pacientes mantenidos con opioides, debe colocarse una vía intravenosa. El uso moderado de naloxona u otro antagonista opioide puede estar justificado en algunos casos, pero se asocia al riesgo de precipitar la aparición de un síndrome de abstinencia agudo.
Aunque no se ha observado rigidez muscular que interfiera con la respiración después del uso de Effentora, es una reacción que puede manifestarse con fentanilo y otros opioides. Si aparece, debe tratarse con respiración asistida, un antagonista de los opioides y, como último recurso, un agente bloqueante neuromuscular.
5. PROPIEDADES FARMACOLÓGICAS
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: analgésicos; opioides Código ATC: N02AB03.
El fentanilo es un analgésico opioide que actúa principalmente sobre los receptores de opioides p. Sus efectos terapéuticos principales son la analgesia y la sedación. Los efectos farmacológicos secundarios son depresión respiratoria, bradicardia, hipotermia, estreñimiento, miosis, dependencia física y euforia.
Los efectos analgésicos del fentanilo están relacionados con su concentración plasmática. En general, la concentración eficaz y la concentración a la que aparece toxicidad aumentan a medida que aumenta la tolerancia a los opioides. La velocidad de aparición de tolerancia varía mucho de una persona a otra. En consecuencia, la dosis de Effentora debe ajustarse individualmente para conseguir el efecto deseado (ver sección 4.2).
Todos los agonistas de los receptores de opioides p, entre ellos el fentanilo, producen depresión respiratoria dependiente de la dosis. El riesgo de depresión respiratoria es menor en pacientes que reciben tratamiento crónico con opioides, puesto que desarrollan tolerancia a los efectos de depresión respiratoria.
La seguridad y eficacia de Effentora se han evaluado en pacientes que recibieron el medicamento al inicio de un episodio de dolor irruptivo. El uso preventivo de Effentora para episodios de dolor predecibles no se ha investigado en ensayos clínicos. Se han realizado dos ensayos doble ciego, aleatorizados, controlados con placebo y cruzados en un total de 248 pacientes con DI y cáncer que experimentaron una media de 1-4 episodios de DI al día durante el tratamiento de mantenimiento con opioides. Durante una fase inicial abierta, se ajustó la dosis en cada paciente hasta establecer la dosis eficaz de Effentora. Los pacientes en los que se estableció una dosis eficaz entraron en la fase doble ciego del estudio. El criterio principal de eficacia fue la valoración por el propio paciente de la intensidad del dolor. Los pacientes valoraron la intensidad del dolor utilizando una escala de 11 puntos. En cada episodio de DI se evaluó la intensidad del dolor antes y en varias ocasiones después del tratamiento.
En el 67% de los pacientes se pudo establecer una dosis eficaz.
En el ensayo clínico pivotal (ensayo 1), el criterio de valoración principal fue la media de la suma de las diferencias en los valores de la intensidad del dolor desde el momento de administrar la dosis hasta 60 minutos después, inclusive (SPID60), que fue estadísticamente significativa respecto a placebo
(p<0,0001).
Ensayo 1: Media (+/- EEM) Diferencias en intensidad del dolor en cada valoración
(Serie completa de análisis)
SPID60 media (+/- DE)
EFFENTORA=9,7(5,58) p<0,0001
Placebo=4,9(4,38)
20
Tiempo transcurrido desde la administración de la medicación del ensayo (minutos)
Grupo de tratamiento
xxx EFFENTORA
★★★
Placebo
+ dmEOOOI Effentora trente a placebo, a tavor de Effentora, mediante un análisis de la varianza
DID=diterencia en intensidad del dolor; EEM=error estándar de la media
(Sene completa de análisis)
SPID30 media (+/- DE)
EFFENTORA=3,2(2,60) p<0,0001
Placebo=2,0(2,21)
O 5 10 15 30 45 60 90 120
Tiempo transcurrido desde la administración de la medicación del ensayo (minutos)
Grupo de tratamiento xxx EFFENTORA *** Placebo
* p<0,01 Effentora frente a placebo, a favor de Effentora, mediante una prueba de rangos con signo de Wilcoxon para una sola muestra
+ p<0,0001 Effentora frente a placebo, a favor de Effentora, mediante una prueba de rangos con signo de Wilcoxon para una sola muestra
DID=diferencia en intensidad del dolor: EEM=error estándar de la media
En el segundo estudio fundamental (ensayo 2), el criterio de valoración principal fue SPID30, que fue también estadísticamente significativo respecto a placebo (p<0,0001).
Se observó una mejora estadísticamente significativa en la diferencia de intensidad del dolor con Effentora frente a placebo ya a los 10 minutos en el Ensayo 1 y a los 15 minutos (primer punto temporal medido) en el Ensayo 2. En los dos ensayos, esas diferencias siguieron siendo significativas en todos los puntos temporales medidos.
5.2 Propiedades farmacocinéticas
Introducción general
El fentanilo es altamente lipofílico y puede ser absorbido muy rápidamente a través de la mucosa bucal y más lentamente por la vía gastrointestinal convencional. Está sujeto a un efecto de primer paso hepático e intestinal, y los metabolitos no contribuyen a los efectos terapéuticos del fentanilo.
La forma de liberación del principio activo se basa en una reacción efervescente que aumenta la velocidad y el grado de absorción del fentanilo a través de la mucosa bucal. Los cambios transitorios en el pH que acompañan a la reacción efervescente pueden optimizar la disolución (a un pH menor) y la permeabilidad de la membrana (a un pH mayor).
El tiempo de disolución (definido como el tiempo que tarda el comprimido en disgregarse totalmente tras su administración bucal) no afecta a la exposición sistémica temprana al fentanilo. El estudio comparativo entre la administración bucal (es decir entre la encía y la mejilla) y la administración sublingual de un comprimido de 400 mcg de Effentora cumplió los criterios de bioequivalencia.
No se han estudiado los efectos de la insuficiencia renal o hepática sobre la farmacocinética de Effentora.
Absorción:
Tras la administración bucal de Effentora, el fentanilo es absorbido rápidamente con una biodisponibilidad absoluta del 65%. El perfil de absorción de Effentora es, en su mayor parte, el resultado de una absorción rápida inicial a través de la mucosa bucal; las concentraciones plasmáticas máximas según las muestras de sangre venosa suelen alcanzarse generalmente en el transcurso de la hora siguiente a la administración bucal. Alrededor del 50% de la dosis total administrada se absorbe rápidamente por la mucosa bucal y pasa a la circulación sistémica. La otra mitad de la dosis total se traga y se absorbe lentamente en el tubo digestivo. Casi el 30% de la cantidad tragada (50% de la dosis total) escapa a la eliminación hepática e intestinal de primer paso y pasa a estar disponible sistémicamente.
En la siguiente tabla se indican los principales parámetros farmacocinéticos.
Parámetros_farmacocinéticos* en sujetos adultos tratados con Effentora
|
Parámetro farmacocinético (media) |
Effentora 400 microgramos |
|
Biodisponibilidad absoluta |
65% (±20%) |
|
Fracción absorbida por la mucosa |
48% (±31,8%) |
|
Tmax (minuto) ** |
46,8 (20-240) |
|
Cmax (ng/ml) |
1,02 (± 0,42) |
|
AUC0-tmax (ng.h/ml) |
0,40 (± 0,18) |
|
AUC0-inf (ng.h/ml) |
6,48 (± 2,98) |
* Basado en muestras de sangre venosa (plasma). Las concentraciones de citrato de fentanilo en suero fueron superiores a las obtenidas en plasma: La AUC y la Cmax séricas fueron superiores a la AUC y la Cmax plasmáticas aproximadamente en un 20% y un 30%, respectivamente. Se desconoce la razón de dicha diferencia.
** Datos de Tmax presentados como mediana (rango).
En estudios farmacocinéticos que compararon la biodisponibilidad absoluta y relativa de Effentora y del citrato de fentanilo bucal (CFB), la velocidad y el grado de absorción del fentanilo de Effentora demostraron que la exposición era un 30%-50% mayor que la obtenida con el citrato de fentanilo transmucosa. Si se cambia desde otro producto de citrato de fentanilo oral, se precisa un ajuste de la dosis independiente con Effentora puesto que la biodisponibilidad difiere notablemente de uno a otro producto. Sin embargo, en estos pacientes se puede considerar una dosis inicial mayor de 100 microgramos.
Concentración plasmática media frente a tiempo Perfiles tras la administración de dosis únicas de EFFENTORA y CFB en sujetos sanos
-©- 400 mcg EFFENTORA

Los datos de CFB se presentan ajustados (de 800 mcg a 400 mcg).
En un ensayo clínico de pacientes con mucositis de grado 1, se observaron diferencias en la exposición con Effentora. La Cmax y la AUC0-8 fueron entre un 1% y un 25% mayores en los pacientes con mucositis que en los pacientes sin mucositis, respectivamente. Las diferencias observadas no fueron clínicamente significativas.
Distribución
El fentanilo es altamente lipofílico y se distribuye rápidamente fuera del sistema vascular, con un elevado volumen de distribución aparente. Tras la administración bucal de Effentora, el fentanilo experimenta una rápida distribución inicial que representa un equilibrio del fentanilo entre el plasma y los tejidos altamente perfundidos (cerebro, corazón y pulmones). Posteriormente, el fentanilo se redistribuye entre el compartimiento de los tejidos profundos (músculos y tejido adiposo) y el plasma.
La unión del fentanilo a las proteínas plasmáticas es del 80% al 85%. La principal proteína de unión es la alfa-1-ácido-glucoproteína, si bien tanto la albúmina como las lipoproteínas contribuyen en cierta medida. La fracción libre de fentanilo aumenta con la acidosis.
Biotransformación
En los ensayos clínicos no se han caracterizado las rutas metabólicas tras la administración bucal de Effentora. El fentanilo se metaboliza a norfentanilo en el hígado y en la mucosa intestinal por acción de la isoforma CYP3A4. El norfentanilo no es activo farmacológicamente en los estudios en animales. Más del 90% de la dosis administrada de fentanilo se elimina por biotransformación en metabolitos inactivos N-desalquilados e hidroxilados.
Eliminación
Tras la administración intravenosa de fentanilo, menos del 7% de la dosis administrada se elimina inalterada en la orina, y solamente un 1% se excreta inalterada en las heces. Los metabolitos se excretan principalmente en la orina, mientras que la excreción fecal es menos importante.
Tras la administración de Effentora, la fase de eliminación terminal de fentanilo es el resultado de la redistribución entre el plasma y el compartimiento de los tejidos profundos. Esta fase de eliminación es lenta, con una mediana de la semivida de eliminación terminal t1/2 de aproximadamente 22 horas tras la administración bucal de la formulación efervescente y de aproximadamente 18 horas tras la administración intravenosa. El aclaramiento en plasma total del fentanilo después de la administración intravenosa es aproximadamente de 42 l/h.
Linealidad/no linealidad
Se ha demostrado la proporcionalidad de la dosis desde 100 microgramos hasta 1.000 microgramos.
5.3 Datos preclínicos sobre seguridad
Los datos de los estudios no clínicos no muestran riesgos especiales para los seres humanos según los estudios convencionales de farmacología de seguridad, toxicidad a dosis repetidas, genotoxicidad y carcinogenicidad.
Los estudios de toxicidad del desarrollo embrionario y fetal llevados a cabo en ratas y conejos no evidenciaron malformaciones ni alteraciones del desarrollo inducidas por el fármaco, administrado durante el período de la organogénesis.
En un estudio de fertilidad y desarrollo embrionario temprano, en ratas, se observó un efecto asociado a los machos a altas dosis (300 mcg/kg/día s.c.) y se considera secundario a los efectos sedantes del fentanilo en estudios animales.
En estudios sobre el desarrollo pre y postnatal en ratas, la tasa de supervivencia de la progenie se redujo significativamente a dosis que causaban toxicidad materna severa. Los hallazgos adicionales en las crías de la generación F1, tras dosis maternales tóxicas, fueron retraso del desarrollo físico, de las funciones sensoriales, reflejos y comportamiento. Dichos efectos pueden ser indirectos debidos a una alteración de los cuidados maternos y/o disminución de la frecuencia de la lactancia o bien un efecto directo del fentanilo sobre las crías.
Los estudios de carcinogenicidad (bioensayo dérmico alternativo de 26 semanas en ratones transgénicos Tg.AC; estudio de carcinogenicidad subcutánea de 2 años en ratas) con fentanilo no pusieron de manifiesto ningún hallazgo indicativo de potencial oncogénico. La evaluación de los cortes laminares de cerebro del estudio de carcinogenicidad en ratas mostró lesiones cerebrales en los animales tratados con dosis altas de citrato de fentanilo. Se desconoce la relevancia de estos hallazgos para los seres humanos.
6. DATOS FARMACÉUTICOS
6.1 Lista de excipientes
Manitol
Carboximetilalmidón sódico tipo A Hidrogenocarbonato de sodio Carbonato de sodio anhidro Ácido cítrico anhidro Estearato de magnesio
6.2 Incompatibilidades
No procede.
6.3 Periodo de validez
3 años
6.4 Precauciones especiales de conservación
Conservar en el embalaje original para protegerlo de la humedad.
6.5 Naturaleza y contenido del envase
Blister laminado de PVC/lámina de aluminio/poliamida/PVC con cierre de papel/poliéster.
Los blister se presentan en cajas de 4 ó 28 comprimidos. Puede que solamente estén comercializados algunos tamaños de envases.
6.6 Precauciones especiales de eliminación
Hay que explicar a los pacientes y a sus cuidadores que desechen todos los comprimidos sin abrir que les sobren cuando ya no necesiten más el tratamiento.
La eliminación del medicamento utilizado o no utilizado pero que ya no se necesita y de todos los materiales que hayan estado en contacto con él se realizará de acuerdo con la normativa local.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V.
Swensweg 5 2031 GA Haarlem Países Bajos
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/08/441/009-010
9. FECHA DE LA PRIMERA AUTORIZACIÓN/RENOVACIÓN DE LA
AUTORIZACIÓN
Fecha de la primera autorización: 20 febrero 2013
10. FECHA DE LA REVISIÓN DEL TEXTO
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos http://www.ema.europa.eu.
A. FABRICANTE(S) RESPONSABLE(S) DE LA LIBERACIÓN DE LOS
LOTES
B. CONDICIONES O RESTRICCIONES DE SUMINISTRO Y USO
C. OTRAS CONDICIONES Y REQUISITOS DE LA AUTORIZACIÓN DE
COMERCIALIZACIÓN
D. CONDICIONES O RESTRICCIONES EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO
A. FABRICANTE(S) RESPONSABLE(S) DE LA LIBERACIÓN DE LOS LOTES
Nombre y dirección del (de los) fabricantc(s) rcsponsablc(s) de la liberación de los lotes
Teva Pharmaceuticals Europe B.V. Swensweg 5 2031 GA HAARLEM Países Bajos
B. CONDICIONES O RESTRICCIONES DE SUMINISTRO Y USO
Medicamento sujeto a prescripción médica especial y restringida (ver Anexo I: Ficha Técnica o Resumen de las Características del Producto, sección 4.2).
C. OTRAS CONDICIONES Y REQUISITOS DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
• Informes periódicos de seguridad (IPS)
El Titular de la Autorización de Comercialización (TAC) presentará los informes periódicos de seguridad para este medicamento de conformidad con las exigencias establecidas en la lista de fechas de referencia de la Unión (lista EURD) prevista en el artículo 107ter, párrafo 7, de la Directiva 2001/83/CE y publicada en el portal web europeo sobre medicamentos.
D. CONDICIONES O RESTRICCIONES EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO
• Plan de gestión de riesgos (PGR)
El TAC realizará las actividades e intervenciones de farmacovigilancia necesarias según lo acordado en la versión del PGR incluido en el Módulo 1.8.2 de la Autorización de Comercialización y en cualquier actualización del PGR que se acuerde posteriormente.
Se debe presentar un PGR actualizado:
• A petición de la Agencia Europea de Medicamentos
• Cuando se modifique el sistema de gestión de riesgos, especialmente como resultado de nueva información disponible que pueda collevar cambios relevantes en el perfil beneficio/riesgo, o como resultado de la consecución de un hito importante (farmacovigilancia o minimización de riesgos).
Si coincide la presentación de un IPS con la actualización del PGR, ambos documentos se pueden presentar conjuntamente.
• Medidas adicionales de minimización de riesgos
En cada estado miembro en el que se comercialice EFFENTORA, el Titular de la Autorización de Comercialización (TAC) acordará un programa educacional actualizado con la autoridad nacional competente. El TAC se asegurará de que, conforme a las discusiones y al acuerdo con las autoridades nacionales competentes en cada estado miembro en el que se comercialice EFFENTORA, todos los médicos que vayan a prescribir EFFENTORA reciban un paquete informativo que contenga los siguientes elementos:
• Ficha técnica o resumen de las características del producto (SmPC) y prospecto
• Material educacional para los médicos
• Material educacional para los pacientes
El material educacional para los médicos constará de cuatro elementos:
• Guía de prescripción de opioides
• Folleto sobre el dolor irruptivo
• Guía de prescripción de EFFENTORA
• Guía de dosificación
Elementos clave que deben incluirse en el material educacional para los médicos:
- EFFENTORA solo podrá ser prescrito por médicos experimentados en la terapia con opioides
en pacientes con cáncer
- EFFENTORA solo se prescribirá a pacientes seleccionados cuidadosamente que sigan
estrictamente
• las instrucciones para el uso del comprimido bucal de fentanilo y de cómo colocar el comprimido
• las instrucciones sobre cómo abrir el blister con cierre a prueba de niños
• la información sobre la indicación correcta y el riesgo de abuso
• la información sobre el proceso de ajuste de la dosis según se indica en la información del producto
- Instrucciones sobre el uso seguro (para evitar el riesgo de sobredosis), sobre la
conservación (para evitar la exposición accidental) y sobre la eliminación del comprimido bucal de fentanilo
- Enunciados en cuadros como los siguientes:
1. Effentora no debe prescribirse para tratar un dolor que no sea dolor irruptivo oncológico
2. Effentora no debe prescribirse a pacientes con dolor de corta duración
3. Effentora no debe prescribirse a pacientes que no estén tomando opioides para el dolor todo el tiempo
4. Effentora no debe prescribirse a pacientes menores de 18 años
El material educacional para los pacientes constará de los tres elementos siguientes:
1. Un documento que explique el proceso de ajuste de la dosis y las recomendaciones de dosis después del inicio del tratamiento
2. Un documento que ofrezca respuestas a posibles preguntas en torno a los siguientes temas:
• ¿Qué es el dolor irruptivo?
• ¿Para qué sirve EFFENTORA?
• ¿Cómo se usa EFFENTORA (cómo se toma, cómo se alcanza la dosis eficaz durante el
proceso de ajuste de la dosis)?
• Posibles efectos adversos (los más probables, cómo reconocerlos y cuándo alertar al
médico)
• Riesgo de interacciones con otros medicamentos
• Principales precauciones de uso: Cómo evitar los riesgos principales (tomar el fármaco
tal como se ha prescrito, seguir con la terapia de mantenimiento con opioides, mantener EFFENTORA fuera de la vista y del alcance de los niños; impedir el robo y el uso inadecuado
• Uso seguro, conservación y eliminación de EFFENTORA.
3. Un diario del dolor para registrar los niveles de dolor que se padecen todos los días, lo que proporcionará a pacientes y médicos una herramienta para realizar un seguimiento de los síntomas diarios y de la eficacia del tratamiento.
ETIQUETADO Y PROSPECTO
A. ETIQUETADO
Effentora 100 microgramos comprimidos bucales Fentanilo
Cada comprimido bucal contiene 100 microgramos de fentanilo (como citrato).
Contiene sodio. Para mayor información consultar el prospecto.
4 comprimidos bucales 28 comprimidos bucales
Vía bucal.
Colocar en la cavidad bucal. No chupar, masticar ni tragar entero. Leer el prospecto antes de utilizar este medicamento.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Este producto sólo debe administrarse a pacientes que ya estén tomando otros opioides.
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V. Swensweg 5, 2031 GA Haarlem Países Bajos
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/08/441/001
EU/1/08/441/002
13. NÚMERO DE LOTE
Lote
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
Effentora 100
1. NOMBRE DEL MEDICAMENTO
Effentora 100 microgramos comprimidos bucales Fentanilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V.
3. FECHA DE CADUCIDAD
EXP
4. NÚMERO DE LOTE
Lot
5. OTROS
1. Rasgar
2. Doblar
3. Despegar
Effentora 200 microgramos comprimidos bucales Fentanilo
Cada comprimido bucal contiene 200 microgramos de fentanilo (como citrato).
Contiene sodio. Para mayor información consultar el prospecto.
4 comprimidos bucales 28 comprimidos bucales
Vía bucal.
Colocar en la cavidad bucal. No chupar, masticar ni tragar entero. Leer el prospecto antes de utilizar este medicamento.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Este producto sólo debe administrarse a pacientes que ya estén tomando otros opioides.
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V. Swensweg 5, 2031 GA Haarlem Países Bajos
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/08/441/003
EU/1/08/441/004
13. NÚMERO DE LOTE
Lote
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
Effentora 200
1. NOMBRE DEL MEDICAMENTO
Effentora 200 microgramos comprimidos bucales Fentanilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V.
3. FECHA DE CADUCIDAD
EXP
4. NÚMERO DE LOTE
Lot
5. OTROS
1. Rasgar
2. Doblar
3. Despegar
Effentora 400 microgramos comprimidos bucales Fentanilo
Cada comprimido bucal contiene 400 microgramos de fentanilo (como citrato).
Contiene sodio. Para mayor información consultar el prospecto.
4 comprimidos bucales 28 comprimidos bucales
Vía bucal.
Colocar en la cavidad bucal. No chupar, masticar ni tragar entero. Leer el prospecto antes de utilizar este medicamento.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Este producto sólo debe administrarse a pacientes que ya estén tomando otros opioides.
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V. Swensweg 5, 2031 GA Haarlem Países Bajos
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/08/441/005
EU/1/08/441/006
13. NÚMERO DE LOTE
Lote
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
Effentora 400
1. NOMBRE DEL MEDICAMENTO
Effentora 400 microgramos comprimidos bucales Fentanilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V.
3. FECHA DE CADUCIDAD
EXP
4. NÚMERO DE LOTE
Lot
5. OTROS
1. Rasgar
2. Doblar
3. Despegar
Effentora 600 microgramos comprimidos bucales Fentanilo
Cada comprimido bucal contiene 600 microgramos de fentanilo (como citrato).
Contiene sodio. Para mayor información consultar el prospecto.
4 comprimidos bucales 28 comprimidos bucales
Vía bucal.
Colocar en la cavidad bucal. No chupar, masticar ni tragar entero. Leer el prospecto antes de utilizar este medicamento.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Este producto sólo debe administrarse a pacientes que ya estén tomando otros opioides.
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V. Swensweg 5, 2031 GA Haarlem Países Bajos
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/08/441/007
EU/1/08/441/008
13. NÚMERO DE LOTE
Lote
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
Effentora 600
1. NOMBRE DEL MEDICAMENTO
Effentora 600 microgramos comprimidos bucales Fentanilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V.
3. FECHA DE CADUCIDAD
EXP
4. NÚMERO DE LOTE
Lot
5. OTROS
1. Rasgar
2. Doblar
3. Despegar
Effentora 800 microgramos comprimidos bucales Fentanilo
Cada comprimido bucal contiene 800 microgramos de fentanilo (como citrato).
Contiene sodio. Para mayor información consultar el prospecto.
4 comprimidos bucales 28 comprimidos bucales
Vía bucal.
Colocar en la cavidad bucal. No chupar, masticar ni tragar entero. Leer el prospecto antes de utilizar este medicamento.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Este producto sólo debe administrarse a pacientes que ya estén tomando otros opioides.
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V. Swensweg 5, 2031 GA Haarlem Países Bajos
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/08/441/009
EU/1/08/441/010
13. NÚMERO DE LOTE
Lote
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
Effentora 800
1. NOMBRE DEL MEDICAMENTO
Effentora 800 microgramos comprimidos bucales Fentanilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
TEVA B.V.
3. FECHA DE CADUCIDAD
EXP
4. NÚMERO DE LOTE
Lot
5. OTROS
1. Rasgar
2. Doblar
3. Despegar
B. PROSPECTO
Prospecto: información para el usuario
Effentora 100 microgramos comprimidos bucales Effentora 200 microgramos comprimidos bucales Effentora 400 microgramos comprimidos bucales Effentora 600 microgramos comprimidos bucales Effentora 800 microgramos comprimidos bucales Fentanilo
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
1. Qué es Effentora y para qué se utiliza
2. Qué necesita saber antes de empezar a usar Effentora
3. Cómo usar Effentora
4. Posibles efectos adversos
5. Conservación de Effentora
6. Contenido del envase e información adicional
1. Qué es Effentora y para qué se utiliza
El principio activo de Effentora es el citrato de fentanilo. Effentora es un medicamento para el alivio del dolor, este medicamento es conocido como un opioide que se utiliza para tratar el dolor irruptivo en pacientes adultos que ya reciben tratamiento de mantenimiento con otros opioides para su dolor persistente (presente todo el tiempo) asociado al cáncer.
El dolor irruptivo es un dolor añadido y repentino que aparece a pesar de estar recibiendo ya el tratamiento analgésico habitual con opioides.
2. Qué necesita saber antes de empezar a usar Effentora
No use Effentora:
• si no está usando regularmente un medicamento opioide prescrito por su médico (p. ej., codeína, fentanilo, hidromorfona, morfina, oxicodona, meperidina), todos los días a la misma hora, al menos durante una semana, para controlar el dolor persistente. Si no ha estado usando esos medicamentos, no use Effentora dado que su uso puede aumentar el riesgo de que su respiración se vuelva más lenta y/o poco profunda, e incluso de que llegue a pararse.
• si es alérgico al fentanilo o a cualquiera de los demás componentes de este medicamento (incluidos en la sección 6).
• si sufre problemas respiratorios graves o enfermedad pulmonar obstructiva grave.
• si padece dolor de corta duración distinto al dolor irruptivo, como el causado por heridas o cirugía, dolor de cabeza o migrañas.
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a usar Effentora.
Durante el tratamiento con Effentora siga utilizando el medicamento opioide analgésico que toma para
su dolor persistente (presente todo el tiempo) asociado al cáncer.
Mientras esté bajo tratamiento con Effentora no debe utilizar otros tratamientos a base de fentanilo que le hubieran prescrito anteriormente para el dolor irruptivo. Si aún conserva estos productos de fentanilo en casa, contacte con el farmacéutico quien le indicará cómo desprenderse de ellos.
Informe a su médico o farmacéutico antes de iniciar el tratamiento con Effentora:
• si el otro medicamento opioide que toma para su dolor persistente (presente todo el tiempo) asociado al cáncer aún no se ha estabilizado.
• si sufre algún trastorno que afecte a su respiración (como asma, sibilancias o dificultad respiratoria).
• si sufre lesiones en la cabeza.
• si presenta una frecuencia cardiaca excepcionalmente baja u otros problemas cardíacos.
• si tiene problemas hepáticos o renales, puesto que esos órganos afectan a la forma en que su cuerpo metaboliza el medicamento.
• si tiene escaso volumen de líquido en la circulación o hipotensión.
• si tiene problemas de corazón, especialmente frecuencia cardiaca baja.
• si toma antidepresivos o antipsicóticos; consulte la sección “Uso de Effentora con otros medicamentos”.
Qué debe hacer si alguien toma accidentalmente Effentora
Si cree que alguien ha tomado accidentalmente Effentora, solicite atención médica inmediata. Trate de mantener a la persona despierta hasta que llegue el servicio de urgencias.
Si alguien toma accidentalmente Effentora, puede tener los mismos efectos secundarios descritos en la sección “Si usa más Effentora del que debe."
Niños y adolescentes
No administre este medicamento a niños de edades comprendidas entre 0 y 18 años.
Uso de Effentora con otros medicamentos
Informe a su médico o farmacéutico antes de iniciar el tratamiento con Effentora si está tomando, ha tomado recientemente o podría tener que tomar cualquier otro medicamento, incluidos los siguientes:
• cualquier medicamento que pueda causarle normalmente somnolencia (que tenga un efecto sedante), como pastillas para dormir, medicamentos para tratar la ansiedad, antihistamínicos o tranquilizantes.
• cualquier medicamento que pueda afectar a la forma en que su organismo metaboliza Effentora, como ritonavir, nelfinavir, amprenavir y fosamprenavir (medicamentos que ayudan a controlar la infección por VIH) u otros inhibidores del llamado CYP3A4, como ketoconazol, itraconazol o fluconazol (utilizado para el tratamiento de infecciones fúngicas), troleandomicina, claritromicina, o eritromicina (medicamentos para el tratamiento de infecciones bacterianas), aprepitant (usado para náuseas intensas) diltiazem y verapamilo (medicamentos para tratar la hipertensión o las enfermedades cardiacas).
• medicamentos llamados inhibidores de la monoamino-oxidasa (MAO) (utilizados para la depresión grave), también si los ha usado en las dos últimas semanas.
• cierto tipo de analgésicos potentes, llamados agonistas/antagonistas parciales, como la buprenorfina, la nalbufina y la pentazocina (medicamentos para tratar el dolor). Mientras utiliza estos medicamentos, podría presentar síntomas de un síndrome de abstinencia (náuseas, vómitos, diarrea, ansiedad, escalofríos, temblor y sudoración).
• El riesgo de efectos adversos aumenta si está tomando medicamentos tales como ciertos antidepresivos o antipsicóticos. Effentora puede interactuar con estos medicamentos y usted puede presentar cambios en el estado mental (p. ej., agitación, alucinaciones, coma) y otros efectos como temperatura corporal mayor de 38°C, aumento de la frecuencia cardiaca, presión arterial inestable y exageración de los reflejos, rigidez muscular, falta de coordinación y/o síntomas gastrointestinales (p. ej., náuseas, vómitos, diarrea). Su medico le dirá si Effentora es adecuado para usted.
Informe a su médico o farmacéutico si está tomando, ha tomado recientemente o podría tener que tomar cualquier otro medicamento.
Uso de Effentora con alimentos, bebidas y alcohol
• Effentora puede administrarse antes o después de las comidas, pero no durante ellas. Puede beber un poco de agua antes de usar Effentora para ayudarse a humedecer la boca, pero no debe beber ni comer nada mientras esté tomando el medicamento.
• No debe beber zumo de pomelo mientras esté usando Effentora, ya puede afectar a la forma en que su organismo metaboliza este medicamento.
• No beba alcohol durante el tratamiento con Effentora. Puede aumentar el riesgo de efectos adversos peligrosos.
Embarazo y lactancia
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
No se debe utilizar Effentora durante el embarazo, salvo que lo haya consultado con su médico.
No debe usar Effentora durante el parto, porque el fentanilo puede causar depresión respiratoria al recién nacido.
El fentanilo puede pasar a la sangre materna y causar efectos adversos en el lactante. No use Effentora si está dando el pecho a su hijo No debe iniciar la lactancia hasta transcurridos al menos 5 días desde la última dosis de Effentora.
Conducción y uso de máquinas
Pregunte a su médico si puede conducir o utilizar máquinas sin peligro después de tomar Effentora.
No conduzca ni utilice maquinas si: siente sueño o mareos, tiene la visión borrosa o ve doble o tiene dificultad para concentrarse. Es importante que sepa cómo reacciona a Effentora antes de conducir o utilizar máquinas.
Effentora contiene sodio
Cada comprimido de Effentora 100 microgramos contiene 10 mg de sodio. Cada comprimido de Effentora 200 microgramos, Effentora 400 microgramos, Effentora 600 microgramos y Effentora 800 microgramos contiene 20 mg de sodio, lo que debe ser tenido en cuenta en pacientes con dietas pobres en sodio y pida consejo a su médico.
3. Cómo usar Effentora
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
Dosificación y frecuencia
Cuando empiece a usar Effentora por primera vez, su médico le ayudará a encontrar la dosis que aliviará su dolor irruptivo. Es muy importante que use Effentora exactamente como el médico le indique. La dosis inicial es de 100 microgramos.
Durante la determinación de la dosis correcta para usted, es posible que su médico le haga tomar más de un comprimidopor episodio. Si no se alivia el dolor irruptivo pasados 30 minutos, use solamente 1 comprimido más de Effentora durante el periodo de ajuste de la dosis.
Una vez haya determinado la dosis correcta con su médico, use 1 comprimido para un episodio de dolor irruptivo como regla general. La dosis de analgésico que necesite puede variar a lo largo del tratamiento. Es posible que necesite dosis más altas. Si no se alivia el dolor irruptivo pasados 30 minutos, use solamente 1 comprimido más de Effentora durante este periodo de reajuste de la dosis. Consulte con su médico si su dosis correcta de Effentora no le alivia el dolor irruptivo. Su médico decidirá si es preciso modificarle la dosis.
Espere por lo menos 4 horas antes de tratar otro episodio de dolor irruptivo con Effentora.
Debe informar al médico inmediatamente si necesita tomar Effentora más de cuatro veces al día, ya que es posible que le cambie la medicación que está recibiendo para controlar el dolor persistente. Cuando el dolor persistente esté controlado de nuevo, puede que su médico tenga que cambiarle la dosis de Effentora. Para un alivio más eficaz, informe a su médico del dolor que sufre usted y de cómo está actuando Effentora en su caso, de manera que pueda modificar la dosis en caso necesario.
No cambie por su cuenta las dosis de Effentora ni de otros analgésicos. Cualquier cambio en la dosificación tiene que ser prescrito y vigilado por su médico.
Si no está seguro de la dosis adecuada, o si desea hacer alguna pregunta sobre el uso de este medicamento, póngase en contacto con su médico.
Forma de administración
La forma de administración de Effentora comprimidos bucales es por vía bucal. Al colocar un comprimido en la boca, éste se disuelve y el medicamento se absorbe por la mucosa bucal y pasa a la sangre. Esta forma de tomar el medicamento permite que sea absorbido rápidamente para aliviar su dolor irruptivo.
Manera de usar el medicamento
• Abra el blister sólo cuando vaya a usar el comprimido. El comprimido debe usarse inmediatamente después de haberlo retirado del blister.
• Separe una de las unidades del blister de la plaqueta rasgando por las perforaciones.
• Doble la unidad de blister a lo largo de la línea indicada.
• Despegue la parte posterior del blister para exponer el comprimido. NO trate de presionar el comprimido para sacarlo del blister, porque eso puede dañarlo.

• Retire el comprimido del blister y colóquelo inmediatamente sin romperlo cerca de una muela, entre la encía y la mejilla (como se indica en la fotografía). También es posible que su médico le indique colocar el comprimido debajo de la lengua.
• No intente triturar ni partir el comprimido.

• No muerda, chupe, mastique ni trague el comprimido, ya que eso hará que tenga un efecto analgésico menor que si sigue estas instrucciones.
• El comprimido debe permanecer entre la mejilla y la encía hasta que se disuelva, lo que suele tardar entre 14 y 25 minutos.
• Puede que sienta una ligera sensación efervescente entre la mejilla y la encía a medida que el comprimido se disuelve.
• En caso de irritación puede cambiar la colocación del comprimido en la encía.
• Al cabo de 30 minutos, si siguen quedando restos del comprimido de Effentora, puede tragarlos con un vaso de agua.
Si usa más Effentora del que debe
• Los efectos adversos más frecuentes son somnolencia, mareo o malestar. Si empieza a sentirse muy mareado o somnoliento antes de que el comprimido se haya disuelto del todo, enjuáguese la boca con agua y escupa de inmediato los restos del comprimido en el lavabo o el inodoro.
• Un efecto adverso grave de Effentora es la respiración lenta y/o poco profunda. Esto puede ocurrir si la dosis de Effentora es demasiado alta o si ha tomado demasiado Effentora. Si ocurre eso, solicite atención médica inmediata.
Si olvidó usar Effentora
Si el dolor irruptivo persiste, puede tomar Effentora según las indicaciones de su médico. Si el dolor irruptivo ha desaparecido, no tome Effentora hasta el siguiente episodio de dolor irruptivo.
Si interrumpe el tratamiento con Effentora
Debe suspender Effentora cuando ya no tenga ningún dolor irruptivo. Sin embargo, debe seguir tomando su medicamento analgésico opioide habitual para tratar el dolor canceroso persistente, tal como le ha indicado su médico. Cuando suspenda el tratamiento con Effentora, puede presentar síntomas de abstinencia similares a los posibles efectos adversos de Effentora. Si presenta síntomas de abstinencia o si le preocupa el alivio del dolor, debe consultar a su médico. Su médico evaluará si necesita medicamentos para reducir o eliminar los síntomas de abstinencia.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran. Si aprecia cualquiera de ellos, informe a su médico.
Los efectos adversos más graves son respiración poco profunda, hipotensión y shock. Effentora, al igual que otros productos a base de fentanilo, puede causar problemas respiratorios muy graves que pueden conducir a la muerte. Si siente mucha somnolencia o tiene respiración lenta y/o poco profunda, usted o quien le cuide deben contactar inmediatamente con su médico y solicitar ayuda urgente.
Efectos adversos muy frecuentes (que pueden afectar a más de 1 de cada 10 pacientes):
• mareo, dolor de cabeza
• náuseas, vómitos
• en el lugar de aplicación del comprimido: dolor, úlcera, irritación, sangrado, entumecimiento, pérdida de sensación, enrojecimiento, hinchazón o manchas
Efectos adversos frecuentes (que pueden afectar hasta a 1 de cada 10 pacientes):
• sensación de ansiedad o confusión, depresión, insomnio
• disminución de peso
• somnolencia, sedación, cansancio excesivo, debilidad, migraña, entumecimiento, inflamación de brazos o piernas, síndrome de abstinencia (que se puede manifestar por la aparición de los siguientes efectos adversos: náuseas, vómitos, diarrea, ansiedad, escalofríos, temblor y sudoración), temblores, caídas, escalofríos
• estreñimiento, inflamación de la boca, sequedad de la boca, diarrea, ardor de estómago, pérdida de apetito, dolor de estómago, molestias de estómago, indigestión, dolor dental, aftas bucales
• picores, sudoración excesiva, erupción
• falta de aliento, dolor de garganta
• disminución de los glóbulos blancos, disminución de los glóbulos rojos, disminución o aumento de la presión sanguínea, frecuencia cardíaca demasiado alta
• dolor muscular, dolor de espalda
fatiga
Efectos adversos poco frecuentes (que pueden afectar hasta 1 de cada 100 pacientes):
• molestias de garganta;
• disminución de las células que ayudan a la sangre a coagularse;
• euforia, nerviosismo, extrañeza, inquietud o lentitud; ver o escuchar cosas que no son reales (alucinaciones), alteración del estado de consciencia, cambios del estado mental, dependencia del medicamento (adicción), desorientación, falta de concentración, pérdida del equilibrio, vértigo, problemas al hablar, zumbidos en el oído, molestias en el oído;
• visión alterada o borrosa, ojos enrojecidos;
• frecuencia cardiaca demasiado baja, sensación de mucho calor (sofocos), hipertensión;
• problemas respiratorios graves, dificultad respiratoria durante el sueño;
• uno o más de los siguientes problemas en la boca: úlcera, pérdida de sensación, malestar, color anormal, alteración de los tejidos blandos, alteración de la lengua, dolor, ampollas o úlceras en la lengua, dolor de encías, labios agrietados trastornos dentales,;
• inflamación del esófago, parálisis intestinal, trastorno de la vesícula biliar;
• sudor frío, edema facial, picores generalizados, pérdida del cabello, calambres musculares, debilidad muscular, malestar general, molestias en el pecho, sed, sensación de frío, sensación de calor, dificultad para orinar;
• malestar general;
• rubor.
Efectos adversos raros (que pueden afectar hasta 1 de cada 1.000 pacientes):
• trastornos del pensamiento, alteración del movimiento
• ampollas en la boca, labios secos, presencia de pus debajo de la piel en la boca
• falta de testosterona, sensación extraña en el ojo, observación de ráfagas de luz, uñas frágiles
• reacciones alérgicas como erupción cutánea, enrojecimiento, hinchazón de labios y cara, urticaria
Frecuencia no conocida:
• Pérdida de la consciencia, paro respiratorio, convulsión (crisis epiléptica)
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Anexo V. .. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Effentora
El analgésico Effentora es muy fuerte y puede ser un riesgo para la vida si lo toma
accidentalmente un niño. Este medicamento debe mantenerse fuera de la vista y del alcance de
los niños.
• No utilice este medicamento después de la fecha de caducidad que aparece en la etiqueta de los blister y en la caja.
• Conservar en el embalaje original para protegerlo de la humedad.
• Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional
Composición de Effentora
El principio activo es fentanilo. Cada comprimido contiene:
• 100 microgramos de fentanilo (como citrato)
• 200 microgramos de fentanilo (como citrato)
• 400 microgramos de fentanilo (como citrato)
• 600 microgramos de fentanilo (como citrato)
• 800 microgramos de fentanilo (como citrato)
Los demás componentes son manitol, carboximetilalmidón sódico tipo A, hidrogenocarbonato de sodio, carbonato de sodio anhidro, ácido cítrico anhidro, estearato de magnesio.
Aspecto del producto y contenido del envase
Los comprimidos bucales son de cara plana, redondos, de bordes biselados y grabados en una cara con una “C” y en la otra con “1” para Effentora 100 microgramos, con “2” para Effentora 200 microgramos, con “4” para Effentora 400 microgramos, con “6” para Effentora 600 microgramos y con “8” para Effentora 800 microgramos.
Cada blister contiene 4 comprimidos bucales, que se presentan en cajas de 4 ó 28 comprimidos bucales.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización
TEVA B.V.
Swensweg 5 2031 GA Haarlem Países Bajos
Responsable de la fabricación
Teva Pharmaceuticals Europe B.V.
Swensweg 5
2031 GA HAARLEM
Países Bajos
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización o llame el siguiente número:
Belgie/Belgique/Belgien
Teva Pharma Belgium N.V./S.A. /AG Tel/Tél: +32 3 820 73 73
Etarapna
TeBa OapMacroTHKMC Etarapna EOOfl Tea.: +359 2 489 95 82
Ceská republika
Teva Pharmaceuticals CR, s.r.o.
Tel: +420 251 007 111
Danmark
Teva Denmark A/S Tlf: +45 44 98 55 11
Deutschland
TEVA GmbH Tel: +49 731 402 08
Lietuva
UAB “Sicor Biotech”
Tel: +370 5 266 02 03
Luxembourg/Luxemburg
Teva Pharma Belgium N.V./S.A./AG. Tél: +32 3 820 73 73
Magyarország
Teva Gyógyszergyár Zrt.
Tel.: (+ 36) 1 288 6400
Malta
Teva Pharmaceuticals Ireland Tel: +353 51 321740
Nederland
Teva Nederland B.V.
Tel: +31 (0) 800 0228 400
|
Eesti Teva Eesti esindus UAB Sicor Biotech Eesti filiaal Tel: + 372 661 0801 |
Norge Teva Norway AS Tlf: +47 66 77 55 90 |
|
ELLáóa Teva E7Mg A.E. T^7: +30 210 72 79 099 |
Osterreich ratiopharm Arzneimittel Vertriebs-GmbH Tel.Nr.: +43/1/97007 0 |
|
España Teva Pharma, S.L.U. Tel: + 34 91 387 32 80 |
Polska Teva Pharmaceuticals Polska Sp. z o.o. Tel.: +48 22 345 93 00 |
|
France Teva Santé Tél: +33 1 55 91 78 00 |
Portugal Teva Pharma - Produtos Farmacéuticos, Lda. Tel: +351 21 476 75 50 |
|
Hrvatska Pliva Hrvatska d.o.o Tel: + 385 1 37 20 000 |
Romania Teva Pharmaceuticals S.R.L. Tel: +4021 230 65 24 |
|
Ireland Teva Pharmaceuticals Ireland Tel: +353 (0) 51 321 740 |
Slovenija Pliva Ljubljana d.o.o. Tel: +386 1 58 90 390 |
|
Ísland Teva Norway AS Sími: +47 66 77 55 90 |
Slovenská republika TEVA Pharmaceuticals Slovakia s.r.o. Tel: +421257267911 |
|
Italia Teva Italia S.r.l. Tel: +39 028917981 |
Suomi/Finland ratiopharm Oy Puh/Tel: +358 20 180 5900 |
|
Kúnpoq Teva E7Mg A.E. Tr(k: +30 210 72 79 099 |
Sverige Teva Sweden AB Tel: +46 (0) 42 12 11 00 |
|
Latvija Sicor Biotech filíale Latvija Tel: +371 67 323 666 |
United Kingdom Teva UK Limited Tel: +44 1977628500 |
Fecha de la última revisión de este prospecto: {MM/AAAA}
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu/
110