Curosurf 240
FICHA TÉCNICA
1. NOMBRE DEL MEDICAMENTO
CUROSURF 120 mg suspensión para instilación endotraqueopulmonar.
CUROSURF 240 mg suspensión para instilación endotraqueopulmonar.
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
CUROSURF 120. Un vial de 1,5 ml contiene:
Surfactante pulmonar porcino: 120 mg.
CUROSURF 240. Un vial de 3,0 ml contiene:
Surfactante pulmonar porcino: 240 mg.
Composición por ml de suspensión: 80 mg/ml de fracción fosfolípida del pulmón porcino, equivalentes a 74 mg/ml de fosfolípidos totales y 0,9 mg/ml de proteínas hidrófobas de bajo peso molecular.
CUROSURF es un surfactante natural, preparado a partir de pulmón porcino, que contiene casi exclusivamente lípidos polares, en particular fosfatidilcolina (alrededor del 70% del contenido total de fosfolípidos) y cerca de un 1% de proteínas hidrófobas específicas de bajo peso molecular, la SP-B y SP-C.
Para consultar la lista completa de excipientes ver sección 6.1.
3. FORMA FARMACÉUTICA
Suspensión para instilación endotraqueopulmonar.
Un vial monodosis contiene una suspensión estéril de color blanco a amarillento para uso endotraqueopulmonar.
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
Tratamiento de niños recién nacidos con síndrome de distrés respiratorio (SDR).
Uso profiláctico en niños prematuros con una edad gestacional menor de 30 semanas, con riesgo de SDR o con evidencia de déficit de surfactante.
4.2 Posología y forma de administración
Posología
Tratamiento
Curosurf debe instilarse por vía intratraqueal, a dosis de 200 mg/kg, que puede administrarse en forma de dosis única, o bien repartida en 2 dosis de 100 mg/kg, la primera de las cuales debe administrarse inmediatamente y la segunda, al cabo de unas 12 horas. En caso de que las
condiciones clínicas continuasen siendo críticas (cociente a/A PO2 < 0,22), podría administrarse una dosis adicional de 100 mg/kg, tras un intervalo de aproximadamente 12 horas.
Es recomendable iniciar el tratamiento lo antes posible, una vez realizado el diagnóstico de SDR.
Profilaxis
Debe administrarse una dosis única de 100-200 mg/kg lo antes posible después del nacimiento (preferentemente dentro de los primeros 15 minutos). Puede darse una dosis adicional de 100 mg/kg a las 6-12 horas después de la primera dosis y luego 12 horas más tarde, en los neonatos que tengan signos persistentes de SDR y sigan requiriendo ventilación asistida (dosis máxima total: 300-400 mg/kg).
Los niños no deben ser intubados únicamente para la administración profiláctica de surfactante. Forma de administración
CUROSURF debe ser solo administrado por personal entrenado y con experiencia en el cuidado, reanimación y estabilización de recién nacidos pretérmino.
CUROSURF se administra vía endotraqueopulmonar en niños cuyo ritmo cardiaco y su concentración arterial de oxígeno o saturación de oxígeno están siendo monitorizadas, como se realiza habitualmente en las unidades de neonatología.
CUROSURF se presenta en viales listos para ser usados que deben conservarse en nevera, entre +2 y + 8oC. Antes de su utilización, el vial debe calentarse a temperatura ambiente, por ejemplo sujetándolo entre las manos durante unos minutos, e invertirse suavemente varias veces, sin agitar, hasta obtener una suspensión uniforme.
La suspensión debe extraerse del vial mediante una aguja y una jeringa estéril siguiendo las instrucciones descritas en la sección 6.6.
CUROSURF puede ser administrado:
a. Desconectando al niño de la ventilación asistida
Desconectar al niño momentáneamente de la ventilación asistida y administrar 1,25 a 2,5 ml/kg (100-200 mg/kg) de la suspensión, como un bolo único, directamente en la parte inferior de la tráquea a través del tubo endotraqueal. Mantener aproximadamente durante un minuto ventilación asistida con ambú y luego conectar de nuevo al niño a la ventilación asistida en las mismas condiciones que antes de la administración. Si se necesitan dosis superiores (1,25 ml/kg) pueden ser administradas de la misma manera;
b. Sin desconectar al niño de la ventilación asistida
Administrar 1,25 a 2,5 ml/kg (100-200 mg/kg) de la suspensión, como un bolo único, directamente en la parte inferior de la tráquea mediante el paso de un catéter a través del puerto de succión y dentro del tubo endotraqueal. Si se necesitan dosis superiores (1,25 ml/kg) pueden ser administradas de la misma manera;
c. Hay una tercera opción de administración a través del tubo endotraqueal en la sala de partos antes de que se inicie la ventilación asistida. En este caso, se usa una técnica de inspiración y la extubación para CPAP es una opción tanto en la sala de partos como más tarde tras la admisión en la unidad de neonatología (Intubación SURfactante Extubación - INSURE).
4.3 Contraindicaciones
Hipersensibilidad al principio activo o a alguno de los excipientes.
4.4 Advertencias y precauciones especiales de empleo
Antes de iniciarse el tratamiento con CUROSURF, deben estabilizarse las condiciones generales del recién nacido. También se recomienda corregir la acidosis, hipotensión, anemia, hipoglicemia e hipotermia.
En el caso de reflujo, se debe discontinuar la administración de CUROSURF, y si es necesario, la presión del pico inspiratorio en el ventilador debe incrementarse hasta que aparezca claridad en el tubo endotraqueal.
Los niños cuya respiración se vuelve considerablemente insuficiente durante o inmediatamente después de la administración pueden tener moco obstruyendo el tubo endotraqueal, particularmente si las secreciones pulmonares eran abundantes antes de la administración del fármaco. La succión antes de la administración puede reducir la probabilidad de que el moco obstruya el tubo endotraqueal. Si se sospecha obstrucción del tubo endotraqueal, y la succión es insuficiente para la limipieza de la obstrucción, el tubo endotraqueal debe ser sustituido inmediatamente.
Sin embargo, la aspiración de las secreciones traqueales no se recomienda hasta pasadas 6 horas tras la administración, a excepción de circunstancias que comporten riesgo vital.
En el caso de que ocurran episodios de bradicardia, hipotensión, y reducción de la saturación de oxígeno (ver sección 4.8) se paralizará la administración de CUROSURF y se considerarán y aplicarán medidas para normalizar el ritmo cardiaco. Tras la estabilización, el niño puede ser tratado con una monitorización adecuada de las constantes vitales.
Tras la administración de CUROSURF, la distensibilidad pulmonar (expansión de los pulmones) y la oxigenación pueden mejorar rápidamente, por lo tanto se requiere un rápido ajuste de las condiciones del respirador.
La mejora del intercambio del gas alveolar puede provocar un rápido incremento de la concentración de oxígeno arterial: por lo que se deberá ajustar rápidamente la concentración de oxígeno inspirado para evitar hiperoxia. Con el objeto de mantener unos niveles adecuados de oxígeno en sangre, además de un análisis sangre-gas periódico, también se deberá tener en cuenta continua monitorización transcutánea de PaO2 o saturación de oxígeno.
La presión positiva continua en la vía nasal (nCPAP) puede ser usada como continuación del tratamiento, pero solo en unidades equipadas para llevar a cabo esta técnica.
Los niños tratados con surfactante deben ser cuidadosamente monitorizados en relación a signos de infección. A los primeros signos de infección, al niño se le debe dar terapia antibiótica adecuada.
En casos de respuesta no-satisfactoria al tratamiento con CUROSURF o rápida recaída, es aconsejable considerar la posibilidad de otras complicaciones de inmadurez como ductus arterioso permeable u otros problemas pulmonares como pneumonía antes de la administración de la siguiente dosis.
Los niños nacidos después de un período muy prolongado tras la rotura de membranas (mayor de 3 semanas) pueden tener algún grado de hipoplasia pulmonar y no responder de forma óptima al surfactante exógeno.
Se espera que la administración del surfactante disminuya la gravedad del SDR pero no elimina totalmente la mortalidad y morbilidad asociadas a la prematuridad, ya que los niños prematuros tienen otras complicaciones asociadas con su inmadurez. Tras la administración de CUROSURF, se ha detectado una depresión transitoria de la actividad eléctrica cerebral, de 2 a 10 minutos de duración. Esto se ha observado en un único estudio por lo que su impacto no está claro.
No hay información disponible de los efectos de dosis iniciales distintas a 100 ó 200 mg/kg, dosificadas más frecuentemente cada 12 horas, o administración de CUROSURF iniciada más tarde de 15 horas tras el diagnóstico de SDR.
La administración de CUROSURF en recién nacidos pretérmino con hipotensión grave no ha sido estudiada.
Advertencias sobre excipientes:
Ambos medicamentos contienen menos de 1 mmol (23 mg) de sodio por dosis, por lo que se considera esencialmente “exento de sodio”.
4.5 Interacción con otros medicamentos y otras formas de interacción
No se han realizado estudios de interacciones.
4.6 Fertilidad, embarazo y lactancia
Embarazo No procede.
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
No procede.
4.8 Reacciones adversas
Las reacciones adversas observadas durante el tratamiento en ensayos clínicos y aquellas recogidas con la experiencia de la post-comercialización, se enumeran a continuación en la tabla inferior según la Clasificación por Órganos y Sistemas (mostradas con los términos preferidos por MedDRA) y por intervalos de frecuencias según las siguientes categorías: muy frecuente (>1/10); frecuentes (>1/100 a <1/10); poco frecuentes (>1/1.000 a <1/100); raras (>1/10.000 a <1/1.000); muy raras (<1/10.000); no conocida (no puede estimarse a partir de los datos disponibles).
|
Clasificación por Órganos y Sistemas |
Reacciones adversas |
Frecuencia |
|
Infecciones e infestaciones |
Sepsis |
Poco frecuente |
|
Trastornos del sistema nervioso |
Hemorragia intracraneal |
Poco frecuente |
|
Trastornos cardiacos |
Bradicardia |
Rara |
|
Trastornos vasculares |
Hipotensión |
Rara |
|
Trastornos respiratorios, torácicos y mediastínicos |
Displasia broncopulmonar |
Rara |
|
Pneumotórax |
Poco frecuente | |
|
Hemorragia pulmonar |
Rara | |
|
Hiperoxia |
No conocida | |
|
Cianosis neonatal |
No conocida | |
|
Apnea |
No conocida | |
|
Exploraciones complementarias |
Reducción de la saturación de oxígeno |
Rara |
|
Electroencefalograma |
No conocida |
|
anormal | ||
|
Lesiones traumáticas, intoxicaciones y complicaciones de procedimientos terapéuticos |
Complicación de intubación endotraqueal |
No conocida |
La apnea, la sepsis y la bradicardia pueden ocurrir como consecuencia de la inmadurez de los neonatos prematuros.
La incidencia de hemorragias intracraneales tras la instilación de CUROSURF se ha relacionado con la reducción de tensión arterial media y picos tempranos en la oxigenación arterial (PaO2). Se recomienda el ajuste inmediato del respirador tras la instilación para evitar picos altos de PaO2.
En los estudios clínicos llevados a cabo hasta la fecha en niños tratados con CUROSURF se ha demostrado una ligera tendencia hacia un aumento en la incidencia de ductus arterioso permeable. Este fenómeno es atribuido a cambios hemodinámicos inducidos por la rápida expansión de los pulmones con la administración de surfactante.
Se ha observado la formación de anticuerpos contra las proteínas que componen CUROSURF, pero sin evidencia de relevancia clínica.
Los recién nacidos pretérmino tienen una incidencia relativamente alta de hemorragia cerebral e isquemia cerebral, notificada como leucomalacia periventricular y anomalías hemodinámicas como ductus arterioso permeable y persistente de circulación fetal a pesar de los cuidados intensivos. Estos niños corren también un alto riesgo de desarrollar infecciones como pneumonía y bacteremia (o septicemia). Durante el periodo perinatal también pueden ocurrir convulsiones.
Los niños pretérmino comúnmente desarrollan trastornos hematológicos y alteraciones electrolíticas que pueden empeorar por enfermedad grave y la ventilación mecánica.
Otras posibles complicaciones directamente relacionadas con enfermedad grave y el uso de ventilación mecánica, necesaria para la reoxigenación, que pueden aparecen en prematuros son: pneumotórax, enfisema pulmonar intersticial y hemorragia pulmonar.
Finalmente, el uso prolongado de altas concentraciones de oxígeno y ventilación mecánica están asociados con el desarrollo de displasia broncopulmonar y retinopatía de prematuridad.
4.9 Sobredosis
No se han descrito casos de sobredosis tras la administración de CUROSURF. De todas formas, en el caso improbable de una sobredosificación accidental, y sólo en caso de claros efectos clínicos sobre la respiración, ventilación u oxigenación del neonato, debe aspirarse la mayor cantidad posible de suspensión y administrar tratamiento de soporte, con atención especial al equilibrio hidroelectrolítico.
5. PROPIEDADES FARMACOLÓGICAS
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: Otros productos del aparato respiratorio, surfactantes pulmonares, código ATC: R07AA02 “Fosfolípidos naturales”.
El surfactante pulmonar es una mezcla de sustancias, principalmente fosfolípidos y proteínas específicas, que tapizan la superficie interna de los alveolos y son capaces de disminuir la tensión superficial.
Este efecto es esencial para estabilizar los alveolos, y para evitar su colapso al final de la espiración, de modo que se mantenga un intercambio de gases adecuado en el ciclo respiratorio.
El déficit de surfactante pulmonar, cualquiera que sea su causa, da lugar a una insuficiencia respiratoria grave, que en los niños prematuros se denomina síndrome de distrés respiratorio (SDR) o enfermedad de la membrana hialina (HMD, por sus siglas en inglés). El SDR es la mayor causa de mortalidad y morbilidad agudas en niños pretérmino y puede originar secuelas respiratorias y neurológicas a largo plazo.
CUROSURF se desarrolló para suplir este déficit de surfactante pulmonar endógeno, mediante la administración de surfactante exógeno intratraqueal.
Las propiedades de superficie de CUROSURF favorecen su distribución uniforme en los pulmones y su difusión en las interfases aire-líquido de los alveolos. Los efectos fisiológicos y terapéuticos de CUROSURF en el déficit de surfactante se han documentado ampliamente en varios modelos animales.
En fetos de conejo inmaduros obtenidos por histerectomía e inmediatamente sacrificados al nacer, la administración de CUROSURF provocó una mejoría considerable de la expansión pulmonar.
En conejos recién nacidos prematuros ventilados con oxígeno al 100%, se produjo una extraordinaria mejoría del volumen corriente y de la distensibilidad toraco-pulmonar, respecto a los animales control, tras la administración de CUROSURF mediante una cánula traqueal.
También en conejos recién nacidos prematuros, el tratamiento con CUROSUF (manteniendo un volumen corriente estandarizado de unos 10 ml/kg) aumentó la distensibilidad del sistema toraco-pulmonar hasta un nivel similar al de los animales recién nacidos maduros.
5.2 Propiedades farmacocinéticas
CUROSURF permanece fundamentalmente en los pulmones tras su administración intratraqueal; la vida media de la dipalmitoilfosfatidilcolina marcada con C14 es de 67 horas en conejos recién nacidos. En el suero y en órganos distintos del pulmón, sólo pueden detectarse trazas de lípidos del surfactante, a las 48 horas de la administración.
5.3 Datos preclínicos sobre seguridad
Los estudios de toxicidad aguda, realizados en distintas especies animales por vía intraperitoneal e intratraqueal, no mostraron signos de toxicidad pulmonar o sistémica ni mortalidad. El estudio de toxicidad subaguda por vía intratraqueal en el perro, conejo y rata (14 días) no mostró efectos clínicos, cambios hematológicos, ni alteraciones macroscópicas. Además, CUROSURF no mostró signos de toxicidad directa en la rata por vía intraperitoneal (4 semanas).
CUROSURF, administrado por vía parenteral en cobayas, no provoca reacciones anafilácticas activas ni estimula la producción de anticuerpos detectables mediante la reacción anafiláctica cutánea pasiva. Tampoco se observó ninguna reación anafiláctica por vía intratraqueal. Además, no existe evidencia de potencial de sensibilización dérmica (prueba de Magnusson y Kligman).
CUROSURF no mostró evidencia de actividad mutagénica ni clastogénica.
6 . DATOS FARMACÉUTICOS
6.1 Lista de excipientes
Cloruro sódico.
Bicarbonato sódico Agua para inyección.

6.2 Incompatibilidades
No procede.
6.3 Periodo de validez
18 meses.
Esta caducidad se refiere al producto sin abrir y conservado correctamente.
6.4 Precauciones especiales de conservación
Conservar en nevera (2 - 8oC), protegido de la luz.
Los viales de CUROSURF sin abrir y sin usar que han estado a temperatura ambiente hasta 24 horas pueden volverse a conservar en nevera para uso posterior.
No pasar de temperatura ambiente a nevera más de una vez.
6.5 Naturaleza y contenido del envase
Vial monodosis de vidrio incoloro neutro, provisto de tapón de goma de clorobutilo y cápsula de plástico y aluminio, conteniendo 1,5 ml de suspensión (Curosurf 120 mg) o 3,0 ml de suspensión (Curosurf 240 mg).
6.6 Precauciones especiales de eliminación y otras manipulaciones
El vial debe calentarse a temperatura ambiente, antes de su uso, e invertirse suavemente varias veces, sin agitar, hasta obtener una suspensión uniforme.
La suspensión debe retirarse del vial usando una aguja y jeringa estéril.
Para extraer la suspensión, siga cuidadosamente las instrucciones descritas a continuación:
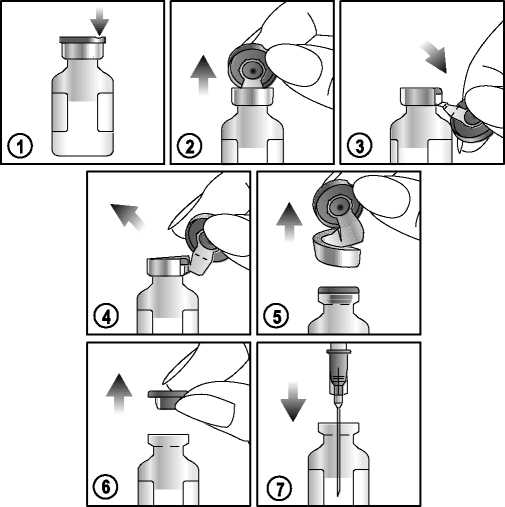
1) Localice la muesca (FLIP <** UP) en el tapón de plástico coloreado.
2) Levante la muesca y tire hacia arriba.
3) Tire del tapón de plástico con la porción del capuchón de aluminio hacia abajo.
4) y 5) Saque todo el anillo arrancando el envoltorio de aluminio.
6 y 7) Saque el tapón de goma para extraer el contenido.
Para uso único. Deseche cualquier cantidad que quedara en el vial. No conserve partes no utilizadas para administraciones posteriores. Los viales calentados no deben volver a introducirse en la nevera.
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo a la normativa local.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
CHIESI ESPAÑA, S.A.
Plaqa d’Europa, 41-43, Planta 10 08908 L’Hospitalet de Llobregat Barcelona
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
CUROSURF 120 N° Registro 59.601
CUROSURF 240 N° Registro 59.600
9. FECHA DE LA PRIMERA AUTORIZACIÓN/ RENOVACIÓN DE LA AUTORIZACIÓN
CUROSURF 120 Agosto 2007 (Renovación)
CUROSURF 240 Agosto 2007 (Renovación
10. FECHA DE LA REVISIÓN DEL TEXTO
Junio/2012
8 de 8