Capd / Dpca 3 Stay Safe Y Sleep Safe, Solucion Para Dialisis Peritoneal
Información obsoleta, busque otroMINISTERIO
DE SANIDAD, POLÍTICA SOCIAL E IGUALDAD
agencia española de medicamentos y productos sanitarios
FICHA TÉCNICA
1. NOMBRE DE LA ESPECIALIDAD FARMACÉUTICA
CAPD / DPCA 3 Stay Safe y Sleep Safe, solución para diálisis peritoneal
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
1 litro contiene:
Cloruro sódico (L)-Lactato sódico Cloruro cálcico x 2H2O Cloruro magnésico x 6 H2O Glucosa monohidrato = 42,5 g Glucosa anhidra
Composición de la solución en mmol/l:
Na+
Ca++
Mg++
Cl-
Lactato Glucosa
Osmolaridad teórica: 511 mOsm/l
pH = 5,5
Para excipientes, ver apartado 6.1
3. FORMA FARMACÉUTICA
Solución para diálisis peritoneal Solución transparente e incolora
4. DATOS CLÍNICOS 4.1. Indicaciones terapéuticas
Insuficiencia renal crónica en fase terminal (descompensada) de cualquier etiología, tratada con diálisis peritoneal.
5,786
3,925
0,2573
0,1017
46,75
134
1,75
0,5
103,5
35
235,8
g
g
g
g
g
mmol/l
mmol/l
mmol/l
mmol/l
mmol/l
mmol/l
Correo electrónicoI
C/ CAMPEZO, 1 - EDIFICIO 8 28022 MADRID

4.2. Posología y Método de administración
Dosificación
Esta solución está indicada exclusivamente para uso intraperitoneal.
La forma, frecuencia de administración y tiempo de permanencia requeridos serán especificados por el médico.
Si no se aconseja otra cosa, los pacientes recibirán una infusión de 2000 ml de solución por intercambio, cuatro veces al día. La solución se drenará después de un tiempo de permanencia entre 2 y 10 horas.
Para cada paciente individual será necesario ajustar la dosis, volumen y número de intercambios.
Si al inicio de la diálisis peritoneal se produce dolor, debido a distensión abdominal, el volumen de solución por intercambio debería reducirse temporalmente a 500 - 1500 ml.
En pacientes corpulentos, y si se ha perdido la función renal residual, será necesario un volumen mayor de solución para diálisis. En estos pacientes, o en pacientes que toleran volúmenes mayores, puede administrarse un volumen de 2500-3000 ml de solución por intercambio.
Si se utiliza una máquina para diálisis peritoneal cíclica continua o intermitente, se recomienda el empleo de bolsas mayores que proporcionen más de un intercambio de solución.
En niños el volumen de solución por intercambio deberá reducirse según la edad, estatura y peso corporal (30 - 40 ml/kg de peso corporal).
No hay recomendaciones especiales de dosificación en ancianos.
Las soluciones de diálisis peritoneal con una concentración elevada de glucosa (2,3% ó 4,25%) se utilizan cuando el peso corporal está por encima del peso seco deseado. La eliminación de líquido aumenta en relación a la concentración de glucosa de la solución para diálisis peritoneal. Estas soluciones deberán usarse con precaución para tratar cuidadosamente la membrana peritoneal, prevenir la deshidratación y mantener la carga de glucosa tan baja como sea posible.
La diálisis deberá realizarse diariamente a las dosis prescritas. La diálisis peritoneal es un tratamiento de larga duración que conlleva la administración repetida de las soluciones individuales.
CAPD / DPCA 3 Stay Safe y Sleep Safe, contiene 42,5 g de glucosa en 1000 ml de solución. Método y duración de la administración:
Para las instrucciones de uso paso a paso, por favor vea el apartado 6.6.
En primer lugar, la bolsa de solución se atempera a la temperatura corporal. El calentamiento se realizará con una placa calefactora. El tiempo de calentamiento es de unos 120 minutos para una bolsa de 2000 ml a una temperatura de 22°C. Pueden verse los detalles en el manual de instrucciones de la placa calefactora. No debe usarse un microondas debido al riesgo de sobrecalentamiento local.
En función de las instrucciones del médico, la dosis debe permanecer en la cavidad peritoneal durante 2-10 horas (tiempo de equilibrio) y posteriormente ser drenada. Según la presión osmótica requerida, CAPD / DPCA 3 Stay Safe y Sleep Safe puede usarse secuencialmente con otras soluciones de diálisis peritoneal con un contenido menor de glucosa (es decir, con menor osmolaridad).
Antes de realizar la diálisis peritoneal domiciliaria debe entrenarse al paciente de forma apropiada, éste debe practicar la técnica y adquirir experiencia en la misma. El entrenamiento debe realizarlo personal cualificado. El facultativo responsable debe asegurarse de que el paciente domina las técnicas de manipulación lo suficiente antes de darle el alta y poder realizar la diálisis peritoneal domiciliaria. En caso de cualquier problema o duda, debe contactarse con el médico responsable. La diálisis peritoneal debe mantenerse durante tanto tiempo como sea necesaria una terapia de sustitución de la función renal.
4.3. Contraindicaciones
Para esta solución de diálisis peritoneal específica:
CAPD / DPCA 3 Stay Safe y Sleep Safe, no debe usarse en pacientes con hipokalemia grave, hipercalcemia grave, hipovolemia e hipotensión arterial.
Para el tratamiento de diálisis peritoneal en general:
No debe iniciarse la diálisis peritoneal en caso de:
• Cirugía o lesión abdominal reciente, historia de cirugía abdominal con adhesiones fibrosas, quemaduras abdominales, perforación de intestino.
• Situaciones inflamatorias extensas de la piel abdominal (dermatitis)
• Enfermedades inflamatorias del intestino (enfermedad de Crohn, colitis ulcerosa, diverticulitis)
• Peritonitis
• Fístula abdominal interna o externa.
• Hernia umbilical, inguinal o abdominal de otro tipo
• Tumores intra-abdominales
• Íleo
• Enfermedades pulmonares (especialmente neumonía)
• Sepsis (infección generalizada de la sangre)
• Acidosis láctica (trastorno metabólico)
• Hiperlipidemia extrema (niveles muy elevados de lípidos en sangre)
• En casos raros de uremia, que no pueden tratarse con diálisis peritoneal
• Caquexia y pérdida importante de peso, particularmente cuando la ingesta de proteínas adecuadas no está garantizada
• En pacientes que están física o mentalmente incapacitados para realizar la diálisis peritoneal tal como les ha enseñado el médico
Si durante la diálisis peritoneal se desarrolla cualquiera de los trastornos anteriores, el médico responsable decidirá como actuar.
4.4. Advertencias especiales y Precauciones de uso
Esta solución sólo puede administrarse después de una cuidadosa evaluación beneficio/riesgo en:
E IGUALDAD_
Agencia española de medicamentos y productos sanitarios
• Perdida de electrolitos debida a vómitos y/o diarrea (en estos casos puede ser necesario un cambio temporal a una solución de diálisis peritoneal conteniendo potasio)
• Hipercalcemia, por ejemplo debido a la administración de captadores de fosfato que contengan calcio y/o vitamina D (puede ser necesario el cambio temporal o permanente a una solución con un menor contenido de calcio).
• Tratamiento con digital: Es obligatoria la monitorización regular de los niveles plasmáticos de potasio. Una hipokalemia grave puede precisar el uso de una solución de diálisis conteniendo potasio junto con consejos dietéticos)
• Pacientes con riñones grandes policísticos.
Debe comprobarse la claridad y volumen del dializado. Una turbidez, que puede ir acompañada de dolor abdominal o no, o sólo dolor abdominal son indicadores de peritonitis.
Durante la diálisis peritoneal se producen pérdidas de proteínas, aminoácidos y vitaminas hidrosolubles. Para evitar déficits debe asegurarse una dieta adecuada o un aporte suplementario.
Las características de transporte de la membrana peritoneal pueden cambiar durante la diálisis peritoneal de larga duración, indicada primariamente por una pérdida de ultrafiltración. En casos graves debe detenerse la diálisis peritoneal e iniciarse la hemodiálisis.
Se recomienda una monitorización regular de los siguientes parámetros:
• Peso corporal, para el reconocimiento inmediato de hiper- y deshidratación
• Sodio, potasio, calcio, magnesio y fosfato séricos, equilibrio ácido-base, gases sanguíneos y proteínas en sangre.
• Creatinina y urea séricas
• Paratormona y otros indicadores del metabolismo óseo
• Azúcar en sangre
• Función renal residual, para adaptar la diálisis peritoneal.
Pacientes ancianos
Antes de iniciar la diálisis peritoneal debe tenerse en cuenta la mayor incidencia de hernias en ancianos.
Manipulación (ver también apartado 6.6)
Ocasionalmente, los envases de plástico pueden deteriorarse durante el transporte o el almacenamiento. Esto puede dar lugar a contaminación con crecimiento de microorganismos en la solución para diálisis. Por tanto, todos los envases deben inspeccionarse cuidadosamente antes de la conexión de la bolsa y utilización de la solución para diálisis peritoneal. Cualquier deterioro, aunque sea pequeño, del conector, tapón, soldaduras del envase o esquinas debe tenerse en cuenta debido al riesgo de contaminación. Las bolsas deterioradas o con el contenido turbio nunca deben utilizarse.
Esta solución debe utilizarse sólo si la solución de diálisis es transparente y el envase está intacto. Cualquier porción de la solución que no se utilice debe desecharse.
La sobrebolsa sólo debe eliminarse antes de la administración
Deben mantenerse condiciones asépticas durante el intercambio de dializado para reducir el riesgo de infección.
La solución para diálisis peritoneal no debe usarse para infusión intravenosa.
4.5. Interacciones con otros medicamentos y otras formas de interacción
La utilización de esta solución para diálisis peritoneal puede producir pérdida de eficacia de otros medicamentos si éstos son dializables a través de la membrana peritoneal. Puede ser necesario ajustar la dosis.
Una marcada reducción de los niveles plasmáticos de potasio puede aumentar la frecuencia de las reacciones adversas asociadas a digital. Los niveles de potasio deben monitorizarse estrechamente en la administración concomitante de digital.
La administración concomitante de medicamentos que contienen calcio o vitamina D puede producir hipercalcemia.
El empleo de agentes diuréticos puede ayudar al mantenimiento de la diuresis residual pero también puede provocar desequilibrios del agua y electrolitos.
En pacientes diabéticos deberá ajustarse la dosis diaria de insulina o antidiabéticos orales, teniendo en cuenta la carga aumentada de glucosa.
4.6. Embarazo y lactancia
No hay datos adecuados sobre el empleo de estas soluciones en estudios en animales o en mujeres embarazadas.
Deben tomarse precauciones cuando se prescriben a mujeres embarazadas o durante el periodo de lactancia.
4.7. Efectos sobre la capacidad de conducir y usar maquinaria
CAPD / DPCA 3 Stay Safe y Sleep Safe, no influye o lo hace de forma insignificante sobre la capacidad para conducir y utilizar maquinaria.
4.8. Reacciones adversas
CAPD / DPCA 3 Stay Safe y Sleep Safe, es una solución electrolítica cuya composición es similar a la sangre.
Las posibles reacciones adversas pueden producirse por la propia diálisis peritoneal o pueden ser inducidas por la solución de diálisis peritoneal.
La peritonitis y las infecciones de la piel en el punto de salida son reacciones adversas muy comunes en la diálisis peritoneal, otras reacciones adversas son menos frecuentes.
Reacciones adversas potenciales debidas a la solución para diálisis peritoneal:
Trastornos del metabolismo y la nutrición
Niveles elevados de azúcar en sangre, hiperlipidemia, aumento del peso corporal debido al aporte continuo de glucosa desde la solución para diálisis peritoneal Trastornos cardíacos y vasculares
Taquicardia, hipotensión, hipertensión
Trastornos respiratorios Disnea
Trastornos renales
Trastornos de los electrolitos, por ej. hipokalemia, hipercalcemia en combinación con un aumento del aporte de calcio. Por ej. por la administración de captadores de fosfato que contengan calcio
Trastornos generales
Mareos, edema, alteración de la hidratación indicada ya sea por una rápida disminución (deshidratación) o aumento (hiperhidratación) del peso corporal. Puede presentarse una deshidratación severa cuando se utilizan soluciones con una concentración mayor de glucosa.
Reacciones adversas potenciales debidas al tratamiento:
Infecciones
Peritonitis, infecciones de la piel en el punto de salida y túnel del catéter; en casos muy raros sepsis
Trastornos respiratorios, torácicos y del mediastino
Disnea causada por elevación del diafragma; dolor en el hombro
Trastornos gastrointestinales
Diarrea; constipación; hernia; distensión abdominal y sensación de plenitud Trastornos generales y condiciones del lugar de administración/catéter
Malestar general, enrojecimiento, edema, costras de exudaciones y dolor en el lugar de salida del catéter
Trastornos relacionados con el procedimiento de diálisis peritoneal
Dializado turbio; trastornos en la entrada y salida de la solución para diálisis.
La peritonitis viene indicada por un dializado turbio. Posteriormente puede desarrollarse dolor abdominal, fiebre y malestar general o, en casos muy raros, sepsis. El paciente debe consultar inmediatamente al médico. La bolsa con el dializado turbio debe cerrarse con un tapón estéril para evaluación de la contaminación microbiológica y recuento de glóbulos blancos.
En casos de infecciones del túnel del catéter y de la piel en el lugar de salida deberá consultarse al médico tan pronto como sea posible.
4.9. Sobredosificación
No se ha informado de situaciones de emergencia relacionadas con una sobredosis.
Cualquier exceso de solución de diálisis puede fácilmente ser drenada a una bolsa vacía. Sin embargo, si los cambios de bolsa son demasiado frecuentes o rápidos pueden producirse estados de deshidratación y/o alteraciones electrolíticas que necesitan atención médica inmediata. Si se ha olvidado algún intercambio, como norma deberían reducirse los tiempos de permanencia de las siguientes bolsas de forma que la cantidad total requerida de solución para diálisis por día (por ej. 4 x 2000 ml) se alcance.
Un balance incorrecto puede llevar a una sobre- o deshidratación y alteraciones electrolíticas.
La consecuencia más probable de una sobredosis CAPD / DPCA 3 Stay Safe y Sleep Safe, es una deshidratación. Una infradosificación o la no continuación del tratamiento pueden provocar una hiperhidratación con consecuencias graves para la vida, edema periférico y descompensación cardíaca y/o otros síntomas de uremia, que pueden poner en peligro la vida del paciente.
Deben aplicarse las normas generalmente aceptadas para cuidados de emergencia y terapia intensiva. El paciente puede precisar una hemodiálisis inmediata.
5. PROPIEDADES FARMACOLÓGICAS
5.1. Propiedades farmacodinámicas
Grupo farmacoterapéutico: Solución para diálisis peritoneal
Código ATC: B05D B
CAPD / DPCA 3 Stay Safe y Sleep Safe, es una solución tamponada de lactato que contiene glucosa y electrolitos, indicada para administración intraperitoneal en el tratamiento de insuficiencia renal terminal de cualquier etiología.
La característica de la diálisis peritoneal continua ambulatoria (CAPD) es la presencia más o menos continua de unos 2 litros de solución para diálisis en la cavidad peritoneal. La solución para diálisis se sustituye por solución nueva entre tres y cinco veces por día.
El principio básico de la técnica de diálisis peritoneal es el uso del peritoneo como una membrana semi-permeable que permite el intercambio de solutos y agua entre la sangre y la solución para diálisis por difusión y convección según sus propiedades físico-químicas.
El perfil de electrolitos de la solución es básicamente el mismo que el del suero fisiológico, aunque se ha adaptado (por ejemplo el contenido de potasio) para la utilización en pacientes urémicos, para permitir una terapia de sustitución de la función renal mediante un intercambio de sustancias y fluido intraperitoneal. Las sustancias que normalmente se eliminan por la orina como productos de desecho urémicos, tales como la urea y creatinina, fosfato inorgánico, ácido úrico, otros solutos y agua, se eliminan del organismo por la solución de diálisis.
El balance de fluidos puede mantenerse mediante la combinación de soluciones con diferente concentración de glucosa, que logran la eliminación de fluidos (ultrafiltración)
La acidosis metabólica como consecuencia de la insuficiencia renal terminal se compensa con la presencia de lactato en la solución. La completa metabolización del lactato da como resultado la formación de bicarbonato.
5.2 Propiedades farmacocinéticas
Los productos urémicos de desecho (por ej. urea, creatinina, ácido úrico), fosfato inorgánico y electrolitos tales como sodio, potasio, calcio y magnesio se eliminan desde el organismo a la solución de diálisis por difusión y/o convección.
La glucosa del dializado se utiliza como agente osmótico en CAPD / DPCA 3 Stay Safe y Sleep Safe. Se absorbe lentamente, reduciendo el gradiente de difusión entre la solución de diálisis y el fluido extracelular. La ultrafiltración es máxima al principio del tiempo de permanencia, alcanzando un pico después de unas 2 ó 3 horas. La absorción posterior empieza con una progresiva pérdida de ultrafiltrado. Después de 4 horas, el promedio de ultrafiltrado es 100 ml con un 1,5%, 400 ml con un 2,3% y 800 ml con un 4,25%. Durante un periodo de diálisis de 6 horas, se absorbe el 60-80% de la glucosa dializada.
La transferencia de calcio depende de la concentración de glucosa en la solución para diálisis, el volumen eliminado, el calcio sérico ionizado y la concentración de calcio en la solución para diálisis. Cuanto mayor sea la concentración de glucosa, el volumen eliminado y la concentración de calcio sérico y menor la concentración de calcio en la solución para diálisis, mayor será la transferencia de calcio desde el paciente al dializado.
5.3. Datos de seguridad preclínicos
No se han realizado estudios preclínicos de toxicidad con CAPD / DPCA 3 Stay Safe y Sleep Safe, pero los estudios clínicos con soluciones para diálisis peritoneal comparables no han revelado riesgos importantes de toxicidad.
6. CARACTERÍSTICAS FARMACÉUTICAS
6.1. Lista de excipientes
Agua para inyectables Ácido clorhídrico Hidróxido sódico
6.2. Incompatibilidades
Debido al riesgo de incompatibilidad y contaminación, sólo se pueden añadir medicamentos bajo prescripción de un médico
Este medicamento no debe utilizarse con otros medicamentos, excepto aquellos mencionados en el apartado 6.6.
6.3. Período de validez
Periodo de validez en el recipiente de venta: 2 años
6.4. Precauciones especiales de conservación No almacenar por debajo de 4°C
6.5. Naturaleza y contenido del envase Sistema Estándar:
El Sistema Estándar se suministra como un sistema de una sola bolsa, consistente en una bolsa de PVC con la solución, un conector Safe lock de policarbonato y un port de inyección de policarbonato / caucho sintético.
Sistema Sleep Safe:
El Sistema Sleep Safe se suministra como un sistema de una sola bolsa sin PVC de 5 litros para ser utilizada en una diálisis peritoneal automatizada, donde se utiliza una máquina cíclica para la infusión y drenaje de la solución de diálisis.
Sistema Andy P.L.U.S.:
El Sistema Andy P.L.U.S. se suministra como un sistema de dos bolsas, consistente en una bolsa de PVC con la solución, con un sistema de conexión de PVC/Policarbonato, un conector macho de policarbonato /silicona y una bolsa de drenaje.
Sistema Stay Safe:
El Sistema Stay Safe se suministra como un sistema de dos bolsas, consistente en una bolsa sin PVC con la solución, fabricada con un film multicapa de poliolefina, un sistema de tubos de poliolefina, un sistema de conexión (DISC) con una llave rotatoria (polipropileno) y una bolsa de drenaje también fabricada con un film multicapa de poliolefina.
6.6. Instrucciones de uso / manipulación
Para un solo uso
La bolsa con la solución se calienta en primer lugar a temperatura corporal. Para las bolsas con un volumen de hasta 3000 ml, esto se tiene que realizar utilizando una placa calefactora apropiada. El tiempo de calentamiento para una bolsa de 2000 ml a una temperatura inicial de 22° C es aproximadamente de 120 min. El control de temperatura se hace automáticamente y se coloca a 39°C ± 1°C. Se puede obtener una información más detallada en el manual de instrucciones del calentador de la bolsa. No se recomienda el uso de horno microondas para calentar la solución debido al riesgo de sobrecalentamiento local. Las bolsas de 3000 ml también se utilizan en combinación con un ciclador (sleep safe). El calentamiento se realiza automáticamente mediante el equipo de calentamiento integrado/escala de pesadas. Después del calentamiento de la solución se puede comenzar con el intercambio de las bolsas.
Instrucciones de uso del conector Safe lock:
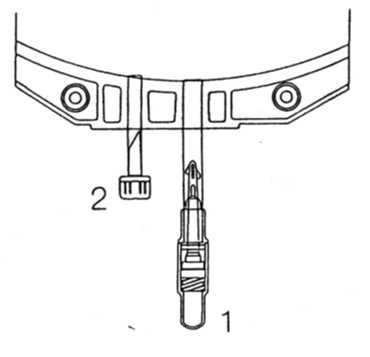
1. Quitar el tapón protector del conector (1) del tubo de conexión.
2. Conectar los tubos a la bolsa.
3. Romper el cierre interior doblando el tubo y el pin a ambos lados en un ángulo mayor de 90°.
4. La bolsa está lista para su uso.
Se puede realizar otra inyección a través de un segundo port de adición (2).
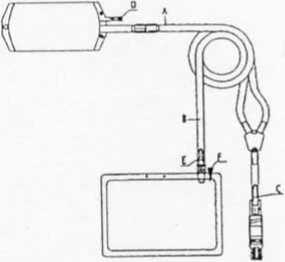
1. Sujetar la sobrebolsa con las dos manos por la marca para su rotura y quitar la sobrebolsa.
2. Sacar el conector del paciente de su envoltorio en la bolsa de drenaje enrollada.
3. Quitar la anilla de la bolsa para drenaje enrollada y estirar la bolsa.
4. Sujetar los tubos por los ptos. A (próximo a la bolsa) y B (próximo a la bolsa de drenaje) y separarlos para desenrollar el equipo de transferencia que está enrollado.
5. Colocar una pinza externa en el tubo de entrada (entre la bo
6. Quitar el tapón protector del conector del paciente.
7. Conectar el tubo al conector del catéter.
8. Romper el pin de los conos de ruptura ( C ) Y (E) doblando el pin a ambos lados en un ángulo mayor de 90°.
9. Abrir la pinza del catéter para permitir el drenaje.
10. Después del drenaje, cerrar la pinza del catéter.
11. Abrir la pinza del tubo de entrada para permitir que la solución fresca purgue cualquier resto de aire que esté en el tubo de entrada a la bolsa de drenaje (2 - 3 segundos aprox.)
12. Colocar una pinza externa en el tubo de drenaje.
13. Abrir la pinza del catéter para permitir la entrada.
14. Después de la entrada, cerrar la pinza del catéter.
15. Colocar la pinza A.N.D.Y. en el tubo del paciente entre la pieza en “Y” y el conector y cerrarla con firmeza. Romper el sistema utilizado por la pieza en “Y” y desecharlo. En el port de administración (D) se pueden inyectar medicaciones diferentes, y se pueden tomar muestras a través del port de muestreo (F) utilizando una técnica aséptica.
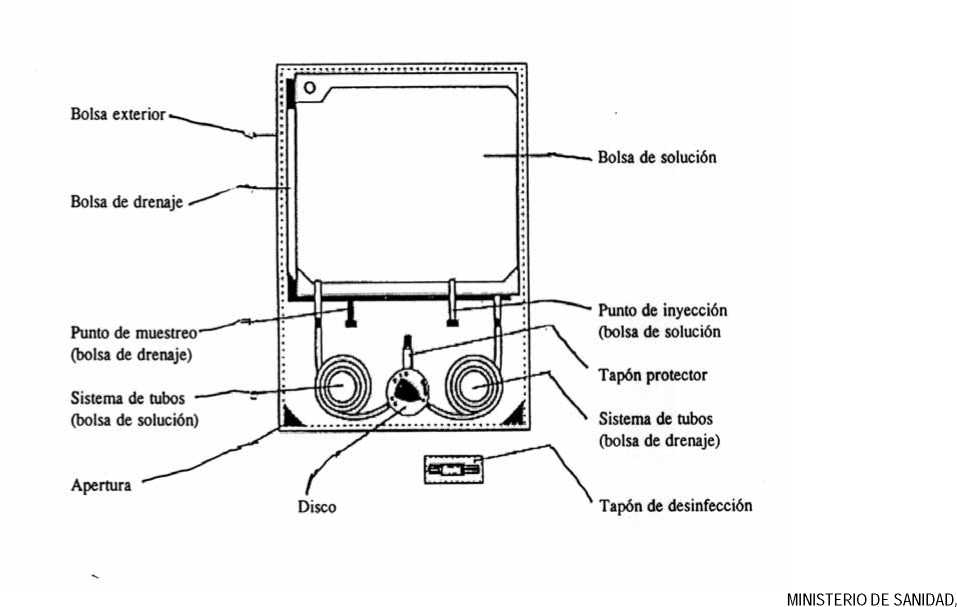
1. Comprobar la bolsa de solución (etiqueta, fecha de caducidad y comprobar que la solución sea clara) - abrir la bolsa exterior y el envoltorio del tapón desinfectante.
2. Lavarse las manos con una solución de lavado antimicrobiana.
3. Colocar el DISC en el organizador (suspender la bolsa de solución por el agujero en el colgador superior del palo - desenrollar la línea "DISC-bolsa de solución"- colocar el DISC en el organizador - después colocar la bolsa de drenaje en el colgador inferior del palo).
4. Colocar el adaptador del catéter en el organizador.
5. Desinfectarse las manos y quitar el tapón protector del DISC.
6. Conectar el adaptador del catéter al DISC.
7. Abrir la pinza del catéter - posición "(" -Empieza el proceso de vaciado
8. Posición de Flush "((" - fluye el dializado fresco a la bolsa de drenaje (aprox. 5 segundos).
9. Llenado - posición "*)(" - conexión entre la bolsa de solución y el catéter.
10. Etapa de seguridad - posición "((((" - cierre automático del adaptador del catéter con el PIN.
11. Desconexión (quitar el adaptador del catéter del DISC) - enroscar el adaptador del catéter al nuevo tapón desinfectante.
12. Cerrar el DISC. Cerrar el DISC con la parte abierta del tapón protector (que está colocado en el agujero de la derecha del organizador).
13. Controlar el dializado drenado y tirarlo.
POLÍTICA SOCIAL E IGUALDAD
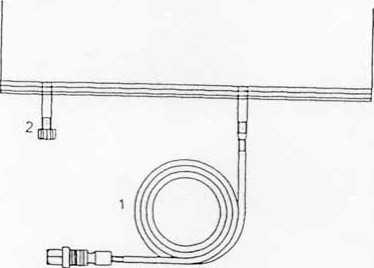
1. Desenrollar el tubo (1) de la bolsa.
2. Insertar el conector en el port libre de la cubeta Sleep-Safe™.
3. La bolsa ya está preparada para su uso con el equipo Sleep-Safe™.
Se puede efectuar una otra inyección a través de un segundo port de administración (2).
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
FRESENIUS MEDICAL CARE ESPAÑA S.A.
Ctra. Vallderiolf, km 0,4
08430 La Roca del Vallés (Barcelona)
8. NÚMERO DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
N° Reg: 61.887
9. FECHA DE LA PRIMERA AUTORIZACIÓN / RENOVACIÓN DE LA AUTORIZACIÓN
28-12-1998
10. FECHA DE LA REVISIÓN (PARCIAL) DEL TEXTO
Octubre 2003
Agencia española de
medicamentos y
productos sanitarios