Aminoplasmal Paed 10% Solucion Para Perfusion
FICHA TÉCNICA
1. NOMBRE DEL MEDICAMENTO
Aminoplasmal Paed 10 % solución para perfusión
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
La solución para perfusión contiene:
|
Aminoácidos: |
por 1 ml |
por 100 ml |
por 250 ml |
|
Isoleucina |
5,10 mg |
0,51 g |
1,28 g |
|
Leucina |
7,60 mg |
0,76 g |
1,90 g |
|
Lisina monohidrato (equivalente en lisina) |
9,88 mg (8,80 mg) |
0,99 g (0,88 g) |
2,47 g (2,20 g) |
|
Metionina |
2,00 mg |
0,20 g |
0,50 g |
|
Fenilalanina |
3,10 mg |
0,31 g |
0,78 g |
|
Treonina |
5,10 mg |
0,51 g |
1,28 g |
|
Triptófano |
4,00 mg |
0,40 g |
1,00 g |
|
Valina |
6,10 mg |
0,61 g |
1,53 g |
|
Arginina |
9,10 mg |
0,91 g |
2,28 g |
|
Histidina |
4,60 mg |
0,46 g |
1,15 g |
|
Alanina |
15,90 mg |
1,59 g |
3,98 g |
|
Glicina |
2,00 mg |
0,20 g |
0,50 g |
|
Ácido aspártico |
6,60 mg |
0,66 g |
1,65 g |
|
Ácido glutámico |
9,30 mg |
0,93 g |
2,33 g |
|
Prolina |
6,10 mg |
0,61 g |
1,53 g |
|
Serina |
2,00 mg |
0,20 g |
0,50 g |
|
N-acetiltirosina (equivalente en tirosina) |
1,30 mg (1,06 mg) |
0,13 g (0,11 g) |
0,33 g (0,27 g) |
|
Acetilcisteína (equivalente en cisteína) |
0,700 mg (0,520 mg) |
0,070 g (0,052 g) |
0,175 g (0,13 g) |
|
Taurina |
0,300 mg |
0,030 g |
0,075 g |
|
por 1 ml |
por 100 ml |
por 250 ml | |
|
Contenido de aminoácidos |
0,1 g |
10 g |
25 g |
|
Contenido de nitrógeno |
0,0152g |
1,52 g |
3,8 g |
Para consultar la lista completa de excipientes, ver sección 6.1.
3. FORMA FARMACÉUTICA
Solución para perfusión
Solución transparente, de incolora hasta un amarillo claro
Energía [kJ/l (kcal/l)]
1.700 (400)
|
Osmolaridad teórica [mOsm/l] |
790 |
|
Acidez (titulación a pH 7,4) |
23 mmol |
|
pH |
aprox. 6,1 |
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
Aporte de aminoácidos como parte de la nutrición parenteral en combinación con soluciones energéticas (glucosa y lípidos) y soluciones que contienen electrolitos para los recién nacidos, a término y prematuros, lactantes y niños, cuando la nutrición oral o por sonda nasogátrica es imposible, insuficiente o está contraindicada.
4.2 Posología y forma de administración
Posología
Población pediátrica
Las dosis para estos grupos etarios, tal y como se indican a continuación, son valores promedio de orientación. La dosis exacta debe ajustarse de forma individual de acuerdo con la edad, el estado del desarrollo, la enfermedad predominante y el tipo de tratamiento.
La administración debe iniciarse por debajo del valor de velocidad de perfusión objetivo e incrementarse hasta el mismo durante la primera hora.
El suministro por vía parenteral de aminoácidos considerado adecuado para la mayoría de los pacientes pediátricos:
Lactantes prematuros: 1,5 - 4,0 g de aminoácidos/kg de peso corporal (p.c.) por día =15 - 40 ml/kg p. c./d
Lactantes recién nacidos a término (de 0 a 27 días): 1,5 - 3,0 g/kg p. c./d = 15 - 30 ml/kg p. c./d Lactantes y niños pequeños (de 28 días a 23 meses): 1,0 - 2,5 g/kg p. c./d = 10 - 25 ml/kg p. c./d Niños (de 2 a 11 años): 1,0 - 2,0 g/kg p. c./d = 10 - 20 ml/kg p. c./d
Para los niños en estado crítico, la ingesta aconsejable de aminoácidos puede ser mayor (hasta 3,0 g de aminoácidos/kg de peso corporal por día).
La velocidad máxima de perfusión de hasta 0,1 g de aminoácidos/kg de peso corporal y hora se corresponde aproximadamente con 1 ml/kg de peso corporal y hora.
Forma de administración Vía intravenosa.
Debido a su elevada osmolaridad, Aminoplasmal Paed 10 % sin diluir solo debe administrarse a través de una vena central. Sin embargo, la dilución suficiente de Aminoplasmal Paed 10 %, por ejemplo, con agua para preparaciones inyectables o con una solución adecuada reduce la osmolaridad y permite la perfusión periférica.
Si son adecuados los suministros concomitantes de energía y electrolitos, no existen restricciones como parte de un régimen de nutrición parenteral.
Aminoplasmal Paed 10 % representa meramente una base para la nutrición parenteral. En pacientes solamente con nutrición parenteral, es necesaria la restitución concomitante con fuentes de energía (teniendo en cuenta las necesidades de ácidos grasos esenciales), electrolitos, vitaminas y oligoelementos.
4.3 Contraindicaciones
• Hipersensibilidad al (a los) principio(s) activo(s) o a alguno de los excipientes incluidos en la sección
6.1
• Estados de hiperhidratación, hipocaliemia
• Errores innatos del metabolismo de los aminoácidos
• Alteraciones metabólicas agudas debido a la hipoxia y la acidosis
• Inestabilidad circulatoria de amenaza a la vida
• Edema pulmonar agudo
• Insuficiencia cardíaca descompensada
Al igual que todas las soluciones que contienen aminoácidos, las contraindicaciones para Aminoplasmal Paed 10 % son la insuficiencia hepática grave, el coma hepático y la insuficiencia renal grave en ausencia de terapia renal de reemplazo.
4.4 Advertencias y precauciones especiales de empleo
Se debe tener precaución si la osmolaridad sérica está aumentada.
Debe tenerse precaución si tiene que restringirse la ingesta de líquidos, como en presencia de hiponatremia.
En particular, se necesita una supervisión más frecuente del estado clínico y de los valores analíticos apropiados en pacientes con:
• Alteraciones del metabolismo de los aminoácidos.
• Alteración hepática, debido al riesgo de recurrencia o exacerbación de los trastornos neurológicos existentes asociados con la hiperamoniemia.
• Insuficiencia renal, sobre todo en presencia de hipercaliemia, o factores de riesgo para el desarrollo o la exacerbación de la acidosis metabólica, o con hiperazotemia debido la alteración de la depuración renal.
La dosis debe ajustarse a la edad, estado nutricional y enfermedad subyacente. Ver sección 4.2.
Además, es esencial que el tratamiento se suplemente mediante el suministro de fuentes adyuvantes de energía (glucosa y lípidos), vitaminas y oligoelementos.
En el caso de micronutrientes, se deben usar las formulaciones pediátricas.
Aminoplasmal Paed 10 % debe diluirse lo suficiente con una solución adecuada antes de administrarse a través de una vena periférica. Ver sección 4.2.
Deben supervisarse el equilibrio hidroelectrolítico, la osmolaridad sérica, el equilibrio acidobásico, los niveles de glucosa en sangre, la función renal y los valores hepáticos durante la duración del tratamiento parenteral, y la frecuencia de la supervisión se determinará mediante la gravedad de la enfermedad subyacente y el estado clínico del paciente.
<sfr>
íwm
ÍTTI
Debe realizarse la determinación de las concentraciones en suero del nitrógeno ureico y de amonio.
Durante el uso a largo plazo (varias semanas), deben supervisarse con más atención los recuentos celulares sanguíneos y los factores de coagulación.
4.5 Interacción con otros medicamentos y otras formas de interacción
No se conocen.
4.6 Fertilidad, embarazo y lactancia
Aminoplasmal Paed 10 % solo está destinado para su uso en la población pediátrica.
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
No procede.
4.8 Reacciones adversas
Pueden producirse reacciones adversas que, sin embargo, no están relacionadas específicamente con el producto sino con la nutrición parenteral en general, especialmente, al inicio de la misma.
Poco frecuentes (>1/1.000 a <1/100):
Trastornos gastrointestinales: náuseas, vómitos
Trastornos generales: cefalea, tiritona, fiebre
Puede producirse tromboflebitis cuando el producto se administra a través de una vena periférica si no está lo suficientemente diluido, debido a la elevada osmolaridad de la solución.
Notificación de sospechas de reacciones adversas
. Se invita a los sistema nacional de
Es importante notificar las sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento profesionales sanitarios a notificar las sospechas de reacciones adversas a través del notificación incluido en el Anexo V.
4.9 Sobredosis
Síntomas
Las velocidades de perfusión demasiado altas pueden conducir a reacciones de intolerancia que se manifiestan en forma de náuseas, vómitos, rubefacción de la cabeza, sensación de calor y pérdidas renales de aminoácidos con desequilibrios consecutivos de los mismos.
Tratamiento
Si se producen reacciones de intolerancia, debe interrumpirse temporalmente la perfusión de aminoácidos y reanudarse posteriormente con una velocidad de perfusión inferior.
ÍTTI
5. PROPIEDADES FARMACOLÓGICAS
5.1 Propiedades farmacodinámicas
Grupo farmacoterapeútico: soluciones para la nutrición parenteral, aminoácidos, código ATC: B05BA01 Mecanismo de acción
La solución para perfusión contiene 19 aminoácidos para cubrir las necesidades proteicas cualitativas del niño:
- todos los aminoácidos esenciales y semiesenciales para los niños
En comparación con las soluciones convencionales de aminoácidos, Aminoplasmal Paed 10 % contiene:
- una proporción relativamente alta de lisina
- taurina
- una proporción relativamente baja de metionina
- una proporción baja de fenilalanina y prolina
Las soluciones no contienen electrolitos adicionales, a fin de excluir cualquier efecto sobre el tratamiento de los electrolitos en los niños durante la reanimación.
Efectos farmacodinámicos
Los aminoácidos representan los componentes básicos para la síntesis de proteínas. Las soluciones puras de aminoácidos se administran como parte del tratamiento de nutrición parenteral junto con fuentes de energía y otros nutrientes, como electrolitos, oligoelementos, vitaminas y líquidos, a fin de mantener y mejorar el estado nutricional del organismo o de minimizar cualquier pérdida de sustancias.
5.2 Propiedades farmacocinéticas
Absorción
Aminoplasmal Paed 10 % se perfunde por vía intravenosa. Por lo tanto, todos los sustratos están disponibles de forma inmediata para su metabolismo.
Distribución
Las concentraciones de aminoácidos libres en el plasma están sujetas a fluctuaciones importantes. Esto se aplica tanto a las concentraciones de los aminoácidos individuales, como a la suma de las mismas. En contraste, las interrelaciones entre los aminoácidos permanecen relativamente constantes, independientemente de la concentración total de los aminoácidos o de los niveles absolutos de concentración de los aminoácidos individuales. Podría parecer que el organismo se esfuerza por mantener el sustrato aminoacídico a un nivel constante dentro de un intervalo fisiológico de referencia y por evitar, en la medida de lo posible, desequilibrios en el patrón de los aminoácidos. En la mayoría de los casos en los que se mantienen las posibilidades de compensación del organismo, los cambios drásticos en la administración de los sustratos solamente conducen a alterar la homeostasis de los aminoácidos en la sangre. Solamente se esperan cambios patológicos típicos en el perfil plasmático de los aminoácidos cuando el índice regulador de los órganos metabólicos básicos, p. ej., el hígado o los riñones, se ven alterados de forma considerable. En caso necesario, dichos cambios pueden tratarse en términos de restauración de la homeostasis, con soluciones de aminoácidos con una composición específica.
ÍTTI
En condiciones patológicas sin suministro exógeno de aminoácidos, se producen cambios típicos importantes en el patrón plasmático de los aminoácidos que, por lo general, afectan tanto a la concentración absoluta de los aminoácidos individuales, como a su composición porcentual en el plasma.
Metabolismo o Biotransformación
Los aminoácidos en su conjunto son un sistema complejo de sustancias que se influyen entre sí. Por un lado, hay una dependencia metabólica directa entre los aminoácidos individuales (por ejemplo: producción de tirosina a través de la hidroxilación de la fenilalanina). Por otro lado, otros mecanismos metabólicos del organismo pueden mostrar una respuesta sensible a un cambio en el patrón de los aminoácidos, mediante la alteración de la concentración de los aminoácidos individuales o de los grupos de aminoácidos (por ejemplo: cambios en la proporción de aminoácidos aromáticos con respecto a la de aminoácidos ramificados). Además, los cambios en las relaciones dentro de un grupo de aminoácidos con una configuración química y un comportamiento metabólico similares, pueden tener efectos sobre el metabolismo general del organismo.
5.3 Datos preclínicos sobre seguridad
No se han realizado estudios preclínicos con Aminoplasmal Paed 10 %.
6 . DATOS FARMACÉUTICOS
6.1 Lista de excipientes
Acido cítrico monohidrato (para el ajuste del pH)
Agua para preparaciones inyectables.
6.2 Incompatibilidades
Este medicamento no debe mezclarse con otros excepto con los mencionados en la sección 6.3.
6.3 Periodo de validez
- Sin abrir (bolsa en envoltura):
2 años
- Después de la primera apertura:
El producto debe usarse inmediatamente.
- Después de la mezcla con otros componentes de la nutrición parenteral:
Aminoplasmal Paed 10 % debe mezclarse con otras soluciones IV, si se ha comprobado de antemano la compatibilidad.
Los datos de compatibilidad para los diferentes aditivos (p. ej., glucosa, lípidos, electrolitos, oligoelementos, vitaminas) y los correspondientes periodos de validez de dichas mezclas pueden ser proporcionados por fabricante bajo solicitud.
Se ha demostrado la estabilidad química y física en uso durante 24 horas entre 2 C y 8 °C más 24 horas a 37 °C después de la mezcla con dichas soluciones.
Desde un punto de vista microbiológico, el producto debe usarse inmediatamente. Si no se usa inmediatamente, las condiciones y tiempos de almacenamiento en uso antes del mismo, son responsabilidad del usuario.
ÍTTI
6.4 Precauciones especiales de conservación
No congelar. Desechar la bolsa si se congela de forma accidental.
Para las condiciones de conservación tras la mezcla de los aditivos, ver sección 6.3.
6.5 Naturaleza y contenido del envase
Aminoplasmal Paed 10 % se suministra en bolsas flexibles hechas de una hoja multicapa (polipropileno, estireno etileno butileno estireno (SEBS) y éter de copoliéster). La capa interna que está en contacto con la solución se compone de polipropileno. Las bolsas contienen 100 ml o 250 ml.
La bolsa está empaquetada en una envoltura protectora. Se ha colocado un absorbente de oxígeno (sobre de material inerte que contiene hidróxido de hierro en polvo) entre la bolsa y la envoltura.
Los diferentes tamaños de envase se presentan en cajas de 12 bolsas. Tamaños de envase: 12 x 100 ml y 12 x 250 ml.
Puede que solamente estén comercializados algunos tamaños de envases.
6.6 Precauciones especiales de eliminación
Ninguna especial para la eliminación del envase, de la envoltura y del absorbente de oxígeno.
No usar si la envoltura se ha abierto con anterioridad o está dañada. Utilizar solamente bolsas que no estén dañadas y en las que la solución de aminoácidos sea transparente y esté libre de partículas.
Aminoplasmal Paed 10 % se suministra en envases de un solo uso. Deben desecharse los residuos no utilizados.
La solución debe llevarse siempre a temperatura ambiente antes de la perfusión.
Es esencial que cualquier mezcla se prepare utilizando técnicas asépticas estrictas, puesto que esta mezcla de nutrientes favorece el crecimiento microbiano.
Aminoplasmal Paed 10 %: Manipulación Figura A: Bolsa y envoltura
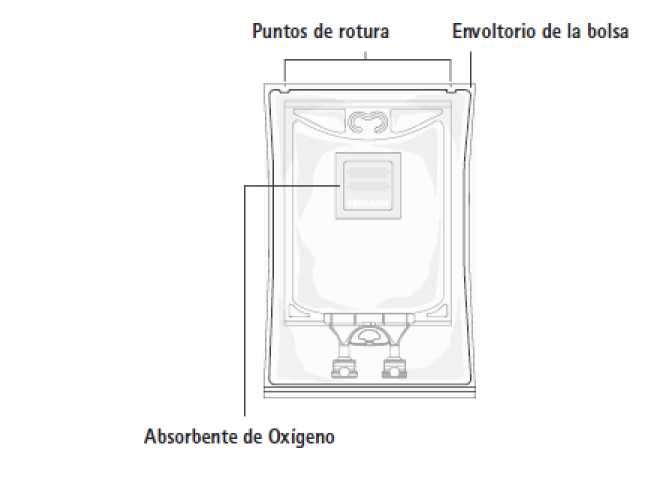
Figura B: Bolsa
Colgador de la bolsa
Puerto t e Infusión
Puerto de Medicación
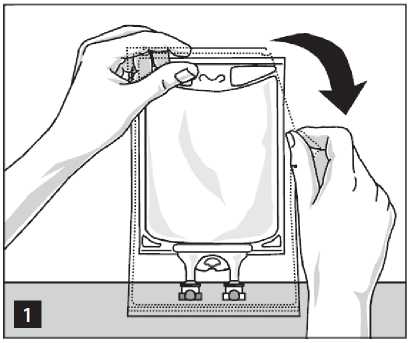
Para abrir:
Retire la bolsa de su envoltura protectora a partir de las muescas rasgadas de la parte superior y extraiga el envase de la solución (figura 1).
Deseche la envoltura y el absorbente de oxígeno.
Compruebe la existencia de fugas. Deseche el producto si la bolsa tiene fugas, puesto que la esterilidad puede estar alterada.
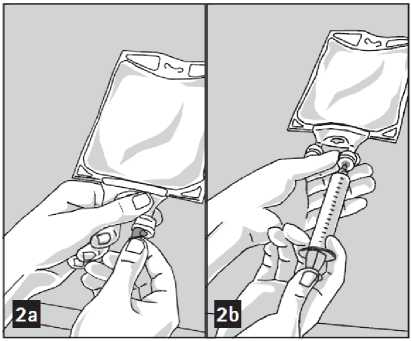
Para añadir el medicamento:
Las mezclas deben prepararse siguiendo técnicas asépticas estrictas.
Pueden añadirse medicamentos suplementarios compatibles a través del puerto para los medicamentos (color transparente).
¿IKfa
1. Prepare el puerto para los medicamentos (color transparente) mediante el retiro de la hoja de aluminio (figura 2a). Tenga en cuenta: la zona por debajo de la hoja del puerto para los medicamentos es estéril.
2. Pinche el puerto resellable para los medicamentos e inyecte el/los aditivo(s) (figura 2b).
3. Mezcle completamente la solución y el medicamento (figura 3a).
4. El puerto para los medicamentos puede limpiarse con un desinfectante (p. ej., isopropanol) antes de volver a pincharlo.
5. Compruebe visualmente la mezcla en busca de partículas (figura 3b).
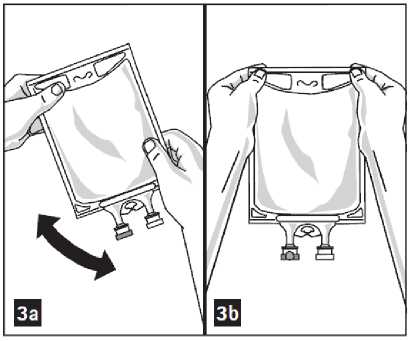
Preparación para su administración:
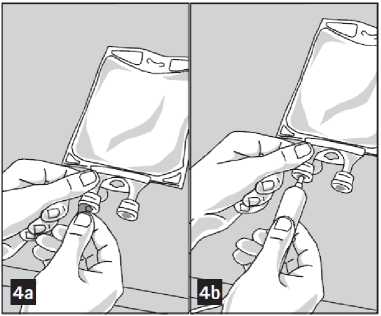
1. Retire la hoja de aluminio del puerto de perfusión (color verde) de la parte inferior del envase (figura 4a) y conecte el equipo de administración (figura 4b): utilice un equipo de perfusión sin toma de aire o cierre la toma de aire de un equipo que la tenga. Siga las instrucciones de uso del equipo de perfusión. Tenga en cuenta: la zona por debajo de la hoja del puerto de perfusión es estéril.
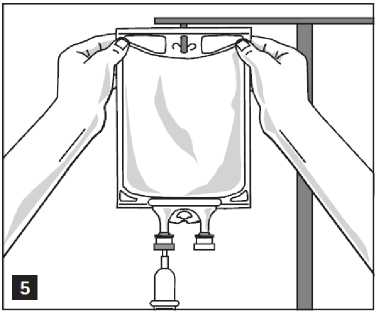
2. Cuelgue la bolsa en un poste IV (figura 5).
Información adicional:
El envase está libre de PVC, DEHP y látex
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
B. Braun Melsungen AG Carl-Braun-StraBe 1 34212 Melsungen
Alemania
"I
an
MINISrSUODE SANIDAD, POLITICA SOCIAL E IGUALDAD Agencia es paño» de medicamentos y oroouctos sallaros
Dirección postal:
34209 Melsungen Alemania
Teléfono: +49/5661/71-0
Fax: +49/5661/71-4567
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
9. FECHA DE LA PRIMERA AUTORIZACIÓN/ RENOVACIÓN DE LA AUTORIZACIÓN
Junio 2014
10. FECHA DE LA REVISIÓN DEL TEXTO Marzo 2014
10 de 10