Vizarsin 100 Mg Comprimidos Recubiertos Con Pelicula Efg
ANEXO I
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
1. NOMBRE DEL MEDICAMENTO
Vizarsin 25 mg comprimidos recubiertos con película Vizarsin50 mg comprimidos recubiertos con película Vizarsin 100 mg comprimidos recubiertos con película
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada comprimido recubierto con película contiene sildenafilo citrato equivalente a 25 mg, 50 mg o 100 mg de sildenafilo.
Excipiente con efecto conocido:
Vizarsin 25 mg comprimidos recubietos con película
Cada comprimido recubierto con película contiene 1,9 mg de lactosa (como monohidrato).
Vizarsin 50 mg comprimidos recubietos con película
Cada comprimido recubierto con película contiene 3,8 mg de lactosa (como monohidrato).
Vizarsín 100 mg comprimidos recubiertos con película
Cada comprimido recubierto con película contiene 7,6 mg de lactosa (como monohidrato).
Para consultar la lista completa de excipientes, ver sección 6.1.
3. FORMA FARMACÉUTICA
Comprimido recubierto con película.
Vizarsin 25 mg comprimidos recubiertos con película: Comprimidos blancos, oblongos y grabados con “25” en una cara.
Vizarsin 50 mgcomprimidos recubiertos con película: Comprimidos blancos, oblongos y grabados con “50” en una cara.
Vizarsin 100 mgcomprimidos recubiertos con película: Comprimidos blancos, oblongos y grabados con “100” en una cara.
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
Vizarsin está indicado en hombres adultos con disfunción eréctil, que es la incapacidad para obtener o mantener una erección suficiente para una actividad sexual satisfactoria.
Para que Vizarsin sea efectivo es necesaria la estimulación sexual.
4.2 Posología y forma de administración
Posología
Uso en adultos
La dosis recomendada es de 50 mg tomados a demanda, aproximadamente una hora antes de la actividad sexual. En base a la eficacia y tolerabilidad, la dosis se puede aumentar a 100 mg o disminuir a 25 mg. La dosis máxima recomendada es de 100 mg. La pauta máxima de dosificación recomendada es de una vez al día. Si se toma Vizarsin con alimentos, el inicio de su acción farmacológica podría retrasarse en comparación a cuando se toma en ayunas (ver sección 5.2).
Poblaciones especiales Pacientes de edad avanzada
No se requiere ajuste de la dosis en pacientes de edad avanzada (pacientes con 65 años de edad o más).
Insuficiencia renal
Las dosis recomendadas descritas en “Uso en adultos” son aplicables a pacientes con insuficiencia renal leve a moderada (aclaramiento de creatinina = 30-80 ml/min).
Como el aclaramiento de sildenafilo se reduce en pacientes con insuficiencia renal grave (aclaramiento de creatinina <30 ml/min) debería considerarse una dosis de 25 mg para estos pacientes. En base a la eficacia y tolerabilidad, se puede incrementar gradualmente la dosis a 50 mg y hasta 100 mg según sea necesario.
Insuficiencia hepática
Como el aclaramiento de sildenafilo se reduce en pacientes con insuficiencia hepática (por ejemplo, cirrosis) debería considerarse una dosis de 25 mg para estos pacientes. En base a la eficacia y tolerabilidad, se puede incrementar gradualmente la dosis a 50 mg y hasta 100 mg según sea necesario.
Población pediátrica
Vizarsin no está indicado en menores de 18 años de edad.
Uso en pacientes en tratamiento con otros medicamentos:
A excepción de ritonavir, en que su administración concomitante con sildenafilo no se aconseja (ver sección 4.4), una dosis inicial de 25 mg debe considerarse en aquellos pacientes que reciben tratamiento concomitante con inhibidores del CYP3A4 (ver sección 4.5).
Con el fin de minimizar la potencial aparición de hipotensión postural, en pacientes que reciban tratamiento con alfabloqueantes, los pacientes deberán encontrarse estables bajo este tratamiento antes de iniciar la administración de sildenafilo. Asimismo, se deberá valorar el inicio del tratamiento con sildenafilo a una dosis de 25 mg (ver secciones 4.4 y 4.5).
Forma de administración
Administración por vía oral.
4.3 Contraindicaciones
Hipersensibilidad al principio activo o a alguno de los excipientes incluidos en la sección 6.1.
De acuerdo con sus conocidos efectos sobre la vía óxido nítrico/guanosina monofosfato cíclica (GMPc) (ver sección 5.1), sildenafilo ha demostrado potenciar los efectos hipotensores de los nitratos, estando contraindicada la administración concomitante de sildenafilo con los dadores de óxido nítrico (tales como nitrito de amilo) o nitratos en cualquiera de sus formas.
La administración conjunta de inhibidores de la PDE5, incluyendo sildenafilo, con estimuladores de la guanilato-ciclasa, como riociguat, está contraindicado ya que puede producir hipotensión sintomática de forma potencial (ver sección 4.5).
No se deben utilizar medicamentos para el tratamiento de la disfunción eréctil, incluyendo sildenafilo, en hombres a los que la actividad sexual esté desaconsejada (por ejemplo: pacientes con disfunciones cardiovasculares graves tales como angina inestable o insuficiencia cardíaca grave).
Vizarsin está contraindicado en pacientes que han perdido la visión en un ojo debido a neuropatía
óptica isquémica anterior no arterítica (NOIA-NA), independientemente de si este episodio se asoció o no con la exposición previa a un inhibidor de la PDE5 (ver sección 4.4).
La seguridad de sildenafilo no ha sido estudiada en los siguientes subgrupos de pacientes y, por lo tanto, su uso está contraindicado en estos pacientes: insuficiencia hepática grave, hipotensión (tensión arterial <90/50 mmHg), historia reciente de accidente isquémico cerebral o infarto de miocardio y trastornos hereditarios degenerativos de la retina conocidos tales como retinitis pigmentosa (una minoría de estos pacientes tienen trastornos genéticos de las fosfodiesterasas de la retina).
4.4 Advertencias y precauciones especiales de empleo
Es recomendable realizar una historia clínica y exploración física del paciente, para diagnosticar la disfunción eréctil y determinar las causas potenciales subyacentes, antes de considerar el tratamiento farmacológico.
Factores de riesgo cardiovascular
Antes de iniciar cualquier tratamiento de la disfunción eréctil, el médico debería considerar el estado cardiovascular de sus pacientes, ya que existe algún riesgo cardíaco asociado con la actividad sexual. Sildenafilo tiene propiedades vasodilatadoras, resultando en una disminución leve y transitoria de la tensión arterial (ver sección 5.1). Antes de prescribir sildenafilo, el médico deberá considerar cuidadosamente si sus pacientes con ciertas patologías subyacentes podrían verse afectados de forma adversa por tales efectos vasodilatadores, especialmente combinados con la actividad sexual. Los pacientes con una mayor susceptibilidad a vasodilatadores incluyen aquellos con obstrucción del flujo ventricular izquierdo (por ejemplo: estenosis aórtica, miocardiopatía hipertrófica obstructiva) o aquellos con el infrecuente síndrome de atrofia sistémica múltiple que se caracteriza por una insuficiencia grave del control autónomo de la presión sanguínea.
Sildenafilo potencia el efecto hipotensor de los nitratos (ver sección 4.3).
Durante la comercialización de sidenafilo, se han notificado acontecimientos cardiovasculares graves, incluyendo infarto de miocardio, angina inestable, muerte cardíaca súbita, arritmia ventricular, hemorragia cerebrovascular, ataque isquémico transitorio, hipertensión e hipotensión, en asociación temporal con el uso de Vizarsin. La mayoría de estos pacientes, aunque no todos, presentabanfactores de riesgo cardiovasculares anteriores. Se ha notificado que muchos acontecimientos tuvieron lugar durante o poco tiempo después de la relación sexual y unos pocos sucedieron poco después del uso de Vizarsin sin actividad sexual. No es posible determinar si estos acontecimientos están directamente relacionados con estos factores o con otros factores.
Priapismo
Los medicamentos para el tratamiento de la disfunción eréctil, incluyendo sildenafilo, se deben utilizar con precaución en pacientes con deformaciones anatómicas del pene (tales como angulación, fibrosis cavernosa o enfermedad de Peyronie), o en pacientes con afecciones que puedan predisponer a priapismo (tales como anemia de células falciformes, mieloma múltiple o leucemia).
En la experiencia postcomercialización se han notificado erecciones prolongadas y priapismo con sildenafilo. En caso de una erección que se prolongue más de 4 horas, el paciente debe buscar atención médica inmediatamente. Si el priapismo no se trata de inmediato, podrían producirse daño tisular del pene y pérdida permanente de la potencia.
Uso concomitante con otros inhibidores de la PDE5 u otros tratamientos para la disfunción eréctil
No se han estudiado la seguridad y eficacia de la asociación de sildenafilo con otros inhibidores de la PDE5, otros tratamientos de la hipertensión arterial pulmonar (HAP) que contienen sildenafilo, u otros tratamientos para la disfunción eréctil. Por lo tanto, no se recomienda el uso de tales asociaciones.
Efectos sobre la visión
De forma espontánea, se han notificado casos de defectos visuales en asociación con la toma de sildenafilo y de otros inhibidores de la PDE5 (ver sección 4.8). De forma espontánea y en un estudio observacional, se han notificado casos de neuropatía óptica isquémica anterior no arterítica, una enfermedad rara, en asociación con la toma de sildenafilo y de otros inhibidores de la PDE5 (ver sección 4.8). Debe advertirse a los pacientes que en el caso de cualquier defecto visual repentino, dejen de tomar Vizarsin y consulten inmediatamente con un médico (ver sección 4.3).
Uso concomitante con ritonavir
No se recomienda la administración simultánea de sildenafilo con ritonavir (ver sección 4.5).
Uso concomitante con alfabloqueantes
Se recomienda tener precaución cuando se administre sildenafilo a pacientes en tratamiento con un alfabloqueante, ya que la administración simultánea de ambos fármacos puede producir hipotensión sintomática en un pequeño número de pacientes más susceptibles de padecerla (ver sección 4.5). Ésta es más probable que ocurra en las 4 horas posteriores a la toma de sildenafilo. Con el fin de minimizar la potencial aparición de hipotensión postural, los pacientes que reciban tratamiento con alfabloqueantes deberán encontrarse hemodinámicamente estables bajo el tratamiento con alfabloqueantes antes de iniciar la administración de sildenafilo. Por otro lado, se deberá valorar iniciar el tratamiento con sildenafilo a una dosis de 25 mg (ver sección 4.2). Asimismo, los médicos deben informar a sus pacientes de qué medidas adoptar en caso de experimentar síntomas de hipotensión postural.
Efectos sobre las hemorragias
Estudios con plaquetas humanas indican que sildenafilo potencia el efecto antiagregante del nitroprusiato sódico in vitro. No existen datos de seguridad sobre la administración de sildenafilo a pacientes con trastornos hemorrágicos o con úlcera péptica activa. Por lo tanto, sildenafilo se debe administrar a estos pacientes sólo tras la evaluación del beneficio-riesgo.
Uso en mujeres
El uso de Vizarsin no está indicado en mujeres.
Excipientes
Vizarsin contiene lactosa. Los pacientes con intolerancia hereditaria a galactosa, con insuficiencia de lactasa de Lapp o con problemas de absorción de glucosa o galactosa, no deben tomar este medicamento.
4.5 Interacción con otros medicamentos y otras formas de interacción
Efectos de otros medicamentos sobre sildenafilo Estudios in vitro
El metabolismo de sildenafilo está mediado predominantemente por el citocromo P450 (CYP) isoformas 3A4 (principalmente) y 2C9 (en menor medida). Por lo tanto, los inhibidores de estas isoenzimas pueden reducir el aclaramiento de sildenafilo y los inductores de estas isoenzimas pueden incrementar el aclaramiento de sildenafilo.
Estudios in vivo
El análisis de los datos farmacocinéticos de los ensayos clínicos, mostró que se produjo una reducción del aclaramiento de sildenafilo cuando se administró concomitantemente con inhibidores del CYP3A4 (tales como ketoconazol, eritromicina, cimetidina). Aunque no se observó aumento de la incidencia de acontecimientos adversos en estos pacientes, cuando sildenafilo se administra concomitantemente con los inhibidores del CYP3A4, se debería considerar una dosis inicial de 25 mg.
La administración conjunta de ritonavir, inhibidor de la proteasa del VIH, el cual presenta una potente acción inhibitoria sobre el citocromo P450, en el estado de equilibrio (500 mg dos veces al día) junto con sildenafilo (dosis única de 100 mg) produjo un aumento del 300% (4 veces superior) en la Cmax de sildenafilo y del 1.000% (11 veces superior) en la AUC plasmática de sildenafilo. A las 24 horas, los niveles plasmáticos de sildenafilo eran todavía aproximadamente 200 ng/ml, en comparación con los aproximadamente 5 ng/ml cuando se administra sólo sildenafilo. Este hecho está en concordancia con los efectos evidentes de ritonavir sobre un gran número de sustratos del citocromo P450. Sildenafilo no presentó ningún efecto sobre la farmacocinética de ritonavir. En base a estos resultados farmacocinéticos, no se aconseja la administración concomitante del sildenafilo con ritonavir (ver sección 4.4) y en ninguna circunstancia la dosis máxima de sildenafilo debe exceder de 25 mg en 48 horas.
La administración conjunta de saquinavir, inhibidor de la proteasa del VIH, que también presenta una acción inhibitoria sobre el citocromo CYP3A4, en el estado de equilibrio (1.200 mg tres veces al día), con sildenafilo (dosis única de 100 mg) produjo un aumento del 140% en la Cmax de sildenafilo y del 210% en la AUC de sildenafilo. Sildenafilo no presentó ningún efecto sobre la farmacocinética de saquinavir (ver sección 4.2). Cabría esperar efectos más intensos con inhibidores más potentes del citocromo CYP 3A4, tales como ketoconazol e itraconazol.
Cuando se administró una dosis única de 100 mg de sildenafilo con eritromicina, un inhibidor moderado del CYP3A4, hubo un incremento del 182% en la exposición sistémica de sildenafilo (AUC) cuando se alcanzó una concentración estable de eritromicina en plasma (500 mg, dos veces al día, durante 5 días). En voluntarios varones sanos, no se observó ninguna evidencia de un efecto con azitromicina (500 mg diarios durante 3 días) sobre el AUC, la Cmax, el tmax, la constante de velocidad de eliminación o la consiguiente semivida de sildenafilo o de su metabolito principal en sangre. Cimetidina (800 mg), un inhibidor del citocromo P450 e inhibidor no específico del CYP3A4, produjo un aumento del 56% de la concentración plasmática de sildenafilo cuando se administró simultáneamente con sildenafilo (50 mg) a voluntarios sanos.
El zumo de pomelo es un inhibidor débil del metabolismo del citocromo CYP3A4 localizado en la pared intestinal que puede provocar pequeños incrementos de los niveles plasmáticos de sildenafilo.
Dosis únicas de antiácido (hidróxido magnésico/hidróxido de aluminio) no afectaron la biodisponibilidad de sildenafilo.
Aunque no se han realizado estudios de interacción específica con todos los fármacos posibles, el análisis de los datos farmacocinéticos no mostró efecto alguno sobre la farmacocinética de sildenafilo cuando se administró concomitantemente con inhibidores del CYP2C9 (tales como tolbutamida, warfarina, fenitoína), inhibidores del CYP2D6 (tales como inhibidores selectivos de la recaptación de serotonina, antidepresivos tricíclicos), tiazidas y diuréticos relacionados (diuréticos de asa y ahorradores de potasio), inhibidores de la enzima conversora de angiotensina, antagonistas del calcio, antagonistas beta-adrenérgicos o inductores del metabolismo del CYP450 (tales como rifampicina, barbitúricos). En un estudio con voluntarios varones sanos, la administración concomitante del antagonista de los receptores de endotelina, bosentan, (un inductor del CYP3A4 [moderado], del CYP2C9 y posiblemente del CYP2C19) en estado de equilibrio (125 mg dos veces al día) con sildenafilo en estado de equilibrio (80 mg tres veces al día) resultó en una disminución de 62,6% y 55,4% del AUC y Cmax de sildenafilo, respectivamente. Por lo tanto, se espera que la administración concomitante de inductores potentes de CYP3A4, como rifampina, causen mayores disminuciones de la concentración plasmática de sildenafilo.
Nicorandil es un híbrido entre un activador de los canales de potasio y un nitrato. Debido a su componente nitrato, tiene el potencial de provocar una interacción grave con sildenafilo.
Efectos de sildenafilo sobre otros medicamentos
Sildenafilo es un inhibidor débil del citocromo P450 isoformas 1A2, 2C9, 2C19, 2D6, 2E1 y 3A4 (IC50 > 150 ^M). Dado que las concentraciones plasmáticas máximas de sildenafilo, tras las dosis recomendadas, son de aproximadamente 1 ^M, no es probable que Vizarsin altere el aclaramiento de los substratos de estas isoenzimas.
No se dispone de datos de interacción de sildenafilo e inhibidores no específicos de la fosfodiesterasa, tales como teofilina o dipiridamol.
Estudios in vivo
De acuerdo con sus efectos conocidos sobre la vía óxido nítrico/GMPc (ver sección 5.1), sildenafilo demostró potenciar los efectos hipotensores de los nitratos. Por lo tanto, su administración concomitante con los dadores del óxido nítrico o nitratos está contraindicada (ver sección 4.3).
Riociguat
Estudios preclínicos mostraron un efecto aditivo de la disminución de la presión arterial sistémica cuando se combinaron inhibidores de la PDE5 con riociguat. Riociguat ha mostrado en ensayos clínicos que aumenta los efectos hipotensores de los inhibidores de la PDE5. En la población estudiada no hubo indicios de un efecto clínico favorable de dicha combinación. El uso concomitante de riociguat con inhibidores de la PDE5, incluyendo sildenafilo, está contraindicado (ver sección 4.3).
La administración concomitante de sildenafilo a pacientes en tratamiento con alfabloqueantes puede producir hipotensión sintomática en un pequeño número de pacientes que puede ser más susceptible de padecerla. Ésta es más probable que ocurra en las 4 horas posteriores a la toma de sildenafilo (ver secciones 4.2 y 4.4). En tres estudios específicos de interacción farmacológica, se administraron simultáneamente el alfabloqueante doxazosina (4 mg y 8 mg) y sildenafilo (25 mg, 50 mg o 100 mg) a pacientes con hiperplasia benigna de próstata (HBP) y que se encontraban ya estables en el tratamiento con doxazosina. En estas poblaciones objeto de estudio, se observaron unas reducciones medias adicionales de la presión arterial en decúbito supino de 7/7 mmHg, de 9/5 mmHg y de 8/4 mmHg, y unas reducciones medias adicionales de la presión arterial en bipedestación de 6/6 mmHg, de 11/4 mmHg y de 4/5 mmHg, respectivamente. Cuando sildenafilo y doxazosina fueron administrados simultáneamente a pacientes estables en el tratamiento con doxazosina, los casos notificados de pacientes que experimentaron hipotensión postural sintomática fueron poco frecuentes. Estos casos incluyeron mareos o sensación de vahído, pero no síncope.
No se han observado interacciones significativas cuando se administró sildenafilo (50 mg) concomitantemente con tolbutamida (250 mg) o warfarina (40 mg), metabolizándose ambos por el CYP2C9.
Sildenafilo (50 mg) no potenció el aumento del tiempo de hemorragia causado por ácido acetilsalicílico (150 mg).
Sildenafilo (50 mg) no potenció los efectos hipotensores del alcohol en voluntarios sanos con niveles máximos medios de alcohol en sangre de 80 mg/dl.
El análisis de todos los datos obtenidos de los siguientes tipos de fármacos antihipertensivos: diuréticos, beta bloqueantes, inhibidores de la ECA, antagonistas de la angiotensina II, fármacos antihipertensivos (vasodilatadores y de acción central), bloqueantes de las neuronas adrenérgicas, calcio antagonistas y bloqueantes alfa-adrenérgicos, mostró que no existen diferencias en el perfil de efectos secundarios en pacientes a los que se administró sildenafilo, en comparación con el tratamiento con placebo. En un estudio de interacción específico, cuando sildenafilo (100 mg) se administró concomitantemente con amlodipino a pacientes hipertensos, la reducción media adicional en la tensión arterial sistólica en posición supina fue de 8 mmHg. La reducción adicional correspondiente de la tensión arterial diastólica en posición supina fue de 7 mmHg. Estas reducciones adicionales en la tensión arterial fueron de una magnitud similar a aquellas observadas cuando se administró sildenafilo como único fármaco a voluntarios sanos (ver sección 5.1).
Sildenafilo (100 mg) no afectó a la farmacocinética del estado de equilibrio de los inhibidores de la proteasa del VIH, saquinavir y ritonavir, los cuales son sustratos del citocromo CYP3A4.
En voluntarios varones sanos, la administración de sildenafilo en estado de equilibrio (80 mg tres veces al día) resultó en un incremento de 49,8% del AUC de bosentan y un incremento de 42% de la Cmax de bosentan (125 mg dos veces al día).
4.6 Fertilidad, embarazo y lactancia
El uso de Vizarsin no está indicado en mujeres.
No se han realizado estudios adecuados y bien controlados en mujeres embarazadas o en periodo de lactancia.
Tras la administración oral de sildenafilo no se observaron efectos adversos relevantes en los estudios de reproducción realizados en ratas y conejos.
No hubo efectos sobre la movilidad ni la morfología de los espermatozoides de voluntarios sanos tras administrarles una sola dosis de 100 mg de sildenafilo por vía oral (ver sección 5.1).
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
No se han realizado estudios sobre la capacidad para conducir y utilizar máquinas.
En los estudios clínicos con sildenafilo se notificaron mareos y trastornos visuales, por lo tanto, los pacientes deben saber cómo reaccionan a Vizarsin antes de conducir vehículos o utilizar máquinas.
4.8 Reacciones adversas
Resumen del perfil de seguridad
El perfil de seguridad de Vizarsin se basa en 9.570 pacientes de 74 ensayos clínicos doble ciego, controlados con placebo. Las reacciones adversas más frecuentemente notificadas en los ensayos clínicos entre los pacientes tratados con sildenafilo fueron dolor de cabeza, rubefacción, dispepsia, congestión nasal, mareo, náuseas, acaloramiento, deterioro visual, cianopsia y visión borrosa.
Las reacciones adversas notificadas durante la experiencia postcomercialización se han recogido cubriendo un período estimado superior a 10 años. Dado que no todas las reacciones adversas se han notificado al titular de la autorización de comercialización e incluido en la base de datos de seguridad, las frecuencias de estas reacciones adversas no pueden determinarse de modo fiable.
Tabla de reacciones adversas
En la tabla de abajo aparecen todas las reacciones adversas clínicamente importantes, que ocurrieron en los ensayos clínicos con una incidencia superior al placebo, listadas según la clasificación por órganos y sistemas muy frecuentes (> 1/10), frecuentes (> 1/100 a < 1/10), poco frecuentes (> 1/1.000 a < 1/100), raras (> 1/10.000 a < 1/1.000), muy raras (< 1/10.000).
Las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada intervalo de frecuencia.
Tabla 1: Reacciones adversas clínicamente importantes notificadas con una incidencia superior a placebo en ensayos clínicos controlados y reacciones adversas clínicamente importantes notificadas a partir de la experiencia postcomercialización.
|
Clasificación por órganos y sistemas |
Muy frecuentes (> 1/10) |
Frecuentes (> 1/100 y <1/10) |
Poco frecuentes (>1/1.000 y <1/100) |
Raras (> 1/10.000 y <1/1.000) |
|
Infecciones e infestaciones |
Rinitis | |||
|
Trastornos del sistema inmunológico |
Hipersensibilidad | |||
|
Trastornos del sistema nervioso |
Cefalea |
Mareo |
Somnolencia, Hipoestesia |
Accidente cerebrovascular, ataque isquémico transitorio, convulsiones , convulsiones recurrentes , síncope |
|
Trastornos oculares |
Distorsión visual de los colores**, deterioro visual, visión borrosa |
Trastornos del lagrimeo***, dolor ocular, fotofobia, fotopsia, hiperemia ocular, claridad visual, conjuntivitis |
Neuropatía óptica isquémica anterior no arterítica (NOIA-NA)*, oclusión vascular retiniana*, hemorragia retiniana, retinopatía arterioesclerótica, trastorno retiniano, glaucoma, defectos del campo visual, diplopía, agudeza visual disminuida, miopía, astenopía, células flotantes en el vítreo, trastorno del iris, midriasis, halo visual, edema del ojo, hinchazón ocular, trastorno del ojo, hiperemia de la conjuntiva, irritación ocular, sensación anormal en el ojo, edema palpebral, cambio de color de la esclerótida | |
|
Trastornos del oído y del laberinto |
Vértigo, acúfenos |
Sordera | ||
|
Trastornos cardiacos |
Taquicardia, palpitaciones |
Muerte cardiaca súbita*, infarto de miocardio, arritmia ventricular , fibrilación auricular, angina inestable | ||
|
Trastornos vasculares |
Rubefacción, acaloramiento |
Hipertensión, hipotensión |
|
Clasificación por órganos y sistemas |
Muy frecuentes (> 1/10) |
Frecuentes (> 1/100 y <1/10) |
Poco frecuentes (>1/1.000 y <1/100) |
Raras (> 1/10.000 y <1/1.000) |
|
Trastornos respiratorios, torácicos y mediastínicos |
Congestión nasal |
Epistaxis, congestión sinusal |
Sensación de opresión en la garganta, edema nasal, sequedad nasal | |
|
Trastornos gastrointestinales |
Náuseas, dispepsia |
Enfermedad por reflujo gastroesofágico, vómitos, dolor en la zona superior del abdomen, boca seca |
Hipoestesia oral | |
|
Trastornos de la piel y del tejido subcutáneo |
Erupción |
Síndrome de Stevens-Johnson (SSJ)*, necrólisis epidérmica tóxica (NET)* | ||
|
Trastornos musculoesqueléticos y del tejido subcutáneo |
Mialgia, dolor en una extremidad | |||
|
Trastornos renales y urinarios |
Hematuria | |||
|
Trastornos del aparato reproductor y de la mama |
Hemorragia peneana priapismo , hematospermia, erección aumentada | |||
|
Trastornos generales y alteraciones en el lugar de administración |
Dolor torácico, fatiga, sensación de calor |
Irritabilidad | ||
|
Exploraciones complementarias |
Frecuencia cardiaca aumentada |
*Notificado únicamente durante la experiencia postcomercialización
**Distorsión visual de los colores: cloropsia, cromatopsia, cianopsia, eritropsia y xantopsia
***Trastornos del lagrimeo: ojo seco, trastorno lagrimal, lagrimeo aumentado
Notificación de sospechas de reacciones adversas
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del sistema nacional de notificación incluido en el Apéndice V.
4.9 Sobredosis
Síntomas
En estudios realizados en voluntarios sanos con dosis únicas de hasta 800 mg, las reacciones adversas fueron similares a las observadas con dosis más bajas, pero la incidencia y gravedad aumentó. Dosis de 200 mg no incrementaron la eficacia pero sí la incidencia de reacciones adversas (cefalea, enrojecimiento, mareos, dispepsia, congestión nasal y trastornos visuales).
Tratamiento
En caso de sobredosis, se deben tomar medidas normales de apoyo. Dado que sildenafilo se une intensamente a proteínas plasmáticas y no se elimina por orina, no se espera que la diálisis renal acelere el aclaramiento del fármaco.
5. PROPIEDADES FARMACOLÓGICAS
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: Urológicos, fármacos utilizados en disfunción eréctil, código ATC: G04BE03.
Mecanismo de acción
Sildenafilo es una terapia de administración oral para el tratamiento de la disfunción eréctil. En condiciones normales, es decir, con estimulación sexual, restaura la función eréctil deteriorada mediante el aumento del flujo sanguíneo al pene.
El mecanismo fisiológico responsable de la erección del pene implica la liberación de óxido nítrico (ON) en los cuerpos cavernosos durante la estimulación sexual. El óxido nítrico activa la enzima guanilatociclasa, lo que da lugar a un aumento de los niveles de guanosina monofosfato cíclica (GMPc), que produce una relajación del músculo liso en los cuerpos cavernosos del pene, permitiendo la afluencia de sangre y subsiguiente llenado de los mismos.
Sildenafilo es un inhibidor potente y selectivo de la fosfodiesterasa tipo 5 (PDE5) específica GMPc de los cuerpos cavernosos, donde la PDE5 es la responsable de la degradación del GMPc. Sildenafilo actúa a nivel periférico sobre la erección. Sildenafilo no tiene un efecto relajante directo sobre los cuerpos cavernosos humanos aislados, pero aumenta potentemente el efecto relajante del ON en este tejido. Cuando se encuentra activada la vía ON/GMPc, como ocurre durante la estimulación sexual, la inhibición de la PDE5 por sildenafilo ocasiona un aumento de los niveles de GMPc en los cuerpos cavernosos. Por lo tanto es necesario estimulación sexual para que sildenafilo produzca sus efectos farmacológicos beneficiosos previstos.
Efectos farmacodinámicos
Los estudios in vitro han mostrado que sildenafilo es selectivo de la PDE5, implicada en el proceso de erección. Su efecto es más potente sobre la PDE5 que sobre otras fosfodiesterasas conocidas. Tiene una selectividad 10 veces mayor que por la PDE6, que participa en el mecanismo de fototransducción en la retina. A las dosis máximas recomendadas, tiene una selectividad 80 veces superior por la PDE1 y 700 veces superior por la PDE2, 3, 4, 7, 8, 9, 10 y 11. Particularmente, sildenafilo es 4.000 veces más selectivo por la PDE5 que por la PDE3, la isoforma fosfodiesterasa específica AMPc relacionada con el control de la contractilidad cardíaca.
Eficacia clínica y seguridad
Dos estudios clínicos fueron específicamente diseñados para evaluar la ventana durante la cual sildenafilo podría producir una erección en respuesta a la estimulación sexual. En un estudio utilizando plestismografia peneana (RigiScan) con pacientes en ayunas, el tiempo mediano de inicio de una erección con rigidez superior al 60% (suficiente para el acto sexual) fue de 25 minutos (rango de 12-37 minutos) tras la administración de sildenafilo. En otro estudio utilizando también RigiScan, sildenafilo, a las 4-5 horas de ser administrado, aún fue capaz de producir una erección en respuesta a la estimulación.
Sildenafilo causa una disminución leve y transitoria en la tensión arterial que, en la mayoría de los casos, no se traduce en efectos clínicos. La disminución máxima media de la tensión arterial sistólica, en posición supina, tras una dosis oral de 100 mg de sildenafilo, fue de 8,4 mmHg y de 5,5 mmHg en la tensión arterial diastólica. Estas disminuciones en la tensión arterial concuerdan con los efectos vasodilatadores de sildenafilo, probablemente debido al aumento en los niveles de GMPc en la musculatura lisa vascular. Dosis únicas orales de sildenafilo de hasta 100 mg en voluntarios sanos no produjeron efectos clínicamente relevantes sobre el ECG.
En un estudio sobre los efectos hemodinámicos de una dosis única de 100 mg de sildenafilo administrada por vía oral en 14 pacientes con enfermedad coronaria obstructiva grave (estenosis >70% de al menos una arteria coronaria), la presión arterial sistólica y diastólica media en reposo disminuyeron alrededor del 7% y 6%, respectivamente, en comparación a los datos basales. La presión arterial sistólica pulmonar media disminuyó un 9%. Sildenafilo no presentó efectos sobre el rendimiento cardíaco, y no afectó al flujo sanguíneo en arterias coronarias estenosadas.
En un estudio de prueba de esfuerzo, doble ciego, controlado con placebo, se evaluó a 144 pacientes con disfunción eréctil y angina estable crónica que estaban tomando medicamentos antianginosos regularmente (excepto nitratos). Los resultados demostraron que no hubo diferencias clínicamente relevantes en el tiempo necesario para desencadenar la aparición de una angina con el uso de sildenafilo en comparación con placebo.
En algunos pacientes, se han detectado diferencias leves y transitorias en la discriminación del color (azul/verde), cuando se utilizó la prueba de tinción Farnsworth-Munsell 100, una hora después de administrar una dosis de 100 mg, sin que se produjeran efectos evidentes a las dos horas de la administración. El mecanismo postulado para este cambio en la discriminación de color se relaciona con la inhibición de la PDE6, que participa en la cascada de fototransducción de la retina. Sildenafilo no tiene efectos sobre la agudeza visual o sensibilidad al contraste. En un estudio controlado con placebo de pequeño tamaño en pacientes con degeneración macular temprana documentada (n=9), se demostró que sildenafilo (dosis única, 100 mg) no produjo cambios significativos en las pruebas visuales realizadas (agudeza visual, test de Amsler, discriminación de los colores de un semáforo simulado, perímetro de Humphrey y fotoestrés).
No hubo ningún efecto sobre la motilidad o la morfología de esperma tras la administración oral de dosis únicas de 100 mg de sildenafilo en voluntarios sanos (ver sección 4.6).
Información adicional sobre ensayos clínicos:
En los ensayos clínicos sildenafilo se administró a más de 8.000 pacientes en edades comprendidas entre los 19 y 87 años. Los siguientes grupos de pacientes estuvieron representados: ancianos (19,9%), pacientes con hipertensión (30,9%), diabetes mellitus (20,3%), enfermedades cardíacas isquémicas (5,8%), hiperlipidemia (19,8%), lesión medular (0,6%), depresión (5,2%), resección transuretral de la próstata (3,7%), prostatectomía radical (3,3%). Los siguientes grupos, no estuvieron bien representados o se excluyeron de los ensayos clínicos: pacientes con cirugía de pelvis, pacientes que han sido sometidos a radioterapia, pacientes con disfunción renal o hepática grave y pacientes con ciertos trastornos cardiovasculares (ver sección 4.3).
En los estudios de dosis fijas, la proporción de pacientes que reconoció que el tratamiento mejoró sus erecciones fue del 62% (25 mg), 74% (50 mg) y 82% (100 mg) en comparación a un 25% con placebo. En ensayos clínicos controlados, la proporción de abandonos atribuibles a sildenafilo fue baja y similar a placebo.
Considerando todos los estudios clínicos, la proporción de pacientes que informaron de mejoría con sildenafilo fue la siguiente: disfunción eréctil psicógena (84%), disfunción eréctil mixta (77%), disfunción eréctil orgánica (68%), ancianos (67%), diabetes mellitus (59%), enfermedad cardíaca isquémica (69%), hipertensión (68%), resección transuretral de la próstata (RTUP) (61%), prostatectomía radical (43%), lesión medular (83%), depresión (75%). La seguridad y eficacia de
sildenafilo se mantuvo en los estudios a largo plazo.
5.2 Propiedades farmacocinéticas
Absorción
Sildenafilo se absorbe rápidamente. Tras la administración oral, en estado de ayuno, se observan concentraciones plasmáticas máximas entre 30 y 120 minutos (media de 60 minutos) post-dosis. La biodisponibilidad oral absoluta media es del 41% (rango del 25 al 63%). Tras la administración oral de sildenafilo el AUC y Cmax aumentaron en proporción a la dosis en el rango de dosis recomendado (25-100 mg).
Cuando sildenafilo se administra con alimentos, la velocidad de absorción disminuye con un retraso medio en la tmax de 60 minutos y una reducción media en la Cmax del 29%.
Distribución
El volumen medio de distribución (Vd) en estado de equilibrio para sildenafilo es de 105 l, indicando una distribución tisular del fármaco. Tras la administración de una dosis única de 100 mg, la concentración plasmática máxima total media de sildenafilo es aproximadamente 440 ng/ml (CV 40%). Dado que sildenafilo (y su metabolito principal circulante N-desmetilo) se encuentra unido a proteínas plasmáticas en un 96%,, esto da como resultado una concentración plasmática libre media de sildenafilo de 18 ng/ml (38 nM). La unión a proteínas es independiente de las concentraciones totales de ambos compuestos.
En el eyaculado de voluntarios sanos que recibían sildenafilo (100 mg como dosis única), se detectó menos del 0,0002% (promedio 188 ng) de la dosis administrada, 90 minutos después de la dosificación.
Biotransformación
Sildenafilo se metaboliza predominantemente por las isoenzimas microsomales hepáticas CYP3A4 (principalmente) y CYP2C9 (en menor medida). El metabolito principal circulante resulta de la N-desmetilación de sildenafilo. Este metabolito tiene un perfil de selectividad por las fosfodiesterasas similar a sildenafilo y la potencia in vitro por PDE5 es de aproximadamente el 50% de la del principio activo original. Las concentraciones plasmáticas de este metabolito son aproximadamente el 40% de las observadas para sildenafilo. El metabolito N-desmetilo continúa metabolizándose, con una vida media terminal de aproximadamente 4 horas.
Eliminación
El aclaramiento total de sildenafilo es de 41 l/hora, con una fase terminal resultante en una vida media de 3-5 horas. Tras la administración oral o intravenosa, sildenafilo se excreta en forma de metabolitos predominantemente en heces (aproximadamente el 80% de la dosis oral administrada) y en menor medida en orina (aproximadamente el 13% de la dosis oral administrada).
Farmacocinética en grupos especiales de pacientes
Personas de edad avanzada:
Sildenafilo mostró un aclaramiento reducido en voluntarios sanos de edad avanzada (más de 65 años), siendo las concentraciones plasmáticas de sildenafilo y de su metabolito activo N-desmetilo un 90% más altas que las observadas en voluntarios sanos jóvenes (18-45 años). La concentración de sildenafilo libre en el plasma fue aproximadamente el 40% mayor, debido al efecto que el envejecimiento ejerce sobre la unión a las proteínas plasmáticas.
Insuficiencia renal:
En voluntarios con insuficiencia renal leve a moderada (aclaramiento de creatinina = 30-80 ml/min), no se alteró la farmacocinética de sildenafilo después de recibir una única dosis oral de 50 mg. El AUC y Cmax medios del metabolito N-desmetilo aumentaron hasta el 126% y hasta el 73% respectivamente, en comparación a voluntarios de la misma edad sin insuficiencia renal. Sin embargo, debido a la elevada variabilidad entre personas, estas diferencias no fueron estadísticamente significativas. En voluntarios con insuficiencia renal grave (aclaramiento de creatinina < 30 ml/min), se redujo el aclaramiento de sildenafilo, con un aumento del AUC y Cmax del 100% y del 88% respectivamente, en comparación a los voluntarios de la misma edad sin insuficiencia renal. Además, los valores de AUC y Cmax para el metabolito N-desmetilo aumentaron significativamente, 200% y 79%, respectivamente.
Insuficiencia hepática:
En voluntarios con cirrosis hepática de leve a moderada (Child-Pugh A y B), el aclaramiento de sildenafilo se redujo, resultando en aumentos del AUC (84%) y Cmax (47%) en comparación con voluntarios de la misma edad sin insuficiencia hepática. La farmacocinética de sildenafilo en pacientes con insuficiencia hepática grave no ha sido estudiada.
5.3 Datos preclínicos sobre seguridad
Los datos de los estudios no clínicos no muestran riesgos especiales para los seres humanos, según los estudios convencionales de farmacología de seguridad, toxicidad a dosis repetidas, genotoxicidad, potencial carcinogénico, toxicidad para la reproducción y el desarrollo.
6. DATOS FARMACÉUTICOS
6.1 Lista de excipientes
Núcleo del comprimido:
Celulosa microcristalina (E460)
Fosfato cálcico hidrogenado anhidro Croscarmelosa sódica Hipromelosa (E464)
Estearato magnésico (E572)
Cubierta pelicular:
Lactosa monohidrato Hipromelosa (E464)
Dióxido de titanio (E171)
Triacetina (E1518)
6.2 Incompatibilidades
No procede.
6.3 Periodo de validez
5 años
6.4 Precauciones especiales de conservación
Este medicamento no requiere condiciones especiales de conservación.
6.5 Naturaleza y contenido del envase
Blíster (lámina PVC/lámina Al): 1 comprimido recubierto con película, en una caja.
Blísters (blíster perforado unidosis, lámina PVC/lámina Al): 4x 1, 8 x 1 o 12 x 1 comprimido recubierto con película, en una caja.
Puede que solamente estén comercializados algunos tamaños de envases.
6.6 Precauciones especiales de eliminación
Ninguna especial.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA, d.d., Novo mesto, Smarjeska cesta 6, 8501 Novo mesto, Eslovenia
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
Vizarsin 25 mg comprimidos recubiertos con película 1 comprimido recubierto con película: EU/1/09/551/001 4 x 1 comprimido recubierto con película: EU/1/09/551/002 8 x 1 comprimidosrecubierto con película: EU/1/09/551/003 12 x 1 comprimido recubierto con película: EU/1/09/551/004
Vizarsin 50 mg comprimidos recubiertos con película 1 comprimido recubierto con película: EU/1/09/551/005 4 x 1 comprimido recubierto con película: EU/1/09/551/006 8 x 1 comprimidosrecubierto con película: EU/1/09/551/007 12 x 1 comprimido recubierto con película: EU/1/09/551/008
Vizarsin 100 mg comprimidos recubiertos con película 1 comprimido recubierto con película: EU/1/09/551/009 4 x 1 comprimido recubierto con película: EU/1/09/551/010 8 x 1 comprimidosrecubierto con película: EU/1/09/551/011 12 x 1 comprimido recubierto con película: EU/1/09/551/012
9. FECHA DE LA PRIMERA AUTORIZACIÓN/RENOVACIÓN DE LA AUTORIZACIÓN
Fecha de la primera autorización: 21 de septiembre de 2009 Fecha de la última renovación: 16 de mayo de 2014
10. FECHA DE LA REVISIÓN DEL TEXTO
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos http://www.ema.europa.eu.
1. NOMBRE DEL MEDICAMENTO
Vizarsin 25 mg comprimidos bucodispersables Vizarsin 50 mg comprimidos bucodispersables Vizarsin 100 mg comprimidos bucodispersables
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada comprimido bucodispersable contiene 25 mg, 50 mg o 100 mg de sildenafilo.
Excipientes con efecto conocido:
Vizarsin 25 mg comprimidos bucodispersables
Cada comprimido bucodispersable contiene 0,375 mg de aspartamo (E951) y 0,00875 mg de sorbitol (E420).
Vizarsin 50 mg comprimidos bucodispersables
Cada comprimido bucodispersable contiene 0,75 mg de aspartamo (E951) y 0,0175 mg de sorbitol (E420).
Vizarsín 100 mg comprimidos bucodispersables
Cada comprimido bucodispersable contiene 1,5 mg de aspartamo (E951) y 0,035 mg de sorbitol (E420).
Para consultar la lista completa de excipientes, ver sección 6.1.
3. FORMA FARMACÉUTICA
Comprimido bucodispersable.
Vizarsin 25 mg comprimidos bucodispersables
Comprimidos blancos o blanquecinos, redondos, biconvexos y eventualmente con manchas más oscuras.
Vizarsin 50 mg comprimidos bucodispersables
Comprimidos blancos o blanquecinos, redondos, biconvexos y eventualmente con manchas más oscuras.
Vizarsín 100 mg comprimidos bucodispersables
Comprimidos blancos o blanquecinos, redondos, biconvexos y eventualmente con manchas más oscuras.
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
Vizarsin está indicado en hombres adultos con disfunción eréctil, que es la incapacidad para obtener o mantener una erección suficiente para una actividad sexual satisfactoria.
Para que Vizarsin sea efectivo es necesaria la estimulación sexual.
4.2 Posología y forma de administración Posología
Uso en adultos
La dosis recomendada es de 50 mg tomados a demanda, aproximadamente una hora antes de la actividad sexual. En base a la eficacia y tolerabilidad, la dosis se puede aumentar a 100 mg o disminuir a 25 mg. La dosis máxima recomendada es de 100 mg. La pauta máxima de dosificación recomendada es de una vez al día. Si se toma Vizarsin con alimentos, el inicio de su acción farmacológica podría retrasarse en comparación a cuando se toma en ayunas (ver sección 5.2).
Poblaciones especiales
Pacientes de edad avanzada
No se requiere ajuste de la dosis en pacientes de edad avanzada (pacientes con 65 años de edad o más).
Insuficiencia renal
Las dosis recomendadas descritas en “Uso en adultos” son aplicables a pacientes con insuficiencia renal leve a moderada (aclaramiento de creatinina = 30-80 ml/min).
Como el aclaramiento de sildenafilo se reduce en pacientes con insuficiencia renal grave (aclaramiento de creatinina <30 ml/min) debería considerarse una dosis de 25 mg para estos pacientes. En base a la eficacia y tolerabilidad, se puede incrementar gradualmente la dosis a 50 mg y hasta 100 mg según sea necesario.
Insuficiencia hepática
Como el aclaramiento de sildenafilo se reduce en pacientes con insuficiencia hepática (por ejemplo, cirrosis) debería considerarse una dosis de 25 mg para estos pacientes. En base a la eficacia y tolerabilidad, se puede incrementar gradualmente la dosis a 50 mg y hasta 100 mg según sea necesario.
Población pediátrica
Vizarsin no está indicado menores de 18 años de edad.
Uso en pacientes en tratamiento con otros medicamentos:
A excepción de ritonavir, en que su administración concomitante con sildenafilo no se aconseja (ver sección 4.4), una dosis inicial de 25 mg debe considerarse en aquellos pacientes que reciben tratamiento concomitante con inhibidores del CYP3A4 (ver sección 4.5).
Con el fin de minimizar la potencial aparición de hipotensión postural, en pacientes que reciban tratamiento con alfabloqueantes, los pacientes deberán encontrarse estables bajo este tratamiento antes de iniciar la administración de sildenafilo. Asimismo, se deberá valorar el inicio del tratamiento con sildenafilo a una dosis de 25 mg (ver secciones 4.4 y 4.5).
Forma de administración
Administración por vía oral.
Se debe colocar el comprimido bucodispersable sobre la lengua, donde se dispersará de manera rápida con la saliva para que pueda tragarse con facilidad. Puede tomarse con o sin líquido. Es complicado sacar íntegramente de la boca el comprimido bucodispersable. El comprimido bucodispersable es frágil, por lo que debe tomarse inmediatamente después de abrir el blíster.
Los pacientes que tengan dificultad para tragar los comprimidos recubiertos de película de Vizarsin pueden utilizar los comprimidos bucodispersables como alternativa.
4.3 Contraindicaciones
Hipersensibilidad al principio activo o a alguno de los excipientes incluidos en la sección 6.1.
De acuerdo con sus conocidos efectos sobre la vía óxido nítrico/guanosina monofosfato cíclica (GMPc) (ver sección 5.1), sildenafilo ha demostrado potenciar los efectos hipotensores de los nitratos, estando contraindicada la administración concomitante de sildenafilo con los dadores de óxido nítrico (tales como nitrito de amilo) o nitratos en cualquiera de sus formas.
La administración conjunta de inhibidores de la PDE5, incluyendo sildenafilo, con estimuladores de la guanilato-ciclasa, como riociguat, está contraindicado ya que puede producir hipotensión sintomática de forma potencial (ver sección 4.5).
No se deben utilizar medicamentos para el tratamiento de la disfunción eréctil, incluyendo sildenafilo, en hombres a los que la actividad sexual esté desaconsejada (por ejemplo: pacientes con disfunciones cardiovasculares graves tales como angina inestable o insuficiencia cardíaca grave).
Vizarsin está contraindicado en pacientes que han perdido la visión en un ojo debido a neuropatía óptica isquémica anterior no arterítica (NOIA-NA), independientemente de si este episodio se asoció o no con la exposición previa a un inhibidor de la PDE5 (ver sección 4.4).
La seguridad de sildenafilo no ha sido estudiada en los siguientes subgrupos de pacientes y, por lo tanto, su uso está contraindicado en estos pacientes: insuficiencia hepática grave, hipotensión (tensión arterial <90/50 mmHg), historia reciente de accidente isquémico cerebral o infarto de miocardio y trastornos hereditarios degenerativos de la retina conocidos tales como retinitis pigmentosa (una minoría de estos pacientes tienen trastornos genéticos de las fosfodiesterasas de la retina).
4.4 Advertencias y precauciones especiales de empleo
Es recomendable realizar una historia clínica y exploración física del paciente, para diagnosticar la disfunción eréctil y determinar las causas potenciales subyacentes, antes de considerar el tratamiento farmacológico.
Factores de riesgo cardiovascular
Antes de iniciar cualquier tratamiento de la disfunción eréctil, el médico debería considerar el estado cardiovascular de sus pacientes, ya que existe algún riesgo cardíaco asociado con la actividad sexual. Sildenafilo tiene propiedades vasodilatadoras, resultando en una disminución leve y transitoria de la tensión arterial (ver sección 5.1). Antes de prescribir sildenafilo, el médico deberá considerar cuidadosamente si sus pacientes con ciertas patologías subyacentes podrían verse afectados de forma adversa por tales efectos vasodilatadores, especialmente combinados con la actividad sexual. Los pacientes con una mayor susceptibilidad a vasodilatadores incluyen aquellos con obstrucción del flujo ventricular izquierdo (por ejemplo: estenosis aórtica, miocardiopatía hipertrófica obstructiva) o aquellos con el infrecuente síndrome de atrofia sistémica múltiple que se caracteriza por una insuficiencia grave del control autónomo de la presión sanguínea.
Sildenafilo potencia el efecto hipotensor de los nitratos (ver sección 4.3).
Durante la comercialización de sildenafilo, se han notificado acontecimientos cardiovasculares graves, incluyendo infarto de miocardio, angina inestable, muerte cardíaca súbita, arritmia ventricular, hemorragia cerebrovascular, ataque isquémico transitorio, hipertensión e hipotensión, en asociación temporal con el uso de Vizarsin. La mayoría de estos pacientes, aunque no todos, presentaban factores de riesgo cardiovasculares anteriores. Se ha notificado que muchos acontecimientos tuvieron lugar durante o poco tiempo después de la relación sexual y unos pocos sucedieron poco después del uso de Vizarsin sin actividad sexual. No es posible determinar si estos acontecimientos están directamente relacionados con estos factores o con otros factores.
Priapismo
Los medicamentos para el tratamiento de la disfunción eréctil, incluyendo sildenafilo, se deben utilizar con precaución en pacientes con deformaciones anatómicas del pene (tales como angulación, fibrosis cavernosa o enfermedad de Peyronie), o en pacientes con afecciones que puedan predisponer a priapismo (tales como anemia de células falciformes, mieloma múltiple o leucemia).
En la experiencia postcomercialización se han notificado erecciones prolongadas y priapismo con sildenafilo. En caso de una erección que se prolongue más de 4 horas, el paciente debe buscar atención médica inmediatamente. Si el priapismo no se trata de inmediato, podrían producirse daño tisular del pene y pérdida permanente de la potencia.
Uso concomitante con otros inhibidores de la PDE5 u otros tratamientos para la disfunción eréctil
No se han estudiado la seguridad y eficacia de la asociación de sildenafilo con otros inhibidores de la PDE5, otros tratamientos de la hipertensión arterial pulmonar (HAP) que contienen sildenafilo, u otros tratamientos para la disfunción eréctil. Por lo tanto, no se recomienda el uso de tales asociaciones.
Efectos sobre la visión
De forma espontánea, se han notificado casos de defectos visuales en asociación con la toma de sildenafilo y de otros inhibidores de la PDE5 (ver sección 4.8). De forma espontánea y en un estudio observacional, se han notificado casos de neuropatía óptica isquémica anterior no arterítica, una enfermedad rara, en asociación con la toma de sildenafilo y de otros inhibidores de la PDE5 (ver sección 4.8). Debe advertirse a los pacientes que en el caso de cualquier defecto visual repentino, dejen de tomar Vizarsin y consulten inmediatamente con un médico (ver sección 4.3).
Uso concomitante con ritonavir
No se recomienda la administración simultánea de sildenafilo con ritonavir (ver sección 4.5).
Uso concomitante con alfabloqueantes
Se recomienda tener precaución cuando se administre sildenafilo a pacientes en tratamiento con un alfa-bloqueante, ya que la administración simultánea de ambos fármacos puede producir hipotensión sintomática en un pequeño número de pacientes más susceptibles de padecerla (ver sección 4.5). Ésta es más probable que ocurra en las 4 horas posteriores a la toma de sildenafilo. Con el fin de minimizar la potencial aparición de hipotensión postural, los pacientes que reciban tratamiento con alfabloqueantes deberán encontrarse hemodinámicamente estables bajo el tratamiento con alfabloqueantes antes de iniciar la administración de sildenafilo. Por otro lado, se deberá valorar iniciar el tratamiento con sildenafilo a una dosis de 25 mg (ver sección 4.2). Asimismo, los médicos deben informar a sus pacientes de qué medidas adoptar en caso de experimentar síntomas de hipotensión postural.
Efectos sobre las hemorragias
Estudios con plaquetas humanas indican que sildenafilo potencia el efecto antiagregante del nitroprusiato sódico in vitro. No existen datos de seguridad sobre la administración de sildenafilo a pacientes con trastornos hemorrágicos o con úlcera péptica activa. Por lo tanto, sildenafilo se debe administrar a estos pacientes sólo tras la evaluación del beneficio-riesgo.
Uso en mujeres
El uso de Vizarsin no está indicado en mujeres.
Excipientes
Vizarsin contiene aspartamo (E951), una fuente de fenilalanina, que puede ser perjudicial para personas con fenilcetonuria.
Vizarsin contiene sorbitol (E420). Los pacientes con intolerancia hereditaria a la fructosa no deben tomar este medicamento.
4.5 Interacción con otros medicamentos y otras formas de interacción
Efectos de otros medicamentos sobre sildenafilo Estudios in vitro:
El metabolismo de sildenafilo está mediado predominantemente por el citocromo P450 (CYP) isoformas 3A4 (principalmente) y 2C9 (en menor medida). Por lo tanto, los inhibidores de estas isoenzimas pueden reducir el aclaramiento de sildenafilo y los inductores de estas isoenzimas pueden incrementar el aclaramiento de sildenafilo.
Estudios in vivo:
El análisis de los datos farmacocinéticos de los ensayos clínicos, mostró que se produjo una reducción del aclaramiento de sildenafilo cuando se administró concomitantemente con inhibidores del CYP3A4 (tales como ketoconazol, eritromicina, cimetidina). Aunque no se observó aumento de la incidencia de acontecimientos adversos en estos pacientes, cuando sildenafilo se administra concomitantemente con los inhibidores del CYP3A4, se debería considerar una dosis inicial de 25 mg.
Riociguat
Estudios preclínicos mostraron un efecto aditivo de la disminución de la presión arterial sistémica cuando se combinaron inhibidores de la PDE5 con riociguat. Riociguat ha mostrado en ensayos clínicos que aumenta los efectos hipotensores de los inhibidores de la PDE5. En la población estudiada no hubo indicios de un efecto clínico favorable de dicha combinación. El uso concomitante de riociguat con inhibidores de la PDE5, incluyendo sildenafilo, está contraindicado (ver sección 4.3).
La administración conjunta de ritonavir, inhibidor de la proteasa del VIH, el cual presenta una potente acción inhibitoria sobre el citocromo P450, en el estado de equilibrio (500 mg dos veces al día) junto con sildenafilo (dosis única de 100 mg) produjo un aumento del 300% (4 veces superior) en la Cmax de sildenafilo y del 1000% (11 veces superior) en la AUC plasmática de sildenafilo. A las 24 horas, los niveles plasmáticos de sildenafilo eran todavía aproximadamente 200 ng/ml, en comparación con los aproximadamente 5 ng/ml cuando se administra sólo sildenafilo. Este hecho está en concordancia con los efectos evidentes de ritonavir sobre un gran número de sustratos del citocromo P450. Sildenafilo no presentó ningún efecto sobre la farmacocinética de ritonavir. En base a estos resultados farmacocinéticos, no se aconseja la administración concomitante del sildenafilo con ritonavir (ver sección 4.4) y en ninguna circunstancia la dosis máxima de sildenafilo debe exceder de 25 mg en 48 horas.
La administración conjunta de saquinavir, inhibidor de la proteasa del VIH, que también presenta una acción inhibitoria sobre el citocromo CYP3A4, en el estado de equilibrio (1.200 mg tres veces al día), con sildenafilo (dosis única de 100 mg) produjo un aumento del 140% en la Cmax de sildenafilo y del 210% en la AUC de sildenafilo. Sildenafilo no presentó ningún efecto sobre la farmacocinética de saquinavir (ver sección 4.2). Cabría esperar efectos más intensos con inhibidores más potentes del citocromo CYP 3A4, tales como ketoconazol e itraconazol.
Cuando se administró una dosis única de 100 mg de sildenafilo con eritromicina, un inhibidor moderado del CYP3A4, hubo un incremento del 182% en la exposición sistémica de sildenafilo (AUC) cuando se alcanzó una concentración estable de eritromicina en plasma (500 mg, dos veces al día, durante 5 días). En voluntarios varones sanos, no se observó ninguna evidencia de un efecto con azitromicina (500 mg diarios durante 3 días) sobre el AUC, la Cmax, el tmax, la constante de velocidad de eliminación o la consiguiente semivida de sildenafilo o de su metabolito principal en sangre. Cimetidina (800 mg), un inhibidor del citocromo P450 e inhibidor no específico del CYP3A4, produjo un aumento del 56% de la concentración plasmática de sildenafilo cuando se administró simultáneamente con sildenafilo (50 mg) a voluntarios sanos.
El zumo de pomelo es un inhibidor débil del metabolismo del citocromo CYP3A4 localizado en la pared intestinal que puede provocar pequeños incrementos de los niveles plasmáticos de sildenafilo.
Dosis únicas de antiácido (hidróxido magnésico/hidróxido de aluminio) no afectaron la
biodisponibilidad de sildenafilo.
Aunque no se han realizado estudios de interacción específica con todos los fármacos posibles, el análisis de los datos farmacocinéticos no mostró efecto alguno sobre la farmacocinética de sildenafilo cuando se administró concomitantemente con inhibidores del CYP2C9 (tales como tolbutamida, warfarina, fenitoína), inhibidores del CYP2D6 (tales como inhibidores selectivos de la recaptación de serotonina, antidepresivos tricíclicos), tiazidas y diuréticos relacionados (diuréticos de asa y ahorradores de potasio), inhibidores de la enzima conversora de angiotensina, antagonistas del calcio, antagonistas beta-adrenérgicos o inductores del metabolismo del CYP450 (tales como rifampicina, barbitúricos). En un estudio con voluntarios varones sanos, la administración concomitante del antagonista de los receptores de endotelina, bosentan, (un inductor del CYP3A4 [moderado], del CYP2C9 y posiblemente del CYP2C19) en estado de equilibrio (125 mg dos veces al día) con sildenafilo en estado de equilibrio (80 mg tres veces al día) resultó en una disminución de 62,6% y 55,4% del AUC y Cmax de sildenafilo, respectivamente. Por lo tanto, se espera que la administración concomitante de inductores potentes de CYP3A4, como rifampina, causen mayores disminuciones de la concentración plasmática de sildenafilo.
Nicorandil es un híbrido entre un activador de los canales de potasio y un nitrato. Debido a su componente nitrato, tiene el provocar de presentar una interacción grave con sildenafilo.
Efectos de sildenafilo sobre otros medicamentos
Estudios in vitro
Sildenafilo es un inhibidor débil del citocromo P450 isoformas 1A2, 2C9, 2C19, 2D6, 2E1 y 3A4 (IC50 > 150 ^M). Dado que las concentraciones plasmáticas máximas de sildenafilo, tras las dosis recomendadas, son de aproximadamente 1 ^M, no es probable que Vizarsin altere el aclaramiento de los substratos de estas isoenzimas.
No se dispone de datos de interacción de sildenafilo e inhibidores no específicos de la fosfodiesterasa, tales como teofilina o dipiridamol.
Estudios in vivo
De acuerdo con sus efectos conocidos sobre la vía óxido nítrico/GMPc (ver sección 5.1), sildenafilo demostró potenciar los efectos hipotensores de los nitratos. Por lo tanto, su administración concomitante con los dadores del óxido nítrico o nitratos está contraindicada (ver sección 4.3).
La administración concomitante de sildenafilo a pacientes en tratamiento con alfabloqueantes puede producir hipotensión sintomática en un pequeño número de pacientes que puede ser más susceptible de padecerla. Ésta es más probable que ocurra en las 4 horas posteriores a la toma de sildenafilo (ver secciones 4.2 y 4.4). En tres estudios específicos de interacción farmacológica, se administraron simultáneamente el alfabloqueante doxazosina (4 mg y 8 mg) y sildenafilo (25 mg, 50 mg o 100 mg) a pacientes con hiperplasia benigna de próstata (HBP) y que se encontraban ya estables en el tratamiento con doxazosina. En estas poblaciones objeto de estudio, se observaron unas reducciones medias adicionales de la presión arterial en decúbito supino de 7/7 mmHg, de 9/5 mmHg y de 8/4 mmHg, y unas reducciones medias adicionales de la presión arterial en bipedestación de 6/6 mmHg, de 11/4 mmHg y de 4/5 mmHg, respectivamente. Cuando sildenafilo y doxazosina fueron administrados simultáneamente a pacientes estables en el tratamiento con doxazosina, los casos notificados de pacientes que experimentaron hipotensión postural sintomática fueron poco frecuentes. Estos casos incluyeron mareos o sensación de vahído, pero no síncope.
No se han observado interacciones significativas cuando se administró sildenafilo (50 mg) concomitantemente con tolbutamida (250 mg) o warfarina (40 mg), metabolizándose ambos por el CYP2C9.
Sildenafilo (50 mg) no potenció el aumento del tiempo de hemorragia causado por ácido acetilsalicílico (150 mg).
Sildenafilo (50 mg) no potenció los efectos hipotensores del alcohol en voluntarios sanos con niveles máximos medios de alcohol en sangre de 80 mg/dl.
El análisis de todos los datos obtenidos de los siguientes tipos de fármacos antihipertensivos: diuréticos, beta bloqueantes, inhibidores de la ECA, antagonistas de la angiotensina II, fármacos antihipertensivos (vasodilatadores y de acción central), bloqueantes de las neuronas adrenérgicas, calcio antagonistas y bloqueantes alfa-adrenérgicos, mostró que no existen diferencias en el perfil de efectos secundarios en pacientes a los que se administró sildenafilo, en comparación con el tratamiento con placebo. En un estudio de interacción específico, cuando sildenafilo (100 mg) se administró concomitantemente con amlodipino a pacientes hipertensos, la reducción media adicional en la tensión arterial sistólica en posición supina fue de 8 mmHg. La reducción adicional correspondiente de la tensión arterial diastólica en posición supina fue de 7 mmHg. Estas reducciones adicionales en la tensión arterial fueron de una magnitud similar a aquellas observadas cuando se administró sildenafilo como único fármaco a voluntarios sanos (ver sección 5.1).
Sildenafilo (100 mg) no afectó a la farmacocinética del estado de equilibrio de los inhibidores de la proteasa del VIH, saquinavir y ritonavir, los cuales son sustratos del citocromo CYP3A4.
En voluntarios varones sanos, la administración de sildenafilo en estado de equilibrio (80 mg tres veces al día) resultó en un incremento de 49,8% del AUC de bosentan y un incremento de 42% de la Cmax de bosentan (125 mg dos veces al día).
4.6 Fertilidad, embarazo y lactancia
El uso de Vizarsin no está indicado en mujeres.
No se han realizado estudios adecuados y bien controlados en mujeres embarazadas o en periodo de lactancia.
Tras la administración oral de sildenafilo no se observaron efectos adversos relevantes en los estudios de reproducción realizados en ratas y conejos.
No hubo efectos sobre la movilidad ni la morfología de los espermatozoides de voluntarios sanos tras administrarles una sola dosis de 100 mg de sildenafilo por vía oral (ver sección 5.1).
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
No se han realizado estudios sobre la capacidad para conducir y utilizar máquinas.
En los ensayos clínicos con sildenafilo se notificaron mareos y trastornos visuales, por lo tanto, los pacientes deben saber cómo reaccionan a Vizarsin antes de conducir vehículos o utilizar máquinas.
4.8 Reacciones adversas
Resumen del perfil de seguridad
El perfil de seguridad de Vizarsin se basa en 9.570 pacientes de 74 ensayos clínicos doble ciego, controlados con placebo. Las reacciones adversas más frecuentemente notificadas en los ensayos clínicos entre los pacientes tratados con sildenafilo fueron dolor de cabeza, rubefacción, dispepsia, congestión nasal, mareo, náuseas, acaloramiento, deterioro visual, cianopsia y visión borrosa.
Las reacciones adversas notificadas durante la experiencia postcomercialización se han recogido cubriendo un período estimado superior a 10 años. Dado que no todas las reacciones adversas se han notificado al titular de la autorización de comercialización e incluido en la base de datos de seguridad, las frecuencias de estas reacciones adversas no pueden determinarse de modo fiable.
Tabla de reacciones adversas
En la tabla de abajo aparecen todas las reacciones adversas clínicamente importantes, que ocurrieron en los ensayos clínicos con una incidencia superior al placebo, listadas según la clasificación por órganos y sistemas muy frecuentes (> 1/10), frecuentes (> 1/100 a < 1/10), poco frecuentes (> 1/1.000 a < 1/100), raras (> 1/10.000 a < 1/1.000), muy raras (< 1/10.000).
Además, la frecuencia de las reacciones adversas clínicamente importantes notificadas a partir de la experiencia postcomercialización, se incluye como frecuencia no conocida.
Tabla 1: Reacciones adversas clínicamente importantes notificadas con una incidencia superior a placebo en ensayos clínicos controlados y reacciones adversas clínicamente importantes notificadas a partir de la experiencia postcomercialización.
|
Clasificación por órganos y sistemas |
Muy frecuentes (> 1/10) |
Frecuentes (>1/100 y <1/10) |
Poco frecuentes (> 1/1.000 y <1/100) |
Raras (> 1/10.000 y <1/1.000) |
|
Infecciones e infestaciones |
Rinitis | |||
|
Trastornos del sistema inmunológico |
Hipersensibilidad | |||
|
Trastornos del sistema nervioso |
Cefalea |
Mareo |
Somnolencia, Hipoestesia |
Accidente cerebrovascular, ataque isquémico transitorio, convulsiones , convulsiones recurrentes , síncope |
|
Trastornos oculares |
Distorsión visual de los colores**, deterioro visual, visión borrosa |
Trastornos del lagrimeo***, dolor ocular, fotofobia, fotopsia, hiperemia ocular, claridad visual, conjuntivitis |
Neuropatía óptica isquémica anterior no arterítica (NOIA-NA)*, oclusión vascular retiniana*, hemorragia retiniana, retinopatía arterioesclerótica, trastorno retiniano, glaucoma, defectos del campo visual, diplopía, agudeza visual disminuida, miopía, astenopía, células flotantes en el vítreo, trastorno del iris, midriasis, halo visual, edema del ojo, hinchazón ocular, trastorno del ojo, hiperemia de la conjuntiva, irritación ocular, sensación anormal en el ojo, edema palpebral, cambio de color de la esclerótida |
|
Clasificación por órganos y sistemas |
Muy frecuentes (> 1/10) |
Frecuentes (>1/100 y <1/10) |
Poco frecuentes (> 1/1.000 y <1/100) |
Raras (> 1/10.000 y <1/1.000) |
|
Trastornos del oído y del laberinto |
Vértigo, acúfenos |
Sordera | ||
|
Trastornos cardiacos |
Taquicardia, palpitaciones |
Muerte cardiaca súbita*, infarto de miocardio, arritmia ventricular , fibrilación auricular, angina inestable | ||
|
Trastornos vasculares |
Rubefacción, acaloramiento |
Hipertensión, hipotensión | ||
|
Trastornos respiratorios, torácicos y mediastínicos |
Congestión nasal |
Epistaxis, congestión sinusal |
Sensación de opresión en la garganta, edema nasal, sequedad nasal | |
|
Trastornos gastrointestinales |
Náuseas, dispepsia |
Enfermedad por reflujo gastroesofágico, vómitos, dolor en la zona superior del abdomen, boca seca |
Hipoestesia oral | |
|
Trastornos de la piel y del tejido subcutáneo |
Erupción |
Síndrome de Stevens-Johnson (SSJ)*, necrólisis epidérmica tóxica (NET)* | ||
|
Trastornos musculoesqueléticos y del tejido subcutáneo |
Mialgia, dolor en una extremidad | |||
|
Trastornos renales y urinarios |
Hematuria | |||
|
Trastornos del aparato reproductor y de la mama |
Hemorragia peneana priapismo , hematospermia, erección aumentada | |||
|
Trastornos generales y alteraciones en el lugar de administración |
Dolor torácico, fatiga, sensación de calor |
Irritabilidad | ||
|
Exploraciones complementarias |
Frecuencia cardiaca aumentada |
*Notificado únicamente durante la experiencia postcomercialización
**Distorsión visual de los colores: cloropsia, cromatopsia, cianopsia, eritropsia y xantopsia ***Trastomos del lagrimeo: ojo seco, trastorno lagrimal, lagrimeo aumentado
Notificación de sospechas de reacciones adversas
. Se invita a los sistema nacional
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento profesionales sanitarios a notificar las sospechas de reacciones adversas a través del de notificación incluido en el Apéndice V.
4.9 Sobredosis
Síntomas
En estudios realizados en voluntarios sanos con dosis únicas de hasta 800 mg, las reacciones adversas fueron similares a las observadas con dosis más bajas, pero la incidencia y gravedad aumentó. Dosis de 200 mg no incrementaron la eficacia pero sí la incidencia de reacciones adversas (cefalea, enrojecimiento, mareos, dispepsia, congestión nasal y trastornos visuales).
Tratamiento
En caso de sobredosis, se deben tomar medidas normales de apoyo. Dado que sildenafilo se une intensamente a proteínas plasmáticas y no se elimina por orina, no se espera que la diálisis renal acelere el aclaramiento del fármaco.
5. PROPIEDADES FARMACOLÓGICAS
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: Urológicos, fármacos utilizados en disfunción eréctil, código ATC: G04BE03.
Mecanismo de acción
Sildenafilo es una terapia de administración oral para el tratamiento de la disfunción eréctil. En condiciones normales, es decir, con estimulación sexual, restaura la función eréctil deteriorada mediante el aumento del flujo sanguíneo al pene.
El mecanismo fisiológico responsable de la erección del pene implica la liberación de óxido nítrico (ON) en los cuerpos cavernosos durante la estimulación sexual. El óxido nítrico activa la enzima guanilatociclasa, lo que da lugar a un aumento de los niveles de guanosina monofosfato cíclica (GMPc), que produce una relajación del músculo liso en los cuerpos cavernosos del pene, permitiendo la afluencia de sangre y subsiguiente llenado de los mismos.
Sildenafilo es un inhibidor potente y selectivo de la fosfodiesterasa tipo 5 (PDE5) específica GMPc de los cuerpos cavernosos, donde la PDE5 es la responsable de la degradación del GMPc. Sildenafilo actúa a nivel periférico sobre la erección. Sildenafilo no tiene un efecto relajante directo sobre los cuerpos cavernosos humanos aislados, pero aumenta potentemente el efecto relajante del ON en este tejido. Cuando se encuentra activada la vía ON/GMPc, como ocurre durante la estimulación sexual, la inhibición de la PDE5 por sildenafilo ocasiona un aumento de los niveles de GMPc en los cuerpos cavernosos. Por lo tanto es necesario estimulación sexual para que sildenafilo produzca sus efectos farmacológicos beneficiosos previstos.
Efectos farmacodinámicos
Los estudios in vitro han mostrado que sildenafilo es selectivo de la PDE5, implicada en el proceso de erección. Su efecto es más potente sobre la PDE5 que sobre otras fosfodiesterasas conocidas. Tiene una selectividad 10 veces mayor que por la PDE6, que participa en el mecanismo de fototransducción en la retina. A las dosis máximas recomendadas, tiene una selectividad 80 veces superior por la PDE1 y 700 veces superior por la PDE2, 3, 4, 7, 8, 9, 10 y 11. Particularmente, sildenafilo es 4.000 veces más selectivo por la PDE5 que por la PDE3, la isoforma fosfodiesterasa específica AMPc relacionada con el control de la contractilidad cardíaca.
Eficacia clínica y seguridad
Dos estudios clínicos fueron específicamente diseñados para evaluar la ventana durante la cual sildenafilo podría producir una erección en respuesta a la estimulación sexual. En un estudio utilizando plestismografía peneana (RigiScan) con pacientes en ayunas, el tiempo mediano de inicio de una erección con rigidez superior al 60% (suficiente para el acto sexual) fue de 25 minutos (rango de 12-37 minutos) tras la administración de sildenafilo. En otro estudio utilizando también RigiScan, sildenafilo, a las 4-5 horas de ser administrado, aún fue capaz de producir una erección en respuesta a la estimulación.
Sildenafilo causa una disminución leve y transitoria en la tensión arterial que, en la mayoría de los casos, no se traduce en efectos clínicos. La disminución máxima media de la tensión arterial sistólica, en posición supina, tras una dosis oral de 100 mg de sildenafilo, fue de 8,4 mmHg y de 5,5 mmHg en la tensión arterial diastólica. Estas disminuciones en la tensión arterial concuerdan con los efectos vasodilatadores de sildenafilo, probablemente debido al aumento en los niveles de GMPc en la musculatura lisa vascular. Dosis únicas orales de sildenafilo de hasta 100 mg en voluntarios sanos no produjeron efectos clínicamente relevantes sobre el ECG.
En un estudio sobre los efectos hemodinámicos de una dosis única de 100 mg de sildenafilo administrada por vía oral en 14 pacientes con enfermedad coronaria obstructiva grave (estenosis >70% de al menos una arteria coronaria), la presión arterial sistólica y diastólica media en reposo disminuyeron alrededor del 7% y 6%, respectivamente, en comparación a los datos basales. La presión arterial sistólica pulmonar media disminuyó un 9%. Sildenafilo no presentó efectos sobre el rendimiento cardíaco, y no afectó al flujo sanguíneo en arterias coronarias estenosadas.
En un estudio de prueba de esfuerzo, doble ciego, controlado con placebo, se evaluó a 144 pacientes con disfunción eréctil y angina estable crónica que estaban tomando medicamentos antianginosos regularmente (excepto nitratos). Los resultados demostraron que no hubo diferencias clínicamente relevantes en el tiempo necesario para desencadenar la aparición de una angina con el uso de sildenafilo en comparación con placebo.
En algunos pacientes, se han detectado diferencias leves y transitorias en la discriminación del color (azul/verde), cuando se utilizó la prueba de tinción Farnsworth-Munsell 100, una hora después de administrar una dosis de 100 mg, sin que se produjeran efectos evidentes a las dos horas de la administración. El mecanismo postulado para este cambio en la discriminación de color se relaciona con la inhibición de la PDE6, que participa en la cascada de fototransducción de la retina. Sildenafilo no tiene efectos sobre la agudeza visual o sensibilidad al contraste. En un estudio controlado con placebo de pequeño tamaño en pacientes con degeneración macular temprana documentada (n=9), se demostró que sildenafilo (dosis única, 100 mg) no produjo cambios significativos en las pruebas visuales realizadas (agudeza visual, test de Amsler, discriminación de los colores de un semáforo simulado, perímetro de Humphrey y fotoestrés).
No hubo ningún efecto sobre la motilidad o la morfología de esperma tras la administración oral de dosis únicas de 100 mg de sildenafilo en voluntarios sanos (ver sección 4.6).
Información adicional sobre ensayos clínicos:
En los ensayos clínicos sildenafilo se administró a más de 8.000 pacientes en edades comprendidas entre los 19 y 87 años. Los siguientes grupos de pacientes estuvieron representados: ancianos (19,9%), pacientes con hipertensión (30,9%), diabetes mellitus (20,3%), enfermedades cardíacas isquémicas (5,8%), hiperlipidemia (19,8%), lesión medular (0,6%), depresión (5,2%), resección transuretral de la próstata (3,7%), prostatectomía radical (3,3%). Los siguientes grupos, no estuvieron bien representados o se excluyeron de los ensayos clínicos: pacientes con cirugía de pelvis, pacientes que han sido sometidos a radioterapia, pacientes con disfunción renal o hepática grave y pacientes con ciertos trastornos cardiovasculares (ver sección 4.3).
En los estudios de dosis fijas, la proporción de pacientes que reconoció que el tratamiento mejoró sus erecciones fue del 62% (25 mg), 74% (50 mg) y 82% (100 mg) en comparación a un 25% con placebo. En ensayos clínicos controlados, la proporción de abandonos atribuibles a sildenafilo fue baja y similar a placebo.
Considerando todos los estudios clínicos, la proporción de pacientes que informaron de mejoría con sildenafilo fue la siguiente: disfunción eréctil psicógena (84%), disfunción eréctil mixta (77%), disfunción eréctil orgánica (68%), ancianos (67%), diabetes mellitus (59%), enfermedad cardíaca isquémica (69%), hipertensión (68%), resección transuretral de la próstata (RTUP) (61%), prostatectomía radical (43%), lesión medular (83%), depresión (75%). La seguridad y eficacia de sildenafilo se mantuvo en los estudios a largo plazo.
5.2 Propiedades farmacocinéticas
Absorción
Sildenafilo se absorbe rápidamente. Tras la administración oral, en estado de ayuno, se observan concentraciones plasmáticas máximas entre 30 y 120 minutos (media de 60 minutos) post-dosis. La biodisponibilidad oral absoluta media es del 41% (rango del 25 al 63%). Tras la administración oral de sildenafilo el AUC y Cmax aumentaron en proporción a la dosis en el rango de dosis recomendado (25-100 mg).
Cuando sildenafilo se administra con alimentos, la velocidad de absorción disminuye con un retraso medio en la tmax de 60 minutos y una reducción media en la Cmax del 29%.
Distribución
El volumen medio de distribución (Vd) en estado de equilibrio para sildenafilo es de 105 l, indicando una distribución tisular del fármaco. Tras la administración de una dosis única de 100 mg, la concentración plasmática máxima total media de sildenafilo es aproximadamente 440 ng/ml (CV 40%). Dado que sildenafilo (y su metabolito principal circulante N-desmetilo) se encuentra unido a proteínas plasmáticas en un 96%,, esto da como resultado una concentración plasmática libre media de sildenafilo de 18 ng/ml (38 nM). La unión a proteínas es independiente de las concentraciones totales de ambos compuestos.
En el eyaculado de voluntarios sanos que recibían sildenafilo (100 mg como dosis única), se detectó menos del 0,0002% (promedio 188 ng) de la dosis administrada, 90 minutos después de la dosificación.
Biotransformación
Sildenafilo se metaboliza predominantemente por las isoenzimas microsomales hepáticas CYP3A4 (principalmente) y CYP2C9 (en menor medida). El metabolito principal circulante resulta de la N-desmetilación de sildenafilo. Este metabolito tiene un perfil de selectividad por las fosfodiesterasas similar a sildenafilo y la potencia in vitro por PDE5 es de aproximadamente el 50% de la del principio activo original. Las concentraciones plasmáticas de este metabolito son aproximadamente el 40% de las observadas para sildenafilo. El metabolito N-desmetilo continúa metabolizándose, con una vida media terminal de aproximadamente 4 horas.
Eliminación
El aclaramiento total de sildenafilo es de 41 l/hora, con una fase terminal resultante en una vida media de 3-5 horas. Tras la administración oral o intravenosa, sildenafilo se excreta en forma de metabolitos predominantemente en heces (aproximadamente el 80% de la dosis oral administrada) y en menor medida en orina (aproximadamente el 13% de la dosis oral administrada).
Farmacocinética en grupos especiales de pacientes
Personas de edad avanzada:
Sildenafilo mostró un aclaramiento reducido en voluntarios sanos de edad avanzada (más de 65 años), siendo las concentraciones plasmáticas de sildenafilo y de su metabolito activo N-desmetilo un 90% más altas que las observadas en voluntarios sanos jóvenes (18-45 años). La concentración de sildenafilo libre en el plasma fue aproximadamente el 40% mayor, debido al efecto que el envejecimiento ejerce sobre la unión a las proteínas plasmáticas.
Insuficiencia renal:
En voluntarios con insuficiencia renal leve a moderada (aclaramiento de creatinina = 30-80 ml/min), no se alteró la farmacocinética de sildenafilo después de recibir una única dosis oral de 50 mg. El AUC y Cmax medios del metabolito N-desmetilo aumentaron hasta el 126% y hasta el 73% respectivamente, en comparación a voluntarios de la misma edad sin insuficiencia renal. Sin embargo, debido a la elevada variabilidad entre personas, estas diferencias no fueron estadísticamente significativas. En voluntarios con insuficiencia renal grave (aclaramiento de creatinina < 30 ml/min), se redujo el aclaramiento de sildenafilo, con un aumento del AUC y Cmax del 100% y del 88% respectivamente, en comparación a los voluntarios de la misma edad sin insuficiencia renal. Además, los valores de AUC y Cmax para el metabolito N-desmetilo aumentaron significativamente, 200% y 79%, respectivamente.
Insuficiencia hepática:
En voluntarios con cirrosis hepática de leve a moderada (Child-Pugh A y B), el aclaramiento de sildenafilo se redujo, resultando en aumentos del AUC (84%) y Cmax (47%) en comparación con voluntarios de la misma edad sin insuficiencia hepática. La farmacocinética de sildenafilo en pacientes con insuficiencia hepática grave no ha sido estudiada.
5.3 Datos preclínicos sobre seguridad
Los datos de los estudios no clínicos no muestran riesgos especiales para los seres humanos, según los estudios convencionales de farmacología de seguridad, toxicidad a dosis repetidas, genotoxicidad, potencial carcinogénico, toxicidad para la reproducción y el desarrollo.
6. DATOS FARMACÉUTICOS
6.1 Lista de excipientes
Hidroxipropilcelulosa (E463)
Manitol (E421)
Aspartamo (E951)
Neohesperidina dihidrochalcona (E959)
Aroma de hierbabuena
Aroma de menta (contiene sorbitol (E420))
Crospovidona
Silicato de calcio
Estearato de magnesio (E572)
6.2 Incompatibilidades
No procede.
6.3 Periodo de validez
2 años
6.4 Precauciones especiales de conservación
No conservar a temperatura superior a 30°C.
Conservar en el embalaje original para protegerlo de la humedad.
6.5 Naturaleza y contenido del envase
Vizarsin 25 mg comprimidos bucodispersables
Blíster (blíster desplegable, poliamida orientada/Aluminio/PVC//PET/Aluminio): 1 comprimido bucodispersable, en una caja.
Blíster (blíster unidosis desplegable perforado, poliamida orientada/Aluminio/PVC//PET/Aluminio): 2 x 1, 4 x 1, 8 x 1 o 12 x 1 comprimido bucodispersable, en una caja.
Vizarsin 50 mg, 100 mg comprimidos bucodispersables
Blíster (blíster desplegable, poliamida orientada/Aluminio/PVC//PET/Aluminio): 1 comprimido bucodispersable, en una caja.
Blíster (blíster unidosis desplegable perforado, poliamida orientada/Aluminio/PVC//PET/Aluminio): 2 x 1, 4 x 1, 8 x 1, 12 x 1 o 24 x 1 comprimido bucodispersable, en una caja.
Puede que solamente estén comercializados algunos tamaños de envases.
6.6 Precauciones especiales de eliminación
Ninguna especial.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
Vizasin 25 mg comprimidos bucodispersables
1 comprimido bucodispersable: EU/1/09/551/013
2 x 1 comprimido bucodispersable: EU/1/09/551/014 4 x 1 comprimido bucodispersable: EU/1/09/551/015 8 x 1 comprimido bucodispersable: EU/1/09/551/016 12 x 1 comprimido bucodispersable: EU/1/09/551/017
Vizasin 50 mg comprimidos bucodispersables
1 comprimido bucodispersable: EU/1/09/551/018
2 x 1 comprimido bucodispersable: EU/1/09/551/019 4 x 1 comprimido bucodispersable: EU/1/09/551/020 8 x 1 comprimido bucodispersable: EU/1/09/551/021 12 x 1 comprimido bucodispersable: EU/1/09/551/021 24 x 1 comprimido bucodispersable: EU/1/09/551/028
Vizasin 100 mg comprimidos bucodispersables
1 comprimido bucodispersable: EU/1/09/551/023
2 x 1 comprimido bucodispersable: EU/1/09/551/024 4 x 1 comprimido bucodispersable: EU/1/09/551/025 8 x 1 comprimido bucodispersable: EU/1/09/551/026 12 x 1 comprimido bucodispersable: EU/1/09/551/027 24 x 1 comprimido bucodispersable: EU/1/09/551/029
9. FECHA DE LA PRIMERA AUTORIZACIÓN/RENOVACIÓN DE LA AUTORIZACIÓN
Fecha de la primera autorización: 21 de septiembre de 2009
Fecha de la última renovación: 16 de mayo de 2014
10. FECHA DE LA REVISIÓN DEL TEXTO
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos http://www.ema.europa.eu.
A. FABRICANTE(S) RESPONSABLE(S) DE LA LIBERACIÓN DE LOS LOTES
B. CONDICIONES O RESTRICCIONES DE SUMINISTRO Y USO
C. OTRAS CONDICIONES Y REQUISITOS DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
D. CONDICIONES O RESTRICCIONES EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO
A. FABRICANTE(S) RESPONSABLE(S) DE LA LIBERACIÓN DE LOS LOTES
Nombre y dirección del (de los) fabricante(s) responsable(s) de la liberación de los lotes
KRKA, d.d., Novo mesto Smarjeska cesta 6 8501 Novo mesto Eslovenia
TAD Pharma GmbH Heinz-Lohmann-StraBe 5 27472 Cuxhaven Alemania
El prospecto impreso del medicamento debe especificar el nombre y direccion del fabricante responsable de la liberacion del lote en cuestión.
B. CONDICIONES O RESTRICCIONES DE SUMINISTRO Y USO
Medicamento sujeto a prescripción médica.
C. OTRAS CONDICIONES Y REQUISITOS DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
• Informes periódicos de seguridad (IPS)
Los requerimientos para la presentación de los informes periódicos de seguridad para este medicamento se establecen en la lista de fechas de referencia de la Unión (lista EURD) prevista en el artículo 107quater, apartado 7, de la Directiva 2001/83/CE y publicada en el portal web europeo sobre medicamentos.
D. CONDICIONES O RESTRICCIONES RELATIVAS AL USO SEGURO Y EFICAZ DEL MEDICAMENTO
• Plan de Gestión de Riesgos (PGR)
No procede.
ETIQUETADO Y PROSPECTO
A. ETIQUETADO
1. NOMBRE DEL MEDICAMENTO
Vizarsin 25 mg comprimidos recubiertos con película Sildenafilo
2. PRINCIPIO(S) ACTIVO(S)
Cada comprimido recubierto con película contiene sildenafilo citrato equivalente a 25 mg de sildenafilo.
3. LISTA DE EXCIPIENTES
Contiene lactosa.
Para mayor información consultar el prospecto.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
1 comprimido recubierto con película 4 x 1 comprimido recubierto con película 8 x 1 comprimido recubierto con película 12 x 1 comprimido recubierto con película
5. FORMA Y VÍA(S) DE ADMINISTRACIÓN
Leer el prospecto antes de utilizar este medicamento. Vía oral.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE
FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Mantener fuera de la vista y del alcance de los niños.
7. OTRA(S) ADVERTENCIA(S) ESPECIAL(ES), SI ES NECESARIO
8. FECHA DE CADUCIDAD
EXP:
9. CONDICIONES ESPECIALES DE CONSERVACIÓN
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA, d.d., Novo mesto, Smarjeska cesta 6, 8501 Novo mesto, Eslovenia
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
1 comprimido recubierto con película: EU/1/09/551/001 4 x 1 comprimido recubierto con película: EU/1/09/551/002 8 x 1 comprimido recubierto con película: EU/1/09/551/003 12 x 1 comprimido recubierto con película: EU/1/09/551/004
13. NÚMERO DE LOTE
Lot:
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
Vizarsin 25 mg
INFORMACIÓN MÍNIMA A INCLUIR EN BLÍSTERS O TIRAS BLÍSTER
1. NOMBRE DEL MEDICAMENTO
Vizarsin 25 mg comprimidos recubiertos con película Sildenafilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA
3. FECHA DE CADUCIDAD
EXP:
4. NÚMERO DE LOTE
Lot:
5. OTROS
1. NOMBRE DEL MEDICAMENTO
Vizarsin 50 mg comprimidos recubiertos con película Sildenafilo
2. PRINCIPIO(S) ACTIVO(S)
Cada comprimido recubierto con película contiene sildenafilo citrato equivalente a 50 mg de sildenafilo.
3. LISTA DE EXCIPIENTES
Contiene lactosa.
Para mayor información consultar el prospecto.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
1 comprimido recubierto con película 4 x 1 comprimido recubierto con película 8 x 1 comprimido recubierto con película 12 x 1 comprimido recubierto con película
5. FORMA Y VÍA(S) DE ADMINISTRACIÓN
Leer el prospecto antes de utilizar este medicamento. Vía oral.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE
FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Mantener fuera de la vista y del alcance de los niños.
7. OTRA(S) ADVERTENCIA(S) ESPECIAL(ES), SI ES NECESARIO
8. FECHA DE CADUCIDAD
EXP:
9. CONDICIONES ESPECIALES DE CONSERVACIÓN
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA, d.d., Novo mesto, Smarjeska cesta 6, 8501 Novo mesto, Eslovenia
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
1 comprimido recubierto con película: EU/1/09/551/005 4 x 1 comprimido recubierto con película: EU/1/09/551/006 8 x 1 comprimido recubierto con película: EU/1/09/551/007 12 x 1 comprimido recubierto con película: EU/1/09/551/008
13. NÚMERO DE LOTE
Lot:
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
Vizarsin 50 mg
INFORMACIÓN MÍNIMA A INCLUIR EN BLÍSTERS O TIRAS BLÍSTER
1. NOMBRE DEL MEDICAMENTO
Vizarsin 50 mg comprimidos recubiertos con película Sildenafilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA
3. FECHA DE CADUCIDAD
EXP:
4. NÚMERO DE LOTE
Lot:
5. OTROS
1. NOMBRE DEL MEDICAMENTO
Vizarsin 100 mg comprimidos recubiertos con película Sildenafilo
2. PRINCIPIO(S) ACTIVO(S)
Cada comprimido recubierto con película contiene sildenafilo citrato equivalente a 100 mg de sildenafilo.
3. LISTA DE EXCIPIENTES
Contiene lactosa.
Para mayor información consultar el prospecto.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
1 comprimido recubierto con película 4 x 1 comprimido recubierto con película 8 x 1 comprimido recubierto con película 12 x 1 comprimido recubierto con película
5. FORMA Y VÍA(S) DE ADMINISTRACIÓN
Leer el prospecto antes de utilizar este medicamento. Vía oral.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE
FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Mantener fuera de la vista y del alcance de los niños.
7. OTRA(S) ADVERTENCIA(S) ESPECIAL(ES), SI ES NECESARIO
8. FECHA DE CADUCIDAD
EXP:
9. CONDICIONES ESPECIALES DE CONSERVACIÓN
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA, d.d., Novo mesto, Smarjeska cesta 6, 8501 Novo mesto, Eslovenia
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
1 comprimido recubierto con película: EU/1/09/551/009 4 x 1 comprimido recubierto con película: EU/1/09/551/010 8 x 1 comprimido recubierto con película: EU/1/09/551/011 12 x 1 comprimido recubierto con película: EU/1/09/551/012
13. NÚMERO DE LOTE
Lot:
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
Vizarsin 100 mg
INFORMACIÓN MÍNIMA A INCLUIR EN BLÍSTERS O TIRAS BLÍSTER
1. NOMBRE DEL MEDICAMENTO
Vizarsin 100 mg comprimidos recubiertos con película Sildenafilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA
3. FECHA DE CADUCIDAD
EXP:
4. NÚMERO DE LOTE
Lot:
5. OTROS
INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR CARTÓN para materiales de acondicionamiento monolingüe y bilingüe
1. NOMBRE DEL MEDICAMENTO
Vizarsin 25 mg comprimidos bucodispersables Sildenafilo
2. PRINCIPIO ACTIVO
Cada comprimido bucodispersable contiene 25 mg de sildenafilo.
3. LISTA DE EXCIPIENTES
Contiene aspartamo (E951) y aroma de menta (sorbitol (E420)). Lea el prospecto para obtener más información.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
1 comprimido bucodispersable
2 x 1 comprimido bucodispersable 4 x 1 comprimido bucodispersable 8 x 1 comprimido bucodispersable 12 x 1 comprimido bucodispersable
5. FORMA Y VÍA(S) DE ADMINISTRACIÓN
Leer el prospecto antes de utilizar este medicamento. Vía oral. Disolver en la boca.
Para blísters de 1 comprimido:
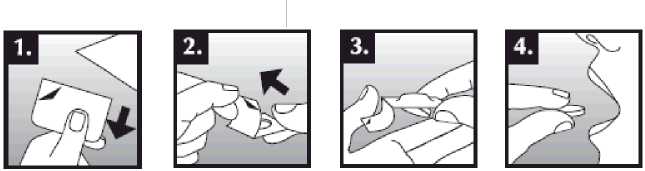
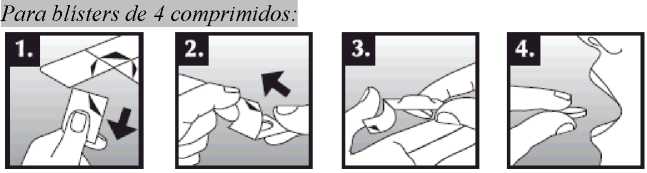
1. Sujete el blíster por los bordes y separe una de las unidades rasgando con cuidado por las marcas troqueladas.
2. Despegue completamente la hoja tirando hacia arriba del borde.
3. Voltee el blíster para colocar el comprimido en su mano.
4. En cuanto haya salido el comprimido, colóqueselo en la lengua.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE
FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Mantener fuera de la vista y del alcance de los niños.
7. OTRA(S) ADVERTENCIA(S) ESPECIAL(ES), SI ES NECESARIO
8. FECHA DE CADUCIDAD
EXP:
9. CONDICIONES ESPECIALES DE CONSERVACIÓN
No conservar a temperatura superior a 30°C.
Conservar en el embalaje original para protegerlo de la humedad.
10. PRECAUCIONES ESPECIALES DE ELIMINACIÓN DEL MEDICAMENTO NO UTILIZADO Y DE LOS MATERIALES DERIVADOS DE SU USO (CUANDO CORRESPONDA)
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
1 comprimido bucodispersable: EU/1/09/551/013
2 x 1 comprimido bucodispersable: EU/1/09/551/014 4 x 1 comprimido bucodispersable: EU/1/09/551/015 8 x 1 comprimido bucodispersable: EU/1/09/551/016 12 x 1 comprimido bucodispersable: EU/1/09/551/017
13. NÚMERO DE LOTE
Lot:
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
Vizarsin 25 mg comprimidos bucodispersables
INFORMACIÓN MÍNIMA A INCLUIR EN BLÍSTERES O TIRAS BLÍSTER para materiales de acondicionamiento monolingüe y bilingüe
1. NOMBRE DEL MEDICAMENTO
Vizarsin 25 mg comprimidos bucodispersables Sildenafilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA
3. FECHA DE CADUCIDAD
EXP:
4. NÚMERO DE LOTE
Lot:
5. OTROS
1. DOBLAR Y TIRAR
2. DESPEGAR
1. NOMBRE DEL MEDICAMENTO
Vizarsin 50 mg comprimidos bucodispersables Sildenafilo
2. PRINCIPIO ACTIVO
Cada comprimido bucodispersable contiene 50 mg de sildenafilo.
3. LISTA DE EXCIPIENTES
Contiene aspartamo (E951) y aroma de menta (sorbitol (E420)). Lea el prospecto para obtener más información.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
1 comprimido bucodispersable
2 x 1 comprimido bucodispersable 4 x 1 comprimido bucodispersable 8 x 1 comprimido bucodispersable 12 x 1 comprimido bucodispersable 24 x 1 comprimido bucodispersable
5. FORMA Y VÍA(S) DE ADMINISTRACIÓN
Leer el prospecto antes de utilizar este medicamento. Vía oral. Disolver en la boca.
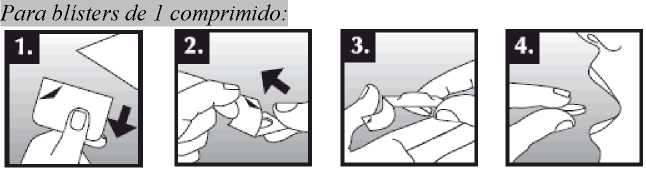
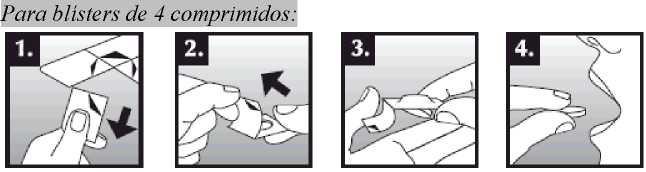
1. Sujete el blíster por los bordes y separe una de las unidades rasgando con cuidado por las marcas troqueladas.
2. Despegue completamente la hoja tirando hacia arriba del borde.
3. Voltee el blíster para colocar el comprimido en su mano.
4. En cuanto haya salido el comprimido, colóqueselo en la lengua.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE
FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Mantener fuera de la vista y del alcance de los niños.
7. OTRA(S) ADVERTENCIA(S) ESPECIAL(ES), SI ES NECESARIO
8. FECHA DE CADUCIDAD
EXP:
9. CONDICIONES ESPECIALES DE CONSERVACIÓN
No conservar a temperatura superior a 30°C.
Conservar en el embalaje original para protegerlo de la humedad.
10. PRECAUCIONES ESPECIALES DE ELIMINACIÓN DEL MEDICAMENTO NO UTILIZADO Y DE LOS MATERIALES DERIVADOS DE SU USO (CUANDO CORRESPONDA)_
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
1 comprimido bucodispersable: EU/1/09/551/018
2 x 1 comprimido bucodispersable: EU/1/09/551/019 4 x 1 comprimido bucodispersable: EU/1/09/551/020 8 x 1 comprimido bucodispersable: EU/1/09/551/021 12 x 1 comprimido bucodispersable: EU/1/09/551/022 24 x 1 comprimido bucodispersable: EU/1/09/551/028
13. NÚMERO DE LOTE
Lot:
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
Vizarsin 50 mg comprimidos bucodispersables
INFORMACIÓN MÍNIMA A INCLUIR EN BLÍSTERES O TIRAS BLÍSTER para materiales de acondicionamiento monolingüe y bilingüe
1. NOMBRE DEL MEDICAMENTO
Vizarsin 50 mg comprimidos bucodispersables Sildenafilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA
3. FECHA DE CADUCIDAD
EXP:
4. NÚMERO DE LOTE
Lot:
5. OTROS
1. DOBLAR Y TIRAR
2. DESPEGAR
1. NOMBRE DEL MEDICAMENTO
Vizarsin 100 mg comprimidos bucodispersables Sildenafilo
2. PRINCIPIO ACTIVO
Cada comprimido bucodispersable contiene 100 mg de sildenafilo.
3. LISTA DE EXCIPIENTES
Contiene aspartamo (E951) y aroma de menta (sorbitol (E420)). Lea el prospecto para obtener más información.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
1 comprimido bucodispersable
2 x 1 comprimido bucodispersable 4 x 1 comprimido bucodispersable 8 x 1 comprimido bucodispersable 12 x 1 comprimido bucodispersable 24 x 1 comprimido bucodispersable
5. FORMA Y VÍA(S) DE ADMINISTRACIÓN
Leer el prospecto antes de utilizar este medicamento. Vía oral. Disolver en la boca.
Para blísters de 1 comprimido:
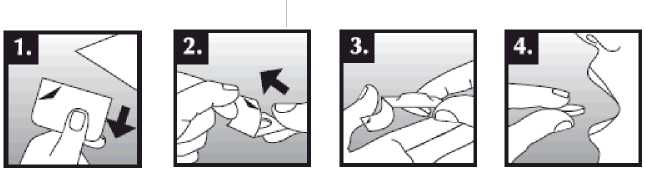
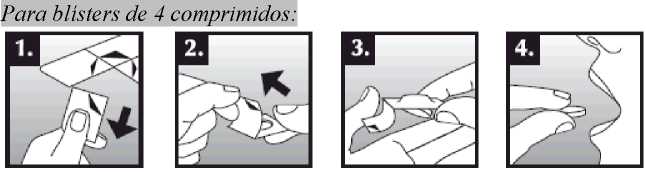
1. Sujete el blíster por los bordes y separe una de las unidades rasgando con cuidado por las marcas troqueladas.
2. Despegue completamente la hoja tirando hacia arriba del borde.
3. Voltee el blíster para colocar el comprimido en su mano.
4. En cuanto haya salido el comprimido, colóqueselo en la lengua.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE
FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Mantener fuera de la vista y del alcance de los niños.
7. OTRA(S) ADVERTENCIA(S) ESPECIAL(ES), SI ES NECESARIO
8. FECHA DE CADUCIDAD
EXP:
9. CONDICIONES ESPECIALES DE CONSERVACIÓN
No conservar a temperatura superior a 30°C.
Conservar en el embalaje original para protegerlo de la humedad.
10. PRECAUCIONES ESPECIALES DE ELIMINACIÓN DEL MEDICAMENTO NO UTILIZADO Y DE LOS MATERIALES DERIVADOS DE SU USO (CUANDO CORRESPONDA)
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
1 comprimido bucodispersable: EU/1/09/551/023
2 x 1 comprimido bucodispersable: EU/1/09/551/024 4 x 1 comprimido bucodispersable: EU/1/09/551/025 8 x 1 comprimido bucodispersable: EU/1/09/551/026 12 x 1 comprimido bucodispersable: EU/1/09/551/027 24 x 1 comprimido bucodispersable: EU/1/09/551/029
13. NÚMERO DE LOTE
Lot:
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
Vizarsin 100 mg comprimidos bucodispersables
INFORMACIÓN MÍNIMA A INCLUIR EN BLÍSTERES O TIRAS BLÍSTER para materiales de acondicionamiento monolingüe y bilingüe
1. NOMBRE DEL MEDICAMENTO
Vizarsin 100 mg comprimidos bucodispersables Sildenafilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA
3. FECHA DE CADUCIDAD
EXP:
4. NÚMERO DE LOTE
Lot:
5. OTROS
1. DOBLAR Y TIRAR
2. DESPEGAR
INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR CARTÓN para materiales de acondicionamiento trilingüe 1. NOMBRE DEL MEDICAMENTO
Vizarsin 25 mg comprimidos bucodispersables Sildenafilo
2. PRINCIPIO ACTIVO
Cada comprimido bucodispersable contiene 25 mg de sildenafilo.
3. LISTA DE EXCIPIENTES
Contiene aspartamo (E951) y aroma de menta (sorbitol (E420)). Lea el prospecto para obtener más información.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
1 comprimido bucodispersable
2 x 1 comprimido bucodispersable 4 x 1 comprimido bucodispersable 8 x 1 comprimido bucodispersable 12 x 1 comprimido bucodispersable
5. FORMA Y VÍA(S) DE ADMINISTRACIÓN
Vía oral.
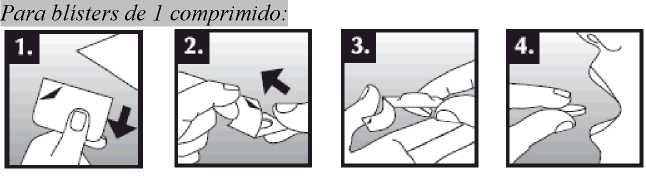
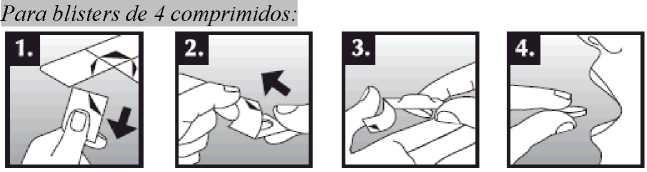
1. Sujete el blíster por los bordes y separe una de las unidades rasgando con cuidado por las marcas troqueladas.
2. Despegue completamente la hoja tirando hacia arriba del borde.
3. Coloque el comprimido en su mano y después en la lengua.
4. Disolver en la boca.
Mantener fuera de la vista y del alcance de los niños.
7. OTRA(S) ADVERTENCIA(S) ESPECIAL(ES), SI ES NECESARIO
8. FECHA DE CADUCIDAD
EXP:
9. CONDICIONES ESPECIALES DE CONSERVACIÓN
No conservar a temperatura superior a 30°C.
Conservar en el embalaje original para protegerlo de la humedad.
10. PRECAUCIONES ESPECIALES DE ELIMINACIÓN DEL MEDICAMENTO NO UTILIZADO Y DE LOS MATERIALES DERIVADOS DE SU USO (CUANDO CORRESPONDA)
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
1 comprimido bucodispersable: EU/1/09/551/013
2 x 1 comprimido bucodispersable: EU/1/09/551/014 4 x 1 comprimido bucodispersable: EU/1/09/551/015 8 x 1 comprimido bucodispersable: EU/1/09/551/016 12 x 1 comprimido bucodispersable: EU/1/09/551/017
13. NÚMERO DE LOTE
Lot:
14. CONDICIONES GENERALES DE DISPENSACIÓN
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
Vizarsin 25 mg comprimidos bucodispersables
INFORMACIÓN MÍNIMA A INCLUIR EN BLÍSTERES O TIRAS BLÍSTER para materiales de acondicionamiento trilingüe
1. NOMBRE DEL MEDICAMENTO
Vizarsin 25 mg comprimidos bucodispersables Sildenafilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA
3. FECHA DE CADUCIDAD
EXP:
4. NÚMERO DE LOTE
Lot:
5. OTROS
1. Tirar
2. Despegar
1. NOMBRE DEL MEDICAMENTO
Vizarsin 50 mg comprimidos bucodispersables Sildenafilo
2. PRINCIPIO ACTIVO
Cada comprimido bucodispersable contiene 50 mg de sildenafilo.
3. LISTA DE EXCIPIENTES
Contiene aspartamo (E951) y aroma de menta (sorbitol (E420)). Lea el prospecto para obtener más información.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
1 comprimido bucodispersable
2 x 1 comprimido bucodispersable 4 x 1 comprimido bucodispersable 8 x 1 comprimido bucodispersable 12 x 1 comprimido bucodispersable 24 x 1 comprimido bucodispersable
5. FORMA Y VÍA(S) DE ADMINISTRACIÓN
Vía oral.
Para blísters de 1 comprimido:
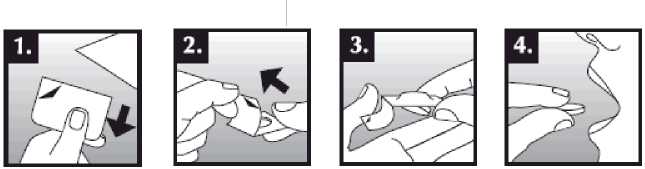
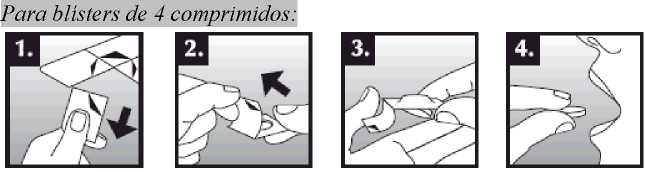
1. Sujete el blíster por los bordes y separe una de las unidades rasgando con cuidado por las marcas troqueladas.
2.
3.
4.
Despegue completamente la hoja tirando hacia arriba del borde.
Coloque el comprimido en su mano y después en la lengua.
Disolver en la boca.
Mantener fuera de la vista y del alcance de los niños.
7. OTRA(S) ADVERTENCIA(S) ESPECIAL(ES), SI ES NECESARIO
8. FECHA DE CADUCIDAD
EXP:
9. CONDICIONES ESPECIALES DE CONSERVACIÓN
No conservar a temperatura superior a 30°C.
Conservar en el embalaje original para protegerlo de la humedad.
10. PRECAUCIONES ESPECIALES DE ELIMINACIÓN DEL MEDICAMENTO NO UTILIZADO Y DE LOS MATERIALES DERIVADOS DE SU USO (CUANDO CORRESPONDA)
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
1 comprimido bucodispersable: EU/1/09/551/018
2 x 1 comprimido bucodispersable: EU/1/09/551/019 4 x 1 comprimido bucodispersable: EU/1/09/551/020 8 x 1 comprimido bucodispersable: EU/1/09/551/021 12 x 1 comprimido bucodispersable: EU/1/09/551/022 24 x 1 comprimido bucodispersable: EU/1/09/551/028
13. NÚMERO DE LOTE
Lot:
14. CONDICIONES GENERALES DE DISPENSACIÓN
15. INSTRUCCIONES DE USO
Vizarsin 50 mg comprimidos bucodispersables
INFORMACIÓN MÍNIMA A INCLUIR EN BLÍSTERES O TIRAS BLÍSTER para materiales de acondicionamiento trilingüe
1. NOMBRE DEL MEDICAMENTO
Vizarsin 50 mg comprimidos bucodispersables Sildenafilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA
3. FECHA DE CADUCIDAD
EXP:
4. NÚMERO DE LOTE
Lot:
5. OTROS
1. Tirar
2. Despegar
1. NOMBRE DEL MEDICAMENTO
Vizarsin 100 mg comprimidos bucodispersables Sildenafilo
2. PRINCIPIO ACTIVO
Cada comprimido bucodispersable contiene 100 mg de sildenafilo.
3. LISTA DE EXCIPIENTES
Contiene aspartamo (E951) y aroma de menta (sorbitol (E420)). Lea el prospecto para obtener más información.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
1 comprimido bucodispersable
2 x 1 comprimido bucodispersable 4 x 1 comprimido bucodispersable 8 x 1 comprimido bucodispersable 12 x 1 comprimido bucodispersable 24 x 1 comprimido bucodispersable
5. FORMA Y VÍA(S) DE ADMINISTRACIÓN
Vía oral.
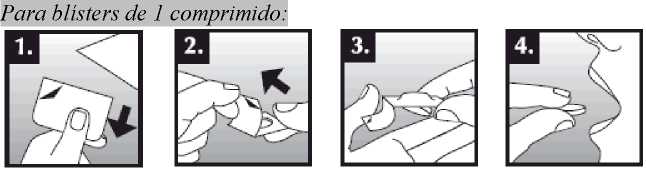
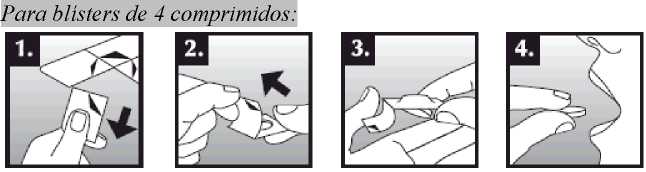
1. Sujete el blíster por los bordes y separe una de las unidades rasgando con cuidado por las marcas troqueladas.
2. Despegue completamente la hoja tirando hacia arriba del borde.
3. Coloque el comprimido en su mano y después en la lengua.
4. Disolver en la boca.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE
FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Mantener fuera de la vista y del alcance de los niños.
7. OTRA(S) ADVERTENCIA(S) ESPECIAL(ES), SI ES NECESARIO
8. FECHA DE CADUCIDAD
EXP:
9. CONDICIONES ESPECIALES DE CONSERVACIÓN
No conservar a temperatura superior a 30°C.
Conservar en el embalaje original para protegerlo de la humedad.
10. PRECAUCIONES ESPECIALES DE ELIMINACIÓN DEL MEDICAMENTO NO UTILIZADO Y DE LOS MATERIALES DERIVADOS DE SU USO (CUANDO CORRESPONDA)_
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
1 comprimido bucodispersable: EU/1/09/551/023
2 x 1 comprimido bucodispersable: EU/1/09/551/024 4 x 1 comprimido bucodispersable: EU/1/09/551/025 8 x 1 comprimido bucodispersable: EU/1/09/551/026 12 x 1 comprimido bucodispersable: EU/1/09/551/027 24 x 1 comprimido bucodispersable: EU/1/09/551/029
13. NÚMERO DE LOTE
Lot:
14. CONDICIONES GENERALES DE DISPENSACIÓN
15. INSTRUCCIONES DE USO
Vizarsin 100 mg comprimidos bucodispersables
INFORMACIÓN MÍNIMA A INCLUIR EN BLÍSTERES O TIRAS BLÍSTER para materiales de acondicionamiento trilingüe
1. NOMBRE DEL MEDICAMENTO
Vizarsin 100 mg comprimidos bucodispersables Sildenafilo
2. NOMBRE DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
KRKA
3. FECHA DE CADUCIDAD
EXP:
4. NÚMERO DE LOTE
Lot:
5. OTROS
1. Tirar
2. Despegar
B. PROSPECTO
Prospecto: información para el usuario
Vizarsin 25 mg comprimidos recubiertos con película
Sildenafilo
Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto:
1. Qué es Vizarsin y para qué se utiliza
2. Qué necesita saber antes de empezar a tomar Vizarsin
3. Cómo tomar Vizarsin
4. Posibles efectos adversos
5 Conservación de Vizarsin
6. Contenido del envase e información adicional
1. Qué es Vizarsin y para qué se utiliza
Vizarsin contiene el principio activo sildenafilo, que pertenece a un grupo de medicamentos denominados inhibidores de la fosfodiesterasa tipo 5 (PDE5). Actúa dilatando los vasos sanguíneos del pene, permitiendo la afluencia de sangre cuando se está sexualmente estimulado. Vizarsin sólo le ayudará a conseguir una erección si se encuentra sexualmente estimulado.
Vizarsin está indicado en el tratamiento de la disfunción eréctil en hombres adultos, a veces denominada impotencia. Esto sucede cuando un varón no puede obtener o mantener una erección firme, adecuada para una actividad sexual satisfactoria.
2. Qué necesita saber antes de empezar a tomar Vizarsin
No tome Vizarsin
- Si es alérgico al sildenafilo o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
- Si está tomando unos medicamentos llamados nitratos, ya que la combinación puede dar lugar a una disminución peligrosa de su presión sanguínea. Consulte con su médico si está tomando cualquiera de estos medicamentos, que a menudo, se administran para aliviar el dolor de angina de pecho (o “dolor de pecho”). Si no está seguro, consulte con su médico o farmacéutico.
- Si está utilizando cualquiera de los medicamentos denominados dadores de óxido nítrico tales como nitrato de amilo (“poppers”), ya que la combinación puede dar lugar a una disminución peligrosa de su presión sanguínea.
- Si está tomando riociguat. Este medicamento se utiliza para tratar la hipertensión arterial pulmonar (es decir, tensión alta en los pulmones) y la hipertensión pulmonar tromboembólica crónica (es decir, tensión alta en los pulmones provocada por coágulos). Los inhibidores de la PDE5, como Vizarsin, han mostrado que producen un incremento del efecto hipotensivo de este medicamento. Si está tomando riociguat o no está seguro consulte a su médico.
- Si tiene un problema grave de corazón o hígado.
- Si ha padecido recientemente un accidente isquémico cerebral o ataque al corazón o si tiene la tensión arterial baja.
- Si padece una rara enfermedad ocular hereditaria (tal como retinitis pigmentosa).
- Si ha experimentado anteriormente una pérdida de la visión debido a una neuropatía óptica
isquémica anterior no arterítica (NOIA-NA).
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a tomar Vizarsin:
- Si padece anemia falciforme (una anormalidad de los glóbulos rojos), leucemia (cáncer de las células sanguíneas), mieloma múltiple (cáncer de médula ósea).
- Si padece una deformidad del pene o enfermedad de Peyronie.
- Si padece problemas del corazón. Su médico debe comprobar cuidadosamente si su corazón
puede soportar el esfuerzo adicional de mantener relaciones sexuales.
- Si padece actualmente úlcera de estómago o problemas hemorrágicos (tales como hemofilia).
- Si experimenta una disminución o pérdida repentina de la visión, deje de tomar Vizarsin y
contacte con su médico inmediatamente.
No se aconseja utilizar Vizarsin simultáneamente con ningún otro tratamiento oral o local para la disfunción eréctil.
No debe tomar Vizarsin con tratamientos para la hipertensión arterial pulmonar (HAP) que contengan sildenafilo o cualquier otro inhibidor de la PDE5.
No debe tomar Vizarsin si no tiene disfunción eréctil.
El uso de Vizarsin no está indicado en mujeres.
Consideraciones especiales en pacientes con problemas renales o hepáticos
Debe comunicar a su médico si tiene problemas renales o hepáticos. Su médico puede decidir reducirle la dosis.
Niños y adolescentes
El uso de Vizarsin no está indicado en personas menores de 18 años.
Uso de Vizarsin con otros medicamentos
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
Los comprimidos de Vizarsin pueden interferir con algunos medicamentos, especialmente los utilizados para tratar el dolor de pecho. En caso de una urgencia médica, debe informar a su médico, farmacéutico o enfermero que está tomando Vizarsin y cuando lo tomó. No debe tomar Vizarsin con otros medicamentos a menos que su médico se lo aconseje.
No debe tomar Vizarsin si está tomando medicamentos denominados nitratos, ya que la combinación de estos medicamentos puede dar lugar a un descenso peligroso de su presión sanguínea. Siempre informe a su médico, farmacéutico o enfermero si está tomando cualquiera de estos medicamentos, que a menudo, se utilizan para aliviar el dolor de la angina de pecho (o “dolor de pecho”).
No debe tomar Vizarsin si está tomando medicamentos denominados dadores de óxido nítrico, tales como nitrito de amilo (“poppers”), ya que la combinación de estos medicamentos también puede dar lugar a un descenso peligroso de su presión sanguínea.
Informe a su médico o farmacéutico si está tomando riociguat.
Si está tomando medicamentos conocidos como inhibidores de la proteasa, como los utilizados en el tratamiento del VIH, su médico puede recomendarle que comience el tratamiento con la dosis más baja (25 mg) de Vizarsin.
Algunos pacientes que están recibiendo un alfabloqueante, medicamento utilizado para el tratamiento de la presión arterial alta o de la hipertrofia prostática, pueden experimentar mareos o sensación de vahído que pueden ser causados por una disminución de la tensión arterial al sentarse o levantarse rápidamente. Algunos pacientes han experimentado estos síntomas al tomar Vizarsin con alfabloqueantes. Esto es más probable que suceda en las 4 horas siguientes a la toma de Vizarsin. Con el fin de disminuir la probabilidad de que ocurran estos síntomas, deberá estar recibiendo su dosis diaria del alfabloqueante de forma regular antes de comenzar con Vizarsin. Su médico puede indicarle que comience el tratamiento con la dosis inferior (25 mg) de Vizarsin.
Uso de Vizarsin con alimentos, bebidas y alcohol
Vizarsin puede tomarse con o sin alimentos. Sin embargo, puede notar que Vizarsin tarde un poco más en hacer efecto si se ingiere con una comida copiosa.
La ingesta de alcohol puede dificultar, temporalmente, la capacidad para obtener una erección. Por lo tanto, para conseguir el máximo beneficio del medicamento, se aconseja no ingerir grandes cantidades de alcohol antes de tomar Vizarsin.
Embarazo, lactancia y fertilidad
El uso de Vizarsin no está indicado en mujeres.
Conducción y uso de máquinas
Vizarsin puede producir mareos y afectar a la visión. Debe saber cómo reacciona usted a Vizarsin antes de conducir vehículos o utilizar maquinaria.
Vizarsin contiene lactosa
Si su médico le ha indicado que padece una intolerancia a ciertos azúcares, consulte con él antes de tomar este medicamento.
3. Cómo tomar Vizarsin
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
La dosis recomendada de inicio es 50 mg.
No se debe tomar Vizarsin más de una vez al día.
Debe tomar Vizarsin aproximadamente una hora antes de que planee tener relaciones sexuales. Trague el comprimido entero con un vaso de agua.
Si nota que la acción de Vizarsin es demasiado fuerte o débil, comuníqueselo a su médico o farmacéutico.
Vizarsin sólo le ayudará a conseguir una erección si se encuentra sexualmente estimulado. El tiempo que necesita Vizarsin para hacer efecto varía de una persona a otra, generalmente oscila entre media y una hora. El efecto de Vizarsin puede retrasarse si lo toma con una comida copiosa.
En el caso de que Vizarsin no le ayude a conseguir una erección o si la erección no se mantiene el
tiempo suficiente para completar el acto sexual, consulte a su médico.
Si toma más Vizarsin del que debe
Puede experimentar un incremento en los efectos adversos y su gravedad. Dosis superiores a 100 mg no aumentan la eficacia.
No debe tomar más comprimidos de los recomendados por el médico.
Contacte con su médico si ha tomado más comprimidos de los aconsejados.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran. Los efectos adversos notificados asociados al uso de Vizarsin son por lo general de intensidad leve a moderada y de corta duración.
Si experimenta cualquiera de los siguientes efectos adversos graves, deje de tomar Vizarsin y busque atención médica inmediatamente:
- Reacción alérgica - esto ocurre con poca frecuencia (puede afectar hasta 1 de cada 100 personas).
Los síntomas incluyen silbido repentino al respirar, dificultad para respirar o mareo, hinchazón de los párpados, cara, labios o garganta.
- Dolores en el pecho - esto ocurre con poca frecuencia.
Si aparecen durante o después de mantener relaciones sexuales:
- Sitúese en una posición semisentada e intente relajarse.
- No use nitratos para tratar el dolor en el pecho.
- Erecciones prolongadas y a veces dolorosas - esto ocurre raramente (puede afectar hasta 1 de cada 1.000 personas).
Si usted tiene una erección que dura más de 4 horas, debe contactar con su médico inmediatamente.
- Disminución repentina o pérdida de la visión - esto ocurre raramente.
- Reacciones graves de la piel - esto ocurre raramente.
Los síntomas pueden incluir descamación grave e hinchazón de la piel, vesiculación bucal, de los genitales y alrededor de los ojos, además de fiebre.
- Convulsiones o ataques - esto ocurre raramente.
Otros efectos adversos:
Muy frecuentes (pueden afectar a más de 1 de cada 10 personas): dolor de cabeza.
Frecuentes (pueden afectar hasta 1 de cada 10 personas): náuseas, enrojecimiento facial, acaloramiento (entre los síntomas se incluye la sensación de calor repentina en la parte superior del cuerpo), indigestión, percepción anormal del color, visión borrosa, deterioro visual, congestión nasal y mareos.
Poco frecuentes (pueden afectar hasta 1 de cada 100 personas): vómitos, erupciones cutáneas, irritación ocular, derrame ocular/ojos rojos, dolor ocular, visión de luces parpadeantes, claridad visual, sensibilidad a la luz, ojos llorosos, palpitaciones, latido cardíaco rápido, presión arterial alta, presión arterial baja, dolor muscular, sensación de somnolencia, sensación al tacto reducido, vértigo, pitidos en los oídos, boca seca, bloqueo o congestión de los senos nasales, inflamación de la mucosa de la nariz (entre los síntomas se incluyen moqueo, estornudos y congestión nasal), dolor en la zona superior del abdomen, enfermedad por reflujo gastroesofágico (entre los síntomas se encuentra el ardor de estómago), sangre presente en orina, dolor en brazos o piernas, sangrado de la nariz, sensación de calor y sensación de cansancio.
Raros (pueden afectar hasta 1 de cada 1.000 personas): desvanecimiento, accidente cerebrovascular, ataque cardíaco, latido cardíaco irregular, disminución transitoria del flujo sanguíneo a algunas partes del cerebro, sensación de opresión en la garganta, adormecimiento de la boca, sangrado en la parte posterior del ojo, visión doble, disminución de la agudeza visual, sensación anormal en el ojo, hinchazón ocular o del párpado, pequeñas partículas o manchas en la vista, visión de halos alrededor de las luces, dilatación de la pupila del ojo, cambio de color de la parte blanca del ojo, sangrado del pene, presencia de sangre en el semen, nariz seca, hinchazón del interior de la nariz, sensación de irritabilidad y disminución o pérdida repentina de la audición.
Durante la experiencia postcomercialización se han comunicado raramente casos de angina inestable (enfermedad cardíaca) y muerte súbita. Cabe destacar que la mayoría de los hombres que experimentaron estos efectos adversos, aunque no todos ellos, tenía problemas cardíacos antes de tomar este medicamento. No es posible determinar si estos efectos adversos estuvieron relacionados directamente con Vizarsin.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Vizarsin
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en el blíster y en la caja después de EXP. La fecha de caducidad es el último día del mes que se indica.
Este medicamento no requiere condiciones especiales de conservación.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional Composición de Vizarsin
- El principio activo es sidenafilo. Cada comprimido recubierto con película contiene sildenafilo citrato equivalente a 25 mg de sildenafilo.
- Los demás componentes son:
Núcleo del comprimido: celulosa microcristalina (E460), fosfato cálcico hidrogenado anhidro,
croscarmelosa sódica, hipromelosa (E464), estearato magnésico (E572).
Cubierta pelicular: lactosa monohidrato, hipromelosa (E464), dióxido de titanio (E171),
triacetina (E1518).
Aspecto del Vizarsin y contenido del envase
Vizarsin 25 mg comprimidos recubiertos con película son blancos, oblongos y llevan grabado “25” en una cara.
Vizarsin 25 mg comprimidos recubiertos con película están disponibles en cajas de 1 comprimido recubierto con película en blíster y también en cajas de 4 x 1, 8 x 1 o 12 x 1 comprimido recubierto con película en blísters perforados unidosis.
Puede que solamente estén comercializados algunos tamaños de envase.
Titular de la autorización de comercialización y responsable de la fabricación
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Belgie/Belgique/Belgien
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091
Etarapna
KPKA Etarapna EOOfl Tea.: + 359 (02) 962 34 50
Ceská republika KRKA CR, s.r.o.
Tel: + 420 (0) 221 115 150
Danmark
KRKA Sverige AB
Tlf: + 46 (0)8 643 67 66 (SE)
Deutschland
TAD Pharma GmbH Tel: + 49 (0) 4721 606-0
Eesti
KRKA, d.d., Novo mesto Eesti filiaal Tel: + 372 (0) 6 671 658
EXláSa
QUALIA PHARMA S.A.
T^: +30 (0)210 2832941
España
KERN PHARMA, S.L.
Tel: + 34 93 700 25 25
Lietuva
UAB KRKA Lietuva Tel: + 370 5 236 27 40
Luxembourg/Luxemburg
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091 (BE)
Magyarország
KRKA Magyarország Kereskedelmi Kft. Tel.: + 361 (0) 355 8490
Malta
E. J. Busuttil Ltd.
Tel: + 356 21 445 885
Nederland
KRKA Belgium, SA.
Tel: +32 (0) 489 304 091 (BE)
Norge
KRKA Sverige AB
Tlf: + 46 (0)8 643 67 66 (SE)
Osterreich
KRKA Pharma GmbH, Wien Tel: + 43 (0)1 66 24 300
Polska
KRKA-POLSKA Sp. z o.o.
Tel.: + 48 (0)22 573 7500
France
KRKA France Eurl Tél: + 33 (0)1 57 40 82 25
Hrvatska
KRKA - FARMA d.o.o. Tel: + 385 1 6312 100
Portugal
KRKA Farmacéutica, Sociedade Unipessoal Lda. Tel: + 351 (0)21 46 43 650
Romania
KRKA Romania S.R.L., Bucharest Tel: + 4 021 310 66 05
Ísland
KRKA Sverige AB
Sími: + 46 (0)8 643 67 66 (SE)
Italia
KRKA Farmaceutici Milano S.r.l. Tel: + 39 02 3300 8841
Kúnpoq
Kipa Pharmacal Ltd.
T^: + 357 24 651 882
Latvija
KRKA Latvija SIA Tel: + 371 6 733 86 10
Slovenská republika
KRKA Slovensko, s.r.o.
Tel: + 421 (0) 2 571 04 501
Suomi/Finland
KRKA Finland Oy Puh/Tel: +358 20 754 5330
Sverige
KRKA Sverige AB
Tel: + 46 (0)8 643 67 66 (SE)
United Kingdom
Consilient Health (UK) Ltd. Tel: + 44(0)203 751 1888
Fecha de la última revisión de este prospecto:
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu.
Prospecto: información para el usuario
Vizarsin 50 mg comprimidos recubiertos con película
Sildenafilo
Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto:
1. Qué es Vizarsin y para qué se utiliza
2. Qué necesita saber antes de empezar a tomar Vizarsin
3. Cómo tomar Vizarsin
4. Posibles efectos adversos
5 Conservación de Vizarsin
6. Contenido del envase e información adicional
1. Qué es Vizarsin y para qué se utiliza
Vizarsin contiene el principio activo sildenafilo, que pertenece a un grupo de medicamentos denominados inhibidores de la fosfodiesterasa tipo 5 (PDE5). Actúa dilatando los vasos sanguíneos del pene, permitiendo la afluencia de sangre cuando se está sexualmente estimulado. Vizarsin sólo le ayudará a conseguir una erección si se encuentra sexualmente estimulado.
Vizarsin está indicado en el tratamiento de la disfunción eréctil en hombres adultos, a veces denominada impotencia. Esto sucede cuando un varón no puede obtener o mantener una erección firme, adecuada para una actividad sexual satisfactoria.
2. Qué necesita saber antes de empezar a tomar Vizarsin
No tome Vizarsin
- Si es alérgico al sildenafilo o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
- Si está tomando unos medicamentos llamados nitratos, ya que la combinación puede dar lugar a una disminución peligrosa de su presión sanguínea. Consulte con su médico si está tomando cualquiera de estos medicamentos, que a menudo, se administran para aliviar el dolor de angina de pecho (o “dolor de pecho”). Si no está seguro, consulte con su médico o farmacéutico.
- Si está utilizando cualquiera de los medicamentos denominados dadores de óxido nítrico tales como nitrato de amilo (“poppers”), ya que la combinación puede dar lugar a una disminución peligrosa de su presión sanguínea.
Si está tomando riociguat. Este medicamento se utiliza para tratar la hipertensión arterial pulmonar (es decir, tensión alta en los pulmones) y la hipertensión pulmonar tromboembólica crónica (es decir, tensión alta en los pulmones provocada por coágulos). Los inhibidores de la PDE5, como Vizarsin, han mostrado que producen un incremento del efecto hipotensivo de este medicamento. Si está tomando riociguat o no está seguro consulte a su médico.
- Si tiene un problema grave de corazón o hígado.
- Si ha padecido recientemente un accidente isquémico cerebral o ataque al corazón o si tiene la tensión arterial baja.
- Si padece una rara enfermedad ocular hereditaria (tal como retinitis pigmentosa).
- Si ha experimentado anteriormente una pérdida de la visión debido a una neuropatía óptica
isquémica anterior no arterítica (NOIA-NA).
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a tomar Vizarsin:
- Si padece anemia falciforme (una anormalidad de los glóbulos rojos), leucemia (cáncer de las células sanguíneas), mieloma múltiple (cáncer de médula ósea).
- Si padece una deformidad del pene o enfermedad de Peyronie.
- Si padece problemas del corazón. Su médico debe comprobar cuidadosamente si su corazón puede soportar el esfuerzo adicional de mantener relaciones sexuales.
- Si padece actualmente úlcera de estómago o problemas hemorrágicos (tales como hemofilia).
- Si experimenta una disminución o pérdida repentina de la visión, deje de tomar Vizarsin y
contacte con su médico inmediatamente.
No se aconseja utilizar Vizarsin simultáneamente con ningún otro tratamiento oral o local para la disfunción eréctil.
No debe tomar Vizarsin con tratamientos para la hipertensión arterial pulmonar (HAP) que contengan sildenafilo o cualquier otro inhibidor de la PDE5.
No debe tomar Vizarsin si no tiene disfunción eréctil.
El uso de Vizarsin no está indicado en mujeres.
Consideraciones especiales en pacientes con problemas renales o hepáticos
Debe comunicar a su médico si tiene problemas renales o hepáticos. Su médico puede decidir reducirle la dosis.
Niños y adolescentes
El uso de Vizarsin no está indicado en personas menores de 18 años.
Uso de Vizarsin con otros medicamentos
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
Los comprimidos de Vizarsin pueden interferir con algunos medicamentos, especialmente los utilizados para tratar el dolor de pecho. En caso de una urgencia médica, debe informar a su médico, farmacéutico o enfermero que está tomando Vizarsin y cuando lo tomó. No debe tomar Vizarsin con otros medicamentos a menos que su médico se lo aconseje.
No debe tomar Vizarsin si está tomando medicamentos denominados nitratos, ya que la combinación de estos medicamentos puede dar lugar a un descenso peligroso de su presión sanguínea. Siempre informe a su médico, farmacéutico o enfermero si está tomando cualquiera de estos medicamentos, que a menudo, se utilizan para aliviar el dolor de la angina de pecho (o “dolor de pecho”).
No debe tomar Vizarsin si está tomando medicamentos denominados dadores de óxido nítrico, tales
como nitrito de amilo (“poppers”), ya que la combinación de estos medicamentos también puede dar lugar a un descenso peligroso de su presión sanguínea.
Informe a su médico o farmacéutico si está tomando riociguat.
Si está tomando medicamentos conocidos como inhibidores de la proteasa, como los utilizados en el tratamiento del VIH, su médico puede recomendarle que comience el tratamiento con la dosis más baja (25 mg) de Vizarsin.
Algunos pacientes que están recibiendo un alfabloqueante, medicamento utilizado para el tratamiento de la presión arterial alta o de la hipertrofia prostática, pueden experimentar mareos o sensación de vahído que pueden ser causados por una disminución de la tensión arterial al sentarse o levantarse rápidamente. Algunos pacientes han experimentado estos síntomas al tomar Vizarsin con alfabloqueantes. Esto es más probable que suceda en las 4 horas siguientes a la toma de Vizarsin. Con el fin de disminuir la probabilidad de que ocurran estos síntomas, deberá estar recibiendo su dosis diaria del alfabloqueante de forma regular antes de comenzar con Vizarsin. Su médico puede indicarle que comience el tratamiento con la dosis inferior (25 mg) de Vizarsin.
Uso de Vizarsin con alimentos, bebidas y alcohol
Vizarsin puede tomarse con o sin alimentos. Sin embargo, puede notar que Vizarsin tarde un poco más en hacer efecto si se ingiere con una comida copiosa.
La ingesta de alcohol puede dificultar, temporalmente, la capacidad para obtener una erección. Por lo tanto, para conseguir el máximo beneficio del medicamento, se aconseja no ingerir grandes cantidades de alcohol antes de tomar Vizarsin.
Embarazo, lactancia y fertilidad
El uso de Vizarsin no está indicado en mujeres.
Conducción y uso de máquinas
Vizarsin puede producir mareos y afectar a la visión. Debe saber cómo reacciona usted a Vizarsin antes de conducir vehículos o utilizar maquinaria.
Vizarsin contiene lactosa
Si su médico le ha indicado que padece una intolerancia a ciertos azúcares, consulte con él antes de tomar este medicamento.
3. Cómo tomar Vizarsin
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
La dosis recomendada de inicio es 50 mg.
No se debe tomar Vizarsin más de una vez al día.
Debe tomar Vizarsin aproximadamente una hora antes de que planee tener relaciones sexuales. Trague el comprimido entero con un vaso de agua.
Si nota que la acción de Vizarsin es demasiado fuerte o débil, comuníqueselo a su médico o farmacéutico.
Vizarsin sólo le ayudará a conseguir una erección si se encuentra sexualmente estimulado. El tiempo que necesita Vizarsin para hacer efecto varía de una persona a otra, generalmente oscila entre media y una hora. El efecto de Vizarsin puede retrasarse si lo toma con una comida copiosa.
En el caso de que Vizarsin no le ayude a conseguir una erección o si la erección no se mantiene el tiempo suficiente para completar el acto sexual, consulte a su médico.
Si toma más Vizarsin del que debe
Puede experimentar un incremento en los efectos adversos y su gravedad. Dosis superiores a 100 mg no aumentan la eficacia.
No debe tomar más comprimidos de los recomendados por el médico.
Contacte con su médico si ha tomado más comprimidos de los aconsejados.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran. Los efectos adversos notificados asociados al uso de Vizarsin son por lo general de intensidad leve a moderada y de corta duración.
Si experimenta cualquiera de los siguientes efectos adversos graves, deje de tomar Vizarsin y busque atención médica inmediatamente:
- Reacción alérgica - esto ocurre con poca frecuencia (puede afectar hasta 1 de cada 100 personas).
Los síntomas incluyen silbido repentino al respirar, dificultad para respirar o mareo, hinchazón de los párpados, cara, labios o garganta.
- Dolores en el pecho - esto ocurre con poca frecuencia.
Si aparecen durante o después de mantener relaciones sexuales:
- Sitúese en una posición semisentada e intente relajarse.
- No use nitratos para tratar el dolor en el pecho.
- Erecciones prolongadas y a veces dolorosas - esto ocurre raramente (puede afectar hasta 1 de cada 1.000 personas).
Si usted tiene una erección que dura más de 4 horas, debe contactar con su médico inmediatamente.
- Disminución repentina o pérdida de la visión - esto ocurre raramente.
- Reacciones graves de la piel - esto ocurre raramente.
Los síntomas pueden incluir descamación grave e hinchazón de la piel, vesiculación bucal, de los genitales y alrededor de los ojos, además de fiebre.
- Convulsiones o ataques - esto ocurre raramente.
Otros efectos adversos:
Muy frecuentes (pueden afectar a más de 1 de cada 10 personas): dolor de cabeza.
Frecuentes (pueden afectar hasta 1 de cada 10 personas): náuseas, enrojecimiento facial, acaloramiento (entre los síntomas se incluye la sensación de calor repentina en la parte superior del cuerpo), indigestión, percepción anormal del color, visión borrosa, deterioro visual, congestión nasal y mareos.
Poco frecuentes (pueden afectar hasta 1 de cada 100 personas): vómitos, erupciones cutáneas, irritación ocular, derrame ocular/ojos rojos, dolor ocular, visión de luces parpadeantes, claridad visual, sensibilidad a la luz, ojos llorosos, palpitaciones, latido cardíaco rápido, presión arterial alta, presión arterial baja, dolor muscular, sensación de somnolencia, sensación al tacto reducido, vértigo, pitidos en los oídos, boca seca, bloqueo o congestión de los senos nasales, inflamación de la mucosa de la nariz (entre los síntomas se incluyen moqueo, estornudos y congestión nasal), dolor en la zona superior del abdomen, enfermedad por reflujo gastroesofágico (entre los síntomas se encuentra el ardor de estómago), sangre presente en orina, dolor en brazos o piernas, sangrado de la nariz, sensación de calor y sensación de cansancio.
Raros (pueden afectar hasta 1 de cada 1.000 personas):): desvanecimiento, accidente cerebrovascular, ataque cardíaco, latido cardíaco irregular, disminución transitoria del flujo sanguíneo a algunas partes del cerebro, sensación de opresión en la garganta, adormecimiento de la boca, sangrado en la parte posterior del ojo, visión doble, disminución de la agudeza visual, sensación anormal en el ojo, hinchazón ocular o del párpado, pequeñas partículas o manchas en la vista, visión de halos alrededor de las luces, dilatación de la pupila del ojo, cambio de color de la parte blanca del ojo, sangrado del pene, presencia de sangre en el semen, nariz seca, hinchazón del interior de la nariz, sensación de irritabilidad y disminución o pérdida repentina de la audición.
Durante la experiencia postcomercialización se han comunicado raramente casos de angina inestable (enfermedad cardíaca) y muerte súbita. Cabe destacar que la mayoría de los hombres que experimentaron estos efectos adversos, aunque no todos ellos, tenía problemas cardíacos antes de tomar este medicamento. No es posible determinar si estos efectos adversos estuvieron relacionados directamente con Vizarsin.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Vizarsin
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en el blíster y en la caja después de EXP. La fecha de caducidad es el último día del mes que se indica.
Este medicamento no requiere condiciones especiales de conservación.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional Composición de Vizarsin
- El principio activo es sidenafilo. Cada comprimido recubierto con película contiene sildenafilo citrato equivalente a 50 mg de sildenafilo.
- Los demás componentes son:
Núcleo del comprimido: celulosa microcristalina (E460), fosfato cálcico hidrogenado anhidro,
croscarmelosa sódica, hipromelosa (E464), estearato magnésico (E572).
Cubierta pelicular: lactosa monohidrato, hipromelosa (E464), dióxido de titanio (E171),
triacetina (E1518).
Aspecto del Vizarsin y contenido del envase
Vizarsin 50 mg comprimidos recubiertos con película son blancos, oblongos y llevan grabado “50” en una cara.
Vizarsin 50 mg comprimidos recubiertos con película están disponibles en cajas de 1 comprimido recubierto con película en blíster y también en cajas de 4 x 1, 8 x 1 o 12 x 1 comprimido recubierto con película en blísters perforados unidosis.
Puede que solamente estén comercializados algunos tamaños de envase.
Titular de la autorización de comercialización y responsable de la fabricación
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Belgie/Belgique/Belgien
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091
Etarapna
KPKA Etarapna EOOfl Tea.: + 359 (02) 962 34 50
Ceská republika KRKA CR, s.r.o.
Tel: + 420 (0) 221 115 150
Danmark
KRKA Sverige AB
Tlf: + 46 (0)8 643 67 66 (SE)
Deutschland
TAD Pharma GmbH Tel: + 49 (0) 4721 606-0
Eesti
KRKA, d.d., Novo mesto Eesti filiaal Tel: + 372 (0) 6 671 658
EXláSa
QUALIA PHARMA S.A.
T^: +30 (0)210 2832941
España
KERN PHARMA, S.L.
Tel: + 34 93 700 25 25
Lietuva
UAB KRKA Lietuva Tel: + 370 5 236 27 40
Luxembourg/Luxemburg
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091 (BE)
Magyarország
KRKA Magyarország Kereskedelmi Kft. Tel.: + 361 (0) 355 8490
Malta
E. J. Busuttil Ltd.
Tel: + 356 21 445 885
Nederland
KRKA Belgium, SA.
Tel: +32 (0) 489 304 091 (BE)
Norge
KRKA Sverige AB
Tlf: + 46 (0)8 643 67 66 (SE)
Osterreich
KRKA Pharma GmbH, Wien Tel: + 43 (0)1 66 24 300
Polska
KRKA-POLSKA Sp. z o.o.
Tel.: + 48 (0)22 573 7500
France
KRKA France Eurl Tél: + 33 (0)1 57 40 82 25
Hrvatska
KRKA - FARMA d.o.o. Tel: + 385 1 6312 100
Portugal
KRKA Farmacéutica, Sociedade Unipessoal Lda. Tel: + 351 (0)21 46 43 650
Romania
KRKA Romania S.R.L., Bucharest Tel: + 4 021 310 66 05
Tel: + 353 1 293 91 80 Ísland
KRKA Sverige AB
Sími: + 46 (0)8 643 67 66 (SE)
Italia
KRKA Farmaceutici Milano S.r.l. Tel: + 39 02 3300 8841
Kúnpoq
Kipa Pharmacal Ltd.
T^: + 357 24 651 882
Latvija
KRKA Latvija SIA Tel: + 371 6 733 86 10
Tel: + 386 (0) 1 47 51 100
Slovenská republika
KRKA Slovensko, s.r.o.
Tel: + 421 (0) 2 571 04 501
Suomi/Finland
KRKA Finland Oy Puh/Tel: +358 20 754 5330
Sverige
KRKA Sverige AB
Tel: + 46 (0)8 643 67 66 (SE)
United Kingdom
Consilient Health (UK) Ltd. Tel: + 44(0)203 751 1888
Fecha de la última revisión de este prospecto:
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu.
Prospecto: información para el usuario
Vizarsin 100 mg comprimidos recubiertos con película
Sildenafilo
Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto:
1. Qué es Vizarsin y para qué se utiliza
2. Qué necesita saber antes de empezar a tomar Vizarsin
3. Cómo tomar Vizarsin
4. Posibles efectos adversos
5 Conservación de Vizarsin
6. Contenido del envase e información adicional
1. Qué es Vizarsin y para qué se utiliza
Vizarsin contiene el principio activo sildenafilo, que pertenece a un grupo de medicamentos denominados inhibidores de la fosfodiesterasa tipo 5 (PDE5). Actúa dilatando los vasos sanguíneos del pene, permitiendo la afluencia de sangre cuando se está sexualmente estimulado. Vizarsin sólo le ayudará a conseguir una erección si se encuentra sexualmente estimulado.
Vizarsin está indicado en el tratamiento de la disfunción eréctil en hombres adultos, a veces denominada impotencia. Esto sucede cuando un varón no puede obtener o mantener una erección firme, adecuada para una actividad sexual satisfactoria.
2. Qué necesita saber antes de empezar a tomar Vizarsin
No tome Vizarsin
- Si es alérgico al sildenafilo o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
- Si está tomando unos medicamentos llamados nitratos, ya que la combinación puede dar lugar a una disminución peligrosa de su presión sanguínea. Consulte con su médico si está tomando cualquiera de estos medicamentos, que a menudo, se administran para aliviar el dolor de angina de pecho (o “dolor de pecho”). Si no está seguro, consulte con su médico o farmacéutico.
- Si está utilizando cualquiera de los medicamentos denominados dadores de óxido nítrico tales como nitrato de amilo (“poppers”), ya que la combinación puede dar lugar a una disminución peligrosa de su presión sanguínea.
- Si está tomando riociguat. Este medicamento se utiliza para tratar la hipertensión arterial pulmonar (es decir, tensión alta en los pulmones) y la hipertensión pulmonar tromboembólica crónica (es decir, tensión alta en los pulmones provocada por coágulos). Los inhibidores de la PDE5, como Vizarsin, han mostrado que producen un incremento del efecto hipotensivo de este medicamento. Si está tomando riociguat o no está seguro consulte a su médico.
- Si tiene un problema grave de corazón o hígado.
- Si ha padecido recientemente un accidente isquémico cerebral o ataque al corazón o si tiene la tensión arterial baja.
- Si padece una rara enfermedad ocular hereditaria (tal como retinitis pigmentosa).
- Si ha experimentado anteriormente una pérdida de la visión debido a una neuropatía óptica
isquémica anterior no arterítica (NOIA-NA).
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a tomar Vizarsin:
- Si padece anemia falciforme (una anormalidad de los glóbulos rojos), leucemia (cáncer de las células sanguíneas), mieloma múltiple (cáncer de médula ósea).
- Si padece una deformidad del pene o enfermedad de Peyronie.
- Si padece problemas del corazón. Su médico debe comprobar cuidadosamente si su corazón puede soportar el esfuerzo adicional de mantener relaciones sexuales.
- Si padece actualmente úlcera de estómago o problemas hemorrágicos (tales como hemofilia).
- Si experimenta una disminución o pérdida repentina de la visión, deje de tomar Vizarsin y
contacte con su médico inmediatamente.
No se aconseja utilizar Vizarsin simultáneamente con ningún otro tratamiento oral o local para la disfunción eréctil.
No debe tomar Vizarsin con tratamientos para la hipertensión arterial pulmonar (HAP) que contengan sildenafilo o cualquier otro inhibidor de la PDE5.
No debe tomar Vizarsin si no tiene disfunción eréctil.
El uso de Vizarsin no está indicado en mujeres.
Consideraciones especiales en pacientes con problemas renales o hepáticos
Debe comunicar a su médico si tiene problemas renales o hepáticos. Su médico puede decidir reducirle la dosis.
Niños y adolescentes
El uso de Vizarsin no está indicado en personas menores de 18 años.
Uso de Vizarsin con otros medicamentos
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
Los comprimidos de Vizarsin pueden interferir con algunos medicamentos, especialmente los utilizados para tratar el dolor de pecho. En caso de una urgencia médica, debe informar a su médico, farmacéutico o enfermero que está tomando Vizarsin y cuando lo tomó. No debe tomar Vizarsin con otros medicamentos a menos que su médico se lo aconseje.
No debe tomar Vizarsin si está tomando medicamentos denominados nitratos, ya que la combinación de estos medicamentos puede dar lugar a un descenso peligroso de su presión sanguínea. Siempre informe a su médico, farmacéutico o enfermero si está tomando cualquiera de estos medicamentos, que a menudo, se utilizan para aliviar el dolor de la angina de pecho (o “dolor de pecho”).
No debe tomar Vizarsin si está tomando medicamentos denominados dadores de óxido nítrico, tales como nitrito de amilo (“poppers”), ya que la combinación de estos medicamentos también puede dar lugar a un descenso peligroso de su presión sanguínea.
Informe a su médico o farmacéutico si está tomando riociguat.
Si está tomando medicamentos conocidos como inhibidores de la proteasa, como los utilizados en el tratamiento del VIH, su médico puede recomendarle que comience el tratamiento con la dosis más baja (25 mg) de Vizarsin.
Algunos pacientes que están recibiendo un alfabloqueante, medicamento utilizado para el tratamiento de la presión arterial alta o de la hipertrofia prostática, pueden experimentar mareos o sensación de vahído que pueden ser causados por una disminución de la tensión arterial al sentarse o levantarse rápidamente. Algunos pacientes han experimentado estos síntomas al tomar Vizarsin con alfabloqueantes. Esto es más probable que suceda en las 4 horas siguientes a la toma de Vizarsin. Con el fin de disminuir la probabilidad de que ocurran estos síntomas, deberá estar recibiendo su dosis diaria del alfabloqueante de forma regular antes de comenzar con Vizarsin. Su médico puede indicarle que comience el tratamiento con la dosis inferior (25 mg) de Vizarsin.
Uso de Vizarsin con alimentos, bebidas y alcohol
Vizarsin puede tomarse con o sin alimentos. Sin embargo, puede notar que Vizarsin tarde un poco más en hacer efecto si se ingiere con una comida copiosa.
La ingesta de alcohol puede dificultar, temporalmente, la capacidad para obtener una erección. Por lo tanto, para conseguir el máximo beneficio del medicamento, se aconseja no ingerir grandes cantidades de alcohol antes de tomar Vizarsin.
Embarazo, lactancia y fertilidad
El uso de Vizarsin no está indicado en mujeres.
Conducción y uso de máquinas
Vizarsin puede producir mareos y afectar a la visión. Debe saber cómo reacciona usted a Vizarsin antes de conducir vehículos o utilizar maquinaria.
Vizarsin contiene lactosa
Si su médico le ha indicado que padece una intolerancia a ciertos azúcares, consulte con él antes de tomar este medicamento.
3. Cómo tomar Vizarsin
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
La dosis recomendada de inicio es 50 mg.
No se debe tomar Vizarsin más de una vez al día.
Debe tomar Vizarsin aproximadamente una hora antes de que planee tener relaciones sexuales. Trague el comprimido entero con un vaso de agua.
Si nota que la acción de Vizarsin es demasiado fuerte o débil, comuníqueselo a su médico o farmacéutico.
Vizarsin sólo le ayudará a conseguir una erección si se encuentra sexualmente estimulado. El tiempo que necesita Vizarsin para hacer efecto varía de una persona a otra, generalmente oscila entre media y una hora. El efecto de Vizarsin puede retrasarse si lo toma con una comida copiosa.
En el caso de que Vizarsin no le ayude a conseguir una erección o si la erección no se mantiene el
tiempo suficiente para completar el acto sexual, consulte a su médico.
Si toma más Vizarsin del que debe
Puede experimentar un incremento en los efectos adversos y su gravedad. Dosis superiores a 100 mg no aumentan la eficacia.
No debe tomar más comprimidos de los recomendados por el médico.
Contacte con su médico si ha tomado más comprimidos de los aconsejados.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran. Los efectos adversos notificados asociados al uso de Vizarsin son por lo general de intensidad leve a moderada y de corta duración.
Si experimenta cualquiera de los siguientes efectos adversos graves, deje de tomar Vizarsin y busque atención médica inmediatamente:
- Reacción alérgica - esto ocurre con poca frecuencia (puede afectar hasta 1 de cada 100 personas).
Los síntomas incluyen silbido repentino al respirar, dificultad para respirar o mareo, hinchazón de los párpados, cara, labios o garganta.
- Dolores en el pecho - esto ocurre con poca frecuencia.
Si aparecen durante o después de mantener relaciones sexuales:
- Sitúese en una posición semisentada e intente relajarse.
- No use nitratos para tratar el dolor en el pecho.
- Erecciones prolongadas y a veces dolorosas - esto ocurre raramente (puede afectar hasta 1 de cada 1.000 personas).
Si usted tiene una erección que dura más de 4 horas, debe contactar con su médico inmediatamente.
- Disminución repentina o pérdida de la visión - esto ocurre raramente.
- Reacciones graves de la piel - esto ocurre raramente.
Los síntomas pueden incluir descamación grave e hinchazón de la piel, vesiculación bucal, de los genitales y alrededor de los ojos, además de fiebre.
- Convulsiones o ataques - esto ocurre raramente.
Otros efectos adversos:
Muy frecuentes (pueden afectar a más de 1 de cada 10 personas): dolor de cabeza.
Frecuentes (pueden afectar hasta 1 de cada 10 personas): náuseas, enrojecimiento facial, acaloramiento (entre los síntomas se incluye la sensación de calor repentina en la parte superior del cuerpo), indigestión, percepción anormal del color, visión borrosa, deterioro visual, congestión nasal y mareos.
Poco frecuentes (pueden afectar hasta 1 de cada 100 personas): vómitos, erupciones cutáneas, irritación ocular, derrame ocular/ojos rojos, dolor ocular, visión de luces parpadeantes, claridad visual, sensibilidad a la luz, ojos llorosos, palpitaciones, latido cardíaco rápido, presión arterial alta, presión
arterial baja, dolor muscular, sensación de somnolencia, sensación al tacto reducido, vértigo, pitidos en los oídos, boca seca, bloqueo o congestión de los senos nasales, inflamación de la mucosa de la nariz (entre los síntomas se incluyen moqueo, estornudos y congestión nasal), dolor en la zona superior del abdomen, enfermedad por reflujo gastroesofágico (entre los síntomas se encuentra el ardor de estómago), sangre presente en orina, dolor en brazos o piernas, sangrado de la nariz, sensación de calor y sensación de cansancio.
Raros (pueden afectar hasta 1 de cada 1.000 personas): desvanecimiento, accidente cerebrovascular, ataque cardíaco, latido cardíaco irregular, disminución transitoria del flujo sanguíneo a algunas partes del cerebro, sensación de opresión en la garganta, adormecimiento de la boca, sangrado en la parte posterior del ojo, visión doble, disminución de la agudeza visual, sensación anormal en el ojo, hinchazón ocular o del párpado, pequeñas partículas o manchas en la vista, visión de halos alrededor de las luces, dilatación de la pupila del ojo, cambio de color de la parte blanca del ojo, sangrado del pene, presencia de sangre en el semen, nariz seca, hinchazón del interior de la nariz, sensación de irritabilidad y disminución o pérdida repentina de la audición.
Durante la experiencia postcomercialización se han comunicado raramente casos de angina inestable (enfermedad cardíaca) y muerte súbita. Cabe destacar que la mayoría de los hombres que experimentaron estos efectos adversos, aunque no todos ellos, tenía problemas cardíacos antes de tomar este medicamento. No es posible determinar si estos efectos adversos estuvieron relacionados directamente con Vizarsin.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Vizarsin
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en el blíster y en la caja después de EXP. La fecha de caducidad es el último día del mes que se indica.
Este medicamento no requiere condiciones especiales de conservación.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional Composición de Vizarsin
- El principio activo es sidenafilo. Cada comprimido recubierto con película contiene sildenafilo citrato equivalente a 100 mg de sildenafilo.
- Los demás componentes son:
Núcleo del comprimido: celulosa microcristalina (E460), fosfato cálcico hidrogenado anhidro,
croscarmelosa sódica, hipromelosa (E464), estearato magnésico (E572).
Cubierta pelicular: lactosa monohidrato, hipromelosa (E464), dióxido de titanio (E171),
triacetina (E1518).
Aspecto del Vizarsin y contenido del envase
Vizarsin 100 mg comprimidos recubiertos con película son blancos, oblongos y llevan grabado “100” en una cara.
Vizarsin 100 mg comprimidos recubiertos con película están disponibles en cajas de 1 comprimido recubierto con película en blíster y también en cajas de 4 x 1, 8 x 1 o 12 x 1 comprimido recubierto con película en blísters perforados unidosis.
Puede que solamente estén comercializados algunos tamaños de envase.
Titular de la autorización de comercialización y responsable de la fabricación
KRKA, d.d., Novo mesto, Smarjeska cesta 6, 8501 Novo mesto, Eslovenia
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Belgie/Belgique/Belgien
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091
Etarapna
KPKA Etarapna EOOfl Tea.: + 359 (02) 962 34 50
Ceská republika KRKA CR, s.r.o.
Tel: + 420 (0) 221 115 150
Danmark
KRKA Sverige AB
Tlf: + 46 (0)8 643 67 66 (SE)
Deutschland
TAD Pharma GmbH Tel: + 49 (0) 4721 606-0
Eesti
KRKA, d.d., Novo mesto Eesti filiaal Tel: + 372 (0) 6 671 658
EXláSa
QUALIA PHARMA S.A.
T^: +30 (0)210 2832941
España
KERN PHARMA, S.L.
Tel: + 34 93 700 25 25
Lietuva
UAB KRKA Lietuva Tel: + 370 5 236 27 40
Luxembourg/Luxemburg
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091 (BE)
Magyarország
KRKA Magyarország Kereskedelmi Kft. Tel.: + 361 (0) 355 8490
Malta
E. J. Busuttil Ltd.
Tel: + 356 21 445 885
Nederland
KRKA Belgium, SA.
Tel: +32 (0) 489 304 091 (BE)
Norge
KRKA Sverige AB
Tlf: + 46 (0)8 643 67 66 (SE)
Osterreich
KRKA Pharma GmbH, Wien Tel: + 43 (0)1 66 24 300
Polska
KRKA-POLSKA Sp. z o.o.
Tel.: + 48 (0)22 573 7500
France
KRKA France Eurl Tél: + 33 (0)1 57 40 82 25
Hrvatska
KRKA - FARMA d.o.o. Tel: + 385 1 6312 100
Portugal
KRKA Farmacéutica, Sociedade Unipessoal Lda. Tel: + 351 (0)21 46 43 650
Romania
KRKA Romania S.R.L., Bucharest Tel: + 4 021 310 66 05
Ísland
KRKA Sverige AB
Sími: + 46 (0)8 643 67 66 (SE)
Italia
KRKA Farmaceutici Milano S.r.l. Tel: + 39 02 3300 8841
Kúnpoq
Kipa Pharmacal Ltd.
T^: + 357 24 651 882
Latvija
KRKA Latvija SIA Tel: + 371 6 733 86 10
Slovenská republika
KRKA Slovensko, s.r.o.
Tel: + 421 (0) 2 571 04 501
Suomi/Finland
KRKA Finland Oy Puh/Tel: +358 20 754 5330
Sverige
KRKA Sverige AB
Tel: + 46 (0)8 643 67 66 (SE)
United Kingdom
Consilient Health (UK) Ltd. Tel: + 44(0)203 751 1888
Fecha de la última revisión de este prospecto:
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu.
Prospecto: información para el usuario
Vizarsin 25 mg comprimidos bucodispersables
Sildenafilo
Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
1. Qué es Vizarsin y para qué se utiliza
2. Qué necesita saber antes de empezar a tomar Vizarsin
3. Cómo tomar Vizarsin
4. Posibles efectos adversos
5. Conservación de Vizarsin
6. Contenido del envase e información adicional
1. Qué es Vizarsin y para qué se utiliza
Vizarsin contiene el principio activo sildenafilo, que pertenece a un grupo de medicamentos denominados inhibidores de la fosfodiesterasa tipo 5 (PDE5). Actúa dilatando los vasos sanguíneos del pene, permitiendo la afluencia de sangre cuando se está sexualmente estimulado. Vizarsin sólo le ayudará a conseguir una erección si se encuentra sexualmente estimulado.
Vizarsin está indicado en el tratamiento de la disfunción eréctil en hombres adultos, a veces denominada impotencia. Esto sucede cuando un varón no puede obtener o mantener una erección firme, adecuada para una actividad sexual satisfactoria.
2. Qué necesita saber antes de empezar a tomar Vizarsin
No tome Vizarsin
- Si es alérgico a sildenafilo o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
- Si está tomando unos medicamentos llamados nitratos, ya que la combinación puede dar lugar a una disminución peligrosa de su presión sanguínea. Consulte con su médico si está tomando cualquiera de estos medicamentos, que a menudo, se administran para aliviar el dolor de angina de pecho (o “dolor de pecho”). Si no está seguro, consulte con su médico o farmacéutico.
- Si está utilizando cualquiera de los medicamentos denominados dadores de óxido nítrico tales como nitrato de amilo (“poppers”), ya que la combinación puede dar lugar a una disminución peligrosa de su presión sanguínea.
- Si está tomando riociguat. Este medicamento se utiliza para tratar la hipertensión arterial pulmonar (es decir, tensión alta en los pulmones) y la hipertensión pulmonar tromboembólica crónica (es decir, tensión alta en los pulmones provocada por coágulos). Los inhibidores de la PDE5, como Vizarsin, han mostrado que producen un incremento del efecto hipotensivo de este medicamento. Si está tomando riociguat o no está seguro consulte a su médico.
- Si tiene un problema grave de corazón o hígado.
- Si ha padecido recientemente un accidente isquémico cerebral o ataque al corazón o si tiene la tensión arterial baja.
- Si padece una rara enfermedad ocular hereditaria (tal como retinitis pigmentosa).
- Si ha experimentado anteriormente una pérdida de la visión debido a una neuropatía óptica isquémica anterior no arterítica (NOIA-NA).
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a tomar Vizarsin:
- Si padece anemia falciforme (una anormalidad de los glóbulos rojos), leucemia (cáncer de las células sanguíneas), mieloma múltiple (cáncer de médula ósea).
- Si padece una deformidad del pene o enfermedad de Peyronie.
- Si padece problemas del corazón. Su médico debe comprobar cuidadosamente si su corazón puede soportar el esfuerzo adicional de mantener relaciones sexuales.
- Si padece actualmente úlcera de estómago o problemas hemorrágicos (tales como hemofilia).
- Si experimenta una disminución o pérdida repentina de la visión, deje de tomar Vizarsin y contacte con su médico inmediatamente.
No se aconseja utilizar Vizarsin simultáneamente con ningún otro tratamiento oral o local para la disfunción eréctil.
No debe tomar Vizarsin con tratamientos para la hipertensión arterial pulmonar (HAP) que contengan sildenafilo o cualquier otro inhibidor de la PDE5.
No debe tomar Vizarsin si no tiene disfunción eréctil.
El uso de Vizarsin no está indicado en mujeres.
Consideraciones especiales en pacientes con problemas renales o hepáticos
Debe comunicar a su médico si tiene problemas renales o hepáticos. Su médico puede decidir reducirle la dosis.
Niños y adolescentes
El uso de Vizarsin no está indicado en personas menores de 18 años.
Uso de Vizarsin con otros medicamentos
Consulte a su médico o farmacéutico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
Vizarsin puede interferir con algunos medicamentos, especialmente los utilizados para tratar el dolor de pecho. En caso de una urgencia médica, debe informar a su médico, farmacéutico o enfermero que está tomando Vizarsin y cuando lo tomó. No debe tomar Vizarsin con otros medicamentos a menos que su médico se lo aconseje.
No debe tomar Vizarsin si está tomando medicamentos denominados nitratos, ya que la combinación de estos medicamentos puede dar lugar a un descenso peligroso de su presión sanguínea. Siempre informe a su médico, farmacéutico o enfermero si está tomando cualquiera de estos medicamentos, que a menudo, se utilizan para aliviar el dolor de la angina de pecho (o “dolor de pecho”).
No debe tomar Vizarsin si está tomando medicamentos denominados dadores de óxido nítrico, tales como nitrito de amilo (“poppers”), ya que la combinación de estos medicamentos también puede dar lugar a un descenso peligroso de su presión sanguínea.
Informe a su médico o farmacéutico si está tomando riociguat.
Si está tomando medicamentos conocidos como inhibidores de la proteasa, como los utilizados en el tratamiento del VIH, su médico puede recomendarle que comience el tratamiento con la dosis más baja (25 mg) de Vizarsin.
Algunos pacientes que están recibiendo un alfabloqueante, medicamento utilizado para el tratamiento de la presión arterial alta o de la hipertrofia prostática, pueden experimentar mareos o sensación de vahído que pueden ser causados por una disminución de la tensión arterial al sentarse o levantarse rápidamente. Algunos pacientes han experimentado estos síntomas al tomar Vizarsin con alfabloqueantes. Esto es más probable que suceda en las 4 horas siguientes a la toma de Vizarsin. Con el fin de disminuir la probabilidad de que ocurran estos síntomas, deberá estar recibiendo su dosis diaria del alfabloqueante de forma regular antes de comenzar con Vizarsin. Su médico puede indicarle que comience el tratamiento con la dosis inferior (25 mg) de Vizarsin.
Uso de Vizarsin con alimentos, bebidas y alcohol
Vizarsin puede tomarse con o sin alimentos. Sin embargo, puede notar que Vizarsin tarde un poco más en hacer efecto si se ingiere con una comida copiosa. Debe tener la boca vacía antes de tomar el comprimido.
La ingesta de alcohol puede dificultar, temporalmente, la capacidad para obtener una erección. Por lo tanto, para conseguir el máximo beneficio del medicamento, se aconseja no ingerir grandes cantidades de alcohol antes de tomar Vizarsin.
Embarazo, lactancia y fertilidad
El uso de Vizarsin no está indicado en mujeres.
Conducción y uso de máquinas
Vizarsin puede producir mareos y afectar a la visión. Debe saber cómo reacciona usted a Vizarsin antes de conducir vehículos o utilizar maquinaria.
Vizarsin contiene aspartamo (E951) y sorbitol (E420)
El aspartamo es una fuente de fenilalanina. Puede ser perjudicial para personas con fenilcetonuria. Vizarsin contiene sorbitol. Si su médico le ha indicado que padece una intoleracia a ciertos azúcares, consulte a su él antes de tomar este medicamento.
3. Cómo tomar Vizarsin
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
La dosis recomendada de inicio es 50 mg.
No se debe tomar Vizarsin más de una vez al día.
No tome Vizarsin comprimidos bucodispersables al mismo tiempo que otras presentaciones de Vizarsin.
Debe tomar Vizarsin aproximadamente una hora antes de que planee tener relaciones sexuales.
Los comprimidos de Vizarsin son frágiles. No debe empujarlos a través de la pared del blíster porque podría romper los comprimidos. No manipule los comprimidos con las manos húmedas, ya que podría romperlos. Para retirar un comprimido siga estos pasos:
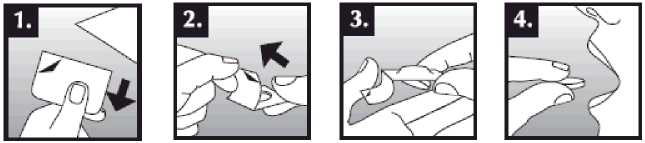
Para blísters de 4 comprimidos:
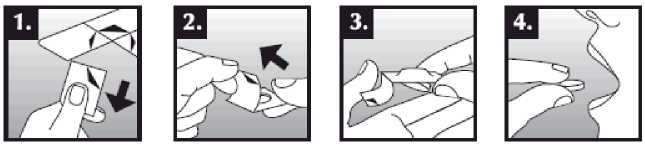
1. Sujete el blíster por los bordes y separe una de las unidades rasgando con cuidado por las marcas troqueladas.
2. Despegue completamente la hoja tirando hacia arriba del borde.
3. Voltee el blíster para colocar el comprimido en su mano.
4. En cuanto haya salido el comprimido, colóqueselo en la lengua.
En unos segundos comenzará a desintegrarse en la boca, por lo que se puede tomar con o sin agua. Debe tener la boca vacía antes de colocarse el comprimido en la lengua.
Si nota que la acción de Vizarsin es demasiado fuerte o débil, comuníqueselo a su médico o farmacéutico.
Vizarsin sólo le ayudará a conseguir una erección si se encuentra sexualmente estimulado. El tiempo que necesita Vizarsin para hacer efecto varía de una persona a otra, generalmente oscila entre media y una hora. El efecto de Vizarsin puede retrasarse si lo toma con una comida copiosa.
En el caso de que Vizarsin no le ayude a conseguir una erección o si la erección no se mantiene el tiempo suficiente para completar el acto sexual, consulte a su médico.
Si toma más Vizarsin del que debe
Puede experimentar un incremento en los efectos adversos y su gravedad. Dosis superiores a 100 mg no aumentan la eficacia.
No debe tomar más comprimidos de los recomendados por el médico.
Contacte con su médico si ha tomado más comprimidos de los aconsejados.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran. Los efectos adversos notificados asociados al uso de Vizarsin son por lo general de intensidad leve a moderada y de corta duración.
Si experimenta cualquiera de los siguientes efectos adversos graves, deje de tomar Vizarsin y busque atención médica inmediatamente:
- Reacción alérgica - esto ocurre con poca frecuencia (puede afectar hasta 1 de cada 100 personas).
Los síntomas incluyen silbido repentino al respirar, dificultad para respirar o mareo, hinchazón de los párpados, cara, labios o garganta.
- Dolores en el pecho - esto ocurre con poca frecuencia.
Si aparecen durante o después de mantener relaciones sexuales:
- Sitúese en una posición semisentada e intente relajarse.
- No use nitratos para tratar el dolor en el pecho.
- Erecciones prolongadas y a veces dolorosas - esto ocurre raramente (puede afectar hasta 1 de cada 1.000 personas).
Si usted tiene una erección que dura más de 4 horas, debe contactar con su médico inmediatamente.
- Disminución repentina o pérdida de la visión - esto ocurre raramente.
- Reacciones graves de la piel - esto ocurre raramente.
Los síntomas pueden incluir descamación grave e hinchazón de la piel, vesiculación bucal, de los genitales y alrededor de los ojos, además de fiebre.
- Convulsiones o ataques - esto ocurre raramente.
Otros efectos adversos:
Muy frecuentes (pueden afectar a más de 1 de cada 10 personas): dolor de cabeza.
Frecuentes (pueden afectar hasta 1 de cada 10 personas): náuseas, enrojecimiento facial, acaloramiento (entre los síntomas se incluye la sensación de calor repentina en la parte superior del cuerpo), indigestión, percepción anormal del color, visión borrosa, deterioro visual, congestión nasal y mareos.
Poco frecuentes (pueden afectar hasta 1 de cada 100 personas): vómitos, erupciones cutáneas, irritación ocular, derrame ocular/ojos rojos, dolor ocular, visión de luces parpadeantes, claridad visual, sensibilidad a la luz, ojos llorosos, palpitaciones, latido cardíaco rápido, presión arterial alta, presión arterial baja, dolor muscular, sensación de somnolencia, sensación al tacto reducido, vértigo, pitidos en los oídos, boca seca, bloqueo o congestión de los senos nasales, inflamación de la mucosa de la nariz (entre los síntomas se incluyen moqueo, estornudos y congestión nasal), dolor en la zona superior del abdomen, enfermedad por reflujo gastroesofágico (entre los síntomas se encuentra el ardor de estómago), sangre presente en orina, dolor en brazos o piernas, sangrado de la nariz, sensación de calor y sensación de cansancio.
Raros (pueden afectar hasta 1 de cada 1.000 personas): desvanecimiento, accidente cerebrovascular, ataque cardíaco, latido cardíaco irregular, disminución transitoria del flujo sanguíneo a algunas partes del cerebro, sensación de opresión en la garganta, adormecimiento de la boca, sangrado en la parte posterior del ojo, visión doble, disminución de la agudeza visual, sensación anormal en el ojo, hinchazón ocular o del párpado, pequeñas partículas o manchas en la vista, visión de halos alrededor de las luces, dilatación de la pupila del ojo, cambio de color de la parte blanca del ojo, sangrado del pene, presencia de sangre en el semen, nariz seca, hinchazón del interior de la nariz, sensación de irritabilidad y disminución o pérdida repentina de la audición.
Durante la experiencia postcomercialización se han comunicado raramente casos de angina inestable (enfermedad cardíaca) y muerte súbita. Cabe destacar que la mayoría de los hombres que experimentaron estos efectos adversos, aunque no todos ellos, tenía problemas cardíacos antes de tomar este medicamento. No es posible determinar si estos efectos adversos estuvieron relacionados directamente con Vizarsin.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se
trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Vizarsin
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la caja y en el blíster después de EXP. La fecha de caducidad es el último día del mes que se indica.
No conservar a temperatura superior a 30°C.
Conservar en el embalaje original para protegerlo de la humedad.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional Composición de Vizarsin
- El principio activo es sildenafilo. Cada comprimido bucodispersable contiene 25 mg de sildenafilo.
- El resto de los ingredientes son hidroxipropilcelulosa (E463), manitol (E421), aspartamo (E951), neohesperidina-dihidrochalcona (E959), aroma de hierbabuena, aroma de menta (que contiene sorbitol (E420)), crospovidona, silicato de calcio y estearato de magnesio (E572).
Aspecto del producto y contenido del envase
Comprimidos blancos o blanquecinos, redondos, biconvexos y eventualmente con manchas más oscuras.
Vizarsin comprimidos bucodispersables están disponible en cajas de 1 comprimido bucodispersable en blíster y también en cajas de 2 x 1, 4 x 1, 8 x 1 o 12 x 1 comprimido bucodispersable en blísters perforados unidosis.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia Responsables de la fabricación
KRKA, d.d., Novo mesto, Smarjeska cesta 6, 8501 Novo mesto, Eslovenia TAD Pharma GmbH, Heinz-Lohmann-StraBe 5, 27472 Cuxhaven, Alemania
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Belgie/Belgique/Belgien
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091
Etarapna
KPKA Etarapua EOOfl Tea.: + 359 (02) 962 34 50
Lietuva
UAB KRKA Lietuva Tel: + 370 5 236 27 40
Luxembourg/Luxemburg
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091 (BE)
|
Ceská republika KRKA CR, s.r.o. Tel: + 420 (0) 221 115 150 |
Magyarország KRKA Magyarország Kereskedelmi Kft. Tel.: + 361 (0) 355 8490 |
|
Danmark KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
Malta E. J. Busuttil Ltd. Tel: + 356 21 445 885 |
|
Deutschland TAD Pharma GmbH Tel: + 49 (0) 4721 606-0 |
Nederland KRKA Belgium, SA. Tel: +32 (0) 489 304 091 (BE) |
|
Eesti KRKA, d.d., Novo mesto Eesti filiaal Tel: + 372 (0) 6 671 658 |
Norge KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
|
EXláSa QUALIA PHARMA S.A. Tn^: +30 (0)210 2832941 |
Osterreich KRKA Pharma GmbH, Wien Tel: + 43 (0)1 66 24 300 |
|
España KERN PHARMA, S.L. Tel: + 34 93 700 25 25 |
Polska KRKA-POLSKA Sp. z o.o. Tel.: + 48 (0)22 573 7500 |
|
France KRKA France Eurl Tél: + 33 (0)1 57 40 82 25 |
Portugal KRKA Farmacéutica, Sociedade Unipessoal Lda. Tel: + 351 (0)21 46 43 650 |
|
Hrvatska KRKA - FARMA d.o.o. Tel: + 385 1 6312 100 |
Romania KRKA Romania S.R.L., Bucharest Tel: + 4 021 310 66 05 |
|
Ireland KRKA Pharma Dublin, Ltd. Tel: + 353 1 293 91 80 |
Slovenija KRKA, d.d., Novo mesto Tel: + 386 (0) 1 47 51 100 |
|
Ísland KRKA Sverige AB Sími: + 46 (0)8 643 67 66 (SE) |
Slovenská republika KRKA Slovensko, s.r.o. Tel: + 421 (0) 2 571 04 501 |
|
Italia KRKA Farmaceutici Milano S.r.l. Tel: + 39 02 3300 8841 |
Suomi/Finland KRKA Finland Oy Puh/Tel: +358 20 754 5330 |
|
Kúnpoq Kipa Pharmacal Ltd. Tn^: + 357 24 651 882 |
Sverige KRKA Sverige AB Tel: + 46 (0)8 643 67 66 (SE) |
|
Latvija KRKA Latvija SIA Tel: + 371 6 733 86 10 |
United Kingdom Consilient Health (UK) Ltd. Tel: + 44(0)203 751 1888 |
|
Fecha de la última revisión de este prospecto: |
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu.
Prospecto: información para el usuario
Vizarsin 50 mg comprimidos bucodispersables
Sildenafilo
Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
1. Qué es Vizarsin y para qué se utiliza
2. Qué necesita saber antes de empezar a tomar Vizarsin
3. Cómo tomar Vizarsin
4. Posibles efectos adversos
5. Conservación de Vizarsin
6. Contenido del envase e información adicional
1. Qué es Vizarsin y para qué se utiliza
Vizarsin contiene el principio activo sildenafilo, que pertenece a un grupo de medicamentos denominados inhibidores de la fosfodiesterasa tipo 5 (PDE5). Actúa dilatando los vasos sanguíneos del pene, permitiendo la afluencia de sangre cuando se está sexualmente estimulado. Vizarsin sólo le ayudará a conseguir una erección si se encuentra sexualmente estimulado.
Vizarsin está indicado en el tratamiento de la disfunción eréctil en hombres adultos, a veces denominada impotencia. Esto sucede cuando un varón no puede obtener o mantener una erección firme, adecuada para una actividad sexual satisfactoria.
2. Qué necesita saber antes de empezar a tomar Vizarsin
No tome Vizarsin
- Si es alérgico a sildenafilo o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
- Si está tomando unos medicamentos llamados nitratos, ya que la combinación puede dar lugar a una disminución peligrosa de su presión sanguínea. Consulte con su médico si está tomando cualquiera de estos medicamentos, que a menudo, se administran para aliviar el dolor de angina de pecho (o “dolor de pecho”). Si no está seguro, consulte con su médico o farmacéutico.
- Si está utilizando cualquiera de los medicamentos denominados dadores de óxido nítrico tales como nitrato de amilo (“poppers”), ya que la combinación puede dar lugar a una disminución peligrosa de su presión sanguínea.
- Si está tomando riociguat. Este medicamento se utiliza para tratar la hipertensión arterial pulmonar (es decir, tensión alta en los pulmones) y la hipertensión pulmonar tromboembólica crónica (es decir, tensión alta en los pulmones provocada por coágulos). Los inhibidores de la PDE5, como Vizarsin, han mostrado que producen un incremento del efecto hipotensivo de este medicamento. Si está tomando riociguat o no está seguro consulte a su médico.
- Si tiene un problema grave de corazón o hígado.
- Si ha padecido recientemente un accidente isquémico cerebral o ataque al corazón o si tiene la tensión arterial baja.
- Si padece una rara enfermedad ocular hereditaria (tal como retinitis pigmentosa).
- Si ha experimentado anteriormente una pérdida de la visión debido a una neuropatía óptica isquémica anterior no arterítica (NOIA-NA).
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a tomar Vizarsin:
- Si padece anemia falciforme (una anormalidad de los glóbulos rojos), leucemia (cáncer de las células sanguíneas), mieloma múltiple (cáncer de médula ósea).
- Si padece una deformidad del pene o enfermedad de Peyronie.
- Si padece problemas del corazón. Su médico debe comprobar cuidadosamente si su corazón puede soportar el esfuerzo adicional de mantener relaciones sexuales.
- Si padece actualmente úlcera de estómago o problemas hemorrágicos (tales como hemofilia).
- Si experimenta una disminución o pérdida repentina de la visión, deje de tomar Vizarsin y contacte con su médico inmediatamente.
No se aconseja utilizar Vizarsin simultáneamente con ningún otro tratamiento oral o local para la disfunción eréctil.
No debe tomar Vizarsin con tratamientos para la hipertensión arterial pulmonar (HAP) que contengan sildenafilo o cualquier otro inhibidor de la PDE5.
No debe tomar Vizarsin si no tiene disfunción eréctil.
El uso de Vizarsin no está indicado en mujeres.
Consideraciones especiales en pacientes con problemas renales o hepáticos
Debe comunicar a su médico si tiene problemas renales o hepáticos. Su médico puede decidir reducirle la dosis.
Niños y adolescentes
El uso de Vizarsin no está indicado en personas menores de 18 años.
Uso de Vizarsin con otros medicamentos
Consulte a su médico o farmacéutico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
Vizarsin puede interferir con algunos medicamentos, especialmente los utilizados para tratar el dolor de pecho. En caso de una urgencia médica, debe informar a su médico, farmacéutico o enfermero que está tomando Vizarsin y cuando lo tomó. No debe tomar Vizarsin con otros medicamentos a menos que su médico se lo aconseje.
No debe tomar Vizarsin si está tomando medicamentos denominados nitratos, ya que la combinación de estos medicamentos puede dar lugar a un descenso peligroso de su presión sanguínea. Siempre informe a su médico, farmacéutico o enfermero si está tomando cualquiera de estos medicamentos, que a menudo, se utilizan para aliviar el dolor de la angina de pecho (o “dolor de pecho”).
No debe tomar Vizarsin si está tomando medicamentos denominados dadores de óxido nítrico, tales como nitrito de amilo (“poppers”), ya que la combinación de estos medicamentos también puede dar lugar a un descenso peligroso de su presión sanguínea.
Informe a su médico o farmacéutico si está tomando riociguat.
Si está tomando medicamentos conocidos como inhibidores de la proteasa, como los utilizados en el tratamiento del VIH, su médico puede recomendarle que comience el tratamiento con la dosis más baja (25 mg) de Vizarsin.
Algunos pacientes que están recibiendo un alfabloqueante, medicamento utilizado para el tratamiento de la presión arterial alta o de la hipertrofia prostática, pueden experimentar mareos o sensación de vahído que pueden ser causados por una disminución de la tensión arterial al sentarse o levantarse rápidamente. Algunos pacientes han experimentado estos síntomas al tomar Vizarsin con alfabloqueantes. Esto es más probable que suceda en las 4 horas siguientes a la toma de Vizarsin. Con el fin de disminuir la probabilidad de que ocurran estos síntomas, deberá estar recibiendo su dosis diaria del alfabloqueante de forma regular antes de comenzar con Vizarsin. Su médico puede indicarle que comience el tratamiento con la dosis inferior (25 mg) de Vizarsin.
Uso de Vizarsin con alimentos, bebidas y alcohol
Vizarsin puede tomarse con o sin alimentos. Sin embargo, puede notar que Vizarsin tarde un poco más en hacer efecto si se ingiere con una comida copiosa. Debe tener la boca vacía antes de tomar el comprimido.
La ingesta de alcohol puede dificultar, temporalmente, la capacidad para obtener una erección. Por lo tanto, para conseguir el máximo beneficio del medicamento, se aconseja no ingerir grandes cantidades de alcohol antes de tomar Vizarsin.
Embarazo, lactancia y fertilidad
El uso de Vizarsin no está indicado en mujeres.
Conducción y uso de máquinas
Vizarsin puede producir mareos y afectar a la visión. Debe saber cómo reacciona usted a Vizarsin antes de conducir vehículos o utilizar maquinaria.
Vizarsin contiene aspartamo (E951) y sorbitol (E420)
El aspartamo es una fuente de fenilalanina. Puede ser perjudicial para personas con fenilcetonuria. Vizarsin contiene sorbitol. Si su médico le ha indicado que padece una intoleracia a ciertos azúcares, consulte a su él antes de tomar este medicamento.
3. Cómo tomar Vizarsin
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
La dosis recomendada de inicio es 50 mg.
No se debe tomar Vizarsin más de una vez al día.
No tome Vizarsin comprimidos bucodispersables al mismo tiempo que otras presentaciones de Vizarsin.
Debe tomar Vizarsin aproximadamente una hora antes de que planee tener relaciones sexuales.
Los comprimidos de Vizarsin son frágiles. No debe empujarlos a través de la pared del blíster porque podría romper los comprimidos. No manipule los comprimidos con las manos húmedas, ya que podría romperlos. Para retirar un comprimido siga estos pasos:
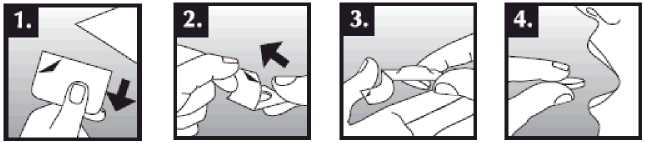
Para blísters de 4 comprimidos:
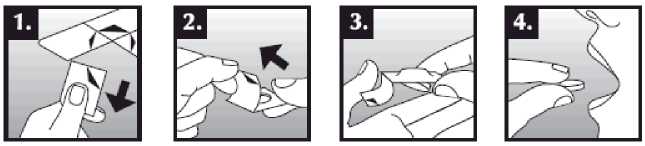
1. Sujete el blíster por los bordes y separe una de las unidades rasgando con cuidado por las marcas troqueladas.
2. Despegue completamente la hoja tirando hacia arriba del borde.
3. Voltee el blíster para colocar el comprimido en su mano.
4. En cuanto haya salido el comprimido, colóqueselo en la lengua.
En unos segundos comenzará a desintegrarse en la boca, por lo que se puede tomar con o sin agua. Debe tener la boca vacía antes de colocarse el comprimido en la lengua.
Si nota que la acción de Vizarsin es demasiado fuerte o débil, comuníqueselo a su médico o farmacéutico.
Vizarsin sólo le ayudará a conseguir una erección si se encuentra sexualmente estimulado. El tiempo que necesita Vizarsin para hacer efecto varía de una persona a otra, generalmente oscila entre media y una hora. El efecto de Vizarsin puede retrasarse si lo toma con una comida copiosa.
En el caso de que Vizarsin no le ayude a conseguir una erección o si la erección no se mantiene el tiempo suficiente para completar el acto sexual, consulte a su médico.
Si toma más Vizarsin del que debe
Puede experimentar un incremento en los efectos adversos y su gravedad. Dosis superiores a 100 mg no aumentan la eficacia.
No debe tomar más comprimidos de los recomendados por el médico.
Contacte con su médico si ha tomado más comprimidos de los aconsejados.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran. Los efectos adversos notificados asociados al uso de Vizarsin son por lo general de intensidad leve a moderada y de corta duración.
Si experimenta cualquiera de los siguientes efectos adversos graves, deje de tomar Vizarsin y busque atención médica inmediatamente:
- Reacción alérgica - esto ocurre con poca frecuencia (puede afectar hasta 1 de cada 100 personas).
Los síntomas incluyen silbido repentino al respirar, dificultad para respirar o mareo, hinchazón de los párpados, cara, labios o garganta.
- Dolores en el pecho - esto ocurre con poca frecuencia.
Si aparecen durante o después de mantener relaciones sexuales:
- Sitúese en una posición semisentada e intente relajarse.
- No use nitratos para tratar el dolor en el pecho.
- Erecciones prolongadas y a veces dolorosas - esto ocurre raramente (puede afectar hasta 1 de cada 1.000 personas).
Si usted tiene una erección que dura más de 4 horas, debe contactar con su médico inmediatamente.
- Disminución repentina o pérdida de la visión - esto ocurre raramente.
- Reacciones graves de la piel - esto ocurre raramente.
Los síntomas pueden incluir descamación grave e hinchazón de la piel, vesiculación bucal, de los genitales y alrededor de los ojos, además de fiebre.
- Convulsiones o ataques - esto ocurre raramente.
Otros efectos adversos:
Muy frecuentes (pueden afectar a más de 1 de cada 10 personas): dolor de cabeza.
Frecuentes (pueden afectar hasta 1 de cada 10 personas): náuseas, enrojecimiento facial, acaloramiento (entre los síntomas se incluye la sensación de calor repentina en la parte superior del cuerpo), indigestión, percepción anormal del color, visión borrosa, deterioro visual, congestión nasal y mareos.
Poco frecuentes (pueden afectar hasta 1 de cada 100 personas): vómitos, erupciones cutáneas, irritación ocular, derrame ocular/ojos rojos, dolor ocular, visión de luces parpadeantes, claridad visual, sensibilidad a la luz, ojos llorosos, palpitaciones, latido cardíaco rápido, presión arterial alta, presión arterial baja, dolor muscular, sensación de somnolencia, sensación al tacto reducido, vértigo, pitidos en los oídos, boca seca, bloqueo o congestión de los senos nasales, inflamación de la mucosa de la nariz (entre los síntomas se incluyen moqueo, estornudos y congestión nasal), dolor en la zona superior del abdomen, enfermedad por reflujo gastroesofágico (entre los síntomas se encuentra el ardor de estómago), sangre presente en orina, dolor en brazos o piernas, sangrado de la nariz, sensación de calor y sensación de cansancio.
Raros (pueden afectar hasta 1 de cada 1.000 personas): desvanecimiento, accidente cerebrovascular, ataque cardíaco, latido cardíaco irregular, disminución transitoria del flujo sanguíneo a algunas partes del cerebro, sensación de opresión en la garganta, adormecimiento de la boca, sangrado en la parte posterior del ojo, visión doble, disminución de la agudeza visual, sensación anormal en el ojo, hinchazón ocular o del párpado, pequeñas partículas o manchas en la vista, visión de halos alrededor de las luces, dilatación de la pupila del ojo, cambio de color de la parte blanca del ojo, sangrado del pene, presencia de sangre en el semen, nariz seca, hinchazón del interior de la nariz, sensación de irritabilidad y disminución o pérdida repentina de la audición.
Durante la experiencia postcomercialización se han comunicado raramente casos de angina inestable (enfermedad cardíaca) y muerte súbita. Cabe destacar que la mayoría de los hombres que experimentaron estos efectos adversos, aunque no todos ellos, tenía problemas cardíacos antes de tomar este medicamento. No es posible determinar si estos efectos adversos estuvieron relacionados directamente con Vizarsin.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se
trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Vizarsin
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la caja y en el blíster después de EXP. La fecha de caducidad es el último día del mes que se indica.
No conservar a temperatura superior a 30°C.
Conservar en el embalaje original para protegerlo de la humedad.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional Composición de Vizarsin
- El principio activo es sildenafilo. Cada comprimido bucodispersable contiene 50 mg de sildenafilo.
- El resto de los ingredientes son hidroxipropilcelulosa (E463), manitol (E421), aspartamo (E951), neohesperidina-dihidrochalcona (E959), aroma de hierbabuena, aroma de menta (que contiene sorbitol (E420)), crospovidona, silicato de calcio y estearato de magnesio (E572).
Aspecto del producto y contenido del envase
Comprimidos blancos o blanquecinos, redondos, biconvexos y eventualmente con manchas más oscuras.
Vizarsin comprimidos bucodispersables están disponible en cajas de 1 comprimido bucodispersable en blíster y también en cajas de 2 x 1, 4 x 1, 8 x 1, 12 x 1 o 24 x 1 comprimido bucodispersable en blísters perforados unidosis.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia Responsables de la fabricación
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia TAD Pharma GmbH, Heinz-Lohmann-StraBe 5, 27472 Cuxhaven, Alemania
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Belgie/Belgique/Belgien
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091
Etarapna
KPKA Etarapua EOOfl Tea.: + 359 (02) 962 34 50
Lietuva
UAB KRKA Lietuva Tel: + 370 5 236 27 40
Luxembourg/Luxemburg
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091 (BE)
|
Ceská republika KRKA CR, s.r.o. Tel: + 420 (0) 221 115 150 |
Magyarország KRKA Magyarország Kereskedelmi Kft. Tel.: + 361 (0) 355 8490 |
|
Danmark KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
Malta E. J. Busuttil Ltd. Tel: + 356 21 445 885 |
|
Deutschland TAD Pharma GmbH Tel: + 49 (0) 4721 606-0 |
Nederland KRKA Belgium, SA. Tel: +32 (0) 489 304 091 (BE) |
|
Eesti KRKA, d.d., Novo mesto Eesti filiaal Tel: + 372 (0) 6 671 658 |
Norge KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
|
EXláSa QUALIA PHARMA S.A. Tn^: +30 (0)210 2832941 |
Osterreich KRKA Pharma GmbH, Wien Tel: + 43 (0)1 66 24 300 |
|
España KERN PHARMA, S.L. Tel: + 34 93 700 25 25 |
Polska KRKA-POLSKA Sp. z o.o. Tel.: + 48 (0)22 573 7500 |
|
France KRKA France Eurl Tél: + 33 (0)1 57 40 82 25 |
Portugal KRKA Farmacéutica, Sociedade Unipessoal Lda. Tel: + 351 (0)21 46 43 650 |
|
Hrvatska KRKA - FARMA d.o.o. Tel: + 385 1 6312 100 |
Romania KRKA Romania S.R.L., Bucharest Tel: + 4 021 310 66 05 |
|
Ireland KRKA Pharma Dublin, Ltd. Tel: + 353 1 293 91 80 |
Slovenija KRKA, d.d., Novo mesto Tel: + 386 (0) 1 47 51 100 |
|
Ísland KRKA Sverige AB Sími: + 46 (0)8 643 67 66 (SE) |
Slovenská republika KRKA Slovensko, s.r.o. Tel: + 421 (0) 2 571 04 501 |
|
Italia KRKA Farmaceutici Milano S.r.l. Tel: + 39 02 3300 8841 |
Suomi/Finland KRKA Finland Oy Puh/Tel: +358 20 754 5330 |
|
Kúnpoq Kipa Pharmacal Ltd. Tn^: + 357 24 651 882 |
Sverige KRKA Sverige AB Tel: + 46 (0)8 643 67 66 (SE) |
|
Latvija KRKA Latvija SIA Tel: + 371 6 733 86 10 |
United Kingdom Consilient Health (UK) Ltd. Tel: + 44(0)203 751 1888 |
|
Fecha de la última revisión de este prospecto: |
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu.
Prospecto: información para el usuario
Vizarsin 100 mg comprimidos bucodispersables
Sildenafilo
Lea todo el prospecto detenidamente antes de empezar a tomar este medicamento, porque contiene información importante para usted.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto
1. Qué es Vizarsin y para qué se utiliza
2. Qué necesita saber antes de empezar a tomar Vizarsin
3. Cómo tomar Vizarsin
4. Posibles efectos adversos
5. Conservación de Vizarsin
6. Contenido del envase e información adicional
1. Qué es Vizarsin y para qué se utiliza
Vizarsin contiene el principio activo sildenafilo, que pertenece a un grupo de medicamentos denominados inhibidores de la fosfodiesterasa tipo 5 (PDE5). Actúa dilatando los vasos sanguíneos del pene, permitiendo la afluencia de sangre cuando se está sexualmente estimulado. Vizarsin sólo le ayudará a conseguir una erección si se encuentra sexualmente estimulado.
Vizarsin está indicado en el tratamiento de la disfunción eréctil en hombres adultos, a veces denominada impotencia. Esto sucede cuando un varón no puede obtener o mantener una erección firme, adecuada para una actividad sexual satisfactoria.
2. Qué necesita saber antes de empezar a tomar Vizarsin
No tome Vizarsin
- Si es alérgico a sildenafilo o a alguno de los demás componentes de este medicamento (incluidos en la sección 6).
- Si está tomando unos medicamentos llamados nitratos, ya que la combinación puede dar lugar a una disminución peligrosa de su presión sanguínea. Consulte con su médico si está tomando cualquiera de estos medicamentos, que a menudo, se administran para aliviar el dolor de angina de pecho (o “dolor de pecho”). Si no está seguro, consulte con su médico o farmacéutico.
- Si está utilizando cualquiera de los medicamentos denominados dadores de óxido nítrico tales como nitrato de amilo (“poppers”), ya que la combinación puede dar lugar a una disminución peligrosa de su presión sanguínea.
- Si está tomando riociguat. Este medicamento se utiliza para tratar la hipertensión arterial pulmonar (es decir, tensión alta en los pulmones) y la hipertensión pulmonar tromboembólica crónica (es decir, tensión alta en los pulmones provocada por coágulos). Los inhibidores de la PDE5, como Vizarsin, han mostrado que producen un incremento del efecto hipotensivo de este medicamento. Si está tomando riociguat o no está seguro consulte a su médico.
- Si tiene un problema grave de corazón o hígado.
- Si ha padecido recientemente un accidente isquémico cerebral o ataque al corazón o si tiene la tensión arterial baja.
- Si padece una rara enfermedad ocular hereditaria (tal como retinitis pigmentosa).
- Si ha experimentado anteriormente una pérdida de la visión debido a una neuropatía óptica
isquémica anterior no arterítica (NOIA-NA).
Advertencias y precauciones
Consulte a su médico o farmacéutico antes de empezar a tomar Vizarsin:
- Si padece anemia falciforme (una anormalidad de los glóbulos rojos), leucemia (cáncer de las células sanguíneas), mieloma múltiple (cáncer de médula ósea).
- Si padece una deformidad del pene o enfermedad de Peyronie.
- Si padece problemas del corazón. Su médico debe comprobar cuidadosamente si su corazón
puede soportar el esfuerzo adicional de mantener relaciones sexuales.
- Si padece actualmente úlcera de estómago o problemas hemorrágicos (tales como hemofilia).
- Si experimenta una disminución o pérdida repentina de la visión, deje de tomar Vizarsin y
contacte con su médico inmediatamente.
No se aconseja utilizar Vizarsin simultáneamente con ningún otro tratamiento oral o local para la disfunción eréctil.
No debe tomar Vizarsin con tratamientos para la hipertensión arterial pulmonar (HAP) que contengan sildenafilo o cualquier otro inhibidor de la PDE5.
No debe tomar Vizarsin si no tiene disfunción eréctil.
El uso de Vizarsin no está indicado en mujeres.
Consideraciones especiales en pacientes con problemas renales o hepáticos
Debe comunicar a su médico si tiene problemas renales o hepáticos. Su médico puede decidir reducirle la dosis.
Niños y adolescentes
El uso de Vizarsin no está indicado en personas menores de 18 años.
Uso de Vizarsin con otros medicamentos
Consulte a su médico o farmacéutico si está utilizando, ha utilizado recientemente o pudiera tener que utilizar cualquier otro medicamento.
Vizarsin puede interferir con algunos medicamentos, especialmente los utilizados para tratar el dolor de pecho. En caso de una urgencia médica, debe informar a su médico, farmacéutico o enfermero que está tomando Vizarsin y cuando lo tomó. No debe tomar Vizarsin con otros medicamentos a menos que su médico se lo aconseje.
No debe tomar Vizarsin si está tomando medicamentos denominados nitratos, ya que la combinación de estos medicamentos puede dar lugar a un descenso peligroso de su presión sanguínea. Siempre informe a su médico, farmacéutico o enfermero si está tomando cualquiera de estos medicamentos, que a menudo, se utilizan para aliviar el dolor de la angina de pecho (o “dolor de pecho”).
No debe tomar Vizarsin si está tomando medicamentos denominados dadores de óxido nítrico, tales como nitrito de amilo (“poppers”), ya que la combinación de estos medicamentos también puede dar lugar a un descenso peligroso de su presión sanguínea.
Informe a su médico o farmacéutico si está tomando riociguat.
Si está tomando medicamentos conocidos como inhibidores de la proteasa, como los utilizados en el tratamiento del VIH, su médico puede recomendarle que comience el tratamiento con la dosis más baja (25 mg) de Vizarsin.
Algunos pacientes que están recibiendo un alfabloqueante, medicamento utilizado para el tratamiento de la presión arterial alta o de la hipertrofia prostática, pueden experimentar mareos o sensación de vahído que pueden ser causados por una disminución de la tensión arterial al sentarse o levantarse rápidamente. Algunos pacientes han experimentado estos síntomas al tomar Vizarsin con alfabloqueantes. Esto es más probable que suceda en las 4 horas siguientes a la toma de Vizarsin. Con el fin de disminuir la probabilidad de que ocurran estos síntomas, deberá estar recibiendo su dosis diaria del alfabloqueante de forma regular antes de comenzar con Vizarsin. Su médico puede indicarle que comience el tratamiento con la dosis inferior (25 mg) de Vizarsin.
Uso de Vizarsin con alimentos, bebidas y alcohol
Vizarsin puede tomarse con o sin alimentos. Sin embargo, puede notar que Vizarsin tarde un poco más en hacer efecto si se ingiere con una comida copiosa. Debe tener la boca vacía antes de tomar el comprimido.
La ingesta de alcohol puede dificultar, temporalmente, la capacidad para obtener una erección. Por lo tanto, para conseguir el máximo beneficio del medicamento, se aconseja no ingerir grandes cantidades de alcohol antes de tomar Vizarsin.
Embarazo, lactancia y fertilidad
El uso de Vizarsin no está indicado en mujeres.
Conducción y uso de máquinas
Vizarsin puede producir mareos y afectar a la visión. Debe saber cómo reacciona usted a Vizarsin antes de conducir vehículos o utilizar maquinaria.
Vizarsin contiene aspartamo (E951) y sorbitol (E420)
El aspartamo es una fuente de fenilalanina. Puede ser perjudicial para personas con fenilcetonuria. Vizarsin contiene sorbitol. Si su médico le ha indicado que padece una intoleracia a ciertos azúcares, consulte a su él antes de tomar este medicamento.
3. Cómo tomar Vizarsin
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
La dosis recomendada de inicio es 50 mg.
No se debe tomar Vizarsin más de una vez al día.
No tome Vizarsin comprimidos bucodispersables al mismo tiempo que otras presentaciones de Vizarsin.
Debe tomar Vizarsin aproximadamente una hora antes de que planee tener relaciones sexuales.
Los comprimidos de Vizarsin son frágiles. No debe empujarlos a través de la pared del blíster porque podría romper los comprimidos. No manipule los comprimidos con las manos húmedas, ya que podría romperlos. Para retirar un comprimido siga estos pasos:
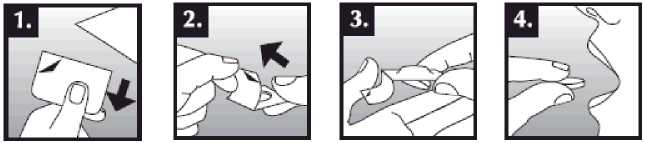
Para blísters de 4 comprimidos:
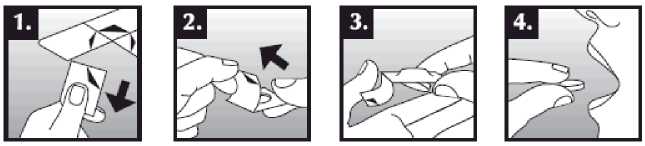
1. Sujete el blíster por los bordes y separe una de las unidades rasgando con cuidado por las marcas troqueladas.
2. Despegue completamente la hoja tirando hacia arriba del borde.
3. Voltee el blíster para colocar el comprimido en su mano.
4. En cuanto haya salido el comprimido, colóqueselo en la lengua.
En unos segundos comenzará a desintegrarse en la boca, por lo que se puede tomar con o sin agua. Debe tener la boca vacía antes de colocarse el comprimido en la lengua.
Si nota que la acción de Vizarsin es demasiado fuerte o débil, comuníqueselo a su médico o farmacéutico.
Vizarsin sólo le ayudará a conseguir una erección si se encuentra sexualmente estimulado. El tiempo que necesita Vizarsin para hacer efecto varía de una persona a otra, generalmente oscila entre media y una hora. El efecto de Vizarsin puede retrasarse si lo toma con una comida copiosa.
En el caso de que Vizarsin no le ayude a conseguir una erección o si la erección no se mantiene el tiempo suficiente para completar el acto sexual, consulte a su médico.
Si toma más Vizarsin del que debe
Puede experimentar un incremento en los efectos adversos y su gravedad. Dosis superiores a 100 mg no aumentan la eficacia.
No debe tomar más comprimidos de los recomendados por el médico.
Contacte con su médico si ha tomado más comprimidos de los aconsejados.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran. Los efectos adversos notificados asociados al uso de Vizarsin son por lo general de intensidad leve a moderada y de corta duración.
Si experimenta cualquiera de los siguientes efectos adversos graves, deje de tomar Vizarsin y busque atención médica inmediatamente:
- Reacción alérgica - esto ocurre con poca frecuencia (puede afectar hasta 1 de cada 100 personas).
Los síntomas incluyen silbido repentino al respirar, dificultad para respirar o mareo, hinchazón de los párpados, cara, labios o garganta.
- Dolores en el pecho - esto ocurre con poca frecuencia.
Si aparecen durante o después de mantener relaciones sexuales:
- Sitúese en una posición semisentada e intente relajarse.
- No use nitratos para tratar el dolor en el pecho.
- Erecciones prolongadas y a veces dolorosas - esto ocurre raramente (puede afectar hasta 1 de cada 1.000 personas).
Si usted tiene una erección que dura más de 4 horas, debe contactar con su médico inmediatamente.
- Disminución repentina o pérdida de la visión - esto ocurre raramente.
- Reacciones graves de la piel - esto ocurre raramente.
Los síntomas pueden incluir descamación grave e hinchazón de la piel, vesiculación bucal, de los genitales y alrededor de los ojos, además de fiebre.
- Convulsiones o ataques - esto ocurre raramente.
Otros efectos adversos:
Muy frecuentes (pueden afectar a más de 1 de cada 10 personas): dolor de cabeza.
Frecuentes (pueden afectar hasta 1 de cada 10 personas): náuseas, enrojecimiento facial, acaloramiento (entre los síntomas se incluye la sensación de calor repentina en la parte superior del cuerpo), indigestión, percepción anormal del color, visión borrosa, deterioro visual, congestión nasal y mareos.
Poco frecuentes (pueden afectar hasta 1 de cada 100 personas): vómitos, erupciones cutáneas, irritación ocular, derrame ocular/ojos rojos, dolor ocular, visión de luces parpadeantes, claridad visual, sensibilidad a la luz, ojos llorosos, palpitaciones, latido cardíaco rápido, presión arterial alta, presión arterial baja, dolor muscular, sensación de somnolencia, sensación al tacto reducido, vértigo, pitidos en los oídos, boca seca, bloqueo o congestión de los senos nasales, inflamación de la mucosa de la nariz (entre los síntomas se incluyen moqueo, estornudos y congestión nasal), dolor en la zona superior del abdomen, enfermedad por reflujo gastroesofágico (entre los síntomas se encuentra el ardor de estómago), sangre presente en orina, dolor en brazos o piernas, sangrado de la nariz, sensación de calor y sensación de cansancio.
Raros (pueden afectar hasta 1 de cada 1.000 personas): desvanecimiento, accidente cerebrovascular, ataque cardíaco, latido cardíaco irregular, disminución transitoria del flujo sanguíneo a algunas partes del cerebro, sensación de opresión en la garganta, adormecimiento de la boca, sangrado en la parte posterior del ojo, visión doble, disminución de la agudeza visual, sensación anormal en el ojo, hinchazón ocular o del párpado, pequeñas partículas o manchas en la vista, visión de halos alrededor de las luces, dilatación de la pupila del ojo, cambio de color de la parte blanca del ojo, sangrado del pene, presencia de sangre en el semen, nariz seca, hinchazón del interior de la nariz, sensación de irritabilidad y disminución o pérdida repentina de la audición.
Durante la experiencia postcomercialización se han comunicado raramente casos de angina inestable (enfermedad cardíaca) y muerte súbita. Cabe destacar que la mayoría de los hombres que experimentaron estos efectos adversos, aunque no todos ellos, tenía problemas cardíacos antes de tomar este medicamento. No es posible determinar si estos efectos adversos estuvieron relacionados directamente con Vizarsin.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se
trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de Vizarsin
Mantener este medicamento fuera de la vista y del alcance de los niños.
No utilice este medicamento después de la fecha de caducidad que aparece en la caja y en el blíster después de EXP. La fecha de caducidad es el último día del mes que se indica.
No conservar a temperatura superior a 30°C.
Conservar en el embalaje original para protegerlo de la humedad.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que ya no necesita. De esta forma, ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional Composición de Vizarsin
- El principio activo es sildenafilo. Cada comprimido bucodispersable contiene 100 mg de sildenafilo.
- El resto de los ingredientes son hidroxipropilcelulosa (E463), manitol (E421), aspartamo (E951), neohesperidina-dihidrochalcona (E959), aroma de hierbabuena, aroma de menta (que contiene sorbitol (E420)), crospovidona, silicato de calcio y estearato de magnesio (E572).
Aspecto del producto y contenido del envase
Comprimidos blancos o blanquecinos, redondos, biconvexos y eventualmente con manchas más oscuras.
Vizarsin comprimidos bucodispersables están disponible en cajas de 1 comprimido bucodispersable en blíster y también en cajas de 2 x 1, 4 x 1, 8 x 1, 12 x 1 o 24 x 1 comprimido bucodispersable en blísters perforados unidosis.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia Responsables de la fabricación
KRKA, d.d., Novo mesto, Smaijeska cesta 6, 8501 Novo mesto, Eslovenia TAD Pharma GmbH, Heinz-Lohmann-StraBe 5, 27472 Cuxhaven, Alemania
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Belgie/Belgique/Belgien
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091
Etarapna
KPKA Etarapua EOOfl Tea.: + 359 (02) 962 34 50
Lietuva
UAB KRKA Lietuva Tel: + 370 5 236 27 40
Luxembourg/Luxemburg
KRKA Belgium, SA.
Tél/Tel: +32 (0) 489 304 091 (BE)
|
Ceská republika KRKA CR, s.r.o. Tel: + 420 (0) 221 115 150 |
Magyarország KRKA Magyarország Kereskedelmi Kft. Tel.: + 361 (0) 355 8490 |
|
Danmark KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
Malta E. J. Busuttil Ltd. Tel: + 356 21 445 885 |
|
Deutschland TAD Pharma GmbH Tel: + 49 (0) 4721 606-0 |
Nederland KRKA Belgium, SA. Tel: +32 (0) 489 304 091 (BE) |
|
Eesti KRKA, d.d., Novo mesto Eesti filiaal Tel: + 372 (0) 6 671 658 |
Norge KRKA Sverige AB Tlf: + 46 (0)8 643 67 66 (SE) |
|
EXláSa QUALIA PHARMA S.A. Tn^: +30 (0)210 2832941 |
Osterreich KRKA Pharma GmbH, Wien Tel: + 43 (0)1 66 24 300 |
|
España KERN PHARMA, S.L. Tel: + 34 93 700 25 25 |
Polska KRKA-POLSKA Sp. z o.o. Tel.: + 48 (0)22 573 7500 |
|
France KRKA France Eurl Tél: + 33 (0)1 57 40 82 25 |
Portugal KRKA Farmacéutica, Sociedade Unipessoal Lda. Tel: + 351 (0)21 46 43 650 |
|
Hrvatska KRKA - FARMA d.o.o. Tel: + 385 1 6312 100 |
Romania KRKA Romania S.R.L., Bucharest Tel: + 4 021 310 66 05 |
|
Ireland KRKA Pharma Dublin, Ltd. Tel: + 353 1 293 91 80 |
Slovenija KRKA, d.d., Novo mesto Tel: + 386 (0) 1 47 51 100 |
|
Ísland KRKA Sverige AB Sími: + 46 (0)8 643 67 66 (SE) |
Slovenská republika KRKA Slovensko, s.r.o. Tel: + 421 (0) 2 571 04 501 |
|
Italia KRKA Farmaceutici Milano S.r.l. Tel: + 39 02 3300 8841 |
Suomi/Finland KRKA Finland Oy Puh/Tel: +358 20 754 5330 |
|
Kúnpoq Kipa Pharmacal Ltd. Tn^: + 357 24 651 882 |
Sverige KRKA Sverige AB Tel: + 46 (0)8 643 67 66 (SE) |
|
Latvija KRKA Latvija SIA Tel: + 371 6 733 86 10 |
United Kingdom Consilient Health (UK) Ltd. Tel: + 44(0)203 751 1888 |
|
Fecha de la última revisión de este prospecto: |
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu.
109