Pecfent 400 Microgramos/Pulverizacion, Solucion Para Pulverizacion Nasal
ANEXO I
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
1. NOMBRE DEL MEDICAMENTO
PecFent 100 microgramos/pulverización, solución para pulverización nasal PecFent 400 microgramos/pulverización, solución para pulverización nasal
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
PecFent 100 microgramos/pulverización, solución para pulverización nasal Cada ml de solución contiene 1000 microgramos de fentanilo (como citrato).
Una pulverización (100 microlitros) contiene 100 microgramos de fentanilo (como citrato). Los frascos contienen:
0,95 ml (950 microgramos de fentanilo) - frasco de 2 pulverizaciones
0
1,55 ml (1550 microgramos de fentanilo) - frasco de 8 pulverizaciones.
PecFent 400 microgramos/pulverización, solución para pulverización nasal Cada ml de solución contiene 4000 microgramos de fentanilo (como citrato)
1 pulverización (100 microlitros) contiene 400 microgramos de fentanilo (como citrato)
Cada frasco contiene 1,55 ml (6200 microgramos de fentanilo)
Excipientes con efecto conocido:
Cada pulverización contiene 0,02 mg de propilparahidroxibenzoato (E216).
Para consultar la lista completa de excipientes, ver sección 6.1.
3. FORMA FARMACÉUTICA
Solución para pulverización nasal (pulverización nasal).
Solución transparente a prácticamente transparente, incolora y acuosa.
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
PecFent está indicado para el tratamiento del dolor irruptivo en los adultos que están recibiendo tratamiento de mantenimiento con opioides para el dolor oncológico crónico. El dolor irruptivo es una exacerbación transitoria del dolor que se produce sobre un dolor de base persistente, por lo demás, controlado.
Los pacientes que reciben tratamiento de mantenimiento con opioides son aquellos que toman como mínimo 60 mg de morfina por vía oral al día, 25 microgramos de fentanilo por vía transdérmica por hora, 30 mg de oxicodona diarios, 8 mg de hidromorfona diarios o una dosis equianalgésica de otro opioide, durante una semana o más.
4.2 Posología y forma de administración
El tratamiento debe ser iniciado y permanecer bajo la supervisión de un médico con experiencia en el tratamiento con opioides en los pacientes con cáncer. Los médicos deben tener en cuenta el potencial de abuso del fentanilo.
Posología
La dosis de PecFent debe ajustarse a una dosis “eficaz” que proporcione una analgesia adecuada y minimice las reacciones adversas, sin causar reacciones adversas excesivas (o intolerables), durante dos episodios de dolor irruptivo tratados consecutivamente. La eficacia de una dosis determinada debe evaluarse durante el siguiente período de 30 minutos.
Se debe vigilar meticulosamente a los pacientes hasta que se alcance una dosis eficaz.
PecFent está disponible en dos concentraciones: 100 microgramos/pulverización y 400 microgramos/pulverización.
Una dosis de PecFent puede consistir en la administración de una pulverización (dosis de 100 microgramos o 400 microgramos) o dos pulverizaciones (dosis de 200 microgramos u 800 microgramos) de la misma concentración (concentración de 100 microgramos o 400 microgramos).
Los pacientes no deben usar más de cuatro dosis al día. Los pacientes deben esperar por lo menos cuatro horas después de una dosis, antes de tratar otro episodio de dolor irruptivo con PecFent.
PecFent puede administrar dosis de 100, 200, 400 y 800 microgramos de la siguiente manera:
|
Dosis requerida (microgramos) |
Concentración del producto (microgramos) |
Cantidad |
|
100 |
100 |
Una pulverización administrada en una fosa nasal |
|
200 |
100 |
Una pulverización administrada en cada fosa nasal |
|
400 |
400 |
Una pulverización administrada en una fosa nasal |
|
800 |
400 |
Una pulverización administrada en cada fosa nasal |
Dosis inicial
• La dosis inicial de PecFent para tratar los episodios de dolor irruptivo es siempre de
100 microgramos (una pulverización), incluso en los pacientes que ya estaban tomando otros productos que contienen fentanilo para el dolor irruptivo y cambian el tratamiento.
• Los pacientes deben esperar por lo menos cuatro horas antes de tratar otro episodio de dolor irruptivo con PecFent.
Método de ajuste de la dosis
• Se debe recetar a los pacientes un frasco (dos pulverizaciones u ocho pulverizaciones) de PecFent 100 microgramos/pulverización para el ajuste inicial de la dosis.
• A los pacientes con dosis inicial de 100 microgramos y que necesiten una dosis más alta debido a una ausencia de efecto, se les puede indicar que usen dos pulverizaciones de 100 microgramos (una en cada fosa nasal) para su siguiente episodio de dolor irruptivo. Si esta dosis no es satisfactoria, se debe recetar al paciente un frasco de PecFent 400 microgramos/pulverización, y se les debe indicar que cambien a una pulverización de 400 microgramos para su siguiente episodio de dolor. Si esta dosis no es satisfactoria, se debe indicar al paciente que aumente a dos pulverizaciones de 400 microgramos (una en cada fosa nasal).
• Desde el inicio del tratamiento, se debe hacer un seguimiento estricto de cada paciente, y la dosis debe ajustarse hasta que se alcance una dosis eficaz, la cual debe confirmarse durante dos episodios de dolor irruptivo tratados consecutivamente.
Ajuste de la dosis en pacientes que cambian entre medicamentos que contienen fentanilo de liberación inmediata
Pueden existir diferencias sustanciales en el perfil farmacocinético de los medicamentos de fentanilo de liberación inmediata, lo que produce diferencias clínicamente importantes en la velocidad y grado de absorción del fentanilo. Por lo tanto, al cambiar entre medicamentos que contienen fentanilo indicados para el tratamiento del dolor irruptivo, incluidas las formulaciones intranasales, es esencial volver a realizar a los pacientes el ajuste de la dosis del medicamento nuevo, y no hacer un cambio de dosis por dosis (microgramo por microgramo).
Tratamiento de mantenimiento
Una vez establecida una dosis eficaz durante el ajuste de la dosis, los pacientes deben seguir tomando esta dosis, hasta un máximo de cuatro dosis al día.
Reajuste de la dosis
En general, la dosis de mantenimiento de PecFent debe aumentarse solo si la dosis actual no trata adecuadamente el dolor irruptivo durante varios episodios consecutivos.
En los pacientes que presenten de manera constante más de cuatro episodios de dolor irruptivo cada 24 horas, puede ser necesario revisar la dosis del tratamiento de base con opioides.
Si las reacciones adversas son intolerables o persistentes, la dosis debe reducirse o el tratamiento con PecFent debe reemplazarse por otro analgésico.
Suspensión definitiva del tratamiento
El tratamiento con PecFent debe interrumpirse definitivamente y de inmediato si el paciente ya no sufre episodios de dolor irruptivo. El tratamiento del dolor de base persistente debe mantenerse de la manera prescrita.
Si se hace necesaria la suspensión definitiva de todo el tratamiento con opioides, el médico debe hacer un seguimiento estricto del paciente, ya que se precisa una disminución gradual de la dosis de opioides a fin de evitar la posibilidad de efectos abruptos de abstinencia.
Poblaciones especiales
Personas de edad avanzada (mayores de 65 años)
En el programa del estudio clínico de PecFent, 104 (26,1 %) pacientes tenían más de 60 años; 67 (16,8 %) más de 65 años y 15 (3,8 %) más de 75 años. No hubo ninguna indicación de que los pacientes de edad avanzada tendieran a ajustar la dosis a dosis más bajas o de que sufrieran más reacciones adversas. No obstante, en vista de la importancia de las funciones renal y hepática en el metabolismo y la depuración del fentanilo, se debe tener más cuidado cuando se use PecFent en las personas de edad avanzada. No se dispone de datos acerca de las propiedades farmacocinéticas de PecFent en los pacientes de edad avanzada.
Insuficiencia hepática o renal
PecFent debe administrarse con precaución a los pacientes con insuficiencia hepática o renal moderada o grave (ver sección 4.4).
Población pediátrica
No se ha establecido todavía la seguridad y eficacia de PecFent en niños y adolescentes menores de 18 años.
No se dispone de datos.
Forma de administración
PecFent se administra solo por vía nasal.
El frasco se debe extraer del envase con cierre de seguridad a prueba de niños inmediatamente antes de su uso, y el tapón protector se debe quitar. El frasco se debe cebar antes del primer uso; para ello, debe sostenerse en posición vertical, y se deben oprimir y soltar los agarres digitales en ambos lados de la boquilla, hasta que aparezca una barra verde en la ventana de recuento (debe aparecer después de cuatro pulverizaciones).
Frasco de 2 pulverizaciones:
El frasco de 2 pulverizaciones no se puede volver a cebar, y una vez que se han utilizado ambas dosis, o si han transcurrido más de 5 días desde el cebado, el frasco y su contenido deben desecharse como se describe en la sección 6.6.
Frasco de 8 pulverizaciones:
Si pasan cinco días sin que se use el producto, se debe volver a cebar pulverizando una vez. Se debe aconsejar al paciente que escriba la fecha del primer uso en el espacio proporcionado en la etiqueta del envase a prueba de niños.
Para administrar PecFent, la boquilla se coloca a corta distancia (aproximadamente 1 cm) en el interior de la fosa nasal, y se apunta ligeramente hacia el puente de la nariz. A continuación, se administra una pulverización; para ello, se oprimen y se sueltan los agarres digitales de cada lado de la boquilla. Se oirá un clic y el número que aparece en el contador avanzará en una unidad.
Se debe indicar a los pacientes que tal vez no sientan la administración de la pulverización, y que, por lo tanto, para confirmar que se ha administrado una pulverización, deben guiarse por el clic que oirán y por el número que avanza en el contador.
Las microgotas de la pulverización de PecFent forman un gel en la nariz. Se debe aconsejar a los pacientes que no se suenen la nariz inmediatamente después de la administración de PecFent.
Se debe volver a tapar el frasco con el tapón protector después de cada uso y el frasco debe volver a colocarse en el envase con cierre de seguridad a prueba de niños, para su conservación segura.
4.3 Contraindicaciones
Hipersensibilidad al principio activo o a alguno de los excipientes incluidos en la sección 6.1.
Pacientes que no estén en tratamiento de mantenimiento con opioides, por el mayor riesgo de depresión respiratoria.
Depresión respiratoria grave o trastornos pulmonares obstructivos graves.
Tratamiento del dolor agudo distinto al dolor irruptivo.
4.4 Advertencias y precauciones especiales de empleo
Se debe indicar a los pacientes y a sus cuidadores que PecFent contiene un principio activo en una cantidad que puede ser mortal para un niño.
A fin de reducir al mínimo los riesgos de reacciones adversas relacionadas con los opioides y para identificar la dosis efectiva, es imprescindible que los profesionales médicos vigilen atentamente a los pacientes durante el proceso de ajuste de la dosis.
Es importante que el tratamiento con opioides de acción prolongada usados para tratar el dolor persistente del paciente se haya estabilizado antes de comenzar el tratamiento con PecFent.
Depresión respiratoria
Hay un riesgo de depresión respiratoria clínicamente significativa asociada con el uso de fentanilo.
Los pacientes con dolor que reciben tratamiento crónico con opioides pueden presentar una tolerancia a la depresión respiratoria y, por tanto, el riesgo de depresión respiratoria en estos pacientes es reducido. El uso simultáneo de depresores del sistema nervioso central puede aumentar el riesgo de depresión respiratoria (ver sección 4.5).
Enfermedad pulmonar crónica
En los pacientes con enfermedades pulmonares obstructivas crónicas, el fentanilo puede causar reacciones adversas más graves. En estos pacientes, los opioides pueden reducir la movilidad respiratoria y aumentar la resistencia de las vías respiratorias.
Aumento de la presión intracraneal
PecFent debe administrarse solo con suma precaución a los pacientes que pueden ser especialmente sensibles a los efectos intracraneales de la retención de CO2, por ejemplo, los que tienen indicios de aumento de la presión intracraneal o alteración de la conciencia. Los opioides pueden enmascarar la evolución clínica de los pacientes con una lesión craneal y solo deben emplearse si ello está clínicamente justificado.
Cardiopatías
El fentanilo puede provocar bradicardia. Por tanto, PecFent debe administrarse con precaución en pacientes con bradiarritmias previas o ya existentes.
Insuficiencia hepática o renal
Además, PecFent debe administrarse con precaución a los pacientes con insuficiencia hepática o renal. No se han evaluado los efectos de la insuficiencia hepática o renal sobre las características farmacocinéticas del medicamento; sin embargo, si se administra por vía intravenosa, se ha demostrado que la depuración del fentanilo está alterada en los pacientes con insuficiencia hepática o renal, debido a las alteraciones en la depuración metabólica y en las proteínas plasmáticas. Por lo tanto, en los pacientes con insuficiencia hepática o renal, moderada o grave, debe tenerse un cuidado especial durante el proceso de ajuste de la dosis.
Debe prestarse una atención especial a los pacientes con hipovolemia o hipotensión.
Potencial de abuso y tolerancia
Después de la administración repetida de opioides como el fentanilo, pueden producirse tolerancia y dependencia física o psicológica. Sin embargo, la adicción yatrógena después del uso terapéutico de los opioides es rara.
Se debe informar a los deportistas de que el tratamiento con fentanilo puede dar resultados positivos en los análisis antidopaje.
Síndrome serotoninérgico
Se recomienda precaución cuando PecFent se administre de forma concomitante con medicamentos que afecten a los sistemas de neurotransmisores serotoninérgicos.
El desarrollo de un síndrome serotoninérgico potencialmente mortal puede aparecer con el uso concomitante de medicamentos serotoninérgicos, como los inhibidores selectivos de la recaptación de serotonina (ISRS) y los inhibidores de la recaptación de serotonina y noradrenalina (IRSN), y con los medicamentos que afectan al metabolismo de la serotonina (incluidos los inhibidores de la monoaminooxidasa [IMAO]). Esto puede ocurrir con la dosis recomendada (ver sección 4.5).
El síndrome serotoninérgico puede incluir cambios en el estado mental (p. ej., agitación, alucinaciones, coma), inestabilidad autonómica (p. ej., taquicardia, presión arterial lábil, hipertermia), anomalías neuromusculares (p. ej., hiperreflexia, descoordinación, rigidez) y/o síntomas gastrointestinales (p. ej., náuseas, vómitos, diarrea).
Si se sospecha de un síndrome serotoninérgico, debe suspenderse el tratamiento con PecFent.
Vía de administración
PecFent solo está indicado para la administración por vía nasal y no se debe administrar por otra vía. Debido a las propiedades fisicoquímicas de los excipientes incluidos en la formulación, debe evitarse en particular la inyección intravenosa o intrarterial.
Enfermedades nasales
Si el paciente sufre episodios recurrentes de epistaxis o molestias nasales mientras toma PecFent, debe plantearse otra forma de administración para el tratamiento del dolor irruptivo.
Excipientes de PecFent
PecFent contiene propilparahidroxibenzoato (E216), que puede causar reacciones alérgicas (posiblemente retardadas) y, excepcionalmente, broncoespasmo (si el medicamento no se administra correctamente).
4.5 Interacción con otros medicamentos y otras formas de interacción
El fentanilo se metaboliza principalmente por medio del sistema de la isoenzima humana citocromo P450 3A4 (CYP3A4); por lo tanto, pueden producirse interacciones potenciales si PecFent se administra al mismo tiempo con medicamentos que afectan a la actividad del CYP3A4. La administración simultánea con medicamentos que inducen la actividad del CYP3A4 puede disminuir la eficacia de PecFent. El uso simultáneo de PecFent con inhibidores potentes del CYP3A4 (por ejemplo, ritonavir, ketoconazol, itraconazol, troleandomicina, claritromicina y nelfinavir) o inhibidores moderados del CYP3A4 (por ejemplo, amprenavir, aprepitant, diltiazem, eritromicina, fluconazol, fosamprenavir, zumo de pomelo y verapamilo) puede producir un aumento de las concentraciones plasmáticas de fentanilo, lo que puede causar reacciones farmacológicas adversas graves, incluso depresión respiratoria mortal. Se debe vigilar estrictamente, durante un tiempo prolongado, a los pacientes que reciben PecFent simultáneamente con inhibidores moderados o potentes del CYP3A4. El aumento de la dosis debe realizarse con precaución.
El uso simultáneo de otros depresores del sistema nervioso central, incluidos otros opioides, sedantes o hipnóticos, anestésicos generales, fenotiazinas, tranquilizantes, relajantes del músculo esquelético, antihistamínicos sedantes y alcohol puede producir efectos depresores aditivos.
Medicamentos serotoninérgicos:
La administración concomitante de fentanilo con un medicamento serotoninérgico, como un inhibidor selectivo de la recaptación de serotonina (ISRS), un inhibidor de la recaptación de serotonina y noradrenalina (IRSN) o un inhibidor de la monoaminooxidasa (IMAO), puede aumentar el riesgo de síndrome serotoninérgico, un trastorno potencialmente mortal.
No se recomienda el uso de PecFent en los pacientes que han recibido inhibidores de la monoaminooxidasa (MAO) en los 14 días anteriores, porque se ha descrito una potenciación intensa e impredecible por los inhibidores de la MAO con los analgésicos opioides.
No se recomienda el uso simultáneo de agonistas o antagonistas parciales de los opioides (por ejemplo, buprenorfina, nalbufina, pentazocina). Tienen una gran afinidad por los receptores de los opioides, con una actividad intrínseca relativamente baja y, por lo tanto, antagonizan parcialmente el efecto analgésico del fentanilo y pueden inducir síntomas de abstinencia en los pacientes dependientes de los opioides.
Se ha demostrado que el uso simultáneo de oximetazolina administrada por vía nasal disminuye la absorción de PecFent (ver sección 5.2). Por lo tanto, durante el ajuste de la dosis, no se recomienda el uso simultáneo de descongestionantes vasoconstrictores administrados por vía nasal, ya que ello puede llevar a ajustar la dosis de los pacientes a una más alta de lo requerido. El tratamiento con mantenimiento con PecFent también puede ser menos eficaz en los pacientes con rinitis si se administra simultáneamente con un descongestionante vasoconstrictor nasal. Si esto ocurre, se debe aconsejar a los pacientes que suspendan la administración del descongestionante.
No se ha evaluado en estudios clínicos el uso simultáneo de PecFent y otros medicamentos (aparte de la oximetazolina) administrados por vía nasal. Deben evitarse otros tratamientos administrados por vía nasal en los 15 minutos posteriores a la administración de PecFent.
4.6 Fertilidad, embarazo y lactancia
Embarazo
No hay datos suficientes relativos al uso de fentanilo en mujeres embarazadas. Los estudios realizados en animales han mostrado toxicidad para la reproducción (ver sección 5.3). Se desconoce el riesgo en los seres humanos. PecFent no deberá utilizarse durante el embarazo excepto si resulta claramente necesario.
Después del tratamiento prolongado, el fentanilo puede causar abstinencia en el recién nacido. Se aconseja no usar fentanilo durante el trabajo de parto y el parto (incluida la intervención cesárea) porque el fentanilo pasa a través de la placenta y puede causar depresión respiratoria en el feto. Si se administra PecFent, debe tenerse fácil acceso a un antídoto para el niño.
Lactancia
El fentanilo pasa a la leche materna, y puede causar sedación y depresión respiratoria en el niño que recibe lactancia materna. Las mujeres que amamantan no deben usar fentanilo y la lactancia materna no se debe reiniciar por lo menos hasta 5 días después de la última administración de fentanilo.
Fertilidad
No hay datos clínicos relativos a los efectos del fentanilo sobre la fertilidad.
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
Los analgésicos opioides pueden alterar la capacidad mental o física requerida para conducir o utilizar máquinas.
Se debe aconsejar a los pacientes que no conduzcan ni utilicen máquinas si presentan somnolencia, mareos, trastornos visuales u otras reacciones adversas que pudieran alterar su capacidad para conducir o utilizar máquinas.
4.8 Reacciones adversas
Resumen del perfil de seguridad
Pueden esperarse las reacciones adversas características de los opioides con PecFent. Con frecuencia, estas cesarán o su intensidad disminuirá con el uso continuado del medicamento, a medida que se ajuste la dosis del paciente hasta encontrar la más adecuada. Sin embargo, las reacciones adversas más graves son depresión respiratoria (que puede llevar a la apnea o a la parada respiratoria), depresión circulatoria, hipotensión y shock, y se debe vigilar a todos los pacientes por si aparecieran estas reacciones.
Los estudios clínicos de PecFent se diseñaron para evaluar la seguridad y la eficacia del tratamiento del dolor irruptivo, y todos los pacientes recibían también tratamientos de base con opioides, como morfina de liberación prolongada y fentanilo transdérmico, para el dolor persistente. Por lo tanto, no es posible separar con certeza los efectos debidos únicamente a PecFent.
Tabla de reacciones adversas
Se han notificado las siguientes reacciones adversas con PecFent y/u otros compuestos que contienen fentanilo provenientes de ensayos clínicos y de la experiencia postcomercialización (frecuencias definidas como muy frecuentes (>1/10); frecuentes (>1/100 a <1/10); poco frecuentes (>1/1.000 a <1/100); raras (>1/10.000 a <1/1.000); muy raras (<1/10.000); frecuencia no conocida (no puede estimarse a partir de los datos disponibles)).
|
Frecuentes |
Poco frecuentes |
Frecuencia no conocida | |
|
Infecciones e infestaciones |
Neumonía Nasofaringitis Faringitis Rinitis | ||
|
Trastornos de la sangre y del sistema linfático |
Neutropenia | ||
|
Trastornos del sistema inmunológico |
Hipersensibilidad | ||
|
Trastornos del metabolismo y de la nutrición |
Deshidratación Hiperglucemia Disminución del apetito Aumento del apetito | ||
|
Trastornos psiquiátricos |
Desorientación |
Abuso de drogas Delirio Alucinaciones Estado de confusión Depresión Trastorno por déficit de atención / hiperactividad Ansiedad Humor eufórico Intranquilidad |
Insomnio |
|
Trastornos del sistema nervioso |
Disgeusia Mareos Somnolencia Cefalea |
Pérdida de la conciencia Depresión del nivel de conciencia Convulsiones Ageusia Anosmia Trastorno de la memoria Parosmia Trastorno del habla Sedación Letargo Temblores | |
|
Trastornos del oído y del laberinto |
Vértigo | ||
|
Trastornos cardiacos |
Cianosis | ||
|
Trastornos vasculares |
Insuficiencia cardiovascular Linfedema Hipotensión Sofocos |
Rubor |
|
Frecuentes |
Poco frecuentes |
Frecuencia no conocida | |
|
Trastornos respiratorios, torácicos y mediastínicos |
Epistaxis Rinorrea Molestias nasales |
Obstrucción de las vías respiratorias altas Dolor faringolaríngeo Rinalgia Trastorno de la mucosa nasal Tos Disnea Estornudos Congestión de las vías respiratorias altas Congestión nasal Hipoestesia intranasal Irritación de la garganta Goteo posnasal Sequedad nasal |
Depresión respiratoria |
|
Trastornos gastrointestinales |
Vómitos Náuseas Estreñimiento |
Perforación intestinal Peritonitis Hipoestesia bucal Parestesia bucal Diarrea Arcadas Dolor abdominal Trastorno de la lengua Úlceras en la boca Dispepsia Sequedad de la boca | |
|
Trastornos de la piel y del tejido subcutáneo |
Prurito |
Hiperhidrosis Urticaria | |
|
Trastornos musculoesqueléticos y del tejido conjuntivo |
Artralgia Espasmos musculares | ||
|
Trastornos renales y urinarios |
Anuria Disuria Proteinuria Dificultad para iniciar la micción | ||
|
Trastornos del aparato reproductor y de la mama |
Hemorragia vaginal | ||
|
Trastornos generales y alteraciones en el lugar de administración |
Dolor torácico no cardiaco Astenia Escalofríos Edema facial Edema periférico Trastorno de la marcha Pirexia Fatiga Malestar Sed |
Síndrome de abstinencia* | |
|
Exploraciones complementarias |
Disminución del recuento de plaquetas Aumento del peso |
|
Frecuentes |
Poco frecuentes |
Frecuencia no conocida | |
|
Lesiones traumáticas, intoxicaciones y complicaciones de procedimientos terapéuticos |
Caídas Uso inadecuado e intencionado de fármacos y drogas Error de la medicación |
*Consultar la siguiente sección a continuación
Descripción de las reacciones adversas seleccionadas
Se han observado con fentanilo transmucosa síntomas de abstinencia a opioides tales como náuseas, vómitos, diarrea, ansiedad, escalofríos, temblores y sudoración.
Notificación de sospechas de reacciones adversas
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del sistema nacional de notificación incluido en el Apéndice V.
4.9 Sobredosis
Se prevé que los síntomas de la sobredosis de fentanilo por la vía nasal sean de naturaleza similar a los del fentanilo y otros opioides por la vía intravenosa, y son una extensión de sus efectos farmacológicos, siendo el efecto significativo más grave la depresión respiratoria.
El tratamiento inmediato de la sobredosis por opioides consiste en asegurar una vía respiratoria permeable, la estimulación física y verbal del paciente, la evaluación del grado de conciencia, el estado ventilatorio y circulatorio, y, si es necesario, la ventilación asistida (apoyo ventilatorio).
Para el tratamiento de la sobredosis (ingestión accidental) de una persona que no ha tomado anteriormente opioides, debe obtenerse un acceso intravenoso y se deben emplear naloxona y otros antagonistas de los opioides, según esté clínicamente indicado. La duración de la depresión respiratoria después de la sobredosis puede ser más prolongada que los efectos de la acción de los antagonistas de los opioides (por ejemplo, la semivida de la naloxona es de 30 a 81 minutos), y puede ser necesaria la administración repetida. Se debe consultar la ficha técnica o resumen de las características del producto del antagonista de los opioides concreto para obtener más información acerca de dicho uso.
Para el tratamiento de la sobredosis en los pacientes en mantenimiento con opioides, debe obtenerse un acceso intravenoso. En algunos casos, puede estar justificado el uso sensato de naloxona u otro antagonista de los opioides; sin embargo, se asocia al riesgo de precipitar un síndrome de abstinencia agudo.
Debe señalarse que, aunque se observaron aumentos estadísticamente significativos de la Cmáx después de una segunda dosis de PecFent administrada una o dos horas después de la dosis inicial, este aumento no se considera lo suficientemente grande como para sugerir que pudiera producirse una acumulación o una sobreexposición clínicamente preocupante, lo que proporciona un amplio margen de seguridad para el intervalo de administración recomendado de cuatro horas.
Aunque no se ha observado rigidez muscular que interfiera con la respiración después del uso de PecFent, esto es posible con el fentanilo y otros opioides. En caso de producirse, debe tratarse mediante ventilación asistida, con un antagonista de los opioides y, como alternativa final, con un bloqueador neuromuscular.
PROPIEDADES FARMACOLÓGICAS
5.
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: Analgésicos, opioides, derivados de la fenilpiperidina; código ATC: N02AB03.
Mecanismo de acción
El fentanilo es un analgésico opioide, que interactúa predominantemente con el receptor p de los opioides. Sus principales efectos terapéuticos son la analgesia y la sedación. Los efectos farmacológicos secundarios son: depresión respiratoria, bradicardia, hipotermia, estreñimiento, miosis, dependencia física y euforia.
Efectos farmacodinámicos
Se ha realizado un estudio doble ciego, aleatorizado, controlado con placebo y cruzado, en el cual 114 pacientes que sufrían, en promedio, de uno a cuatro episodios de dolor irruptivo al día mientras tomaban un tratamiento de mantenimiento con opioides, entraron en una fase inicial y abierta de ajuste de la dosis, a fin de identificar una dosis eficaz de PecFent (estudio CP043). Los pacientes que entraron en la fase de doble ciego recibieron tratamiento para hasta 10 episodios de dolor irruptivo bien con PecFent (7 episodios) o con placebo (3 episodios) conforme a un orden aleatorio.
De los pacientes que entraron en la fase de ajuste de la dosis, solo en siete (6,1 %) no se pudo ajustar la dosis para alcanzar una dosis eficaz, debido a la ausencia de eficacia, y seis (5,3 %) abandonaron el estudio a causa de reacciones adversas.
El criterio principal de valoración fue la comparación entre la diferencia sumada de la intensidad del dolor 30 minutos después de la administración del medicamento (DSID30), que fue de 6,57 en los episodios tratados con PecFent, en comparación con 4,45 en el caso del placebo (p<0,0001). La DSID de los episodios tratados con PecFent también fue significativamente diferente en relación con el placebo, a los 10, 15, 45 y 60 minutos después de la administración.
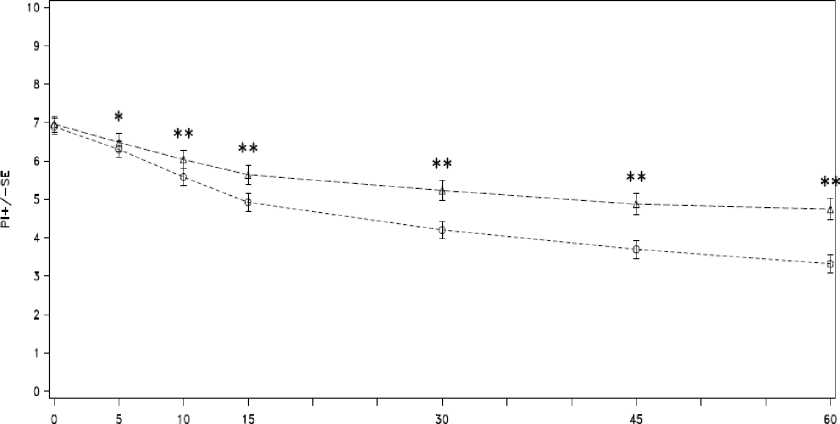
Las puntuaciones medias de intensidad del dolor (73 pacientes) de todos los episodios tratados con PecFent (459 episodios), en comparación con los tratados con placebo (200 episodios), fueron significativamente inferiores, a los 5, 10, 15, 30, 45 y 60 minutos después de la administración (véase la figura 1).
Intensidad del dolor ± e.e.
Figura 1. Media (± e.e.) de la puntuación de intensidad del dolor en cada punto temporal (población con intención de tratar modificada)
_ Tiempo (minutos) _
——- PecFent —t.—p|;j.- i-| ;
Nota: Puntuaciones de intensidad del dolor (media de las medias de los pacientes) después de la administración de PecFent y placebo. * Diferencia significativa detectada en el nivel a <0,05 entre PecFent y placebo en ese punto temporal.
** Diferencia significativa detectada en el nivel a <0,01 entre PecFent y placebo en ese punto temporal.
La eficacia superior de PecFent frente al placebo fue respaldada por los datos de los criterios de valoración secundarios, incluido el número de episodios de dolor irruptivo con un alivio del dolor clínicamente significativo, definido como una reducción en la puntuación de la intensidad del dolor de al menos 2 (Figura 2).
Figura 2: Alivio del dolor clínicamente significativo - PecFent frente al placebo: % de episodios de los pacientes con una reducción en la intensidad del dolor >2 puntos
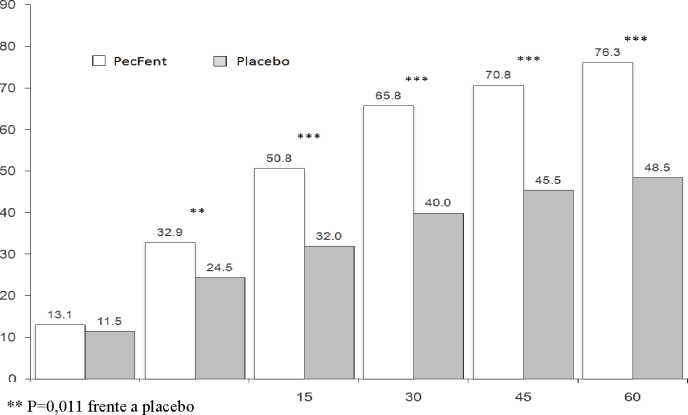
*** P<0,0001 frente a placebo Tiempo desde la administración (minutos)
En un estudio doble ciego, aleatorizado y controlado con un comparador (estudio 044), de un diseño parecido al del estudio 043, realizado en pacientes tolerantes a los opioides, con dolor irruptivo oncológico, que recibían dosis estables de opioides programados regularmente, se demostró que PecFent fue superior al sulfato de morfina de liberación inmediata. La superioridad se demostró por el criterio principal de valoración, la diferencia de la intensidad del dolor al cabo de 15 minutos, que fue de 3,02 en los pacientes tratados con PecFent, en comparación con 2,69 en los tratados con sulfato de morfina de liberación inmediata (p=0,0396).
En un estudio de seguridad abierto y a largo plazo (estudio 045), 355 pacientes entraron en la fase de tratamiento de 16 semanas, durante la cual 42 227 episodios de dolor irruptivo oncológico recibieron tratamiento con PecFent. Cien de estos pacientes continuaron el tratamiento durante un período de hasta 26 meses, en una fase de ampliación. De los 355 pacientes tratados en la fase abierta de tratamiento, el 90 % no precisó un aumento de la dosis.
En el estudio aleatorizado, controlado con placebo (CP043), en el 9,4 % de los 459 episodios de dolor irruptivo tratados con PecFent en 73 pacientes se tuvo que utilizar otros medicamentos adicionales (de rescate) en el plazo de 60 minutos de la administración. Durante el estudio abierto, a más largo plazo (CP045), esto ocurrió en el 6,0 % de los 42 227 episodios en 355 pacientes tratados con PecFent durante los 159 días de tratamiento.
5.2 Propiedades farmacocinéticas
Introducción general
El fentanilo es muy lipofílico y puede absorberse muy rápidamente a través de la mucosa nasal y más lentamente por la vía digestiva. Sufre un metabolismo hepático e intestinal de primer paso, y los metabolitos no contribuyen a los efectos terapéuticos del fentanilo.
PecFent utiliza el sistema PecSys de administración nasal de fármacos para modular la administración y la absorción del fentanilo. El sistema PecSys permite pulverizar el producto en la zona frontal de la cavidad nasal como una vaporización fina de microgotas, que se gelifican al entrar en contacto con los iones de calcio presentes en la mucosa nasal. El fentanilo se difunde desde el gel y se absorbe a través de la mucosa nasal; esta absorción del fentanilo modulada por gel restringe el valor máximo en la concentración plasmática (Cmáx), mientras que permite que se alcance pronto ese valor máximo (Tmáx).
Absorción
En un estudio farmacocinético de comparación entre PecFent (100, 200, 400 y 800 pg) con citrato de fentanilo oral transmucosa (CFOT, 200 pg), se demostró que el fentanilo se absorbe rápidamente después de la administración de una dosis única de PecFent por vía intranasal, con una mediana de Tmáx de 15 a 21 minutos (el Tmáx del CFOT fue de aproximadamente 90 minutos). La variabilidad de las propiedades farmacocinéticas del fentanilo fue considerable después del tratamiento tanto con PecFent como con CFOT. La biodisponibilidad relativa del fentanilo procedente del tratamiento con PecFent, en comparación con 200 pg de CFOT, fue de aproximadamente el 120 %.
Los principales parámetros farmacocinéticos se muestran en la siguiente tabla.
Parámetros farmacocinéticos en pacientes adultos que recibieron PecFent y CFOT.
|
Parámetros farmacocinéticos (media (%CV)) |
PecF |
7ent |
CFOT | ||
|
100 pg |
200 pg |
400 pg |
800 pg |
200 pg | |
|
Tmáx (horas)* |
0,33 (0,08-1,50) |
0,25 (0,17-1,60) |
0,35 (0,25-0,75) |
0,34 (0,17-3,00) |
1,50 (0,50-8,00) |
|
Cmáx (pg/ml) |
351,5 (51,3) |
780,8 (48,4) |
1552,1 (26,2) |
2844,0 (56,0) |
317,4 (29,9) |
|
AUC (pg.hora/ml) |
2460,5 (17,9) |
4359,9 (29,8) |
7513,4 (26,7) |
17272 (48,9) |
3735,0 (32,8) |
|
t1/2 (hora) |
21,9 (13,6) |
24,9 (51,3) |
15,0 (24,7) |
24,9 (92,5) |
18,6 (31,4) |
*Datos correspondientes al Tmáx presentados como mediana (intervalo).
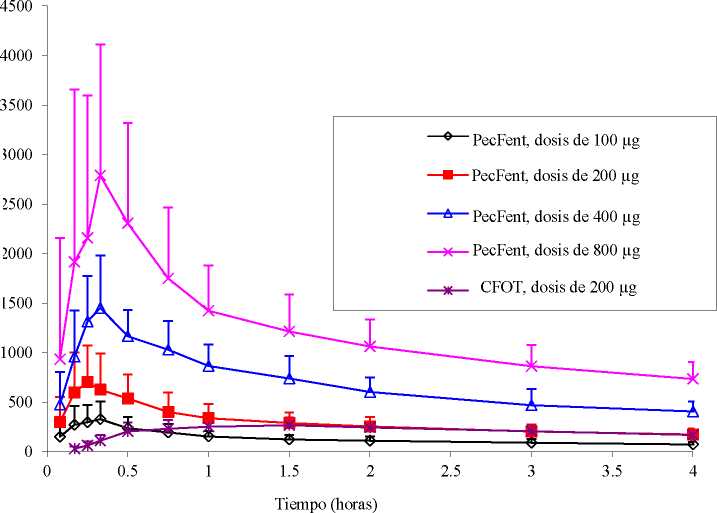
Las curvas correspondientes a cada nivel de dosis tienen formas parecidas y el aumento de los niveles de dosis produce el aumento de las concentraciones plasmáticas de fentanilo. Se demostró la proporcionalidad de la dosis para la Cmáx y el área debajo de la curva (AUC) dentro del intervalo de dosis de 100 a 800 microgramos (véase la figura 3). Si se cambia el tratamiento del dolor irruptivo de otro producto de fentanilo a PecFent, se requiere un ajuste independiente de la dosis de PecFent, ya que la biodisponibilidad entre los productos difiere significativamente.
Figura 3. Concentraciones plasmáticas medias de fentanilo después de dosis únicas de PecFent y CFOT en personas sanas
Se realizó un estudio farmacocinético para evaluar la absorción y la tolerabilidad de una dosis única de PecFent en pacientes con rinitis alérgica estacional, inducida por el polen, mediante la comparación de los estados no expuesto, expuesto agudamente (con rinitis), y expuesto agudamente y luego tratado con oximetazolina.
No hubo ningún efecto clínicamente significativo de la rinitis aguda sobre la Cmáx, el Tmáx o la exposición total al fentanilo, cuando se compararon los estados no expuesto y expuesto agudamente. Después del tratamiento del estado de rinitis aguda con oximetazolina, hubo reducciones de la Cmáx y de la exposición, y aumentos del Tmáx que fueron estadística y, posiblemente, clínicamente significativos.
Distribución
El fentanilo es muy lipofílico y se distribuye bien más allá del aparato vascular, con un volumen aparente de distribución grande. Los datos en animales han demostrado que, después de la absorción, el fentanilo se distribuye rápidamente por el encéfalo, el corazón, los pulmones, los riñones y el bazo, y a continuación, hay una redistribución más lenta a los músculos y el tejido graso.
La fijación del fentanilo a las proteínas plasmáticas es del 80 al 85 %. La principal proteína de unión es la a-1-ácido glucoproteína, pero tanto la albúmina como las lipoproteínas contribuyen en cierta medida. La fracción libre del fentanilo aumenta con la acidosis.
Biotransformación
No se han establecido las características de las vías metabólicas después de la administración nasal de PecFent en estudios clínicos. El fentanilo se metaboliza en el hígado, y la isoforma del citocromo CYP3A4 lo transforma en norfentanilo. Este no es farmacológicamente activo en estudios en animales. Se elimina más del 90 % mediante la biotransformación a metabolitos inactivos, N-desalquilados e hidroxilados.
Eliminación
No se han establecido las características de la eliminación del fentanilo después de la administración intranasal de PecFent en un estudio de equilibrio de masa. Menos del 7 % de una dosis administrada de fentanilo se excreta sin modificar en la orina y solo aproximadamente el 1 % se excreta sin modificar en las heces. Los metabolitos se excretan principalmente en la orina, mientras que la excreción fecal es menos importante.
La depuración plasmática total del fentanilo después de la administración por vía intravenosa es de aproximadamente 42 L/h.
Linealidad/No linealidad
Se demostró la proporcionalidad de la dosis para la Cmáx y el AUC dentro de los límites de dosis de 100 a 800 pg.
No se ha estudiado el efecto de la insuficiencia renal o hepática sobre las características farmacocinéticas de PecFent.
5.3 Datos preclínicos sobre seguridad
Los datos de los estudios no clínicos no muestran riesgos especiales para los seres humanos según los estudios convencionales de farmacología de seguridad, toxicidad a dosis repetidas, genotoxicidad y potencial carcinogénico.
En los estudios de toxicidad del desarrollo embriofetal realizados en ratas y conejos no se reveló ninguna malformación ni variación del desarrollo inducidas por el compuesto, cuando se administró durante el período de organogénesis.
En un estudio de fertilidad y desarrollo embrionario temprano en ratas, se observó un efecto mediado por los machos a dosis altas (300 mcg/Kg/día, por vía s.c.) y es compatible con los efectos sedantes del fentanilo en estudios en animales.
En estudios de desarrollo prenatal y posnatal en ratas, la tasa de supervivencia de las crías disminuyó significativamente a dosis que causaron una toxicidad materna grave. Otras observaciones con dosis tóxicas para las madres en crías F1 fueron el retraso del desarrollo físico, de las funciones sensitivas, de los reflejos y del comportamiento.
Estos efectos pudieron ser indirectos, debidos a la alteración de la atención materna o a una disminución de la tasa de lactancia, o bien un efecto directo del fentanilo sobre las crías.
Los estudios de carcinogenicidad (bioensayo alternativo dérmico de 26 semanas en ratones transgénicos Tg.AC; estudio de carcinogenicidad por vía subcutánea durante dos años en ratas) con fentanilo no arrojaron ningún resultado indicativo de potencial carcinogénico. La evaluación de los cortes laminares de cerebro del estudio de carcinogenicidad en ratas mostró lesiones cerebrales en los animales tratados con dosis altas de citrato de fentanilo. Se desconoce la relevancia de estos hallazgos para los seres humanos.
DATOS FARMACÉUTICOS
6.
6.1 Lista de excipientes
Pectina (E440)
Manitol (E421)
Alcohol feniletílico Propilparahidroxibenzoato (E216)
Sacarosa
Ácido clorhídrico (al 0,36 %) o hidróxido de sodio (para el ajuste del pH)
Agua purificada
6.2 Incompatibilidades
No procede.
6.3 Periodo de validez
Frasco de 2 pulverizaciones: 18 meses
Tras el cebado, utilizar dentro de los 5 días posteriores.
Frasco de 8 pulverizaciones :3 años Después del primer uso: 60 días
6.4 Precauciones especiales de conservación
No conservar a temperatura superior a 25°C.
No congelar.
Conservar el frasco dentro del envase a prueba de niños para protegerlo de la luz.
Conservar siempre el frasco dentro del envase a prueba de niños, incluso cuando esté terminado.
6.5 Naturaleza y contenido del envase
Frasco (vidrio transparente de tipo I) con una bomba de dosificación incluida, que incorpora un dosímetro audible y un tapón protector (tapón blanco opaco para el frasco de 2 pulverizaciones y tapón translúcido para el de 8 pulverizaciones). En cada caso el medicamento está acondicionado en un envase a prueba de niños, parecido a una concha de almeja.
Los frascos contienen:
0,95 ml que asegura la administración de dos pulverizaciones completas o
1,55 ml que asegura la administración de ocho pulverizaciones completas.
Los frascos en sus envases a prueba de niños se suministran en cajas que contienen:
Para el frasco de 2 pulverizaciones: 1 frasco Para el frasco de 8 pulverizaciones: 1, 4 o 12 frascos.
Puede que solamente estén comercializados algunos tamaños de envases o presentaciones.
6.6 Precauciones especiales de eliminación
Los frascos de PecFent parcialmente utilizados pueden contener medicamento suficiente como para ser perjudicial o mortal para un niño. Incluso si queda poco o nada de medicamento en el frasco, PecFent se debe eliminar correctamente, de acuerdo con los siguientes pasos:
o Se debe indicar a los pacientes y a los cuidadores que eliminen correctamente todos los frascos de PecFent sin utilizar, parcialmente utilizados o utilizados. Se debe informar al paciente sobre cómo hacerlo correctamente.
o Si quedan en el frasco pulverizaciones terapéuticas que no se quieren, se debe indicar al paciente que las expulse del siguiente modo:
Frasco de 2 pulverizaciones:
o Dirigir el pulverizador lejos de sí mismo (y de cualquier otra persona) y expulsar la
pulverización restante hasta que aparezca el número "2" rojo en la ventana de recuento y no se puedan obtener más pulverizaciones terapéuticas completas del frasco. o Después de que el dosímetro haya avanzado a "2", el paciente debe continuar oprimiendo los agarres digitales (encontrará mayor resistencia) un total de cuatro veces para expulsar cualquier resto de medicamento del frasco.
o Después de haber emitido las 2 pulverizaciones terapéuticas, el paciente no escuchará un clic y el dosímetro no avanzará más allá del "2"; las pulverizaciones emitidas a partir de ese momento no serán pulverizaciones completas, y no se deben usar terapéuticamente.
Frasco de 8 pulverizaciones:
o Dirigir el pulverizador lejos de sí mismo (y de cualquier otra persona) y expulsar la
pulverización restante hasta que aparezca el número “8” rojo en la ventana de recuento y no se puedan obtener más pulverizaciones terapéuticas completas del frasco. o Después de que el dosímetro haya avanzado al “8”, el paciente debe continuar oprimiendo los agarres digitales (encontrará mayor resistencia) un total de cuatro veces para expulsar cualquier resto de medicamento del frasco.
o Después de haber emitido las 8 pulverizaciones terapéuticas, el paciente no escuchará un clic y el dosímetro no avanzará más allá del “8”; las pulverizaciones emitidas a partir de este momento no serán pulverizaciones completas y no se deben utilizar terapéuticamente.
Apenas PecFent ya no sea necesario, se debe aconsejar a los pacientes y a las personas que vivan en su domicilio que eliminen sistemáticamente y lo antes posible los frascos restantes de una receta; para ello, deben volver a colocarlos en el envase a prueba de niños y desecharlos, según las normativas locales, o devolverlos a la farmacia.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Archimedes Development Ltd Albert Einstein Centre
Nottingham Science and Technology Park, University Boulevard
Nottingham
NG7 2TN
Reino Unido
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/10/644/007
EU/1/10/644/001
EU/1/10/644/002
EU/1/10/644/005
EU/1/10/644/003
EU/1/10/644/004
EU/1/10/644/006
9. FECHA DE LA PRIMERA AUTORIZACIÓN/RENOVACIÓN DE LA AUTORIZACIÓN
Fecha de la primera autorización: 31/agosto/2010 Fecha de la última renovación: 17/julio/2015
10. FECHA DE LA REVISIÓN DEL TEXTO
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos http://www.ema.europa.eu/.
A. FABRICANTE RESPONSABLE DE LA LIBERACIÓN DE LOS LOTES
B. CONDICIONES O RESTRICCIONES DE SUMINISTRO Y USO
C. OTRAS CONDICIONES Y REQUISITOS DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
D. CONDICIONES O RESTRICIONES EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO
A. FABRICANTE RESPONSABLE DE LA LIBERACIÓN DE LOS LOTES
Nombre y dirección del fabricante responsable de la liberación de los lotes
L. Molteni & C dei F. LLi Alitti Societá di Esercizio S.p.A
Strada Statale 67
Tosco Romagnola
Fraz. Granatieri
IT-50018 Scandicci (FI)
Italia
B. CONDICIONES O RESTRICCIONES DE SUMINISTRO Y USO
Medicamento sujeto a prescripción médica especial y restringida (ver Anexo I: Ficha Técnica o Resumen de las Características del Producto, sección 4.2).
C. OTRAS CONDICIONES Y REQUISITOS DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
• Informes periódicos de seguridad (IPS)
El Titular de la Autorización de Comercialización (TAC) presentará los informes periódicos de seguridad para este medicamento de conformidad con las exigencias establecidas en la lista de fechas de referencia de la Unión (lista EURD) prevista en el artículo 107ter, párrafo 7, de la Directiva 2001/83/CE y publicada en el portal web europeo sobre medicamentos.
D. CONDICIONES O RESTRICCIONES EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO
• Plan de Gestión de Riesgos (PGR)
El TAC realizará las actividades e intervenciones de farmacovigilancia necesarias según lo acordado en la versión del PGR incluido en el Módulo 1.8.2 de la Autorización de Comercialización y en cualquier actualización del PGR que se acuerde posteriormente.
Se debe presentar un PGR actualizado:
• A petición de la Agencia Europea de Medicamentos.
• Cuando se modifique el sistema de gestión de riesgos, especialmente como resultado de nueva información disponible que pueda conllevar cambios relevantes en el perfil beneficio/riesgo, o como resultado de la consecución de un hito importante (farmacovigilancia o minimización de riesgos).
Si coincide la presentación de un IPS con la actualización del PGR, ambos documentos se pueden presentar conjuntamente.
• Medidas adicionales de minimización de riesgos
Antes del lanzamiento en cada estado miembro, el TAC acordará el material educativo final con la Autoridad Nacional Competente.
El TAC debe asegurar que, en el momento del lanzamiento del medicamento, todos los médicos, farmacéuticos y pacientes con intención de prescribir/dispensar/usar PecFent dispongan del material educativo que contiene información sobre el uso seguro y correcto del medicamento.
El material educativo para los pacientes debe destacar lo siguiente:
• Instrucciones de uso del dispositivo de pulverización nasal
• Instrucciones de apertura y cierre de la caja a prueba de niños
• Información sobre la indicación correcta
• Únicamente usar PecFent pulverización nasal si utiliza otro opioide de uso diario para el dolor
• Únicamente usar PecFent pulverización nasal si tiene episodios de dolor oncológico irruptivo
• No usar PecFent pulverización nasal para el tratamiento de cualquier otro dolor de corta duración o episodio de dolor
• No usar PecFent pulverización nasal para el tratamiento de más de cuatro episodios de dolor oncológico irruptivo al día
• Únicamente usar PecFent pulverización nasal si ha recibido la información adecuada sobre el uso del dispositivo y las precauciones de seguridad del médico prescriptor y/o del farmacéutico
• Todos los dispositivos sin utilizar o envases vacíos se deben devolver sistemáticamente conforme a la normativa local
El material educativo para los médicos debe destacar lo siguiente:
• PecFent pulverización nasal debe prescribirse únicamente por médicos con experiencia en el uso de la terapia con opioides en pacientes con cáncer
• Los médicos que prescriban PecFent pulverización nasal deben realizar una selección crítica de los pacientes y seguir estrictamente:
o Las instrucciones de uso del dispositivo de pulverización nasal
o Las instrucciones de apertura y cierre de la caja a prueba de niños
o La información sobre la indicación correcta
• PecFent pulverización nasal no debe usarse para el tratamiento de cualquier otro dolor de corta duración o episodio de dolor
• Todos los dispositivos sin utilizar o envases vacíos se deben devolver sistemáticamente conforme a la normativa local
• El médico debe utilizar la lista de comprobación para prescriptores
El material educativo para los farmacéuticos debe destacar lo siguiente:
• PecFent pulverización nasal está únicamente indicado para el control del dolor irruptivo en adultos que ya reciben terapia de mantenimiento con opioides para el dolor oncológico crónico
• PecFent pulverización nasal no debe usarse para el tratamiento de cualquier otro dolor de corta duración o episodio de dolor
• El farmacéutico debe estar familiarizado con el material educativo de PecFent pulverización nasal antes de utilizarlo en su farmacia
• Las concentraciones de dosis de PecFent pulverización nasal no pueden compararse con otros medicamentos PecFent
• Instrucciones de uso del dispositivo de pulverización nasal
• Instrucciones de apertura y cierre de la caja a prueba de niños
• El farmacéutico debe informar a los pacientes que para prevenir el robo y mal uso de PecFent
pulverización nasal tienen que guardarlo en un lugar seguro para evitar un mal uso o uso indebido
• Todos los dispositivos sin utilizar o envases vacíos se deben devolver sistemáticamente conforme a la normativa local
• El farmacéutico debe utilizar la lista de comprobación para farmacéuticos
ETIQUETADO Y PROSPECTO
A. ETIQUETADO
INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR CAJA
1. NOMBRE DEL MEDICAMENTO
PecFent 100 microgramos/pulverización, solución para pulverización nasal Fentanilo
2. PRINCIPIO(S) ACTIVO(S)
Cada pulverización contiene 100 microgramos de fentanilo (como citrato). Cada ml de solución contiene 1000 microgramos de fentanilo (como citrato).
3. LISTA DE EXCIPIENTES
También contiene: pectina (E440), manitol (E421), alcohol feniletílico, propilparahidroxibenzoato (E216), sacarosa, agua purificada y ácido clorhídrico (al 0,36 %) o hidróxido de sodio para el ajuste del pH. Ver información adicional en el prospecto.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
Solución para pulverización nasal
I Frasco de 2 pulverizaciones:]
1 frasco - 0,95 ml (2 pulverizaciones) por frasco
I Frasco de 8 pulverizaciones:]
1 frasco - 1,55 ml (8 pulverizaciones) por frasco 4 frascos - 1,55 ml (8 pulverizaciones) por frasco 12 frascos - 1,55 ml (8 pulverizaciones) por frasco
5. FORMA Y VÍA(S) DE ADMINISTRACIÓN
Leer el prospecto antes de utilizar este medicamento.
Vía nasal.
I Frasco de 2 pulverizaciones:]
Si no se ha utilizado el pulverizador dentro de los 5 días posteriores al cebado, se debe desechar. [Frasco de 8 pulverizaciones:]
Si pasan cinco días sin que se use PecFent, volver a cebar pulverizando una vez.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Mantener fuera de la vista y del alcance de los niños.
7. OTRA(S) ADVERTENCIA(S) ESPECIAL(ES), SI ES NECESARIO
Este medicamento solo deben utilizarlo los pacientes que toman otros opioides.
8. FECHA DE CADUCIDAD
CAD
I Frasco de 2 pulverizaciones:]
Tras el cebado, utilizar dentro de los 5 días posteriores. I Frasco de 8 pulverizaciones:]
Después del primer uso, usar en un máximo de 60 días.
9. CONDICIONES ESPECIALES DE CONSERVACIÓN
No conservar a temperatura superior a 25°C.
No congelar.
Conservar el frasco dentro del envase a prueba de niños para protegerlo de la luz.
Conservar siempre el frasco de PecFent dentro del envase a prueba de niños, incluso cuando esté vacío.
10. PRECAUCIONES ESPECIALES DE ELIMINACIÓN DEL MEDICAMENTO NO UTILIZADO Y DE LOS MATERIALES DERIVADOS DE SU USO (CUANDO CORRESPONDA)
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Archimedes Development Ltd
Nottingham
NG7 2TN
Reino Unido
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/10/644/007 100 microgramos, 1 frasco de 2 pulverizaciones
EU/1/10/644/001 100 microgramos, 1 frasco de 8 pulverizaciones EU/1/10/644/002 100 microgramos, 4 frascos de 8 pulverizaciones EU/1/10/644/005 100 microgramos, 12 frascos de 8 pulverizaciones
13. NÚMERO DE LOTE
Lote
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
PecFent 100
INFORMACIÓN QUE DEBE FIGURAR EN EL ENVASE A PRUEBA DE NIÑOS
1. NOMBRE DEL MEDICAMENTO
PecFent 100 microgramos/pulverización, pulverización nasal Fentanilo
2. PRINCIPIO(S) ACTIVO(S)
Cada pulverización contiene 100 microgramos de fentanilo (como citrato).
3. LISTA DE EXCIPIENTES
También contiene: pectina (E440), manitol (E421), alcohol feniletílico, propilparahidroxibenzoato (E216), sacarosa, agua purificada y ácido clorhídrico (al 0,36 %) o hidróxido de sodio para el ajuste del pH. Ver información adicional en el prospecto.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
5. FORMA Y VÍA(S) DE ADMINISTRACIÓN
Vía nasal.
Leer el prospecto antes de utilizar este medicamento.
I Frasco de 2 pulverizaciones:]
Si no se ha utilizado el pulverizador dentro de los 5 días posteriores al cebado, se debe desechar.
[Frasco de 8 pulverizaciones:]
Si pasan cinco días sin que se use PecFent, volver a cebar pulverizando una vez.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Mantener fuera de la vista y del alcance de los niños.
7. OTRA(S) ADVERTENCIA(S) ESPECIAL(ES), SI ES NECESARIO
Este medicamento solo deben utilizarlo los pacientes que toman otros opioides.
8. FECHA DE CADUCIDAD
Frasco de 2 pulverizaciones:
Tras el cebado, utilizar dentro de los 5 días posteriores. Fecha de cebado: ..........
Frasco de 8 pulverizaciones:
Después del primer uso, usar en un máximo de 60 días. Fecha del primer uso:...............
9. CONDICIONES ESPECIALES DE CONSERVACIÓN
No conservar a temperatura superior a 25°C.
No congelar.
Conservar el frasco dentro del envase a prueba de niños para protegerlo de la luz.
Conservar siempre el frasco de PecFent dentro del envase a prueba de niños, incluso cuando esté vacío.
10. PRECAUCIONES ESPECIALES DE ELIMINACIÓN DEL MEDICAMENTO NO UTILIZADO Y DE LOS MATERIALES DERIVADOS DE SU USO (CUANDO CORRESPONDA)_
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Archimedes Development Ltd
Nottingham
NG7 2TN
Reino Unido
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
13. NÚMERO DE LOTE
14. CONDICIONES GENERALES DE DISPENSACIÓN
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
INFORMACIÓN MÍNIMA QUE DEBE INCLUIRSE EN PEQUEÑOS ACONDICIONAMIENTOS PRIMARIOS
ETIQUETA DEL FRASCO
1. NOMBRE DEL MEDICAMENTO Y VÍA(S) DE ADMINISTRACIÓN
PecFent 100 microgramos/pulverización, pulverización nasal
Fentanilo
Vía nasal
2. FORMA DE ADMINISTRACIÓN
3. FECHA DE CADUCIDAD
CAD
4. NÚMERO DE LOTE
Lote
5. CONTENIDO EN PESO, EN VOLUMEN O EN UNIDADES
0,95 ml - 2 pulverizaciones 1,55 ml - 8 pulverizaciones
6. OTROS
INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR CAJA
1. NOMBRE DEL MEDICAMENTO
PecFent 400 microgramos /pulverización, solución para pulverización nasal Fentanilo
2. PRINCIPIO(S) ACTIVO(S)
Cada pulverización contiene 400 microgramos de fentanilo (como citrato). Cada ml de solución contiene 4000 microgramos de fentanilo (como citrato).
3. LISTA DE EXCIPIENTES
También contiene: pectina (E440), manitol (E421), alcohol feniletílico, propilparahidroxibenzoato (E216), sacarosa, agua purificada y ácido clorhídrico (al 0,36 %) o hidróxido de sodio para el ajuste del pH. Ver información adicional en el prospecto.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
Solución para pulverización nasal 1 frasco - 1,55 ml (8 pulverizaciones) por frasco 4 frascos - 1,55 ml (8 pulverizaciones) por frasco 12 frascos - 1,55 ml (8 pulverizaciones) por frasco
5. FORMA Y VÍA(S) DE ADMINISTRACIÓN
Leer el prospecto antes de utilizar este medicamento.
Vía nasal.
Si pasan cinco días sin que se use PecFent, volver a cebar pulverizando una vez.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Mantener fuera de la vista y del alcance de los niños.
7. OTRA(S) ADVERTENCIA(S) ESPECIAL(ES), SI ES NECESARIO
Este medicamento solo deben utilizarlo los pacientes que toman otros opioides.
8. FECHA DE CADUCIDAD
CAD
Después del primer uso, usar en un máximo de 60 días.
No conservar a temperatura superior a 25°C.
No congelar.
Conservar el frasco dentro del envase a prueba de niños para protegerlo de la luz.
Conservar siempre el frasco de PecFent dentro del envase a prueba de niños, incluso cuando esté terminado.
10. PRECAUCIONES ESPECIALES DE ELIMINACIÓN DEL MEDICAMENTO NO UTILIZADO Y DE LOS MATERIALES DERIVADOS DE SU USO (CUANDO CORRESPONDA)_
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Archimedes Development Ltd
Nottingham
NG7 2TN
Reino Unido
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/10/644/003400 microgramos, 1 frasco de 8 pulverizaciones EU/1/10/644/004 400 microgramos, 4 frascos de 8 pulverizaciones
EU/1/10/644/006 400 microgramos, 12 frascos de 8 pulverizaciones
13. NÚMERO DE LOTE
Lote
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
PecFent 400
INFORMACIÓN QUE DEBE FIGURAR EN EL ENVASE A PRUEBA DE NIÑOS
1. NOMBRE DEL MEDICAMENTO
PecFent 400 microgramos/pulverización, pulverización nasal Fentanilo
Cada pulverización contiene 400 microgramos de fentanilo (como citrato).
3. LISTA DE EXCIPIENTES
También contiene: pectina (E440), manitol (E421), alcohol feniletílico, propilparahidroxibenzoato (E216), sacarosa, agua purificada y ácido clorhídrico (al 0,36 %) o hidróxido de sodio para el ajuste del pH. Ver información adicional en el prospecto.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
Vía nasal.
Leer el prospecto antes de utilizar este medicamento.
Si pasan cinco días sin que se use PecFent, volver a cebar pulverizando una vez.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Mantener fuera de la vista y del alcance de los niños.
Este medicamento solo deben utilizarlo los pacientes que toman otros opioides.
8. FECHA DE CADUCIDAD
Después del primer uso, usar en un máximo de 60 días. Fecha del primer uso:...............
No conservar a temperatura superior a 25°C.
No congelar.
Conservar el frasco dentro del envase a prueba de niños para protegerlo de la luz.
Conservar siempre el frasco de PecFent dentro del envase a prueba de niños, incluso cuando esté vacío.
10. PRECAUCIONES ESPECIALES DE ELIMINACIÓN DEL MEDICAMENTO NO UTILIZADO Y DE LOS MATERIALES DERIVADOS DE SU USO (CUANDO CORRESPONDA)_
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Archimedes Development Ltd
Nottingham
NG7 2TN
Reino Unido
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
13. NÚMERO DE LOTE
14. CONDICIONES GENERALES DE DISPENSACIÓN
15. INSTRUCCIONES DE USO
16. INFORMACIÓN EN BRAILLE
INFORMACIÓN MÍNIMA QUE DEBE INCLUIRSE EN PEQUEÑOS ACONDICIONAMIENTOS PRIMARIOS
ETIQUETA DEL FRASCO
1. NOMBRE DEL MEDICAMENTO Y VÍA(S) DE ADMINISTRACIÓN
PecFent 400 microgramos/pulverización, pulverización nasal
Fentanilo
Vía nasal
2. FORMA DE ADMINISTRACIÓN
3. FECHA DE CADUCIDAD
CAD
4. NÚMERO DE LOTE
Lote
5. CONTENIDO EN PESO, EN VOLUMEN O EN UNIDADES
1,55 ml - 8 pulverizaciones
6. OTROS
B. PROSPECTO
Prospecto: información para el usuario
PecFent 100 microgramos/pulverización, solución para pulverización nasal PecFent 400 microgramos/pulverización, solución para pulverización nasal
Fentanilo
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
• Conserve este prospecto, ya que puede tener que volver a leerlo.
• Si tiene alguna duda, consulte a su médico o farmacéutico.
• Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
• Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto:
1. Qué es PecFent y para qué se utiliza
2. Qué necesita saber antes de empezar a usar PecFent
3. Cómo usar PecFent
4. Posibles efectos adversos
5. Conservación de PecFent
6. Contenido del envase e información adicional
1. Qué es PecFent y para qué se utiliza
Qué es PecFent
PecFent contiene fentanilo, que es un potente medicamento para el alivio del dolor, conocido como un
analgésico opioide.
Para qué se utiliza PecFent
PecFent se utiliza en los adultos con cáncer para un tipo de dolor llamado dolor “irruptivo”.
• Este tipo de dolor aparece repentinamente.
• Se presenta aunque se haya tomado el analgésico opioide habitual (por ejemplo, morfina, fentanilo, oxicodona o hidromorfona) para controlar el dolor de base constante.
PecFent solo debe ser utilizado por los adultos que estén tomando ya otros opioides diariamente para
el dolor constante causado por el cáncer.
Cómo actúa PecFent
PecFent es una solución para pulverización nasal.
• Cuando se pulveriza PecFent en la nariz, las diminutas microgotas de la pulverización forman un gel fino.
• El fentanilo se absorbe rápidamente a través de la mucosa de la nariz y pasa directamente a la circulación sanguínea.
• Esto significa que el medicamento llega rápidamente a su organismo para aliviarle el dolor irruptivo.
2. Qué necesita saber antes de empezar a usar PecFent
No use PecFent:
• Si es alérgico al fentanilo o a cualquiera de los demás componentes de este medicamento (incluidos en la sección 6).
• Si no está usando regularmente un medicamento opioide prescrito por su médico (p. ej., codeína, fentanilo, hidromorfona, morfina, oxicodona, meperidina), todos los días a la misma hora, al menos durante una semana, para controlar el dolor persistente. Si no ha estado usando esos medicamentos, no use PecFent dado que su uso puede aumentar el riesgo de que su respiración se vuelva más lenta y/o poco profunda, e incluso de que llegue a pararse.
• Si padece dolor de corta duración distinto al dolor irruptivo.
• Si sufre un problema respiratorio o pulmonar grave.
No use PecFent si alguna de las condiciones anteriores se aplica en su caso. Si tiene dudas, consulte a su médico o farmacéutico antes de usar PecFent.
Advertencias y precauciones
Mantenga PecFent fuera del alcance de los niños
• Debe mantener PecFent dentro del envase de almacenamiento a prueba de niños cuando no esté usándolo, aunque haya usado las ocho pulverizaciones. Esto se debe a que PecFent es potencialmente mortal si un niño lo toma por accidente.
Consulte a su médico o farmacéutico antes de usar PecFent:
• Si no ha estado tomando la misma dosis diaria de su opioide, durante algún tiempo, para el dolor constante que padece.
• Si sufre problemas respiratorios, como asma, silbidos o dificultad para respirar.
• Si sufre un golpe fuerte en la cabeza.
• Si tiene problemas de corazón, especialmente frecuencia cardiaca baja.
• Si tiene la tensión arterial baja o una cantidad baja de líquido en la circulación.
• Si padece problemas de los riñones o del hígado ya que pueden afectar a la manera en que su organismo descompone el medicamento.
• Si toma antidepresivos o antipsicóticos, consulte la sección “Uso de PecFent con otros medicamentos”.
Si alguna de las condiciones anteriores se aplica en su caso (o no está seguro), consulte a su médico o farmacéutico antes de usar PecFent.
• Si es deportista, PecFent puede dar resultados positivos en las pruebas antidopaje.
Informe también a su médico si después de usar PecFent:
• Sufre hemorragias nasales recurrentes; el médico puede aconsejar un tratamiento alternativo.
• Considera que PecFent es cada vez menos eficaz en el tratamiento de los episodios de dolor irruptivo.
• Cree que se está volviendo adicto a PecFent.
Niños y adolescentes
No se ha aprobado el uso de PecFent en niños menores de 18 años.
Uso de PecFent con otros medicamentos
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o podría tener que utilizar cualquier otro medicamento.
En concreto, informe a su médico o farmacéutico antes de usar PecFent si está tomando o ha tomado recientemente cualquiera de los siguientes medicamentos:
• Medicamentos que pudieran causar somnolencia, como las pastillas para dormir, tranquilizantes, relajantes musculares, medicamentos para la ansiedad o medicamentos para las alergias (antihistamínicos).
• Medicamentos para la depresión llamados “inhibidores de la monoaminooxidasa” (IMAO). Informe a su médico o farmacéutico si ha estado tomando un IMAO en las dos semanas anteriores al uso de PecFent.
El riesgo de efectos adversos aumenta si está tomando medicamentos tales como ciertos antidepresivos o antipsicóticos. PecFent puede interactuar con estos medicamentos y usted puede presentar cambios en el estado mental (p. ej., agitación, alucinaciones, coma) y otros efectos como temperatura corporal mayor de 38°C, aumento de la frecuencia cardiaca, presión arterial inestable y exageración de los reflejos, rigidez muscular, falta de coordinación y/o síntomas gastrointestinales (p. ej., náuseas, vómitos, diarrea). Su médico le dirá si PecFent es adecuado para usted.
• Pulverizaciones nasales para tratar la nariz tapada (que contienen un descongestionante como la oximetazolina).
• Medicamentos que pudieran tener un efecto en la manera en que su organismo descompone PecFent, entre ellos:
o Medicamentos para la infección por el VIH (por ejemplo, ritonavir, nelfinavir, amprenavir o fosamprenavir).
o Medicamentos para las infecciones por hongos (por ejemplo, ketoconazol, itraconazol o fluconazol).
o Medicamentos para las infecciones bacterianas (por ejemplo, troleandomicina, claritromicina o eritromicina). o “Aprepitant”, usado para aliviar las náuseas.
o “Diltiazem” y “verapamilo”, usados para la hipertensión o los problemas del corazón. o Otros medicamentos para el dolor llamados agonistas/antagonistas parciales, como la buprenorfina, la nalbufina y la pentazocina. Podría experimentar síntomas del síndrome de abstinencia (náuseas, vómitos, diarrea, ansiedad, escalofríos, temblores y sudoración) mientras utiliza estos medicamentos.
Si alguna de las condiciones anteriores se aplica en su caso (o no está seguro), consulte a su médico o farmacéutico antes de usar PecFent.
No use ningún otro tipo de pulverización nasal por lo menos 15 minutos después de usar PecFent.
Uso de PecFent con alimentos, bebidas y alcohol
• No beba alcohol mientras usa PecFent, ya que puede aumentar el riesgo de sufrir efectos adversos graves.
• No beba zumo de pomelo mientras usa PecFent, ya que puede afectar a la manera en que su organismo descompone el medicamento.
Embarazo, lactancia y fertilidad
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
• No use PecFent si está embarazada o pudiera quedarse embarazada, a menos que su médico le haya dicho que lo haga.
• No use PecFent durante el parto ya que puede causar problemas respiratorios a su bebé.
• No use PecFent durante el período de lactancia, ya que el medicamento puede llegar a la leche materna y causar efectos adversos en el niño lactante.
• No debe iniciar la lactancia antes de transcurridos 5 días desde la última dosis de PecFent.
Conducción y uso de máquinas
• Consulte a su médico si es seguro conducir o utilizar máquinas o herramientas mientras toma PecFent.
• Puede sentirse somnoliento, mareado o puede tener problemas de visión después de usar PecFent. Si le ocurre esto, no conduzca ni utilice herramientas o máquinas.
• No conduzca ni utilice herramientas o máquinas hasta que no sepa cómo le hace sentirse este medicamento.
PecFent contiene propilparahidroxibenzoato (E216).
Puede causar reacciones alérgicas (posiblemente retardadas) y, excepcionalmente, broncoespasmo (si no usa la pulverización nasal correctamente).
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
PecFent se presenta en dos concentraciones diferentes: un frasco de 100 microgramos por pulverización y un frasco de 400 microgramos por pulverización. Asegúrese de usar la concentración que el médico le haya recetado.
Qué cantidad usar de PecFent
• Una dosis para tratar un episodio de dolor irruptivo podría consistir en una o dos pulverizaciones (una en cada fosa nasal). Su médico le dirá cuántas pulverizaciones (una o dos) debe usar para tratar el episodio de dolor irruptivo.
• No use una dosis mayor que la que el médico le recete para un único episodio de dolor irruptivo.
• No use PecFent más de cuatro veces al día.
• Espere por lo menos cuatro horas para tomar la siguiente dosis de PecFent.
Dosis inicial
• La dosis inicial es de 100 microgramos.
• Consiste en una sola pulverización en una fosa nasal del frasco de 100 microgramos por pulverización.
• Consulte las instrucciones sobre cómo usar una dosis en “Uso del frasco de PecFent”. Búsqueda de la dosis correcta
• Su médico le ayudará a encontrar la dosis correcta para aliviarle el dolor irruptivo. Es muy importante que siga las instrucciones del médico.
• Informe al médico acerca de su dolor y del efecto que tiene PecFent. Su médico decidirá si es necesario cambiar la dosis de PecFent.
• No se cambie usted mismo la dosis.
Una vez que haya encontrado la dosis correcta
• Informe a su médico si la dosis que recibe de PecFent no le alivia el dolor irruptivo. Su médico decidirá si es necesario cambiar la dosis. No se cambie usted mismo la dosis de PecFent o de otros medicamentos para el dolor.
• Informe inmediatamente a su médico si tiene más de cuatro episodios diarios de dolor irruptivo. Puede que su médico le cambie la medicación para el dolor constante. Una vez que el dolor constante esté controlado, puede que su médico le cambie la dosis de PecFent.
Si no está seguro acerca de la dosis correcta o qué cantidad de PecFent debe utilizar, pregunte a su médico.
Instrucciones sobre cómo abrir y cerrar el envase a prueba de niños
abrir
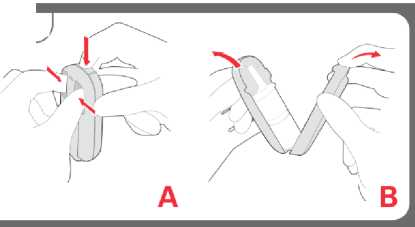
cerrar
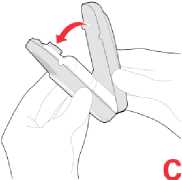
A Introduzca los dedos en las cavidades traseras y apriete mientras empuja hacia abajo el botón superior.
B Abra.
C Cierre (escuche el clic de confirmación).
Preparación del frasco de PecFent para su uso
Antes de usar un frasco nuevo de PecFent, debe prepararlo para su uso. Esto se llama “cebado”.
Para cebar el frasco, siga estas instrucciones:
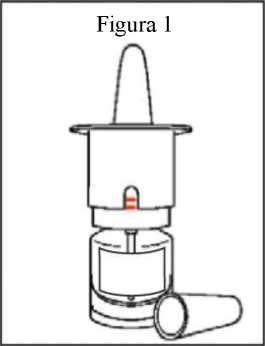
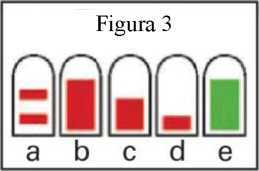
1. Un frasco nuevo de PecFent mostrará dos líneas rojas en la ventana de recuento de la parte superior blanca de plástico del frasco (figuras 1 y 3a).
2. Retire el tapón protector de plástico transparente de la boquilla (figura 1).
3. Apunte el pulverizador nasal lejos de usted (y de otras personas).
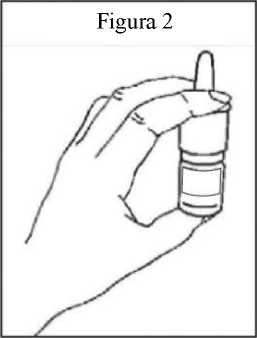
4. Sostenga el pulverizador nasal PecFent en posición vertical, con el pulgar en el fondo del frasco, y los dedos índice y corazón en los agarres digitales de cada lado de la boquilla (figura 2).
5. Oprima firmemente hacia abajo los agarres digitales, hasta oír un “clic”; luego, suelte los agarres (figura 2). Oirá un segundo “clic” y aparecerá una única barra roja y grande en la ventana de recuento (figura 3b).
6. Repita tres veces el paso 5. Cuando repita el paso 5, la barra roja empequeñecerá cada vez más, hasta que vea una barra verde en la ventana de recuento (figura 3b-e). La barra verde significa que el pulverizador nasal PecFent está listo para usar.
7. Limpie la boquilla con un pañuelo de papel y tire el pañuelo al inodoro.
8. Si no va a usar inmediatamente el medicamento, vuelva a colocar el tapón protector. A continuación, coloque el frasco de PecFent dentro del envase de almacenamiento a prueba de niños. Si pasan cinco días sin que se use PecFent, volver a cebar pulverizando una vez.
PecFent solo se debe utilizar pulverizándose en las fosas nasales.
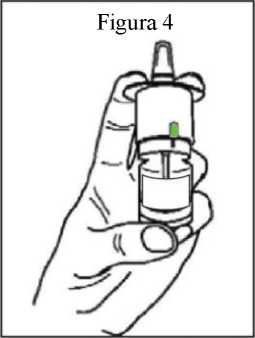
1. Compruebe que haya una barra verde o un número en la ventana de recuento (figura 4): esto confirma que el frasco de PecFent se ha cebado (consulte “Preparación del frasco de PecFent para su uso”, más arriba).
2. Suénese la nariz si considera que debe hacerlo.
3. Siéntese con la cabeza en posición vertical.
4. Retire el tapón protector de la boquilla.
5. Sostenga el frasco de PecFent con el pulgar en el fondo del frasco, y los dedos índice y corazón en los agarres digitales (figura 4).
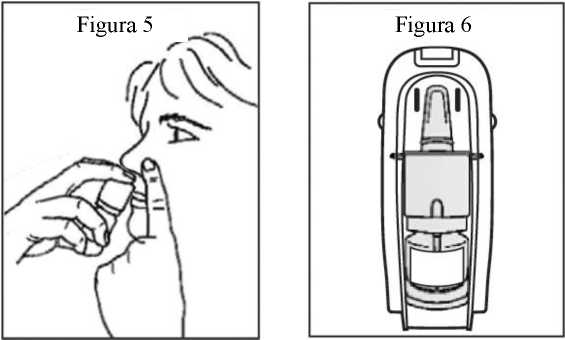
6. Coloque la boquilla a corta distancia (aproximadamente 1 cm) en el interior de la fosa nasal. Apunte hacia las paredes de la nariz. Así inclinará ligeramente el frasco (figura 5).
7. Cierre la otra fosa nasal con un dedo de la otra mano (figura 5).
8. Oprima firmemente los agarres digitales para pulverizar PecFent en la fosa nasal. Cuando oiga un clic, suelte los agarres. Nota: Tal vez no sienta nada en la nariz; no crea que esto significa que el pulverizador no funciona; déjese llevar por el clic y el contador numérico.
9. Inspire lentamente por la nariz y expulse el aire por la boca.
10. El contador numérico avanzará después de cada uso y mostrará cuántas pulverizaciones se han usado.
11. Si el médico le ha recetado una segunda pulverización, repita los puntos 5 a 9, usando la otra fosa nasal.
No use una dosis mayor que la que el médico le recete para tratar un único episodio de dolor.
12. Después de cada uso, vuelva a colocar el frasco en el envase a prueba de niños. Mantenga el medicamento fuera de la vista y del alcance de los niños (figura 6).
13. Quédese sentado por lo menos un minuto después de usar el pulverizador nasal.
Número de pulverizaciones en un frasco de PecFent
En cada frasco de PecFent hay ocho pulverizaciones completas.
• Después de la primera pulverización, aparecerá el número 1 en la ventana de recuento. La numeración avanzará conforme utilice el pulverizador.
• Cuando vea un 8 rojo en la ventana de recuento, se ha acabado el frasco y ya no podrá obtener más pulverizaciones completas.
Eliminación de PecFent sin utilizar
• Si puede ver un número, que no sea el 8 en la ventana de recuento, NO ha utilizado las 8 pulverizaciones del frasco. Siguen quedando dosis de PecFent en el frasco.
• Debe expulsar las dosis de PecFent restantes del frasco apuntando el pulverizador nasal lejos de usted (y de cualquier otra persona) y oprimiendo y soltando los agarres hasta que el número “8” rojo aparezca en la ventana de recuento.
Cuando vea el número “8” en la ventana de recuento, sigue quedando medicamento en el frasco que debe expulsar.
• Tendrá que oprimir y soltar los agarres digitales 4 veces más mientras apunta el pulverizador nasal lejos de usted (y de cualquier otra persona).
• Encontrará una mayor resistencia cuando oprima, y los agarres digitales solo avanzarán un poco.
• NO oirá un clic cuando oprima.
• El dosímetro permanecerá en el número “8”.
• Ponga el tapón protector en el frasco del pulverizador.
• Vuelva a colocar el frasco dentro del envase a prueba de niños.
• Pregunte en su farmacia local sobre la eliminación de los frascos vacíos (ver “Conservación de PecFent”).
Si el pulverizador nasal PecFent está bloqueado o no pulveriza correctamente
• Si el pulverizador está bloqueado, apunte lejos de usted (y de cualquier otra persona) y empuje la bomba firmemente hacia abajo. De esta manera despejará cualquier bloqueo.
• Si el pulverizador nasal sigue sin funcionar correctamente, deseche el frasco defectuoso y comience uno nuevo. Informe a su médico de lo que ha sucedido. No trate nunca de arreglar usted mismo el pulverizador nasal ni trate de desarmarlo, ya que podría administrarle una dosis equivocada.
Deseche el frasco de PecFent y empiece uno nuevo:
• Si han pasado 60 días o más desde que lo cebó o usó el frasco por primera vez.
Si usa más PecFent del que debe
• Si usa más PecFent del que debiera, tal vez se sienta somnoliento, con náuseas, mareado, o tal vez tenga una respiración lenta o superficial. Si se siente muy mareado, muy somnoliento, o si tiene una respiración lenta o superficial, llame a una ambulancia o pídale a alguien que lo haga inmediatamente.
Si interrumpe el tratamiento con PecFent
Si ya no sufre dolor irruptivo, consulte a su médico antes de interrumpir el tratamiento con PecFent y siga sus indicaciones. Sin embargo, debe seguir tomando otro opioide para tratar el dolor constante. Tal vez su médico tenga que comprobar la dosis.
Puede experimentar síntomas de abstinencia similares a los posibles efectos adversos de PecFent cuando deje de usar PecFent. Si experimenta síntomas de abstinencia, se debe poner en contacto con su médico. Su médico evaluará si necesita algún medicamento para reducir o eliminar los síntomas de abstinencia.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Llame a una ambulancia o pídale a alguien que lo haga inmediatamente en cualquiera de los siguientes casos:
• Si se siente muy mareado o se desmaya.
• Si siente mucho sueño.
• Si tiene una respiración lenta o superficial.
• Si tiene la piel fría y húmeda, está pálido, tiene el pulso débil u otros signos de shock.
Si usted o la persona que lo cuida nota alguno de los efectos anteriores, llame inmediatamente a una ambulancia.
Efectos adversos frecuentes (pueden afectar hasta 1 de cada 10 personas):
• No saber dónde está (desorientación)
• Cambio en el gusto
• Mareos
• Náuseas o vómitos
• Somnolencia, dolor de cabeza
• Sangrado por la nariz, molestia en la nariz, nariz que moquea
• Estreñimiento
• Picor en la piel
Efectos adversos poco frecuentes (pueden afectar hasta 1 de cada 100 personas):
• Infección respiratoria
• Dolor, molestia o inflamación de la garganta o la nariz
• Tos, estornudos, catarro o resfriado, cambios en el líquido producido por la nariz
• Reacción alérgica, erupción cutánea
• Pérdida o aumento del apetito, aumento de peso
• Deshidratación, sed
• Abuso o mal uso del medicamento
• Ver u oír cosas que en realidad no existen (alucinaciones o delirio), sensación de confusión
• Depresión, preocupación, lentitud o intranquilidad
• Pérdida de la concentración o aumento de la actividad
• Pérdida de la memoria
• Sensación de estar “colocado”
• Ser menos consciente o falto de respuesta, pérdida de la conciencia
• Convulsión (crisis epiléptica)
• Convulsiones o temblores musculares
• Pérdida del gusto, pérdida o cambio del olfato
• Dificultad para hablar
• Coloración azul de la piel
• Vértigo, caídas, malestar general
• Funcionamiento inadecuado del calor y la circulación, sensación de sofocos o fiebre, escalofríos, sudoración excesiva
• Hinchazón de las partes blandas
• Tensión arterial baja
• Bloqueo de la tráquea
• Dificultad para respirar
• Hemorragia vaginal
• Desgarro intestinal o inflamación de la mucosa del estómago
• Adormecimiento u hormigueos en la boca, la lengua o la nariz, u otros problemas en la lengua, úlceras en la boca, sequedad de la boca
• Diarrea
• Arcadas, dolor de estómago, indigestión.
• Molestia o dolor en las articulaciones
• Dificultad o incapacidad para beber agua
• Dolor en el pecho
• Sensación de cansancio o debilidad, problemas para moverse
• Cambios en las células de la sangre (detectados por análisis de laboratorio)
• Aumento de azúcar en sangre
• Proteína en la orina
Otros efectos adversos (frecuencia no conocida [no puede estimarse a partir de los datos disponibles]):
• Problemas respiratorios graves
• Rubor
• Insomnio
• Síndrome de abstinencia (se puede manifestar con la aparición de los siguientes efectos adversos: náuseas, vómitos, diarrea, ansiedad, escalofríos, temblores y sudoración).
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de PecFent
Mantener este medicamento fuera de la vista y del alcance de los niños. PecFent podría ser
potencialmente mortal si un niño lo toma por accidente.
• No utilice este medicamento después de la fecha de caducidad que aparece en la caja y en el frasco después de “CAD”. La fecha de caducidad es el último día del mes que se indica.
• No conservar PecFent a una temperatura superior a 25°C.
• No congelar.
• Conservar el frasco en su envase a prueba de niños para protegerlo de la luz.
• Conservar siempre el frasco de PecFent dentro del envase a prueba de niños, incluso cuando esté terminado.
• No usar durante más de 60 días después del primer uso (ya sea el cebado o el uso para tratar un episodio de dolor irruptivo).
• El PecFent que ha caducado o que ya no se necesite puede contener, no obstante, una cantidad suficiente de medicamento para ser perjudicial para otras personas, especialmente los niños. PecFent no se debe tirar por los desagües ni a la basura. Cualquier resto de PecFent que no se quiera se debe desechar lo antes posible siguiendo las instrucciones facilitadas en Eliminación de PecFent sin utilizar. Cualquier frasco vacío debe volverse a colocar en su envase a prueba de niños y desecharse; para ello, debe llevarse a la farmacia o proceder según indiquen las normativas locales.
6. Contenido del envase e información adicional Composición de PecFent
El principio activo es el fentanilo.
• PecFent 100 microgramos/pulverización, solución para pulverización nasal Cada ml de solución contiene 1000 microgramos de fentanilo (como citrato).
Una pulverización (100 microlitros) contiene 100 microgramos de fentanilo (como citrato).
• PecFent 400 microgramos/pulverización, solución para pulverización nasal Cada ml de solución contiene 4000 microgramos de fentanilo (como citrato).
Una pulverización (100 microlitros) contiene 400 microgramos de fentanilo (como citrato).
Los demás componentes (excipientes) son pectina (E440), manitol (E421), alcohol feniletílico, propilparahidroxibenzoato (E216), sacarosa, agua purificada, y ácido clorhídrico o hidróxido de sodio para el ajuste del pH.
Aspecto del producto y contenido del envase
El medicamento es una solución de pulverización nasal transparente a casi transparente e incolora. Está contenida en un frasco de vidrio transparente, provisto de una bomba de dosificación. La bomba tiene un contador de pulverizaciones que tiene un ruido de “clic”, por lo que puede oír y ver que la pulverización se ha administrado y un tapón protector. Después de cebar el frasco de PecFent (preparado para su uso), administra ocho pulverizaciones completas. Cada frasco de PecFent se suministra en un envase a prueba de niños.
Los frascos de PecFent en sus envases a prueba de niños se suministran en cajas que contienen 1, 4 o 12 frascos.
Puede que solamente estén comercializados algunos tamaños de envases.
Titular de la autorización de comercialización
Archimedes Development Ltd
Nottingham
NG7 2TN
Reino Unido
Responsable de la fabricación
L. Molteni & C. dei F.lli Alitti Societá di Esercizio S.p.A Strada Statale 67 Tosco Romagnola,
Fraz. Granatieri - 50018 Scandicci (FI)
Italia
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Belgie/Belgique/Belgien
Luxembourg/Luxemburg
Archimedes Pharma Ltd Royaume-Uni
Tél/Tel: + 44 (0)1896 664000 Etnrapna
Archimedes Pharma Ltd BenHKOÓpHTaHHa (OóegHHeHOTO KpancTBo) Ten.: + 44 (0)1896 664000
Ceská republika
Archimedes Pharma Ltd Spojené království (Velká Británie)
Tel: + 44 (0)1896 664000
Danmark
Kyowa Kirin Filial af Kyowa Kirin AB, Sverige
Tlf: +46 8 50 90 74 10
Deutschland
Kyowa Kirin GmbH Tel: +49 (0) 211/416 119-0
Magyarország
Archimedes Pharma Ltd Egyesült Királyság (Nagy-Britannia) Tel: + 44 (0)1896 664000
Malta
Archimedes Pharma Ltd
Ir-Renju Unit
Tel: + 44 (0)1896 664000
Nederland
Kyowa Kirin Pharma BV Tel: +31 (0)900 1231236
Vereinigtes Konigreich Tel: + 44 (0)1896 664000
|
ELXúóa ANABIQIII IKE T^: + 2102711020 |
Polska Molteni Farmaceutici Polska Sp. z o.o. Tel: + 48 (012) 653 15 71 |
|
España Kyowa Kirin Farmacéutica S.L.U Tel: + 34 (0) 91 3510373 |
Portugal Archimedes Pharma Ltd Reino Unido Tel: + 44 (0)1896 664000 |
|
France Kyowa Kirin Pharma SAS: Tél : +33(0)1 55 39 14 30 |
Romania Archimedes Pharma Ltd Marea Britanie Tel: + 44 (0)1896 664000 |
|
Hrvatska Archimedes Pharma Ltd Ujedinjeno Kraljevstvo (Velika Britanija) Tel: + 44 (0)1896 664000 |
Slovenija Archimedes Pharma Ltd Zdruzeno kraljestvo (Velika Britanija) Tel: + 44 (0)1896 664000 |
|
Ireland Archimedes Pharma Ltd UK Tel: + 44 (0)1896 664000 |
Slovenská republika Archimedes Pharma Ltd Spojené kráfovstvo (Vel’ká Británia) Tel: + 44 (0)1896 664000 |
|
Ísland Archimedes Pharma Ltd Sameinaóa konungsd^mió (Bretland) Sími: + 44 (0)1896 664000 |
Suomi/Finland Kyowa Kirin AB filial i Finland Puh/Tel: +358 10 23 55 560 |
|
Italia L. Molteni & C. dei F.lli Alitti Societá di Esercizio S.p.A. Tel: + 39.055.73611 |
Sverige Kyowa Kirin AB Tel: +46 8 50 90 74 10 |
|
Kúnpoq CENTROM PHARMA LIMITED Tr(k: + 357 22 692094 Latvija Archimedes Pharma Ltd Lielbritánija Tel: + 44 (0)1896 664000 |
United Kingdom Archimedes Pharma Ltd Tel: + 44 (0)1896 664000 |
Fecha de la última revisión de este prospecto: {MM/AAAA}.
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu/.
B. PROSPECTO
Prospecto: información para el usuario
PecFent 100 microgramos/pulverización, solución para pulverización nasal, frasco de dos
pulverizaciones
Fentanilo
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento, porque contiene información importante para usted.
• Conserve este prospecto, ya que puede tener que volver a leerlo.
• Si tiene alguna duda, consulte a su médico o farmacéutico.
• Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
• Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto:
1. Qué es PecFent y para qué se utiliza
3. Qué necesita saber antes de empezar a usar PecFent
3. Cómo usar PecFent
4. Posibles efectos adversos
5. Conservación de PecFent
6. Contenido del envase e información adicional
1. Qué es PecFent y para qué se utiliza
Qué es PecFent
PecFent contiene fentanilo, que es un potente medicamento para el alivio del dolor, conocido como un
analgésico opioide.
Para qué se utiliza PecFent
PecFent se utiliza en los adultos con cáncer para un tipo de dolor llamado dolor “irruptivo”.
• Este tipo de dolor aparece repentinamente.
• Se presenta aunque se haya tomado el analgésico opioide habitual (por ejemplo, morfina, fentanilo, oxicodona o hidromorfona) para controlar el dolor de base constante.
PecFent solo debe ser utilizado por los adultos que estén tomando ya otros opioides diariamente para
el dolor constante causado por el cáncer.
Cómo actúa PecFent
PecFent es una solución para pulverización nasal.
• Cuando se pulveriza PecFent en la nariz, las diminutas microgotas de la pulverización forman un gel fino.
• El fentanilo se absorbe rápidamente a través de la mucosa de la nariz y pasa directamente a la circulación sanguínea.
• Esto significa que el medicamento llega rápidamente a su organismo para aliviarle el dolor irruptivo.
2. Qué necesita saber antes de empezar a usar PecFent
No use PecFent:
• Si es alérgico al fentanilo o a cualquiera de los demás componentes de este medicamento (incluidos en la sección 6).
• Si no está usando regularmente un medicamento opioide prescrito por su médico (p. ej., codeína, fentanilo, hidromorfona, morfina, oxicodona, meperidina), todos los días a la misma hora, al menos durante una semana, para controlar el dolor persistente. Si no ha estado usando esos medicamentos, no use PecFent dado que su uso puede aumentar el riesgo de que su respiración se vuelva más lenta y/o poco profunda, e incluso de que llegue a pararse.
• Si padece dolor de corta duración distinto al dolor irruptivo.
• Si sufre un problema respiratorio o pulmonar grave.
No use PecFent si alguna de las condiciones anteriores se aplica en su caso. Si tiene dudas, consulte a su médico o farmacéutico antes de usar PecFent.
Advertencias y precauciones
Mantenga PecFent fuera del alcance de los niños
• Debe mantener PecFent dentro del envase de almacenamiento a prueba de niños cuando no esté usándolo, aunque haya usado las 2 pulverizaciones. Esto se debe a que PecFent es potencialmente mortal si un niño lo toma por accidente.
Consulte a su médico o farmacéutico antes de usar PecFent:
• Si no ha estado tomando la misma dosis diaria de su opioide, durante algún tiempo, para el dolor constante que padece.
• Si sufre problemas respiratorios, como asma, silbidos o dificultad para respirar.
• Si sufre un golpe fuerte en la cabeza.
• Si tiene problemas de corazón, especialmente frecuencia cardiaca baja.
• Si tiene la tensión arterial baja o una cantidad baja de líquido en la circulación.
• Si padece problemas de los riñones o del hígado ya que pueden afectar a la manera en que su organismo descompone el medicamento.
• Si toma antidepresivos o antipsicóticos, consulte la sección “Uso de PecFent con otros medicamentos”.
Si alguna de las condiciones anteriores se aplica en su caso (o no está seguro), consulte a su médico o farmacéutico antes de usar PecFent.
• Si es deportista, PecFent puede dar resultados positivos en las pruebas antidopaje.
Informe también a su médico si después de usar PecFent:
• Sufre hemorragias nasales recurrentes; el médico puede aconsejar un tratamiento alternativo.
• Considera que PecFent es cada vez menos eficaz en el tratamiento de los episodios de dolor irruptivo.
• Cree que se está volviendo adicto a PecFent.
Niños y adolescentes
No se ha aprobado el uso de PecFent en niños menores de 18 años.
Uso de PecFent con otros medicamentos
Informe a su médico o farmacéutico si está utilizando, ha utilizado recientemente o podría tener que utilizar cualquier otro medicamento.
En concreto, informe a su médico o farmacéutico antes de usar PecFent si está tomando o ha tomado recientemente cualquiera de los siguientes medicamentos:
• Medicamentos que pudieran causar somnolencia, como las pastillas para dormir, tranquilizantes, relajantes musculares, medicamentos para la ansiedad o medicamentos para las alergias (antihistamínicos).
• Medicamentos para la depresión llamados “inhibidores de la monoaminooxidasa” (IMAO). Informe a su médico o farmacéutico si ha estado tomando un IMAO en las dos semanas anteriores al uso de PecFent.
El riesgo de efectos adversos aumenta si está tomando medicamentos tales como ciertos antidepresivos o antipsicóticos. PecFent puede interactuar con estos medicamentos y usted puede presentar cambios en el estado mental (p. ej., agitación, alucinaciones, coma) y otros efectos como temperatura corporal mayor de 38°C, aumento de la frecuencia cardiaca, presión arterial inestable y exageración de los reflejos, rigidez muscular, falta de coordinación y/o síntomas gastrointestinales (p. ej., náuseas, vómitos, diarrea). Su médico le dirá si PecFent es adecuado para usted.
• Pulverizaciones nasales para tratar la nariz tapada (que contienen un descongestionante como la oximetazolina).
• Medicamentos que pudieran tener un efecto en la manera en que su organismo descompone PecFent, entre ellos:
o Medicamentos para la infección por el VIH (por ejemplo, ritonavir, nelfinavir, amprenavir o fosamprenavir).
o Medicamentos para las infecciones por hongos (por ejemplo, ketoconazol, itraconazol o fluconazol).
o Medicamentos para las infecciones bacterianas (por ejemplo, troleandomicina, claritromicina o eritromicina). o “Aprepitant”, usado para aliviar las náuseas.
o “Diltiazem” y “verapamilo”, usados para la hipertensión o los problemas del corazón. o Otros medicamentos para el dolor llamados agonistas/antagonistas parciales, como la buprenorfina, la nalbufina y la pentazocina. Podría experimentar síntomas del síndrome de abstinencia (náuseas, vómitos, diarrea, ansiedad, escalofríos, temblores y sudoración) mientras utiliza estos medicamentos.
Si alguna de las condiciones anteriores se aplica en su caso (o no está seguro), consulte a su médico o farmacéutico antes de usar PecFent.
No use ningún otro tipo de pulverización nasal por lo menos 15 minutos después de usar PecFent.
Uso de PecFent con alimentos, bebidas y alcohol
• No beba alcohol mientras usa PecFent, ya que puede aumentar el riesgo de sufrir efectos adversos graves.
• No beba zumo de pomelo mientras usa PecFent, ya que puede afectar a la manera en que su organismo descompone el medicamento.
Embarazo, lactancia y fertilidad
Si está embarazada o en periodo de lactancia, cree que podría estar embarazada o tiene intención de quedarse embarazada, consulte a su médico o farmacéutico antes de utilizar este medicamento.
• No use PecFent si está embarazada o pudiera quedarse embarazada, a menos que su médico le haya dicho que lo haga.
• No use PecFent durante el parto ya que puede causar problemas respiratorios a su bebé.
• No use PecFent durante el período de lactancia, ya que el medicamento puede llegar a la leche materna y causar efectos adversos en el niño lactante.
• No debe iniciar la lactancia antes de transcurridos 5 días desde la última dosis de PecFent.
Conducción y uso de máquinas
• Consulte a su médico si es seguro conducir o utilizar máquinas o herramientas mientras toma PecFent.
• Puede sentirse somnoliento, mareado o puede tener problemas de visión después de usar PecFent. Si le ocurre esto, no conduzca ni utilice herramientas o máquinas.
• No conduzca ni utilice herramientas o máquinas hasta que no sepa cómo le hace sentirse este medicamento.
PecFent contiene propilparahidroxibenzoato (E216).
Puede causar reacciones alérgicas (posiblemente retardadas) y, excepcionalmente, broncoespasmo (si no usa la pulverización nasal correctamente).
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico o farmacéutico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
PecFent se presenta en dos concentraciones diferentes: un frasco de 100 microgramos por pulverización y un frasco de 400 microgramos por pulverización. Asegúrese de usar la concentración que el médico le haya recetado.
Qué cantidad usar de PecFent
• Una dosis para tratar un episodio de dolor irruptivo podría consistir en una o dos pulverizaciones (una en cada fosa nasal). Su médico le dirá cuántas pulverizaciones (una o dos) debe usar para tratar el episodio de dolor irruptivo.
• No use una dosis mayor que la que el médico le recete para un único episodio de dolor irruptivo.
• No use PecFent más de cuatro veces al día.
• Espere por lo menos cuatro horas para tomar la siguiente dosis de PecFent.
Dosis inicial
• La dosis inicial es de 100 microgramos.
• Consiste en una sola pulverización en una fosa nasal del frasco de 100 microgramos por pulverización.
• Consulte las instrucciones sobre cómo usar una dosis en “Uso del frasco de PecFent”. Búsqueda de la dosis correcta
• Su médico le ayudará a encontrar la dosis correcta para aliviarle el dolor irruptivo. Es muy importante que siga las instrucciones del médico.
• Informe al médico acerca de su dolor y del efecto que tiene PecFent. Su médico decidirá si es necesario cambiar la dosis de PecFent.
• No se cambie usted mismo la dosis.
Una vez que haya encontrado la dosis correcta
• Informe a su médico si la dosis que recibe de PecFent no le alivia el dolor irruptivo. Su médico decidirá si es necesario cambiar la dosis. No se cambie usted mismo la dosis de PecFent o de otros medicamentos para el dolor.
• Informe inmediatamente a su médico si tiene más de cuatro episodios diarios de dolor irruptivo. Puede que su médico le cambie la medicación para el dolor constante. Una vez que el dolor constante esté controlado, puede que su médico le cambie la dosis de PecFent.
Si no está seguro acerca de la dosis correcta o qué cantidad de PecFent debe utilizar, pregunte a su médico.
Instrucciones sobre cómo abrir y cerrar el envase a prueba de niños
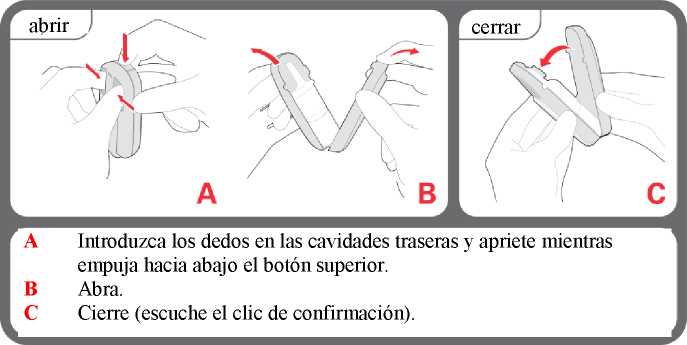
Preparación del frasco de PecFent para su uso
Antes de usar un frasco nuevo de PecFent, debe prepararlo para su uso. Esto se llama “cebado”. Se
recomienda cebar el frasco inmediatamente antes de usar, no por anticipado. (Nota: Este frasco de 2
pulverizaciones no se puede volver a cebar. Si no se ha utilizado el pulverizador dentro de los 5 días
posteriores al cebado, el frasco se debe desechar).
Para cebar el frasco, siga estas instrucciones:
1. Un frasco nuevo de PecFent mostrará dos líneas rojas en la ventana de recuento de la parte superior blanca de plástico del frasco (figuras 1 y 3a).
2. Retire el tapón protector de plástico blanco de la boquilla (figura 1).
3. Apunte el pulverizador nasal lejos de usted (y de otras personas).
4. Sostenga el pulverizador nasal PecFent en posición vertical, con el pulgar en el fondo del frasco, y los dedos índice y corazón en los agarres digitales de cada lado de la boquilla (figura 2).
5. Oprima firmemente hacia abajo los agarres digitales, hasta oír un “clic”; luego, suelte los agarres (figura 2). Oirá un segundo “clic” y aparecerá una única barra roja y grande en la ventana de recuento (figura 3b).
6. Repita tres veces el paso 5. Cuando repita el paso 5, la barra roja empequeñecerá cada vez más, hasta que vea una barra verde en la ventana de recuento (figura 3b-e). La barra verde significa que el pulverizador nasal PecFent está listo para usar.
7. Limpie la boquilla con un pañuelo de papel y tire el pañuelo al inodoro.
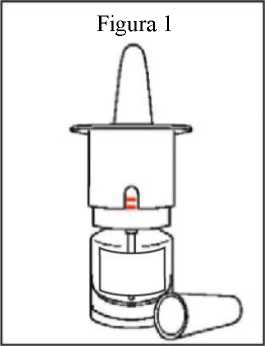
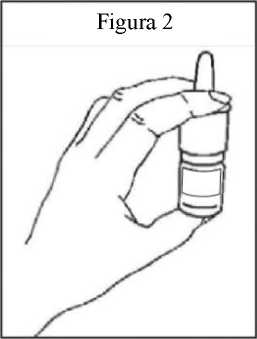
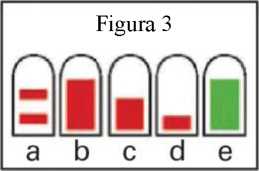
PecFent solo se debe utilizar pulverizándose en las fosas nasales.
1. Compruebe que haya una barra verde o un número en la ventana de recuento (figura 4): esto confirma que el frasco de PecFent se ha cebado (consulte “Preparación del frasco de PecFent para su uso”, más arriba).
2. Suénese la nariz si considera que debe hacerlo.
3. Siéntese con la cabeza en posición vertical.
4. Retire el tapón protector de la boquilla.
5. Sostenga el frasco de PecFent con el pulgar en el fondo del frasco, y los dedos índice y corazón en los agarres digitales (figura 4).
6. Coloque la boquilla a corta distancia (aproximadamente 1 cm) en el interior de la fosa nasal. Apunte hacia las paredes de la nariz. Así inclinará ligeramente el frasco (figura 5).
7. Cierre la otra fosa nasal con un dedo de la otra mano (figura 5).
8. Oprima firmemente los agarres digitales para pulverizar PecFent en la fosa nasal. Cuando oiga un clic, suelte los agarres. Nota: Tal vez no sienta nada en la nariz; no crea que esto significa que el pulverizador no funciona; déjese llevar por el clic y el contador numérico.
9. Inspire lentamente por la nariz y expulse el aire por la boca.
10. El contador numérico avanzará después de cada uso y mostrará cuántas pulverizaciones se han usado.
11. Si el médico le ha recetado una segunda pulverización, repita los puntos 5 a 9, usando la otra fosa nasal.
No use una dosis mayor que la que el médico le recete para tratar un único episodio de dolor.
12. Después de cada uso, vuelva a colocar el frasco en el envase a prueba de niños. Mantenga el medicamento fuera de la vista y del alcance de los niños (figura 6).
13. Quédese sentado por lo menos un minuto después de usar el pulverizador nasal.
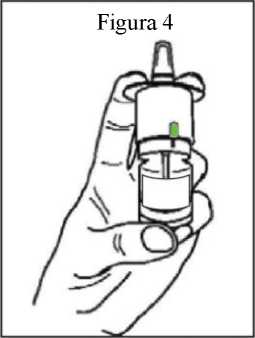
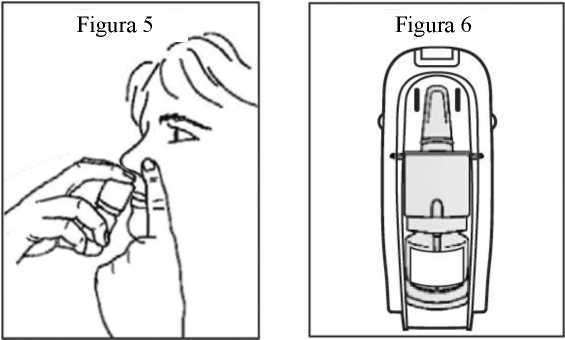
Número de pulverizaciones en este frasco de PecFent
En cada frasco de PecFent hay 2 pulverizaciones completas.
• Después de la primera pulverización, aparecerá el número 1 en la ventana de recuento. La numeración avanzará al número 2 al volver a utilizar el pulverizador.
• Cuando vea un 2 rojo en la ventana de recuento, se ha acabado el frasco y ya no podrá obtener más pulverizaciones completas.
Eliminación de PecFent sin utilizar
• Si puede ver un número, que no sea el 2 en la ventana de recuento, NO ha utilizado las pulverizaciones del frasco. Siguen quedando dosis de PecFent en el frasco.
• Debe expulsar las dosis de PecFent restantes del frasco apuntando el pulverizador nasal lejos de usted (y de cualquier otra persona) y oprimiendo y soltando los agarres hasta que el número “2” rojo aparezca en la ventana de recuento.
Cuando vea el número “2” en la ventana de recuento, sigue quedando medicamento en el frasco que debe expulsar.
• Tendrá que oprimir y soltar los agarres digitales 4 veces más mientras apunta el pulverizador nasal lejos de usted (y de cualquier otra persona).
• Encontrará una mayor resistencia cuando oprima, y los agarres digitales solo avanzarán un poco.
• NO oirá un clic cuando oprima.
• El dosímetro permanecerá en el número “2”.
• Ponga el tapón protector en el frasco del pulverizador.
• Vuelva a colocar el frasco dentro del envase a prueba de niños.
• Pregunte en su farmacia local sobre la eliminación de los frascos vacíos (ver “Conservación de PecFent”).
Si el pulverizador nasal PecFent está bloqueado o no pulveriza correctamente
• Si el pulverizador está bloqueado, apunte lejos de usted (y de cualquier otra persona) y empuje la bomba firmemente hacia abajo. De esta manera despejará cualquier bloqueo.
• Si el pulverizador nasal sigue sin funcionar correctamente, deseche el frasco defectuoso y comience uno nuevo. Informe a su médico de lo que ha sucedido. No trate nunca de arreglar usted mismo el pulverizador nasal ni trate de desarmarlo, ya que podría administrarle una dosis equivocada.
Deseche el frasco de PecFent y empiece uno nuevo:
• Si han pasado más de 5 días desde que cebó el frasco por primera vez.
Si usa más PecFent del que debe
• Si usa más PecFent del que debiera, tal vez se sienta somnoliento, con náuseas, mareado, o tal vez tenga una respiración lenta o superficial. Si se siente muy mareado, muy somnoliento, o si tiene una respiración lenta o superficial, llame a una ambulancia o pídale a alguien que lo haga inmediatamente.
Si interrumpe el tratamiento con PecFent
Si ya no sufre dolor irruptivo, consulte a su médico antes de interrumpir el tratamiento con PecFent y siga sus indicaciones. Sin embargo, debe seguir tomando otro opioide para tratar el dolor constante. Tal vez su médico tenga que comprobar la dosis.
Puede experimentar síntomas de abstinencia similares a los posibles efectos adversos de PecFent cuando deje de usar PecFent. Si experimenta síntomas de abstinencia, se debe poner en contacto con su médico. Su médico evaluará si necesita algún medicamento para reducir o eliminar los síntomas de abstinencia.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
Llame a una ambulancia o pídale a alguien que lo haga inmediatamente en cualquiera de los siguientes casos:
• Si se siente muy mareado o se desmaya.
• Si siente mucho sueño.
• Si tiene una respiración lenta o superficial.
• Si tiene la piel fría y húmeda, está pálido, tiene el pulso débil u otros signos de shock.
Si usted o la persona que lo cuida nota alguno de los efectos anteriores, llame inmediatamente a una ambulancia.
Efectos adversos frecuentes (pueden afectar hasta 1 de cada 10 personas):
• No saber dónde está (desorientación)
• Cambio en el gusto
• Mareos
• Náuseas o vómitos
• Somnolencia, dolor de cabeza
• Sangrado por la nariz, molestia en la nariz, nariz que moquea
• Estreñimiento
• Picor en la piel
Efectos adversos poco frecuentes (pueden afectar hasta 1 de cada 100 personas):
• Infección respiratoria
• Dolor, molestia o inflamación de la garganta o la nariz
• Tos, estornudos, catarro o resfriado, cambios en el líquido producido por la nariz
• Reacción alérgica, erupción cutánea
• Pérdida o aumento del apetito, aumento de peso
• Deshidratación, sed
• Abuso o mal uso del medicamento
• Ver u oír cosas que en realidad no existen (alucinaciones o delirio), sensación de confusión
• Depresión, preocupación, lentitud o intranquilidad
• Pérdida de la concentración o aumento de la actividad
• Pérdida de la memoria
• Sensación de estar “colocado”
• Ser menos consciente o falto de respuesta, pérdida de la conciencia
• Convulsión (crisis epiléptica)
• Convulsiones o temblores musculares
• Pérdida del gusto, pérdida o cambio del olfato
• Dificultad para hablar
• Coloración azul de la piel
• Vértigo, caídas, malestar general
• Funcionamiento inadecuado del calor y la circulación, sensación de sofocos o fiebre, escalofríos, sudoración excesiva
• Hinchazón de las partes blandas
• Tensión arterial baja
• Bloqueo de la tráquea
• Dificultad para respirar
• Hemorragia vaginal
• Desgarro intestinal o inflamación de la mucosa del estómago
• Adormecimiento u hormigueos en la boca, la lengua o la nariz, u otros problemas en la lengua, úlceras en la boca, sequedad de la boca
• Diarrea
• Arcadas, dolor de estómago, indigestión.
• Molestia o dolor en las articulaciones
• Dificultad o incapacidad para beber agua
• Dolor en el pecho
• Sensación de cansancio o debilidad, problemas para moverse
• Cambios en las células de la sangre (detectados por análisis de laboratorio)
• Aumento de azúcar en sangre
• Proteína en la orina
Otros efectos adversos (frecuencia no conocida [no puede estimarse a partir de los datos disponibles]):
• Problemas respiratorios graves
• Rubor
• Insomnio
• Síndrome de abstinencia (se puede manifestar con la aparición de los siguientes efectos adversos: náuseas, vómitos, diarrea, ansiedad, escalofríos, temblores y sudoración).
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Apéndice V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de PecFent
Mantener este medicamento fuera de la vista y del alcance de los niños. PecFent podría ser
potencialmente mortal si un niño lo toma por accidente.
• No utilice este medicamento después de la fecha de caducidad que aparece en la caja y en el frasco después de “CAD”. La fecha de caducidad es el último día del mes que se indica.
• No conservar PecFent a una temperatura superior a 25°C.
• No congelar.
• Conservar el frasco en su envase a prueba de niños para protegerlo de la luz.
• Conservar siempre el frasco de PecFent dentro del envase a prueba de niños, incluso cuando esté terminado.
• No usar durante más de 5 días después del primer uso (ya sea el cebado o el uso para tratar un episodio de dolor irruptivo).
• El PecFent que ha caducado o que ya no se necesite puede contener, no obstante, una cantidad suficiente de medicamento para ser perjudicial para otras personas, especialmente los niños. PecFent no se debe tirar por los desagües ni a la basura. Cualquier resto de PecFent que no se quiera se debe desechar lo antes posible siguiendo las instrucciones facilitadas en Eliminación de PecFent sin utilizar. Cualquier frasco vacío debe volverse a colocar en su envase a prueba de niños y desecharse; para ello, debe llevarse a la farmacia o proceder según indiquen las normativas locales.
6. Contenido del envase e información adicional Composición de PecFent
El principio activo es el fentanilo.
• PecFent 100 microgramos/pulverización, solución para pulverización nasal Cada ml de solución contiene 1000 microgramos de fentanilo (como citrato).
Una pulverización (100 microlitros) contiene 100 microgramos de fentanilo (como citrato).
Los demás componentes (excipientes) son pectina (E440), manitol (E421), alcohol feniletílico, propilparahidroxibenzoato (E216), sacarosa, agua purificada, y ácido clorhídrico o hidróxido de sodio para el ajuste del pH.
Aspecto del producto y contenido del envase
El medicamento es una solución de pulverización nasal transparente a casi transparente e incolora.
Está contenida en un frasco de vidrio transparente, provisto de una bomba de dosificación. La bomba tiene un contador de pulverizaciones que tiene un ruido de “clic”, por lo que puede oír y ver que la pulverización se ha administrado y un tapón protector. Después de cebar el frasco de PecFent (preparado para su uso), administra 1 pulverizacion completa. Cada frasco de PecFent se suministra en un envase a prueba de niños.
Los frascos de PecFent de 2 pulverizaciones en sus envases a prueba de niños se suministran en una caja que contiene 1 frasco.
Titular de la autorización de comercialización
Archimedes Development Ltd
Nottingham
NG7 2TN
Reino Unido
Responsable de la fabricación
L. Molteni & C. dei F.lli Alitti Societá di Esercizio S.p.A Strada Statale 67 Tosco Romagnola,
Fraz. Granatieri - 50018 Scandicci (FI)
Italia
Pueden solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización:
Belgie/Belgique/Belgien
Luxembourg/Luxemburg
Archimedes Pharma Ltd Royaume-Uni
Tél/Tel: + 44 (0)1896 664000 Etnrapna
Archimedes Pharma Ltd BenHKOÓpHTaHHa (OóegHHeHOTO KpancTBo) Ten.: + 44 (0)1896 664000
Ceská republika
Archimedes Pharma Ltd Spojené království (Velká Británie)
Tel: + 44 (0)1896 664000
Danmark
Kyowa Kirin Filial af Kyowa Kirin AB, Sverige
Tlf: +46 8 50 90 74 10
Deutschland
Kyowa Kirin GmbH Tel: +49 (0) 211/416 119-0
Magyarország
Archimedes Pharma Ltd Egyesült Királyság (Nagy-Britannia) Tel: + 44 (0)1896 664000
Malta
Archimedes Pharma Ltd
Ir-Renju Unit
Tel: + 44 (0)1896 664000
Nederland
Kyowa Kirin Pharma BV Tel: +31 (0)900 1231236
Vereinigtes Konigreich Tel: + 44 (0)1896 664000
|
ELXáóa ANABIQIII IKE T^: + 2102711020 |
Polska Molteni Farmaceutici Polska Sp. z o.o. Tel: + 48 (012) 653 15 71 |
|
España Kyowa Kirin Farmacéutica S.L.U Tel: + 34 (0) 91 3510373 |
Portugal Archimedes Pharma Ltd Reino Unido Tel: + 44 (0)1896 664000 |
|
France Kyowa Kirin Pharma SAS: Tél : +33(0)1 55 39 14 30 |
Romania Archimedes Pharma Ltd Marea Britanie Tel: + 44 (0)1896 664000 |
|
Hrvatska Archimedes Pharma Ltd Ujedinjeno Kraljevstvo (Velika Britanija) Tel: + 44 (0)1896 664000 |
Slovenija Archimedes Pharma Ltd Zdruzeno kraljestvo (Velika Britanija) Tel: + 44 (0)1896 664000 |
|
Ireland Archimedes Pharma Ltd UK Tel: + 44 (0)1896 664000 |
Slovenská republika Archimedes Pharma Ltd Spojené kráfovstvo (Vel’ká Británia) Tel: + 44 (0)1896 664000 |
|
Ísland Archimedes Pharma Ltd Sameinaóa konungsd^mió (Bretland) Sími: + 44 (0)1896 664000 |
Suomi/Finland Kyowa Kirin AB filial i Finland Puh/Tel: +358 10 23 55 560 |
|
Italia L. Molteni & C. dei F.lli Alitti Societá di Esercizio S.p.A. Tel: + 39.055.73611 |
Sverige Kyowa Kirin AB Tel: +46 8 50 90 74 10 |
|
Kúnpoq CENTROM PHARMA LIMITED Tr(k: + 357 22 692094 Latvija Archimedes Pharma Ltd Lielbritánija Tel: + 44 (0)1896 664000 |
United Kingdom Archimedes Pharma Ltd Tel: + 44 (0)1896 664000 |
Fecha de la última revisión de este prospecto: {MM/AAAA}.
Otras fuentes de información
La información detallada de este medicamento está disponible en la página web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu/.
59