Ovestinon 1 Mg/G Crema Vaginal
FICHA TÉCNICA
1. NOMBRE DEL MEDICAMENTO
Ovestinon 1 mg/g crema vaginal
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada gramo de crema contiene 1 mg de estriol.
Excipientes: alcohol cetílico, alcohol estearílico y otros excipientes.
Para consultar la lista completa de excipientes, ver sección 6.1.
3. FORMA FARMACÉUTICA
Crema vaginal. Es una masa homogénea, suave, de color blanco a casi blanco de consistencia cremosa.
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
Terapia hormonal de sustitución para el tratamiento de la atrofia del tracto génito-urinario bajo asociada con la deficiencia de estrógenos, bien sea en el climaterio femenino o tras castración quirúrgica, que produce dispareunia, sequedad y prurito vaginales.
Terapia pre y postoperatoria en mujeres postmenopáusicas en cirugía vaginal.
Como ayuda diagnóstica en caso de frotis cervical atrófico dudoso (Papanicolau).
4.2 Posología y forma de administración
Para la atrofia del tracto génito-urinario bajo:
1 aplicación de crema al día durante las primeras semanas (2-3 semanas), y en función del alivio de los síntomas, reducir la dosis hasta llegar a una dosis de mantenimiento (por ejemplo, 1 aplicación de crema dos veces por semana).
Como tratamiento pre y postoperatorio en mujeres postmenopáusicas en cirugía vaginal:
1 aplicación de crema al día las 2 semanas antes de la cirugía; 1 aplicación de crema dos veces por semana durante las 2 semanas después de la operación. Después de la operación, el tratamiento puede comenzarse tan pronto como la aplicación de la crema sea posible, normalmente un mínimo de 2 semanas.
Como ayuda diagnóstica en caso de frotis cervical atrófico dudoso (Papanicolau):
1 aplicación de crema al día durante la semana anterior a la realización del siguiente frotis.
Tanto para el comienzo como para la continuación del tratamiento de los síntomas climatéricos deberá utilizarse en todos los casos la dosis mínima eficaz durante el tiempo de tratamiento lo más corto posible (ver también sección 4.4).
En mujeres que no tomen terapia hormonal de sustitución o en mujeres que cambian de una terapia hormonal de sustitución continua combinada, el tratamiento puede iniciarse cualquier día. Las mujeres que cambian a partir de un régimen de terapia hormonal de sustitución cíclica deberán iniciar el tratamiento con Ovestinon una semana después de finalizar el ciclo.
Forma de administración
Ovestinon 1 mg/g crema vaginal debe administrarse por vía intravaginal. 1 aplicación de crema antes de acostarse.
Una aplicación (aplicador lleno hasta la marca) contiene 0,5 g de Ovestinon 1 mg/g crema vaginal, que corresponde a 0,5 mg de estriol.
Instrucciones de uso para la paciente:
1. Destapar el tubo, invertir el tapón y utilizar la punta aguda para abrir el precinto del tubo.
2. Tirar del émbolo del aplicador hasta la marca y enroscarlo en el tubo.
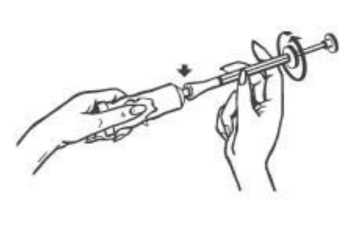
3. Apretar el tubo hasta que penetre suficiente crema en el aplicador para llenarlo hasta la marca.
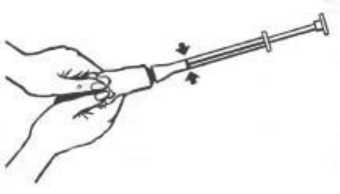
4. Desenroscar el aplicador y volver a tapar el tubo.
5. Para aplicar la crema, acostarse e introducir el extremo del aplicador profundamente en la vagina
6. Empujar lentamente el émbolo hasta que el aplicador quede vacío.
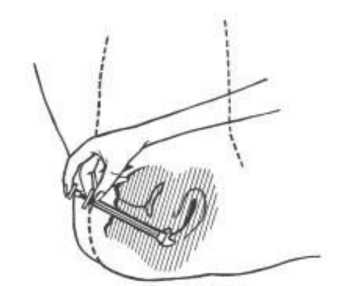
Después de usarlo, sacar el émbolo y lavarlo con el aplicador en agua jabonosa templada, enjuagando bien a continuación. No usar detergentes.
NO PONER EL APLICADOR EN AGUA CALIENTE O HIRVIENDO En caso de olvido de una dosis
En caso de olvido de una dosis, ésta debe administrarse tan pronto como se recuerde, excepto en el caso de que se recuerde en el día de la dosis siguiente. En esta situación, la dosis olvidada debe suprimirse y continuar con el esquema de dosificación habitual. Nunca deben administrarse dos dosis el mismo día.
4.3 Contraindicaciones
• Cáncer de mama, antecedentes personales o sospecha del mismo;
• Tumores estrógeno dependientes malignos o sospecha de los mismos (p. ej. cáncer de endometrio);
• Hemorragia vaginal no diagnosticada;
• Hiperplasia de endometrio no tratada;
• Tromboembolismo venoso (TEV) o antecedentes del mismo (trombosis venosa profunda, embolismo pulmonar);
• Alteración trombofílica conocida (por ejemplo, deficiencia de proteína C, proteína S o de antitrombina, ver sección 4.4);
• Enfermedad tromboembólica arterial activa o reciente (p. ej. angina, infarto de miocardio);
• Enfermedad hepática aguda o antecedente de enfermedad hepática mientras las pruebas de función hepática sigan alteradas;
• Hipersensibilidad al principio activo o a alguno de los excipientes;
• Porfiria.
4.4 Advertencias y precauciones especiales de empleo
• Para el tratamiento de los síntomas climatéricos, la terapia hormonal de sustitución (THS) sólo debe iniciarse cuando los síntomas afectan negativamente la calidad de vida de la mujer. En todos los casos debe realizarse, al menos anualmente, una valoración cuidadosa de los riesgos y beneficios y la THS solamente debe mantenerse mientras los beneficios superen los riesgos.
• La evidencia sobre los riesgos asociados con la THS en el tratamiento de la menopausia prematura es limitada. Sin embargo, debido al bajo nivel de riesgo absoluto en mujeres más jóvenes, el equilibrio entre beneficio y riesgo para estas mujeres puede ser más favorable que para mujeres de más edad.
Reconocimiento y controles médicos
• Antes de iniciar o reinstaurar una THS, debe realizarse una historia clínica completa personal y familiar. La exploración física (incluyendo mamas y pelvis), debe tener en cuenta la historia clínica así como las contraindicaciones y las advertencias para el uso de la THS.
Se recomiendan exámenes médicos regulares durante el tratamiento, cuya naturaleza y frecuencia estarán en función de las condiciones de cada mujer. Debe orientarse a las mujeres acerca de cuáles son los cambios que detecten en sus pechos de los que deben informar a su médico o enfermera (ver “Cáncer de mama” más adelante). Las exploraciones, incluyendo técnicas de imagen apropiadas como la mamografía, deben realizarse periódicamente de acuerdo con las guías de práctica clínica aceptadas, adaptándolas a las necesidades clínicas de cada caso.
Se deberá siempre considerar la administración de la menor dosis y la duración de tratamiento más corta.
Si aparece cualquiera de estas situaciones o ha ocurrido previamente y/o se han agravado durante el
embarazo o durante un tratamiento hormonal previo debe vigilarse estrechamente a la paciente.
Las condiciones que seguidamente se enumeran pueden recurrir o agravarse durante el tratamiento con
Ovestinon:
• Leiomioma (fibroma uterino) o endometriosis;
• Factores de riesgo para trastornos tromboembólicos (ver a continuación);
• Factores de riesgo para tumores estrógeno dependientes, por ejemplo cáncer de mama en familiares de primer grado;
• Hipertensión arterial;
• Trastornos hepáticos (por ejemplo adenoma hepático);
• Trastornos renales;
• Diabetes mellitus con o sin afectación vascular;
• Colelitiasis;
• Migraña o cefalea (grave);
• Lupus eritematoso sistémico (LES);
• Antecedentes de hiperplasia de endometrio (ver a continuación);
• Epilepsia;
• Asma;
• Otosclerosis;
• Prurito.
Si se diagnostica un empeoramiento de cualquiera de las condiciones anteriores o se sospecha su aparición durante el tratamiento con THS, deberán reevaluarse los beneficios y riesgos de la THS y en base a ello la pertinencia de continuar el tratamiento.
Razones para suspender la terapia inmediatamente:
La terapia debe suspenderse en las siguientes situaciones:
• Ictericia o deterioro de la función hepática;
• Aumento significativo en la presión arterial;
• Aparición por primera vez de cefalea tipo migraña;
• Embarazo;
• Aparición de cualquiera de las condiciones descritas en la sección 4.3.
Hiperplasia y carcinoma endometrial
Para evitar la estimulación endometrial, la dosis diaria no debe exceder de 1 aplicación de crema al día (0,5 mg de estriol) ni tampoco debe utilizarse esta dosis máxima (1 aplicación de crema) durante más de 23 semanas. Un estudio epidemiológico ha mostrado que el tratamiento prolongado con dosis bajas de estriol por vía oral, pero no vaginal, puede aumentar el riesgo de cáncer de endometrio. El riesgo aumentó con la duración del tratamiento y desapareció en el curso de un año después de discontinuarlo. El aumento del riesgo se concentró principalmente en tumores menos invasivos y muy diferenciados.
Durante los primeros meses de tratamiento pueden producirse hemorragias y sangrados irregulares. Especialmente si estas hemorragias aparecen después de algún tiempo de haber iniciado el tratamiento o persisten una vez que el tratamiento se ha interrumpido, deberá investigarse la etiología de la hemorragia, realizando incluso una biopsia endometrial para excluir malignidad endometrial. Se aconsejará a la paciente que contacte con el médico si se produce sangrado vaginal.
Cáncer de mama
• La terapia hormonal sustitutiva puede aumentar la densidad mamográfica. Esto puede complicar la detección radiológica del cáncer de mama. En estudios clínicos se ha comunicado que la probabilidad de desarrollar un aumento de la densidad mamográfica era menor en sujetos tratados con estriol que en sujetos tratados con otros estrógenos.
La evidencia disponible indica un mayor riesgo de padecer cáncer de mama en mujeres que toman THS con combinación de estrógeno-progestágeno y posiblemente también con estrógenos solos, lo cual depende de la duración de la THS.
Terapia combinada de estrógeno-progestágeno:
- El ensayo clínico aleatorizado controlado con placebo Women’s Health Initiative (WHI) y otros estudios epidemiológicos coinciden en mostrar un aumento del riesgo de cáncer de mama en mujeres que toman una combinación de estrógeno-progestágeno en la THS, que empieza a manifestarse después de unos 3 años de tratamiento (ver sección 4.8).
Terapia de estrógeno sólo:
- El ensayo WHI no reveló ningún aumento de riesgo de cáncer de mama en mujeres
histerectomizadas en THS con estrógeno sólo. Estudios observacionales han revelado en su mayoría un ligero aumento del riesgo de un diagnóstico de cáncer de mama, el cual es sustancialmente menor que el encontrado en las usuarias de combinaciones de estrógeno-progestágeno (ver sección 4.8).
El exceso de riesgo comienza a ser evidente a los pocos años de uso, retornando a los valores basales
después de unos años (aproximadamente 5 años) tras suspender el tratamiento.
• No se conoce si Ovestinon supone el mismo riesgo. En un reciente estudio caso-control basado en población, en 3.345 mujeres con cáncer de mama invasivo y 3.454 controles, no se encontró una asociación del estriol con el aumento del riesgo de cáncer de mama, como sucede con otros estrógenos. Sin embargo, las implicaciones clínicas de estos resultados todavía son desconocidas. Por tanto, es importante que este riesgo de diagnóstico de cáncer de mama se discuta con la paciente y se sopese frente a los beneficios conocidos de la THS.
Cáncer de ovario
• El cáncer de ovario es mucho más raro que el cáncer de mama. El tratamiento a largo plazo con THS (al menos de 5 a 10 años) con medicamentos que contienen estrógeno sólo se ha asociado con un riesgo ligeramente mayor de cáncer de ovario (ver sección 4.8). Algunos ensayos, incluido el Women’s Health Initiative (WHI) indican que el uso a largo plazo de THS combinada puede originar un riesgo similar, o ligeramente menor (ver sección 4.8). No está claro si el uso a largo plazo de estrógenos de baja potencia (como Ovestinon) supone un riesgo diferente al de otros medicamentos con estrógeno sólo.
Tromboembolismo venoso
• La THS se asocia con un riesgo de 1,3 a 3 veces de desarrollar tromboembolismo venoso (TEV), esto es, trombosis venosa profunda o embolia pulmonar. La aparición de TEV es más probable durante el primer año de tratamiento con THS que posteriormente (ver sección 4.8).
• Estos estudios no incluyeron Ovestinon, y en ausencia de datos, se desconoce si Ovestinon conlleva el mismo riesgo.
Deberá evaluarse cuidadosamente en consulta con la paciente el balance riesgo/beneficio de la THS cuando esté presente algún factor de riesgo de aparición de TEV que no constituya una contraindicación.
• Las pacientes con patologías trombofílicas conocidas tienen un mayor riesgo de TEV y la THS puede aumentar este riesgo. La THS está contraindicada en estas pacientes (ver sección 4.3).
• Los factores de riesgo generalmente reconocidos de TEV incluyen el uso de estrógenos, edad avanzada, cirugía mayor, inmovilidad prolongada, obesidad (índice de masa corporal > 30 Kg/m2), embarazo/postparto, lupus eritematoso sistémico (LES) y cáncer. No existe consenso acerca del posible papel de las varices en la aparición del TEV.
Al igual que para todas las pacientes en postoperatorio, debe considerarse la adopción de medidas profilácticas tras la cirugía para prevenir el TEV. Si tras una cirugía programada sigue un periodo de inmovilización prolongada se recomienda interrumpir temporalmente el tratamiento de 4 a 6 semanas antes de la intervención quirúrgica. El tratamiento no debe reiniciarse hasta que la mujer haya recobrado completamente la movilidad.
• Si Ovestinon se utiliza para la indicación "terapia pre y postoperatoria en mujeres postmenopáusicas en cirugía vaginal" debe considerarse la adopción de un tratamiento profiláctico contra la trombosis.
• A las mujeres sin antecedentes personales de TEV, pero con un familiar de primer grado con un historial de trombosis en edad temprana, se les puede ofrecer un cribado después un asesoramiento detallado con respecto a sus limitaciones (sólo una parte de las anomalías
trombofilicas son identificadas mediante cribado). En caso de que se detecte una anomalía trombofílica que produce trombosis en algunos miembros de la familia o si la anomalía es "grave" (por ejemplo, deficiencia de antitrombina, proteína S, proteína C o una combinación de anomalías), la THS está contraindicada.
• Las mujeres que ya estén siendo tratadas con anticoagulantes requieren una valoración cuidadosa de los beneficios y los riesgos de la THS antes de comenzar el tratamiento.
• El tratamiento debe interrumpirse si aparece un cuadro de TEV tras iniciar el tratamiento con Ovestinon. Las mujeres deben ser advertidas de que se pongan inmediatamente en contacto con su médico cuando observen la aparición de un síntoma que pueda sugerir un episodio tromboembólico (p. ej. tumefacción dolorosa de una pierna, dolor repentino en el pecho, disnea).
Enfermedad cardiovascular
No deberá utilizarse la THS para prevenir enfermedades cardiovasculares.
• Los datos de ensayos clínicos controlados aleatorizados no han mostrado evidencia de protección contra el infarto de miocardio en mujeres con enfermedad cardiovascular o sin ella que recibieron THS combinada de estrógeno-progestágeno o de estrógeno sólo.
Terapia combinada de estrógeno-progestágeno:
El riesgo relativo de arteriopatía coronaria durante la THS combinada de estrógeno-progestágeno aumenta ligeramente. Ya que el riesgo basal absoluto de padecer arteriopatía coronaria está claramente relacionado con la edad, el número de casos adicionales de arteriopatía coronaria debido al uso de estrógeno-progestágeno es muy bajo en mujeres sanas cerca de la menopausia, aunque se irá elevando cuanto más avanzada sea la edad de la paciente.
Terapia de estrógeno sólo:
Datos de estudios aleatorizados y controlados no encontraron un mayor riesgo de arteriopatía coronaria en mujeres histerectomizadas en terapia de estrógeno sólo.
Accidente cerebrovascular isquémico
Las terapias combinadas de estrógeno-progestágeno y la terapia con estrógeno sólo, están asociadas con un aumento del riesgo de accidente cerebrovascular isquémico de hasta 1,5 veces. El riesgo relativo no cambia con la edad ni con el tiempo transcurrido desde la menopausia. Sin embargo, como el riesgo basal de accidente cerebrovascular está claramente relacionado con la edad, el riesgo total en mujeres usuarias de THS aumenta con la edad (ver sección 4.8).
Para otros productos de THS no existen hasta el momento ensayos controlados randomizados que evalúen el riesgo de morbilidad o mortalidad cardiovascular o de accidente vascular cerebral asociado a THS. Por lo tanto, no existen datos para avalar la conclusión que la frecuencia de acontecimientos cardiovasculares o de accidentes vasculares cerebrales pueda ser diferente con Ovestinon.
Otras condiciones
• Se deberá vigilar estrechamente a las pacientes con disfunción renal o cardiaca ya que los estrógenos pueden causar retención de líquidos.
• Estriol es un inhibidor débil de las gonadotrofinas sin otros efectos significativos en el sistema endocrino.
• Las mujeres con hipertrigliceridemia pre-existente deberán ser estrechamente vigiladas durante el tratamiento sustitutivo con estrógenos u hormonas, dado que se han descrito raramente casos de elevaciones importantes de triglicéridos plasmáticos, que han dado lugar a un cuadro de pancreatitis con el tratamiento oral con estrógeno en pacientes con esta alteración.
• Aunque los datos recogidos hasta la actualidad sugieren que los estrógenos no alteran el metabolismo de los carbohidratos, las mujeres diabéticas deberán ser controladas al principio del tratamiento hasta que no se disponga de más información.
• Los estrógenos aumentan la unión de globulina tiroidea (TBG), dando lugar a niveles aumentados de hormona tiroidea circulante, como refleja la PBI (yodo ligado a proteína), los niveles de T4 (determinados por columna o radioinmunoensayo) o los niveles de T3 (determinados por radioinmunoensayo). La recaptación de T3 está disminuida, lo que refleja el aumento de TBG. Las concentraciones de T3 y T4 libres no se modifican. Las concentraciones séricas de otras proteínas de unión pueden también verse modificadas, entre ellas la globulina de unión a corticoides (CBG), la globulina de unión a hormonas sexuales (SHBG), lo que dará lugar a una elevación de los niveles de corticosteroides y esteroides séricos respectivamente. Las concentraciones de hormona libre o biológicamente activa no se modifican. Otras proteínas plasmáticas como el sustrato renina/angiotensinógeno, alfa-1-antitripsina o ceruloplasmina, pueden verse también incrementadas.
• La THS no mejora la función cognitiva. Existen datos que muestran un incremento del riesgo de probable demencia en mujeres que comienzan el tratamiento continuo combinado o con estrógeno sólo después de los 65 años.
• Deberá advertirse a las mujeres que Ovestinon no es un anticonceptivo, ni restablecerá la fertilidad.
Información importante sobre algunos de los componentes de Ovestinon 1 mg/g crema vaginal
Por contener alcohol cetílico y alcohol estearílico puede provocar reacciones locales en la piel (como dermatitis de contacto).
4.5 Interacción con otros medicamentos y otras formas de interacción
Aunque los datos son limitados, podrían ocurrir interacciones entre Ovestinon y otros medicamentos. Las siguientes interacciones se han descrito con el uso de anticonceptivos orales combinados y podrían ser relevantes también para Ovestinon.
El metabolismo de los estrógenos puede estar aumentado con el uso concomitante de sustancias que se conoce que inducen las enzimas metabolizadoras de fármacos, específicamente las enzimas del citocromo P450, tales como anticonvulsivantes (p. ej. hidantoínas, barbitúricos, carbamazepina), anti-infecciosos (p. ej. griseofulvina, rifamicinas, los agentes anti-retrovirales nevirapina, efavirenz) y preparaciones a base de plantas medicinales que contengan hierba de San Juan (Hypericum perforatum).
Se deberá tener precaución si la mujer está tomando inhibidores de la proteasa (p. ej. ritonavir y nelfinavir), que son inhibidores potentes de las enzimas del citocromo P450, pero por el contrario, muestran propiedades inductoras cuando se utilizan de forma concomitante con hormonas esteroideas.
Clínicamente, un aumento en el metabolismo de los estrógenos puede traducirse en una reducción de la efectividad de Ovestinon y en cambios en el patrón de los sangrados uterinos.
Estriol posiblemente puede aumentar los efectos farmacológicos de los corticosteroides, succinilcolina, teofilinas y troleandomicina.
4.6 Fertilidad, embarazo y lactancia
Ovestinon no debe utilizarse durante el embarazo. Si se produce el embarazo durante el tratamiento con Ovestinon, éste debe interrumpirse inmediatamente. Los resultados de la mayoría de los estudios epidemiológicos realizados hasta la fecha en los que se refería una exposición fetal inadvertida a estrógenos no mostraron efectos teratógenos o fetotóxicos.
Ovestinon no está indicado durante la lactancia. El estriol se excreta en la leche materna y puede disminuir la producción de leche.
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
No se conoce que Ovestinon tenga algún efecto en el estado de alerta y la concentración.
4.8 Reacciones adversas
Se han notificado en la literatura y la farmacovigilancia las siguientes reacciones adversas:
|
Sistema orgánico |
Reacciones adversas* |
Frecuencia |
|
Trastornos del aparato reproductor y de la mama |
Molestia en mama y dolor de mama |
Poco frecuentes |
|
Trastornos generales y alteraciones en el lugar de administración |
Irritación de la zona de aplicación y prurito en la zona de aplicación |
Poco frecuentes |
|
Trastornos del sistema nervioso |
Cefalea |
Raras |
|
Trastornos oculares |
Alteraciones visuales |
Raras |
|
Trastornos vasculares |
Hipertensión Calambres en las piernas |
Raras |
|
Trastornos musculoesqueléticos y del tejido conjuntivo |
Calambres en las piernas |
Raras |
* MedDRA versión 9.1
Estas reacciones adversas normalmente son transitorias, pero pueden ser indicativas de que la dosificación es demasiado alta.
Se han descrito otras reacciones adversas asociadas con el tratamiento de estrógeno sólo o combinado con progestágenos.
• neoplasias estrógeno-dependientes benignas o malignas, p. ej. cáncer de endometrio.
No se conoce con certeza la seguridad endometrial a largo plazo o con el uso repetido de estrógenos vaginales de uso tópico. Por lo tanto, en el caso de que se repitiera el tratamiento, éste debe ser revisado al menos una vez al año, prestando especial atención a cualquier síntoma de la hiperplasia o carcinoma endometrial. Ver más información en las secciones 4.3 y 4.4.
• alteraciones subcutáneas y de la piel: cloasma, eritema multiforme, eritema nodoso, púrpura vascular, dermatitis de contacto, alteraciones de la pigmentación, prurito generalizado y exantema,
• alteración de la vesícula biliar;
• probable demencia a partir de los 65 años (ver sección 4.4).
Riesgo de cáncer de mama
- Se ha notificado un aumento del riesgo hasta 2 veces mayor de un diagnóstico de cáncer de mama en mujeres que tomaron terapia combinada de estrógeno-progestágeno durante más
de 5 años.
- Cualquier aumento en el riesgo en las usuarias que tomaron terapia de estrógeno sólo es sustancialmente menor que el observado en las usuarias de terapia combinada de estrógeno-progestágeno.
- El nivel de riesgo depende de la duración del uso (ver sección 4.4).
- Los resultados del mayor ensayo aleatorizado controlado con placebo realizado (WHI) y del mayor estudio epidemiológico (MWS) se presentan a continuación:

Estudio Million Women - Riesgo adicional estimado de cáncer de mama tras 5 años de uso
|
Rango de edad (años) |
Casos adicionales por cada 1000 no usuarias de THS en un período de 5 años * |
Cociente de riesgo # |
Casos adicionales por cada 1000 usuarias de THS en un período de 5 años (IC 95%) |
|
THS con estrógeno sólo | |||
|
50-65 |
9-12 |
1,2 |
1-2 (0-3) |
|
THS combinada estrógeno-progestágeno | |||
|
50-65 |
9-12 |
1,7 |
6 (5-7) |
# Cociente global de riesgo. El cociente de riesgo no es constante sino que aumentará conforme se alargue la duración de uso.
* Conforme a las tasas basales de incidencia en los países desarrollados.
Ensayo WHI en EEUU - Riesgo adicional de cáncer de mama tras 5 años de uso
|
Rango de edad (años) |
Incidencia por cada 1000 mujeres en grupo placebo en un período de 5 años |
Cociente de riesgo e IC 95% |
Casos adicionales por cada 1000 usuarias de THS en un período de 5 años con IC 95% |
|
Estrógeno sólo (Estrógenos conjugados equinos) | |||
|
50-79 |
21 |
0,8 (0,7 - 1,0) |
-4 (-6 - 0)* |
|
Estrógenos conjugados equinos y acetato de medroxiprogesterona $ | |||
|
50-79 |
14 |
1,2 (1,0 - 1,5) |
+4 (0 - 9) |
{ Cuando el análisis se restringió a mujeres que no habían usado THS antes del estudio no hubo aumento de riesgo evidente durante los primeros 5 años de tratamiento. Después de 5 años el riesgo era más alto que en las no usuarias.
* Ensayo WHI en mujeres histerectomizadas, que no mostró un aumento de riesgo de cáncer de mama en dichas mujeres.
Cáncer de ovario
El uso a largo plazo de THS con estrógeno sólo y combinada estrógeno-progestágeno, se ha asociado con un riesgo ligeramente mayor de cáncer de ovario. En el ensayo Million Women Study para usuarias de THS en un período de 5 años se detectó un caso adicional por cada 2500 usuarias.
Riesgo de tromboembolismo venoso
La THS se asocia con un aumento del riesgo relativo de 1,3 a 3 veces de desarrollar tromboembolismo venoso (TEV), esto es, trombosis venosa profunda o embolia pulmonar. La aparición de TEV es más probable durante el primer año de tratamiento con terapia hormonal (ver sección 4.4). Los datos de los ensayos WHI se presentan a continuación:

Ensayo WHI - Riesgo adicional de TEV tras 5 años de uso
|
Rango de edad (años) |
Incidencia por cada 1000 mujeres en grupo placebo en un período de 5 años |
Cociente de riesgo e IC 95% |
Casos adicionales por cada 1000 usuarias de THS |
|
Estrógeno sólo (oral)* | |||
|
50-59 |
7 |
1,2 (0.6 - 2,4) |
1 (-3 - 10) |
|
Combinación de estrógeno-progestágeno (oral) | |||
|
50-59 |
4 |
2,3 (1,2 - 4,3) |
5 (1 - 13) |
* Ensayo en mujeres histerectomizadas.
Riesgo de arteriopatía coronaria
El riesgo de arteriopatía coronaria es ligeramente mayor en las usuarias de THS combinada estrógeno-progestágeno a partir de los 60 años de edad (ver sección 4.4).
Riesgo de accidente cerebrovascular isquémico
La terapia con estrógeno sólo y las terapias combinadas de estrógeno-progestágeno, están asociadas con un aumento relativo del riesgo de accidente cerebrovascular isquémico de hasta 1,5 veces. El riesgo de accidente cerebrovascular hemorrágico no se incrementa durante el uso de la THS.
El riesgo relativo no depende de la edad o la duración del uso, sin embargo, como el riesgo basal está claramente relacionado con la edad, el riesgo total de accidente cerebrovascular en mujeres en THS aumenta con la edad (ver sección 4.4).
Ensayo combinado WHI - Riesgo adicional de accidente cerebrovascular isquémico* tras 5 años de uso
|
Rango de edad (años) |
Incidencia por cada 1000 mujeres en grupo placebo en un período de 5 años |
Cociente de riesgo e IC 95% |
Casos adicionales por cada 1000 usuarias de THS en un período de 5 años |
|
50-59 |
8 |
1,3 (1,1- 1,6) |
3 (1-5) |
* No se diferenció entre el accidente cerebrovascular isquémico y el ictus hemorrágico.
Notificación de sospechas de reacciones adversas:
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del Sistema Español de Farmacovigilancia de medicamentos de Uso Humano: https://www.notificaram.es
4.9 Sobredosis
La toxicidad aguda de estriol en animales es muy baja. La sobredosificación con Ovestinon tras administración vaginal es improbable. Sin embargo, si se ingieren grandes cantidades de estriol pueden aparecer náuseas, vómitos y sangrado por deprivación en mujeres. No se conoce un antídoto específico. Puede administrarse tratamiento sintomático en caso necesario.
5. PROPIEDADES FARMACOLÓGICAS
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: Estrógenos. Estrógenos naturales y semisintéticos, monofármacos, código ATC: G03CA04.
Ovestinon contiene la hormona femenina natural estriol. Al contrario que otros estrógenos, estriol es un estrógeno de acción breve, porque su tiempo de retención en los núcleos de las células endometriales es corto. Sustituye la falta de producción estrogénica en mujeres menopáusicas, y alivia los síntomas de la menopausia. Estriol es particularmente eficaz en el tratamiento de los síntomas génito-urinarios. En caso de atrofia del tracto génito-urinario bajo, estriol induce la normalización del epitelio urogenital y ayuda a restaurar la microflora normal y el pH fisiológico de la vagina. En consecuencia, ayuda a prevenir las infecciones del epitelio urogenital.
Información de los ensayos clínicos:
• El alivio de los síntomas menopáusicos se produjo durante las primeras semanas de tratamiento.
• Raramente se ha citado sangrado vaginal tras el tratamiento con Ovestinon.
5.2 Propiedades farmacocinéticas
La administración vaginal de estriol asegura una disponibilidad óptima en el lugar de acción. Estriol también se absorbe a la circulación general, y esto se demuestra por el incremento de los niveles plasmáticos de estriol no conjugado.
Los niveles plasmáticos máximos se alcanzan en 1-2 horas después de la aplicación. Tras la aplicación vaginal de 0,5 mg de estriol la Cmax es de aproximadamente 100 pg/ml, la Cmin es aproximadamente de 25 pg/ml y la Cpromedi0 es de aproximadamente 70 pg/ml. Después de 3 semanas de administración diaria de 0,5 mg de estriol vaginal, la Cpromedio disminuye a 40 pg/ml.
Casi todo el estriol (90%) se fija a la albúmina plasmática y a diferencia de otros estrógenos, apenas se une a la globulina transportadora de hormonas sexuales (SHBG). El metabolismo de estriol consiste principalmente en conjugación y desconjugación durante la circulación enterohepática. El estriol, ya que es un producto metabólico final, se excreta principalmente por la orina en su forma conjugada. Únicamente una pequeña parte (± 2%) se excreta por las heces, principalmente como estriol no conjugado.
5.3 Datos preclínicos sobre seguridad
Dado que estriol es una hormona natural presente de forma continuada en el organismo femenino durante los años fértiles, no se realizó un desarrollo toxicológico de este principio activo.
6 . DATOS FARMACÉUTICOS 6.1 Lista de excipientes
octildodecanol cera de ésteres cetílicos glicerol (E-422) alcohol cetílico alcohol estearílico polisorbato 60 estearato de sorbitán
ácido láctico
dihidrocloruro de clorhexidina hidróxido de sodio agua purificada
6.2 Incompatibilidades
No aplicable.
6.3 Periodo de validez
3 años.
6.4 Precauciones especiales de conservación
No conservar a temperatura superior a 25° C.
No congelar.
6.5 Naturaleza y contenido del envase
Tubos de aluminio con barniz interior y tapón de rosca de polietileno, envasados en cajas de cartón. Cada caja contiene un tubo con 15 g de crema y un aplicador. El aplicador plástico es un cuerpo de estireno acrilonitrilo y un émbolo de polietileno.
6.6 Precauciones especiales de eliminación y otras manipulaciones
Ninguna especial.
La eliminación del medicamento no utilizado y de todos los materiales que hayan estado en contacto con él, se realizará de acuerdo con la normativa local.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
ASPEN PHARMA TRADING LTD 3016 Lake Drive, Citywest Campus 24- Dublin Irlanda
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
61533
9. FECHA DE LA PRIMERA AUTORIZACIÓN/ RENOVACIÓN DE LA AUTORIZACIÓN
22 de diciembre de 1998
10. FECHA DE LA REVISIÓN DEL TEXTO
Julio 2013
12 de 12