Methergin 0,2 Mg/Ml Solucion Inyectable
FICHA TÉCNICA
1. NOMBRE DEL MEDICAMENTO
Methergín 0,2 mg/ml solución inyectable
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada mililitro de solución inyectable contiene 0,20 mg de metilergometrina (en forma de maleato).
Para consultar la lista completa de excipientes, ver sección 6.1
3. FORMA FARMACÉUTICA
Solución inyectable.
Solución transparente e incolora.
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
Methergín inyectable está indicado en mujeres adultas en el tratamiento de:
- Atonía y hemorragias del alumbramiento y del posparto.
- Alumbramiento dirigido, maniobra de Credé.
- Hemorragias uterinas en el curso de cesáreas.
- Subinvolución uterina, loquiómetra.
- Hemorragias tardías del parto.
- Hemorragias del aborto, abortos iniciados e incompletos.
- Legrados.
4.2 Posología y forma de administración
4.2.1 Posología
Alumbramiento dirigido
La inyección intramuscular (i.m.) es la vía recomendada de administración. Cuando se administra intravenosamente (i.v.) la dosis debe administrarse lentamente durante un periodo no inferior a 60 segundos (ver sección 4.4.).
La dosis recomendada de Methergín es 1 ml (0,2 mg) i.m ó 0,5 a 1 ml (0,1 a 0,2 mg) por administración i.v. lenta cuando aparece el hombro anterior, o como máximo inmediatamente después de la salida del niño.
En algún caso puede ser conveniente ayudar manualmente a la expulsión de la placenta.
En caso de parto bajo anestesia, la dosis recomendada es de 1 ml (0,2 mg) por inyección i.v. lenta.
Atonía uterina
La inyección intramuscular (i.m.) es la vía recomendada de administración. Cuando se administra por vía intravenosa (i.v.) la dosis debe administrarse lentamente durante un periodo de no inferior a 60 segundos (ver sección 4.4.).
La dosis recomendada de Methergin es 1 ml (0,2 mg) i.m. o de 0,5 a 1 ml (0,1 a 0,2 mg) i.v. lenta. La dosis puede repetirse cada 2 a 4 horas si es necesario, hasta cinco dosis en 24 horas.
Cesárea
ml (0,1 a 0,2 mg) i.v. o intramural. mg) i.m. o s.c. hasta tres veces al día y
Después de la extracción del niño 1 ml (0,2 mg) i.m. o de 0,5 a 1
Hemorragia puerperal, subinvolución uterina, loquiómetra La dosis recomendada de Methergín es 0,5 a 1 ml (0,1 a 0,2 normalmente durante 5 días.
Poblaciones especiales
Insuficiencia renal y hepática Se ha de tener precaución en presencia de trastornos de la función hepática y renal (ver sección 4.4.).
4.2.2 Forma de administración
Para consultar las instrucciones de administración del medicamento, ver secciones 4.4. y 6.6.
4.3 Contraindicaciones
• Embarazo, inercia uterina primaria o secundaria
• Periodos de dilatación y expulsión, hasta que aparezca el hombro anterior (Methergín no debe emplearse para la inducción o activación del parto)
• Hipertensión severa
• Pre-eclampsia y eclampsia
• Vasculopatías oclusivas (incluido el angor pectoris)
• Sepsis
• Hipersensibilidad conocida a metilergometrina, a los alcaloides del cornezuelo o a alguno de los excipientes incluidos en la sección 6.1.
4.4 Advertencias y precauciones especiales de empleo
Recomendaciones generales de administración
En la presentación de nalgas y otras presentaciones anormales Methergín no deberá administrarse hasta después del nacimiento del niño, en los partos múltiples se deberá esperar hasta el nacimiento del último niño.
El alumbramiento dirigido requiere supervisión obstétrica.
La inyección intramuscular es la vía de administración recomendada. Las inyecciones intravenosas deberán administrarse lentamente durante un periodo no inferior a 60 segundos. Deberá evitarse la inyección intra-o peri-arterial.
Errores de medicación
Se han notificado administraciones accidentales en recién nacidos.
En estos casos de sobredosis en neonatos los síntomas de sobredosis notificados han sido depresión respiratoria, convulsiones, cianosis y oliguria. Además, se ha notificado encefalopatía en los neonatos con signos y síntomas como irritabilidad, agitación y letargia.
El tratamiento debe ser sintomático: en los casos graves se requirieron medidas de soporte respiratorio y cardiovascular. Se han notificados casos mortales en ausencia de un tratamiento adecuado (ver sección 4.9).
Hipertensión y trastornos de la función renal y hepática
Se deberá administrar con precaución en casos de hipertensión leve o moderada o si existe alteración de la función hepática o renal.
Enfermedad coronaria arterial
Las pacientes con enfermedad coronaria arterial o con factores de riesgo de enfermedad coronaria arterial (ej. fumar, obesidad, diabetes, colesterol alto) pueden ser más susceptibles a desarrollar isquemia o infarto de miocardio debido a los vasoespasmos inducidos por metilergometrina (ver sección 4.8.).
4.5 Interacción con otros medicamentos y otras formas de interacción
Interacciones por el uso concomitante, no recomendado
Inhibidores de CYP3A4
Debe evitarse el uso concomitante de Methergín con inhibidores potentes de CYP3A como antibióticos macrólidos (ej. troleandomicina, eritromicina, claritromicina) inhibidores HIV -proteasa o inhibidores de la transcriptasa inversa (ej. ritonavir, indinavir, nelfinavir, delavirdina) o antifúngicos azólicos (ej. itraconazol, voriconazol), ya que puede producirse una mayor exposicióna metilergometrina y un aumento de toxicidad al cornezuelo (vasoespasmo e isquemia en las extremidades y en otros tejidos).
Bromocriptina
El uso concomitante de la bromocriptina y Methergín en el puerperio no está recomendado ya que metilergometrina puede aumentar el efecto vasoconstrictor de otros alcaloides del cornezuelo.
Prostaglandinas
Las prostaglandinas (sulprostona, dinoprostona, misoprostol) facilita la contracción del miometrio, por tanto Methergín puede potenciar la acción uterina de las prostaglandinas y viceversa. No se recomienda el uso concomitante con estos tres medicamentos.
Interacciones a tener en cuenta
Inhibidores débiles a moderados de CYP3A4
Ha de tenerse precaución cuando se utilice Methergín con inhibidores menos potentes de CYP3A dado que puede producirse una mayor exposición a metilergometrina (cimetidina, delavirdina, zumo de pomelo, quinupristina, dalfopristina)
Vasoconstrictores, triptanes, simpaticomiméticos y otros alcaloides del cornezuelo
Ha de tenerse precaución cuando Methergín es utilizado concomitantemente con otros vasoconstrictores u otros alcaloides del cornezuelo. La metilergometrina puede potenciar los efectos vasoconstrictores/vasopresores de otros fármacos, como triptanes (agonistas del receptor 5HT1B/1D), los simpaticomiméticos, (incluyendo los anestésicos locales), tabaco, alcaloides del cornezuelo o ergotamina
Betabloqueantes
Se ha de tener precaución en el uso concomitante de Methergín con betabloqueantes. La administración concomitante con betabloqueantes puede aumentar la acción vasoconstrictora de los alcaloides del cornezuelo
Inductores de CYP3A4
Medicamentos inductores de CYP3A4 (nevirapina, rifampicina) son fuertes inductores de CYP3A4 podrían disminuir la acción farmacológica de Methergín.
Trinitrato de glicerilo y otros medicamentos antianginosos
Metilergometrina provoca vasoconstricción y puede reducirel efecto del trinitrato de glicerilo y otros medicamentosantianginosos.
Anestésicos
Anestésicos como el halotano y metoxiflurano pueden reducir la potencia oxitocítica del Methergín (ver sección 4.2.).
Sin interacción
No se han detectado interacciones con la administración concomitante de Methergín con oxitocina. Para la prevención y tratamiento de la hemorragia uterina mediante inyección i.m. puede ser conveniente la combinación de estos dos uterotónicos, ya que la oxitocina tiene un corto periodo de latencia, mientras que Methergín posee una prolongada duración de acción.
4.6 Fertilidad, embarazo y lactancia
4.6.1 Embarazo
El uso de Methergín en el embarazo está contraindicado por su potente acción uterotónica.
4.6.2 Lactancia
Methergín puede reducir la secreción de leche materna y ser excretado en la leche (ver sección 5.1 y 5.2). Durante el tratamiento continuo, el fármaco también se excreta por la leche.. Se han detectado casos aislados de intoxicación en lactantes cuyas madres habían recibido el fármaco durante varios días. Se observó uno o más de los siguientes síntomas (que desaparecieron con la eliminación de la medicación): elevación de la presión arterial, bradicardia o taquicardia, vómitos, diarrea, agitación y convulsiones.
Dados los posibles efectos sobre el niño y la reducción de la secreción de leche provocada por Methergín, no se recomienda su uso durante la lactancia. Las mujeres no deben dar el pecho mientras estén en tratamiento con Methergín al menos que haya transcurrido 12 horas desde la última administración. La leche producida durante este periodo ha de desecharse (ver sección 4.4).
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
La metilergometrina puede producir vértigos y convulsiones. Por tanto debe tenerse precaución al conducir vehículos o utilizar maquinaria, especialmente al inicio del tratamiento.
4.8 Reacciones adversas
La vía intravenosa tiene una mayor incidencia de aparición de efectos adversos, y afectan principalmente a la contracción de la musculatura lisa uterina, gastrointestinal, vascular y bronquial.
Las reacciones adversas (Tabla 1) se clasifican de acuerdo a la base de datos de clasificación de órganos del sistema MedDRA. Las reacciones adversas se ordenan por frecuencias de la siguiente forma: muy frecuentes l > 1/10; frecuentes > 1/100 a < 1/10 ; poco frecuentes > 1/1.000 a < 1/100; raras > 1/10.000 a < 1/1.000; muy raras < 1/10.000. Dentro de cada frecuencia, se ordena por gravedad.
Trastornos del sistema inmunológico Muy raras:
reacciones anafilácticas
Trastornos del sistema nervioso Frecuentes:
Poco frecuentes:
Muy raras:
cefaleas
mareos, convulsión alucinaciones
Trastornos del oído y del laberinto Muy raras:
tinitus
Trastornos cardiacos
Poco frecuentes: Raras:
Muy raras:
dolor de pecho
bradicardia; taquicardia; palpitaciones infarto de miocardio, arterioespasmo coronario
Trastornos vasculares Frecuentes:
Poco frecuentes: Raras:
Muy raras:
hipertensión
hipotensión
vasoconstricción, vasoespasmo,
arteriales
tromboflebitis
espasmos
Trastornos respiratorios, torácicos y mediastínicos
Muy raras: congestión nasal
Trastornos gastrointestinales Poco frecuentes:
Muy raras:
vómitos, náuseas diarrea
Trastornos de la piel y del tejido subcutáneo Frecuentes:
Poco frecuentes:
erupciones cutáneas aumento de la sudoración
Trastornos musculoesqueléticos y del tejido conjuntivo
Muy raras: espasmos musculares
Embarazo, puerperio y enfermedades perinatales Frecuentes:
dolor abdominal (causado por contracciones uterinas)
Las siguientes reacciones adversas provienen de la información post-comercialización con Methergín de los informes de casos espontáneos y de casos descritos en la bibliografía. Debido a que estas reacciones
son informadas de forma voluntaria de una población de tamaño desconocido, no es posible estimar la frecuencia por lo que se categorizan como frecuencia no conocida. Las reacciones adversas se listan de acuerdo a la base de datos de clasificación de órganos del sistema MedDRA. Dentro de cada grupo, las reacciones adversas se ordenan por gravedad decreciente.
Trastornos del sistema nervioso Accidente cerebrovascular, parestesias
Trastornos cardiacos
Fibrilación ventricular, taquicardia ventricular, angina de pecho, bloqueo atrioventricular
Notificación de sospechas de reacciones adversas
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del Sistema Español de Farmacovigilancia de medicamentos de Uso Humano: https://www.notificaram.es.
4.9 Sobredosis
Síntomas
Una intoxicación por sobredosificación con el preparado produciría: Náuseas, vómitos, hipertensión o hipotensión, adormecimiento, hormigueo y dolor en las extremidades, depresión respiratoria, convulsiones, coma.
Tratamiento
Tratamiento sintomático bajo estrecha monitorización del sistema respiratorio y cardiovascular.
Si se requiere sedación, debe utilizarse una benzodiazepina.
En caso de arterioespasmo severo, deben administrarse vasodilatadores, por ej. nitroprusiato sódico o dihidralazina. En constricción coronaria debe administrarse un tratamiento antianginoso apropiado (p. ej. nitratos).
4.9.1 Población pediátrica
Se han notificado administraciones accidentales en recién nacidos.
En estos casos de sobredosis en neonatos los síntomas de sobredosis notificados han sido depresión respiratoria, convulsiones, cianosis y oliguria. Además, se ha notificado encefalopatía en los neonatos con signos y síntomas como irritabilidad, agitación y letargia.
El tratamiento debe ser sintomático: en los casos graves se requirieron medidas de soporte respiratorio y cardiovascular. Se han notificado casos mortales en ausencia de un tratamiento adecuado (ver sección 4.4).
5. PROPIEDADES FARMACOLÓGICAS
Código ATC
Grupo farmacoterapéutico: oxitocíticos (Código ATC: G02A B01)
5.1 Propiedades farmacodinámicas
5.1.1 Mecanismo de acción
La metilergometrina, derivado semisintético del alcaloide natural ergometrina, es un potente y específico agente uterotónico. Actúa directamente sobre la musculatura lisa del útero e incrementa el tono basal, la frecuencia y la amplitud de las contracciones rítmicas. En comparación con otros alcaloides de la ergotamina, sus efectos en el sistema cardiovascular y sistema nervioso central son menos pronunciados.
5.1.2 Efectos farmacodinámicos
El elevado y selectivo efecto oxitocítico de la metilergometrina es el resultado de su comportamiento específico como agonista parcial y antagonista de los receptores serotoninérgicos, dopaminérgicos y a-adrenérgicos. Sin embargo, esto no evita totalmente las complicaciones vasoconstrictoras (ver sección 4.8.).
5.2 Propiedades farmacocinéticas
El inicio de acción de Methergín 0,2 mg/ml solución inyectable tiene lugar de 30 a 60 segundos después de su administración i.v. y de 2 a 5 minutos después de su administración i.m. y tiene una duración de 4 a 6 horas.
5.2.1 Absorción
Para una inyección i.m. de 0,2 mg la Cmax fue 5.918 ± 1.952 picogramos/mL y tmax 0,41 ± 0,21 horas. La biodisponibilidad oral fue equivalente a la de la solución i.m. administrada oralmente y proporcional a la dosis siguiendo una administración de 0,1, 0,2 y 0,4 mg. Después de una inyección i.m., la extensión de la absorción fue un 25 % superior que en la administración oral.
5.2.2 Distribución
Tras la inyección intravenosa, la metilergometrina es rápidamente distribuida de plasma a tejido periférico en aproximadamente 2 ó 3 minutos.
En mujeres voluntarias sanas el volumen de distribución es de 56,1 + 17,0 litros. Se desconoce si el fármaco atraviesa la barrera hematoencefálica.
5.2.3 Metabolismo o Biotransformación
La metilergometrina se metaboliza principalmente en el hígado. En el hombre no se ha estudiado la ruta metabólica. Los estudios in vitro muestran la N-desmetilación y la hidroxilación del anillo fenilo.
5.2.4 Eliminación
En voluntarias sanas el aclaramiento plasmático es de 14,4 + 4,5 litros por hora y la semivida de eliminación 3,29 + 1,31 horas tras la administración oral. Un estudio en voluntarias sanas demostró que solo aproximadamente un 3 % de la dosis oral se eliminaba como fármaco inalterado en la orina. El medicamento se elimina principalmente con la bilis en las heces. La metilergometrina también se excreta por la leche. Tras una hora de la administración oral única de 250 microgramos de metilergometrina, se halló un porcentaje leche-plasma de 0,18±0,03. La vida media de la metilergometrina registrada en leche es de 2,3 ± 0,3 h.
5.2.5 Linealidad/ No linealidad
La biodisponibilidad oral fue proporcional a la dosis siguiendo una administración de 0,1, 0,2 y 0,4 mg. Estudios de biodisponibilidad/bioequivalencia
La biodisponibilidad oral fue equivalente a la solución i.m. administrada oralmente.
5.3 Datos preclínicos sobre seguridad
El potencial genotóxico de la metilergometrina no se ha determinado. No existen estudios que evalúen el potencial carcinogénico de la metilergometrina. No se han realizado con metilergometirina estudios en animales estándares de fertilidad y de estudios de toxicidad en la reproducción.
6 . DATOS FARMACÉUTICOS
6.1 Lista de excipientes
Methergín 0,2 mg/ml solución inyectable: ácido maleico, cloruro de sodio y agua para preparaciones inyectables.
6.2 Incompatibilidades
Ninguna conocida.
6.3 Periodo de validez
3 años.
6.4 Precauciones especiales de conservación
Proteger de la luz. Conservar en nevera (entre 2 y 8°C). No congelar.
Las ampollas pueden almacenarse durante 14 días sin nevera pero no por encima de 25 °C
6.5 Naturaleza y contenido del envase
Ampollas de vidrio transparente.
6.6 Precauciones especiales de eliminación Instrucciones de uso/manipulación
Administrar únicamente si la solución es transparente e incolora.
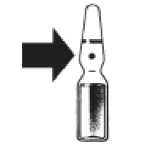
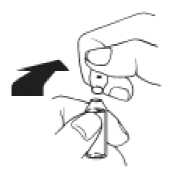

Ampolla rompible. Línea de ruptura por debajo del punto coloreado.
Colocar el pulgar por encima del punto coloreado y romper la ampolla presionando hacia atrás.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Mizar Farmacéutica, S.L.
Gran Via de les Corts Catalanes, 764 08013 - Barcelona (España)
MINISTER10DE )E
SAN IDAD, POLITICA LITIGA
SOCIAL E IGUALDAD IALDAD
Agencia esparto» de cSacse-
medicamentos y ¡y
Sfoouctos san-tanos taws
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
MINISTER10DE )E SANIDAD, POLITICA LITIGA SOCIAL E IGUALDAD IALDAD Agencia esparto» de cSacse-medicamentos y ¡y Sfoouctos san-tanos taws
25.658
9. FECHA DE LA PRIMERA AUTORIZACIÓN/ RENOVACIÓN DE LA AUTORIZACIÓN
Fecha de la primera autorización: 22/marzo/1956 Fecha de la última renovación: 30/abril/2008
10. FECHA DE LA REVISIÓN DEL TEXTO
Junio 2015
9 de 9