Duotrav 40 Microgramos/Ml + 5 Mg/Ml Colirio En Solucion
ANEXO I
FICHA TÉCNICA O RESUMEN DE LAS CARACTERÍSTICAS DEL PRODUCTO
1. NOMBRE DEL MEDICAMENTO
DuoTrav 40 microgramos/ml + 5 mg/ml colirio en solución.
2. COMPOSICIÓN CUALITATIVA Y CUANTITATIVA
Cada ml de solución contiene 40 microgramos de travoprost y 5 mg de timolol (como maleato de timolol).
Excipiente(s) con efecto conocido:
Cada ml de solución contiene polyquaternium-1 (POLYQUAD) 10 microgramos, propilenglicol 5 mg, aceite de ricino hidrogenado y polioxietilenado 40 1 mg (ver sección 4.4).
Para consultar la lista completa de excipientes, ver sección 6.1.
3. FORMA FARMACÉUTICA
Colirio en solución (colirio).
Solución incolora y transparente.
4. DATOS CLÍNICOS
4.1 Indicaciones terapéuticas
DuoTrav está indicado en adultos para la reducción de la presión intraocular (PIO) en pacientes con glaucoma de ángulo abierto o hipertensión ocular que responden de forma insuficiente a los betabloqueantes o análogos de prostaglandinas oftálmicos (ver sección 5.1).
4.2 Posología y forma de administración
Posología
Uso en adultos, incluidos pacientes de edad avanzada
La dosis es de una gota de DuoTrav en el saco conjuntival del ojo(s) afectado(s) una vez al día por la mañana o por la noche. Debe administrarse cada día a la misma hora.
Si se olvida una dosis, debe continuarse el tratamiento con la siguiente dosis, tal como estaba planificado. La dosis no debe sobrepasar de una gota diaria en el ojo(s) afectado(s).
Poblaciones especiales Insuficiencia hepática y renal
No se han realizado estudios con DuoTrav ni con timolol 5 mg/ml colirio en pacientes con insuficiencia hepática o renal.
Travoprost se ha estudiado en pacientes con insuficiencia hepática de leve a grave y en pacientes con insuficiencia renal de leve a grave (aclaramiento de creatinina de tan sólo 14 ml/min). No fue necesario un ajuste de la dosis en estos pacientes.
Es poco probable que pacientes con insuficiencia hepática o renal requieran un ajuste de la dosis con DuoTrav (ver sección 5.2).
Población pediátrica
No se ha establecido la seguridad y eficacia de DuoTrav en niños y adolescentes menores de 18 años. No hay datos disponibles.
Forma de administración Vía oftálmica.
El paciente debe retirar el envoltorio protector inmediatamente antes de la primera utilización. Para evitar una posible contaminación de la punta del cuentagotas y de la solución, debe tenerse la precaución de no tocar los párpados, áreas circundantes ni otras superficies con la punta del frasco.
La absorción sistémica se reduce cuando se ocluye el conducto nasolagrimal o se cierran los ojos durante 2 minutos. Esto puede producir una disminución de las reacciones adversas sistémicas y un aumento de la actividad local (ver sección 4.4).
Si se emplea más de un fármaco por vía oftálmica, las aplicaciones deben espaciarse al menos 5 minutos (ver sección 4.5).
Cuando DuoTrav vaya a sustituir a otro medicamento antiglaucomatoso oftálmico, se debe interrumpir la administración de ese otro medicamento e iniciar la administración de DuoTrav al día siguiente.
Debe instruirse a los pacientes para que se retiren las lentes de contacto blandas antes de la aplicación de DuoTrav y esperen 15 minutos después de la instilación de la dosis antes de colocarse las lentes de contacto (ver sección 4.4).
4.3 Contraindicaciones
Hipersensibilidad a los principios activos o a alguno de los excipientes incluidos en la sección 6.1. Hipersensibilidad a otros betabloqueantes.
Enfermedad reactiva de las vías respiratorias incluyendo asma bronquial o historial de asma bronquial, enfermedad pulmonar obstructiva crónica grave.
Bradicardia sinusal, síndrome del seno enfermo, incluyendo bloqueo sinoauricular, bloqueo auriculoventricular de segundo o tercer grado no controlado por marcapasos. Insuficiencia cardiaca evidente, shock cardiogénico.
Rinitis alérgica grave y distrofias corneales.
4.4 Advertencias y precauciones especiales de empleo
Efectos sistémicos
Al igual que otros fármacos oftálmicos de aplicación tópica, travoprost y timolol se absorben sistémicamente. Debido al componente beta adrenérgico, timolol, se pueden producir el mismo tipo de reacciones adversas cardiovasculares, pulmonares y de otro tipo que se observan con los medicamentos betabloqueantes adrenérgicos sistémicos. La incidencia de RAMs sistémicas después de administración oftálmica es inferior a la de administración sistémica. Para reducir la absorción sistémica, ver sección 4.2.
Trastornos cardíacos
En pacientes con enfermedades cardiovasculares (p.ej. cardiopatía coronaria, angina Prinzmetal e insuficiencia cardiaca) e hipotensión, se debe valorar críticamente el tratamiento con betabloqueantes y se debe considerar un tratamiento con otros principios activos. En pacientes con enfermedades cardiovasculares se deben vigilar los signos de deterioro de estas enfermedades y de reacciones adversas.
Debido a su efecto negativo sobre el tiempo de conducción, los betabloqueantes solo deben administrarse con precaución en pacientes con bloqueo cardiaco de primer grado.
Trastornos vasculares
Se deben tratar con precaución los pacientes con trastornos/alteraciones circulatorias periféricas graves (p.ej. formas graves de la enfermedad de Raynaud o síndrome de Raynaud).
Trastornos respiratorios
En pacientes asmáticos se han notificado reacciones respiratorias, incluyendo muerte debida a broncoespasmo, después de la administración de algún betabloqueante oftálmico.
DuoTrav se debe utilizar con precaución en pacientes con enfermedad pulmonar obstructiva crónica (EPOC) leve o moderada y únicamente si el beneficio potencial supera al riesgo potencial.
Hipoglucemia/diabetes
Los betabloqueantes se deben administrar con precaución en pacientes propensos a hipoglucemia espontánea o en pacientes con diabetes lábil, ya que los betabloqueantes pueden enmascarar los signos y síntomas de hipoglucemia aguda.
Debilidad muscular
Se ha notificado que los medicamentos betabloqueantes adrenérgicos potencian la debilidad muscular consistente en determinados síntomas miasténicos (p.ej. diplopía, ptosis y debilidad generalizada).
Enfermedades corneales
Los betabloqueantes oftálmicos pueden producir sequedad de los ojos. Los pacientes con trastornos corneales se deben tratar con precaución.
Desprendimiento coroidal
Se ha notificado desprendimiento coroidal con administración de terapia supresiva acuosa (p.ej. timolol, acetazolamida) tras procedimientos de filtración.
Otros fármacos betabloqueadores
Cuando se administra timolol a pacientes que ya están recibiendo un medicamento betabloqueante sistémico, se puede potenciar el efecto sobre la presión intraocular o los efectos sistémicos conocidos de betabloqueo. Se debe controlar estrechamente la respuesta de estos pacientes. No se recomienda el uso de dos fármacos bloqueantes beta-adrenérgicos tópicos (ver sección 4.5).
Anestesia quirúrgica
Las preparaciones oftálmicas de betabloqueantes pueden bloquear los efectos beta-agonistas sistémicos, p.ej. los de la adrenalina. Se debe informar al anestesista si el paciente está utilizando timolol.
Hipertiroidismo
Los betabloqueantes también pueden enmascarar los signos de hipertiroidismo.
Contacto con la piel
Las prostaglandinas y los análogos a las prostaglandinas son sustancias biológicamente activas que pueden absorberse a través de la piel. Las mujeres embarazadas o que estén tratando de quedarse embarazadas deben tomar las precauciones adecuadas para evitar el contacto directo con el contenido del frasco. En el caso improbable de contacto con una cantidad importante del contenido del frasco, límpiese de inmediato y minuciosamente la zona expuesta.
Reacciones anafilácticas
Los pacientes con historial de atopia o reacción anafiláctica grave a diversos alergenos, durante el tratamiento con betabloqueantes, pueden ser más reactivos a exposiciones repetidas con estos alergenos y no responder a la dosis habitual de adrenalina que se emplea para tratar las reacciones anafilácticas.
Tratamiento concomitante
Timolol puede interaccionar con otros medicamentos (ver sección 4.5).
No se recomienda la administración local de dos prostaglandinas.
Efectos oculares
Travoprost puede modificar gradualmente el color del ojo al aumentar el número de melanosomas (gránulos de pigmento) de los melanocitos. Antes de instaurar el tratamiento debe informarse a los pacientes de la posibilidad de un cambio permanente en el color de los ojos. El tratamiento unilateral puede dar lugar a una heterocromía permanente. Actualmente se desconocen los efectos a largo plazo sobre los melanocitos y sus consecuencias. El cambio de color del iris se produce lentamente y puede no ser apreciable durante meses o años. Esta alteración en el color del ojo se ha observado predominantemente en pacientes con iris de coloración mixta, es decir, marrón azulada, marrón grisácea, marrón amarillenta y marrón verdosa; no obstante, también se ha observado en pacientes con ojos marrones. Generalmente la pigmentación marrón alrededor de la pupila se extiende concéntricamente hacia la periferia de los ojos afectados, aunque todo o parte del iris puede volverse de un tono más marrón. No se ha observado incremento del pigmento marrón del iris tras interrumpir el tratamiento.
En ensayos clínicos controlados se ha notificado que la utilización de travoprost está relacionada con la aparición de oscurecimiento de la piel periorbital y/o del párpado.
Se ha observado con análogos de prostaglandinas cambios periorbitales y en el párpado incluyendo profundización del surco del párpado.
Travoprost puede alterar gradualmente las pestañas del ojo(s) tratado(s); estos cambios se observaron aproximadamente en la mitad de los pacientes de los ensayos clínicos y consisten en: aumento de la longitud, grosor, pigmentación y/o número de pestañas. Actualmente se desconoce el mecanismo de los cambios en las pestañas y sus consecuencias a largo plazo.
Se ha observado que travoprost provoca un ligero aumento de la fisura palpebral en estudios con monos. No obstante, este efecto no se observó durante los estudios clínicos y se considera que es específico de la especie.
No se tiene experiencia con DuoTrav en afecciones oculares inflamatorias, ni en glaucoma congénito, de ángulo estrecho, de ángulo cerrado, o neovascular y sólo se dispone de experiencia limitada en enfermedad ocular tiroidea, en glaucoma de ángulo abierto de pacientes pseudofáquicos y en glaucoma pigmentario o pseudoexfoliativo.
Se ha notificado edema macular durante el tratamiento con análogos de la prostaglandina F2a.
Se recomienda precaución cuando se utiliza DuoTrav en pacientes afáquicos, pacientes pseudofáquicos con cápsula posterior del cristalino desgarrada o con lente intraocular implantada en la cámara anterior, o en pacientes con factores conocidos de riesgo de edema macular quístico.
DuoTrav puede utilizarse, con precaución en pacientes con factores de riesgo conocidos que predispongan a iritis/uveítis y en pacientes con una inflamación intraocular activa.
Excipientes
DuoTrav contiene propilenglicol que puede producir irritación de la piel.
DuoTrav contiene aceite de ricino hidrogenado y polioxietilenado 40 el cual puede causar reacciones cutáneas.
Debe instruirse a los pacientes para que se retiren las lentes de contacto antes de la aplicación de DuoTrav y esperen 15 minutos después de la instilación de la dosis antes de colocarse las lentes de contacto (ver sección 4.2).
4.5 Interacción con otros medicamentos y otras formas de interacción
No se han realizado estudios fármaco específicos de interacciones con travoprost o timolol.
Cuando se administra una solución oftálmica betabloqueante concomitantemente con bloqueantes orales de los canales de calcio, fármacos bloqueantes beta-adrenérgicos, antiarrítmicos (incluyendo amiodarona), glucósidos digitálicos, parasimpaticomiméticos, guanetidina existe un potencial de efectos aditivos que provoca hipotensión y/o marcada bradicardia.
El empleo de betabloqueantes puede potenciar la reacción hipertensiva por retirada súbita de clonidina.
Se ha notificado la potenciación del betabloqueo sistémico (ej. disminución de frecuencia cardíaca, depresión) durante el tratamiento combinado con inhibidores CYP2D6 (ej. quinidina, fluoxetina, paroxetina) y timolol.
Se ha notificado ocasionalmente midriasis producida por el uso concomitante de betabloqueantes oftálmicos y adrenalina (epinefrina).
Los betabloqueantes pueden incrementar el efecto hipoglucémico de los antidiabéticos. Los betabloqueantes pueden enmascarar los signos y síntomas de hipoglucemia (ver sección 4.4).
4.6 Fertilidad, embarazo y lactancia
Mujeres en edad fértil/anticoncepción
DuoTrav no debe utilizarse en mujeres que pueden quedarse embarazadas a no ser que se adopten medidas anticonceptivas adecuadas (ver sección 5.3).
Embarazo
Travoprost tiene efectos farmacológicos dañinos en el embarazo y/o el feto/recién nacido.
No hay datos o éstos son limitados relativos al uso de DuoTrav o de cada uno de los componentes en mujeres embarazadas. No debe utilizarse timolol durante el embarazo a no ser que sea realmente necesario.
Estudios epidemiológicos no revelaron efectos de malformación, aunque muestran un riesgo de retraso en el crecimiento intrauterino cuando se administran betabloqueantes por vía oral. Además, se han observado en neonatos signos y síntomas de betabloqueo (p.ej. bradicardia, hipotensión, dificultad respiratoria e hipoglucemia) cuando se han administrado betabloqueantes hasta el parto. Se debe monitorizar rigurosamente al neonato durante los primeros días de vida, si se administra DuoTrav hasta el parto.
No debe utilizarse DuoTrav durante el embarazo a no ser que sea realmente necesario. Para reducir la absorción sistémica, ver sección 4.2.
Lactancia
Se desconoce si travoprost procedente del colirio es excretado en la leche materna humana. Los estudios en animales muestran excreción de travoprost y metabolitos en la leche materna. Timolol se excreta en la leche materna teniendo el potencial de causar reacciones adversas graves en el niño lactante. Sin embargo, a las dosis terapéuticas de timolol colirio no es probable que se pueda presentar una cantidad suficiente en la leche materna que pueda causar síntomas clínicos de betabloqueo en niños lactantes. Para reducir la absorción sistémica, ver sección 4.2.
No se recomienda el empleo de DuoTrav en mujeres en período de lactancia.
Fertilidad
No existen datos en relación a los efectos de DuoTrav sobre la fertilidad humana. Estudios en animales no mostraron efectos de travoprost ni timolol sobre la fertilidad con dosis más de 250 veces superiores a la dosis oftálmica máxima recomendada para humanos.
4.7 Efectos sobre la capacidad para conducir y utilizar máquinas
La influencia de DuoTrav sobre la capacidad para conducir y utilizar máquinas es nula o insignificante.
Como con cualquier colirio, la visión borrosa transitoria y otras alteraciones visuales pueden ocurrir. Si aparece visión borrosa durante la instilación, el paciente debe esperar hasta que la visión sea nítida antes de conducir o utilizar máquinas.
4.8 Reacciones adversas
Resumen del perfil de seguridad
En ensayos clínicos que incluyeron 2170 pacientes tratados con DuoTrav, la reacción adversa notificada con más frecuencia relacionada con el tratamiento fue hiperemia ocular (12,0%).
Resumen tabulado de reacciones adversas
En la siguiente tabla se enumeran las reacciones adversas que se observaron en los ensayos clínicos o durante la experiencia postcomercialización. Se distribuyen según la clasificación de órganos y sistemas y se clasifican según el siguiente criterio: muy frecuentes (>1/10), frecuentes (>1/100 a <1/10), poco frecuentes (>1/1.000 a < 1/100), raras (>1/10.000 a < 1/1.000), muy raras (<1/10.000), o frecuencia no conocida (no puede estimarse a partir de los datos disponibles). Las reacciones adversas se enumeran en orden decreciente de gravedad dentro de cada grupo de frecuencia.
|
Clasificación de órganos del sistema |
Frecuencia |
Reacciones adversas |
|
Trastornos del sistema inmunológico |
Poco frecuentes |
hipersensibilidad. |
|
Trastornos psiquiátricos |
Raras |
nerviosismo. |
|
No conocida |
depresión. | |
|
Trastornos del sistema nervioso |
Poco frecuentes |
mareo, cefalea. |
|
No conocida |
accidente cerebrovascular, sincope, parestesia. | |
|
Trastornos oculares |
Muy frecuentes |
hiperemia ocular. |
|
Frecuentes |
queratitis punteada, dolor ocular, alteración visual, visión borrosa, ojo seco, prurito ocular, molestia ocular, irritación ocular. | |
|
Poco frecuentes |
queratitis, iritis, conjuntivitis, inflamación en la cámara anterior, blefaritis, fotofobia, agudeza visual disminuida, astenopia, hinchazón ocular, aumento del lagrimeo, eritema del párpado, crecimiento de pestañas, alergia ocular, edema conjuntival, edema del párpado. | |
|
Raras |
erosión corneal, meibomitis, hemorragia conjuntival, costra en margen de párpado, triquiasis, distiquiasis. | |
|
No conocida |
edema macular, ptosis palpebral, alteración corneal. |
|
Trastornos cardiacos |
Poco frecuentes Raras No conocida |
bradicardia. arritmia, frecuencia cardiaca irregular. insuficiencia cardiaca, taquicardia, dolor torácico, palpitaciones. |
|
Trastornos vasculares |
Poco frecuentes |
hipertensión, hipotensión. |
|
No conocida |
edema periférico. | |
|
Trastornos respiratorios, torácicos y mediastínicos |
Poco frecuentes Raras |
disnea, goteo postnasal. disfonía, broncoespasmo, tos, irritación de garganta, dolor orofaríngeo, molestia nasal. |
|
No conocida |
asma. | |
|
Trastornos gastrointestinales |
No conocida |
disgeusia. |
|
Trastornos hepatobiliares |
Raras |
aumento de la alanina aminotransferasa, aumento del aspartato aminotransferasa. |
|
Trastornos de la piel y tejido subcutáneo |
Poco frecuentes Raras |
dermatitis de contacto, hipertricosis. urticaria, cambio de color de la piel, alopecia, hiperpigmentación de la piel (periocular). |
|
No conocida |
rash. | |
|
Trastornos musculoesqueléticos y del tejido conjuntivo |
Raras |
dolor en las extremidades. |
|
Trastornos renales y urinarios |
Raras |
cromaturia. |
|
Trastornos generales y alteraciones en el lugar de administración |
Raras |
sed, fatiga. |
Las siguientes reacciones adversas adicionales que se han observado con uno de los principios activos y que podrían tener lugar con DuoTrav son:
Travoprost
|
Clasificación de órganos del sistema |
Término preferido MedDRA |
|
Trastornos oculares |
uveítis, trastorno conjuntival, folículos conjuntivales, hiperpigmentación del iris. |
|
Trastornos de la piel y el tejido subcutáneo |
exfoliación de la piel. |
Timolol
Al igual que otros medicamentos oftálmicos aplicados por vía tópica, timolol se absorbe en la circulación sistémica. Esto puede causar reacciones adversas similares a las observadas con fármacos betabloqueantes sistémicos. El listado de reacciones adversas incluye las reacciones observadas dentro de la clase de betabloqueantes oftálmicos. La incidencia de RAMs sistémicas después de administración oftálmica es inferior a la de administración sistémica. Para reducir la absorción sistémica, ver sección 4.2.
|
Clasificación de órganos del sistema |
Término preferido MedDRA |
|
Trastornos del sistema inmunológico |
Reacciones alérgicas sistémicas incluyendo angioedema, urticaria, erupción generalizada y localizada, prurito, anafilaxia. |
|
Trastornos del metabolismo y de la nutrición |
Hipoglucemia. |
|
Trastornos psiquiátricos |
Insomnio, pesadillas, pérdida de memoria. |
|
Trastornos del sistema nervioso |
Isquemia cerebral, incremento de los signos y síntomas de miastenia gravis. |
|
Trastornos oculares |
Signos y síntomas de irritación ocular (p.ej. quemazón, punzada, picor, lagrimeo, enrojecimiento), desprendimiento coroidal después de cirugía de filtración (ver sección 4.4 Advertencias y precauciones especiales de empleo), sensibilidad corneal disminuida, diplopía. |
|
Trastornos cardiacos |
Dolor torácico, palpitaciones, edema, insuficiencia cardiaca congestiva, bloqueo auriculoventricular, parada cardiaca. |
|
Trastornos vasculares |
Fenómeno de Raynaud, frío en pies y manos. |
|
Trastornos respiratorios, torácicos y mediastínicos |
Broncoespasmo (predominantemente en pacientes con enfermedad broncoespástica preexistente). |
|
Trastornos gastrointestinales |
Disgeusia, náuseas, dispepsia, diarrea, boca seca, dolor abdominal, vómitos. |
|
Trastornos de la piel y del tejido subcutáneo |
Rash psoriasiforme o exacerbación de psoriasis. |
|
Trastornos musculoesqueléticos y del tejido conjuntivo |
Mialgia. |
|
Trastornos del aparato reproductor y de la mama |
Disfunción sexual, libido disminuida. |
|
Trastornos generales y alteraciones en el lugar de administración |
Astenia. |
Notificación de sospechas de reacciones adversas
Es importante notificar sospechas de reacciones adversas al medicamento tras su autorización. Ello permite una supervisión continuada de la relación beneficio/riesgo del medicamento. Se invita a los profesionales sanitarios a notificar las sospechas de reacciones adversas a través del sistema nacional de notificación incluido en el Anexo V.
4.9 Sobredosis
No es probable que se produzca una sobredosis oftálmica con DuoTrav ni que se asocie con toxicidad
En caso de ingestión accidental, los síntomas de sobredosis por betabloqueantes sistémicos pueden incluir bradicardia, hipotensión, broncoespasmo e insuficiencia cardíaca.
Si se produce una sobredosis con DuoTrav, el tratamiento debe ser sintomático y de mantenimiento. Timolol no se dializa fácilmente.
PROPIEDADES FARMACOLÓGICAS
5.
5.1 Propiedades farmacodinámicas
Grupo farmacoterapéutico: Oftalmológicos; Preparados antiglaucoma y mióticos, Código ATC: S01ED51.
Mecanismo de acción
DuoTrav contiene dos sustancias activas: travoprost y maleato de timolol. Estos dos componentes disminuyen la presión intraocular mediante mecanismos de acción complementarios y la combinación de sus efectos produce una reducción adicional de la PIO en comparación con cada uno de los componentes por separado.
Travoprost, un análogo de la prostaglandina F2a, es un agonista completo muy selectivo. Posee una elevada afinidad por el receptor PF de prostaglandinas y reduce la presión intraocular aumentando el drenaje del humor acuoso a través de las vías malla trabecular y uveoscleral. La reducción de la PIO en humanos se inicia aproximadamente 2 horas tras la administración y el efecto máximo se alcanza después de 12 horas. La reducción significativa de la presión intraocular puede mantenerse con una dosis única durante períodos superiores a 24 horas.
Timolol es un fármaco bloqueante adrenérgico no selectivo que carece de actividad simpaticomimética intrínseca, actividad depresora directa del miocardio o actividad estabilizadora de membrana. Los estudios en humanos con tonografía y fluorofotometría sugieren que su acción predominante se relaciona con reducción de la formación de humor acuoso y con un leve incremento del flujo de salida.
Farmacología secundaria
Travoprost aumentó significativamente el flujo sanguíneo de la papila óptica en conejos tras 7 días de administración oftálmica (1,4 microgramos, una vez al día).
Efectos farmacodinámicos
Efectos clínicos
En un ensayo clínico controlado de 12 meses, en pacientes con glaucoma de ángulo abierto o hipertensión ocular y PIO basal media de 25 a 27 mmHg, el efecto medio de disminución de la PIO de DuoTrav administrado una vez al día por la mañana, fue de 8 a 10 mmHg. La no inferioridad de DuoTrav frente a latanoprost 50 microgramos/ml + timolol 5 mg/ml respecto a la reducción media de la PIO se demostró en todas las visitas a través de todos los controles a distintos tiempos.
En un ensayo clínico controlado, de 3 meses, en pacientes con glaucoma de ángulo abierto o hipertensión ocular y PIO basal media de 27 a 30 mmHg, el efecto medio de disminución de la PIO de DuoTrav administrado una vez al día por la mañana fue de 9 a 12 mmHg y fue hasta 2 mmHg superior al de travoprost 40 microgramos/ml administrado una vez al día por la noche y de 2 a 3 mmHg superior al de timolol 5 mg/ml administrado dos veces al día. Se observó una reducción estadísticamente superior en la PIO media de la mañana (8AM-24 horas después de la última dosis de DuoTrav) en comparación con travoprost en todas las visitas a lo largo del ensayo.
En dos ensayos clínicos controlados, de tres meses, en pacientes con glaucoma de ángulo abierto o hipertensión ocular y PIO basal media de 23 a 26 mmHg, el efecto medio de disminución de la PIO de DuoTrav administrado una vez al día por la mañana fue de 7 a 9 mmHg. Las reducciones de la PIO media fueron no inferiores, aunque numéricamente más bajas, que las alcanzadas con el tratamiento concomitante con travoprost 40 microgramos/ml administrado una vez al día por la noche y timolol 5 mg/ml administrado una vez al día por la mañana.
En un ensayo clínico controlado, de 6 semanas, en pacientes con glaucoma de ángulo abierto o hipertensión ocular y PIO basal media de 24 a 26 mmHg, el efecto medio de disminución de la PIO de
DuoTrav (conservante-polyquatemium-1) administrado una vez al día por la mañana fue de 8 mmHg, equivalente a la de DuoTrav (conservante-cloruro de benzalconio).
En estos ensayos los criterios de inclusión fueron comunes a excepción del criterio de la PIO basal y de la respuesta al tratamiento previo de la PIO. En el desarrollo clínico de DuoTrav se incluyeron pacientes no tratados previamente y pacientes en tratamiento. La respuesta insuficiente a la monoterapia no fue un criterio de inclusión.
Los datos existentes sugieren que la administración por la noche podría tener algunas ventajas en la reducción de la PIO media. Cuando se recomienda la administración por la mañana en vez de por la noche, se debería considerar la comodidad del paciente y la probabilidad de cumplimiento del tratamiento.
5.2 Propiedades farmacocinéticas
Absorción
Travoprost y timolol se absorben a través de la córnea. Travoprost es un profármaco en forma de éster que se hidroliza rápidamente a ácido libre activo en la córnea. Después de administrar DuoTrav PQ una vez al día en sujetos sanos (N=22) durante 5 días, travoprost ácido libre no fue cuantificable en muestras de plasma de la mayoría de los sujetos (94,4%) y generalmente no fue detectable una hora después de la administración. Las concentraciones oscilaron desde 0,01 a 0,03 ng/ml cuando pudieron valorarse (límite de cuantificación del método > 0,01 ng/ml). Tras la administración de DuoTrav una vez al día, el estado estacionario medio de timolol Cmáx fue de 1,34ng/ml y la Tmáx fue aproximadamente de 0,69 horas.
Distribución
Después de la administración oftálmica de DuoTrav, travoprost ácido libre puede determinarse en el humor acuoso de animales durante las primeras horas y en el plasma humano únicamente durante la primera hora. Timolol puede determinarse en el humor acuoso humano después de la administración oftálmica de timolol y en el plasma durante hasta 12 horas después de la administración oftálmica de DuoTrav.
Biotransformación
La metabolización es la principal vía de eliminación de travoprost y del ácido libre activo. Las vías sistémicas de metabolización son paralelas a las de la prostaglandina endógena F2a las cuales se caracterizan por la reducción del doble enlace 13-14, oxidación del 15-hidroxilo y lisis p-oxidativa de la parte superior de la cadena.
Timolol se metaboliza por dos vías. Una ruta produce una cadena lateral de etanolamina en el anillo de tiadiazol y la otra forma una cadena lateral etanólica en el nitrógeno morfolínico y una segunda cadena lateral similar con un grupo carbonilo adyacente al nitrógeno. La tJ/2 plasmática de timolol después de la administración oftálmica de DuoTrav es de 4 horas.
Eliminación
Travoprost ácido libre y sus metabolitos se excretan principalmente por vía renal. Menos del 2% de una dosis oftálmica de travoprost se recuperó en orina como ácido libre. Timolol y sus metabolitos se excretan mayoritariamente por vía renal. Aproximadamente el 20% de una dosis de timolol se excreta inalterado en la orina y el resto se excreta, también en orina, en forma de metabolitos.
5.3 Datos preclínicos sobre seguridad
En monos, la administración de DuoTrav dos veces al día mostró inducir un aumento de la fisura palpebral y aumentar la pigmentación del iris de forma similar a la observada con la administración oftálmica de prostanoides.
En cultivos de células corneales humanas y tras administración oftálmica en conejos, DuoTrav conservado con polyquaternium-1 produjo mínima toxicidad en la superficie ocular, en comparación con el colirio conservado con cloruro de benzalconio.
Travoprost
La administración ocular oftálmica de travoprost en monos a concentraciones de hasta 0,012% en el ojo derecho, dos veces al día durante un año, no provocó toxicidad sistémica.
Se han realizado estudios de toxicidad de reproducción con travoprost por vía sistémica en ratas, ratones y conejos. Los hallazgos de embrioletalidad temprana, pérdida tras implantación y fetotoxicidad se relacionan con la actividad agonista del receptor PF del útero. En ratas gestantes, la administración sistémica de travoprost a dosis de más de 200 veces la dosis clínica durante el período de organogénesis dio lugar a un aumento en la incidencia de malformaciones. Se detectaron niveles bajos de radioactividad en el líquido amniótico y en los tejidos fetales de ratas gestantes a las que se administró 3H-travoprost. Los estudios de reproducción y desarrollo han mostrado un potente efecto sobre la pérdida fetal, con un elevado índice en ratas y ratones (180 pg/ml y 30 pg/ml plamáticos, respectivamente) a exposiciones de 1,2 a 6 veces la exposición clínica (hasta 25 pg/ml).
Timolol
Datos preclínicos basados en estudios convencionales de seguridad farmacológica, toxicidad a dosis múltiple, genotoxicidad y potencial carcinogénico, revelaron que timolol no presenta especial riesgo en humanos. Estudios de toxicidad sobre la reproducción con timolol mostraron osificación fetal retardada en ratas sin efectos adversos en el desarrollo posnatal (7.000 veces la dosis clínica) y un incremento de resorción fetal en conejos (14.000 veces la dosis clínica).
6. DATOS FARMACÉUTICOS
6.1 Lista de excipientes
Polyquaternium-1.
Manitol (E421).
Propilenglicol (E1520).
Aceite de ricino hidrogenado y polioxietilenado 40 (HCO-40).
Ácido bórico.
Cloruro de sodio.
Hidróxido de sodio y/o ácido clorhídrico (para ajustar el pH).
Agua purificada.
6.2 Incompatibilidades
No procede.
6.3 Período de validez
2 años
Desechar 4 semanas después de la primera apertura del envase.
6.4 Precauciones especiales de conservación No conservar a temperatura superior a 30°C.
6.5 Naturaleza y contenido del recipiente
Frasco oval de 2,5 ml de Polipropileno (PP) o Polietileno de Baja Densidad (LDPE) y gotero dispensador de PP o LDPE con tapón de rosca de PP, presentado en un envoltorio.
Envases de 1, 3 o 6 frascos.
Puede que solamente estén comercializados algunos tamaños de envases.
6.6 Precauciones especiales de eliminación
Ninguna especial.
7. TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Alcon Laboratories (UK) Ltd.
Frimley Business Park Frimley Camberley Surrey GU16 7SR Reino Unido.
8. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
EU/1/06/338/001 -6
9. FECHA DE LA PRIMERA AUTORIZACIÓN/RENOVACIÓN DE LA AUTORIZACIÓN
Fecha de autorización: 24/04/06 Fecha de la última revalidación: 07/10/10
10. FECHA DE LA REVISIÓN DEL TEXTO
La información detallada de este medicamento está disponible en la página Web de la Agencia Europea de Medicamentos http://www.ema.europa.eu
A. FABRICANTE(S) RESPONSABLE(S) DE LA LIBERACIÓN DE LOS LOTES
B. CONDICIONES O RESTRICCIONES DE SUMINISTRO Y USO
C. OTRAS CONDICIONES Y REQUISITOS DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
D. CONDICIONES O RESTRICCIONES EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO
A. FABRICANTE(S) RESPONSABLE(S) DE LA LIBERACIÓN DE LOS LOTES
Nombre y dirección de los fabricantes responsables de la liberación de los lotes
S.A. Alcon Couvreur N.V.,
Rijksweg 14,
B-2870,
Puurs,
Bélgica
or
Alcon Cusí, S.A.,
Camil Fabra 58,
08320 El Masnou,
Barcelona,
España
El prospecto impreso del medicamento debe especificar el nombre y dirección del fabricante responsable de la liberación del lote en cuestión.
B. CONDICIONES O RESTRICCIONES DE SUMINISTRO Y USO
Medicamento sujeto a prescripción médica.
C. OTRAS CONDICIONES Y REQUISITOS DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
• Informes periódicos de seguridad
El Titular de la Autorización de Comercialización presentará los informes periódicos de seguridad para este medicamento de conformidad con las exigencias establecidas en la lista de fechas de referencia de la Unión (lista EURD) prevista en el artículo 107ter, párrafo 7 de la Directiva 2001/83/CE y publicada en el portal web europeo sobre medicamentos.
D. CONDICIONES O RESTRICCIONES EN RELACIÓN CON LA UTILIZACIÓN SEGURA Y EFICAZ DEL MEDICAMENTO
• Plan de Gestión de Riesgos (PGR)
El TAC realizará las actividades e intervenciones de farmacovigilancia necesarias según lo acordado en la versión del PGR incluido en el Módulo 1.8.2 de la Autorización de Comercialización y en cualquier actualización del PGR que se acuerde posteriormente.
Se debe presentar un PGR actualizado:
• A petición de la Agencia Europea de Medicamentos.
• Cuando se modifique el sistema de gestión de riesgos, especialmente como resultado de nueva información disponible que pueda conllevar cambios relevantes en el perfil beneficio/riesgo, o como resultado de la consecución de un hito importante (farmacovigilancia o minimización de riesgos).
Si coincide la presentación de un IPS con la actualización del PGR, ambos documentos se pueden presentar conjuntamente.
INFORMACIÓN QUE DEBE FIGURAR EN EL EMBALAJE EXTERIOR
CAJA PARA UN FRASCO DE 2,5 ml + CAJA PARA 3 FRASCOS DE 2,5 ml + CAJA PARA
6 FRASCOS DE 2,5 ml
1. NOMBRE DEL MEDICAMENTO
DuoTrav 40 microgramos/ml + 5 mg/ml colirio en solución. travoprost/timolol.
2. PRINCIPIO(S) ACTIVO(S)
Cada ml de solución contiene 40 microgramos de travoprost y 5 mg de timolol (como maleato de timolol)
3. LISTA DE EXCIPIENTES
Contiene:Polyquaternium-1, manitol (E421), propilenglicol (E1520), aceite de ricino hidrogenado y polioxietilenado 40 (HCO-40), ácido bórico, cloruro de sodio, hidróxido de sodio y/o ácido clorhídrico (para ajustar pH), agua purificada.
Para mayor información consultar el prospecto.
4. FORMA FARMACÉUTICA Y CONTENIDO DEL ENVASE
Colirio en solución 1 x 2,5 ml.
3 x 2,5 ml.
6 x 2,5 ml.
5. FORMA Y VÍA(S) DE ADMINISTRACIÓN
Vía oftálmica.
Leer el prospecto antes de utilizar este medicamento.
6. ADVERTENCIA ESPECIAL DE QUE EL MEDICAMENTO DEBE MANTENERSE FUERA DE LA VISTA Y DEL ALCANCE DE LOS NIÑOS
Mantener fuera de la vista y del alcance de los niños.
7. OTRA(S) ADVERTENCIA(S) ESPECIAL(ES), SI ES NECESARIO
8. FECHA DE CADUCIDAD
CAD.
Desechar 4 semanas después de la primera apertura del envase. Fecha de apertura.
9. CONDICIONES ESPECIALES DE CONSERVACIÓN
No conservar a temperatura superior a 30°C
10. PRECAUCIONES ESPECIALES DE ELIMINACIÓN DEL MEDICAMENTO NO UTILIZADO Y DE LOS MATERIALES DERIVADOS DE SU USO (CUANDO CORRESPONDA)
11. NOMBRE Y DIRECCIÓN DEL TITULAR DE LA AUTORIZACIÓN DE COMERCIALIZACIÓN
Alcon Laboratories (UK) Ltd.,
Frimley Business Park
Frimley
Camberley
Surrey GU16 7SR
Reino Unido.
12. NÚMERO(S) DE AUTORIZACIÓN DE COMERCIALIZACIÓN
- Frasco de PP Frasco de PP Frasco de PP
- Frasco de LDPE
- Frasco de LDPE
- Frasco de LDPE
EU/1/06/338/001 1 x 2,5 ml EU/1/06/338/002 3 x 2,5 ml EU/1/06/338/003 6 x 2,5 ml EU/1/06/338/004 1 x 2,5 ml EU/1/06/338/005 3 x 2,5 ml EU/1/06/338/006 6 x 2,5 ml
13. NÚMERO DE LOTE
Lote.
14. CONDICIONES GENERALES DE DISPENSACIÓN
Medicamento sujeto a prescripción médica.
15. INSTRUCCIONES DE USO
16 INFORMACIÓN EN BRAILLE
duotrav
INFORMACIÓN MÍNIMA QUE DEBE INCLUIRSE EN PEQUEÑOS ACONDICIONAMIENTOS PRIMARIOS ETIQUETA DEL FRASCO
1. NOMBRE DEL MEDICAMENTO Y VÍA(S) DE ADMINISTRACIÓN
DuoTrav 40 microgramos/ml + 5 mg/ml colirio. travoprost/timolol.
Vía oftálmica.
2. FORMA DE ADMINISTRACIÓN
Leer el prospecto antes de utilizar este medicamento. <Abrir aquí>
3. FECHA DE CADUCIDAD
CAD.
Desechar 4 semanas después de la primera apertura. Fecha de apertura.
4. NÚMERO DE LOTE
Lote.
5. CONTENIDO EN PESO, EN VOLUMEN O EN UNIDADES
2,5 ml.
6. OTROS
INFORMACIÓN MÍNIMA QUE DEBE INCLUIRSE EN PEQUEÑOS ACONDICIONAMIENTOS PRIMARIOS
BOLSA ENVOLTORIO
1. NOMBRE DEL MEDICAMENTO Y VÍA(S) DE ADMINISTRACIÓN
DuoTrav 40 microgramos/ml + 5 mg/ml colirio. travoprost/timolol.
2. FORMA DE ADMINISTRACIÓN
Leer el prospecto antes de utilizar este medicamento.
3. FECHA DE CADUCIDAD
CAD.
Desechar 4 semanas después de la primera apertura.
4. NÚMERO DE LOTE
Lote.
5. CONTENIDO EN PESO, EN VOLUMEN O EN UNIDADES
2,5 ml.
6. OTROS
DuoTrav 40 microgramos/ml + 5 mg/ml colirio en solución
travoprost/timolol
Lea todo el prospecto detenidamente antes de empezar a usar este medicamento.
- Conserve este prospecto, ya que puede tener que volver a leerlo.
- Si tiene alguna duda, consulte a su médico o farmacéutico.
- Este medicamento se le ha recetado solamente a usted, y no debe dárselo a otras personas aunque tengan los mismos síntomas que usted, ya que puede perjudicarles.
- Si experimenta efectos adversos, consulte a su médico o farmacéutico, incluso si se trata de efectos adversos que no aparecen en este prospecto. Ver sección 4.
Contenido del prospecto:
1. Qué es DuoTrav y para qué se utiliza
2. Qué necesita saber antes de empezar a usar DuoTrav
3. Cómo usar DuoT rav
4. Posibles efectos adversos
5. Conservación de DuoTrav
6. Contenido del envase e información adicional
1. Qué es DuoTrav y para qué se utiliza
DuoTrav colirio en solución es una asociación de dos sustancias activas (travoprost y timolol). Travoprost es un análogo de las prostaglandinas que actúa aumentando el flujo de salida del líquido del ojo, y por lo tanto disminuye la presión en el ojo. Timolol es un betabloqueante que actúa reduciendo la formación de fluido en el interior del ojo. Las dos sustancias actúan juntas para reducir la presión en el interior del ojo.
DuoTrav colirio se utiliza para tratar la presión elevada de los ojos en adultos, incluidos pacientes de edad avanzada. Esta presión puede dar lugar a una enfermedad llamada glaucoma.
2. Qué necesita saber antes de empezar a usar DuoTrav
No use DuoTrav colirio en solución
• si es alérgico a travoprost, prostaglandinas, timolol, betabloqueantes o a cualquiera de los demás componentes.
• si actualmente padece o ha padecido en el pasado problemas respiratorios como asma, bronquitis obstructiva crónica grave (afección del pulmón grave que puede causar sibilancias, dificultad para respirar y/o tos persistente) u otros tipos de problemas respiratorios.
• si padece fiebre del heno grave.
• si padece un ritmo cardiaco lento, insuficiencia cardiaca o trastornos del ritmo cardiaco (latidos irregulares del corazón).
• si la superficie de su ojo está nublada.
Consulte a su médico si se encuentra en alguna de estas situaciones.
Advertencias y precauciones
Antes de empezar a utilizar este medicamento informe a su médico si actualmente padece o ha
padecido en el pasado
• enfermedad cardiaca coronaria (los síntomas pueden incluir opresión o dolor en el pecho, falta de aliento o ahogo), insuficiencia cardiaca, tensión arterial baja,
• alteraciones del ritmo cardiaco tales como latido lento del corazón.
• problemas respiratorios, asma o enfermedad pulmonar obstructiva crónica
• enfermedad debida a mala circulación sanguínea (tales como enfermedad de Raynaud o síndrome de Raynaud)
• diabetes ya que timolol puede enmascarar los signos y síntomas de azúcar bajo en sangre
• hiperactividad de la glándula del tiroides ya que timolol puede enmascarar los signos y síntomas de enfermedad del tiroides
• Si está a punto de someterse a una operación, informe a su médico que está utilizando DuoTrav ya que timolol puede cambiar los efectos de algunos medicamentos que se utilizan durante la anestesia.
• Si tiene miastenia gravis (debilidad muscular crónica).
• Si sufre cualquier reacción alérgica grave (erupción en la piel, enrojecimiento y picor en el ojo) mientras utiliza DuoTrav, cualquiera que sea la causa, el tratamiento con adrenalina puede no ser tan efectivo. Por lo tanto, cuando reciba cualquier otro tratamiento, comunique al médico que está utilizando DuoTrav.
• Si ha padecido operación de cataratas, consulte a su médico antes de empezar a utilizar DuoTrav.
• Si sufre o ha sufrido anteriormente una inflamación del ojo, consulte a su médico antes de empezar a utilizar DuoTrav.
• DuoTrav puede cambiar el color de su iris (la parte coloreada de su ojo). Este cambio puede ser permanente.
• DuoTrav puede aumentar la longitud, grosor, color y/o número de sus pestañas y puede causar crecimiento inusual de vello en sus párpados.
• Travoprost puede absorberse a través de la piel; por ello las mujeres embarazadas o que estén intentando quedarse embarazadas no deben utilizarlo. En caso de contacto del medicamento con la piel, debe eliminarse lavando inmediatamente.
Niños
DuoTrav no debe utilizarse en niños y adolescentes menores de 18 años de edad.
Uso de DuoTrav con otros medicamentos
DuoTrav puede afectar o puede ser afectado por otros medicamentos que usted esté utilizando, incluyendo otros colirios para el tratamiento del glaucoma. Consulte a su médico si está utilizando o piensa utilizar medicamentos para disminuir la tensión arterial, medicamentos para el corazón incluyendo quinidina (utilizado para tratar afecciones del corazón y algunos tipos de malaria), medicamentos para tratar la diabetes o antidepresivos conocidos como fluoxetina y paroxetina.
Informe a su médico o farmacéutico si está utilizando o ha utilizado recientemente otros medicamentos, incluso los adquiridos sin receta.
Embarazo, lactancia y fertilidad
No utilice DuoTrav si está embarazada a menos que su médico lo considere necesario. Si usted puede quedarse embarazada debe utilizar un método anticonceptivo adecuado mientras esté utilizando el medicamento.
No utilice DuoTrav si amamanta a un bebé. DuoTrav puede pasar a la leche materna.
Consulte a su médico antes de utilizar cualquier medicamento durante la lactancia.
Conducción y uso de máquinas
Inmediatamente después de la aplicación de DuoTrav puede notar que su visión se vuelve borrosa. No conduzca ni utilice máquinas hasta que hayan desaparecido estos efectos.
DuoTrav contiene aceite de ricino hidrogenado y polioxietilenado y propilenglicol que pueden causar reacciones en la piel e irritación.
3. Cómo usar DuoTrav
Siga exactamente las instrucciones de administración de este medicamento indicadas por su médico. En caso de duda, consulte de nuevo a su médico o farmacéutico.
La dosis recomendada es
Una gota en el ojo u ojo(s) afectado(s), una vez al día- por la mañana o por la noche. Úselo a la misma hora cada día.
Sólo debe aplicarse DuoTrav en los dos ojos si su médico así se lo ha recomendado. Siga el tratamiento durante todo el período de tiempo indicado por su médico.
DuoTrav sólo debe utilizarse como gotas para los ojos.
1
2
3

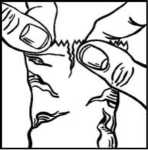
• Inmediatamente antes de utilizar un frasco por primera vez, abra la bolsa envoltorio, saque el frasco (Figura 1) y anote la fecha de apertura en el espacio reservado de la etiqueta.
• Coja el frasco de DuoTrav y sitúese ante un espejo.
• Lávese las manos.
• Desenrosque el tapón.
• Sostenga el frasco, boca abajo, entre los dedos.
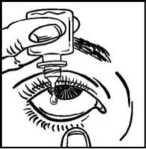
• Incline la cabeza hacia atrás. Separe suavemente el párpado del ojo con un dedo, hasta que se forme una bolsa, en la que deberá caer la gota (Figura 2).
• Acerque la punta del frasco al ojo. Puede serle útil el espejo.
• No toque el ojo, el párpado, zonas próximas ni otras superficies con el cuentagotas, porque las
gotas podrían infectarse.
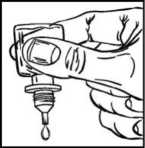
• Apriete suavemente el frasco para que caiga una gota de DuoTrav cada vez (Figura 3).
• Después de utilizar DuoTrav, presione con el dedo el borde del ojo, junto a la nariz durante 2
minutos (Figura 4). Esto ayuda a evitar que DuoTrav pase al resto del cuerpo.
• Si se aplica gotas en ambos ojos, repita los puntos anteriores para el otro ojo.
• Enrosque bien el tapón en el frasco inmediatamente después de utilizar el producto.
• Utilice un solo frasco a la vez. No abra la bolsa hasta que necesite utilizar el frasco.
Para más información ver cara posterior.
Cantidad a utilizar
Ver cara anterior del prospecto
Si una gota cae fuera del ojo, inténtelo de nuevo.
Si usa más DuoTrav del que debe, puede eliminarlo lavando los ojos con agua templada. No se aplique más gotas hasta que vuelva a tocarle.
Si olvidó usar DuoTrav, continúe con la siguiente dosis que estaba prevista. No se aplique una dosis doble para compensar la dosis olvidada. La dosis no debería sobrepasar de 1 gota al día en el ojo(s) afectado(s).
Si deja de usar DuoTrav sin consultar con su médico, la presión en su ojo no estará controlada lo que le podría provocar pérdida de visión.
Si está utilizando otro colirio, espere por lo menos 5 minutos entre la aplicación de DuoTrav y de las otras gotas.
Si lleva lentes de contacto blandas no se aplique las gotas mientras las lleve puestas. Después de aplicar las gotas, espere 15 minutos antes de volver a colocarse las lentes.
Si tiene cualquier otra duda sobre el uso de este medicamento, pregunte a su médico o farmacéutico.
4. Posibles efectos adversos
Al igual que todos los medicamentos, este medicamento puede producir efectos adversos, aunque no todas las personas los sufran.
A menos que los efectos sean graves, siga normalmente con el tratamiento. Si estos efectos le preocupan, consulte a su médico o farmacéutico. No deje de aplicarse DuoTrav sin consultar a su médico.
Efectos adversos muy frecuentes
(pueden afectar más de 1 de cada 10 personas)
Efectos en el ojo enrojecimiento del ojo
Efectos adversos frecuentes
(pueden afectar hasta 1 de cada 10 personas)
Efectos en el ojo
inflamación con daño en la superficie del ojo, dolor ocular, visión borrosa, visión anormal, ojo seco, picor ocular, molestia ocular, signos y síntomas de irritación en el ojo (p.ej. quemazón, punzada).
Efectos adversos poco frecuentes
(pueden afectar hasta 1 de cada 100 personas)
Efectos en el ojo
inflamación de la superficie del ojo, inflamación del párpado, hinchazón de la conjuntiva, aumento del crecimiento de las pestañas, inflamación del iris, inflamación del ojo, sensibilidad a la luz, disminución de la visión, vista cansada, alergia ocular, hinchazón en el ojo, aumento de la producción de lágrimas, enrojecimiento del párpado, cambio de color del párpado.
Otros efectos
alergia al medicamento, mareo, dolor de cabeza, aumento o disminución de la presión sanguínea, falta de aliento, crecimiento excesivo del vello, goteo en la parte posterior de la garganta, inflamación y picor en la piel, frecuencia cardiaca disminuida.
Efectos adversos raros
(pueden afectar hasta 1 de cada 1000 personas)
Efectos en el ojo
adelgazamiento de la superficie del ojo, inflamación de las glándulas del párpado, vaso sanguíneo roto en el ojo, costras en el párpado, crecimiento y posicionamiento anormal de las pestañas.
Otros efectos
nerviosismo, frecuencia cardiaca irregular, pérdida del pelo, trastornos en la voz, dificultad para respirar, tos, irritación de garganta, urticaria, valores anormales en las pruebas en sangre del riñón, decoloración de la piel, oscurecimiento de la piel, sed, cansancio, sensación extraña dentro de la nariz, orina coloreada, dolor en manos y pies.
Frecuencia no conocida
(no puede estimarse a partir de los datos disponibles)
Efectos en el ojo
párpado caído (provocando que el ojo quede medio cerrado).
Otros efectos
erupción en la piel, insuficiencia cardiaca, dolor de pecho, embolia cerebral, desvanecimiento, depresión, asma, incremento ritmo cardíaco, sensación de hormigueo o entumecimiento, palpitaciones, inflamación en los miembros inferiores, mal sabor.
Adicionalmente:
DuoTrav es una asociación de 2 sustancias activas. Al igual que otros medicamentos administrados en los ojos, travoprost y timolol (un betabloqueante) se absorben en sangre. Esto puede causar efectos adversos similares a los observados con medicamentos betabloqueantes intravenosos y/o orales. La incidencia de efectos adversos después de administración oftálmica es inferior a los medicamentos que por ejemplo, se administran por la boca o inyectados. Los efectos adversos listados incluyen reacciones observadas dentro de la clase de los betabloqueantes cuando se utilizan para tratar afecciones del ojo, son los siguientes:
Efectos en el ojo: inflamación del párpado, inflamación de la córnea, desprendimiento de la capa de debajo de la retina que contiene los vasos sanguíneos los cuales pueden causar alteraciones de la visión después de operación de filtración, sensibilidad de la cornea disminuida, erosión de la córnea (daño de la capa anterior del globo ocular), visión doble, cambios en el color del iris.
Otros efectos:
Corazón y circulación: frecuencia cardiaca lenta, palpitaciones, edema (acumulación de líquido), cambios en el ritmo o la frecuencia de los latidos del corazón, insuficiencia cardiaca congestiva (enfermedad del corazón con dificultad para respirar e hinchazón de los pies y piernas debido a la acumulación de líquido), tipo de trastorno del ritmo cardiaco, ataque al corazón, disminución de la tensión arterial, fenómeno de Raynaud, frío en pies y manos, reducción del riego sanguíneo al cerebro.
Respiratorio: Constricción de las vías respiratorias en los pulmones (predominantemente en pacientes con enfermedad preexistente), dificultad para respirar, nariz taponada.
Sistema nervioso y trastornos generales: dificultad para dormir (insomnio), pesadillas, pérdida de memoria, pérdida de fuerza y energía.
Gástrico: alteración del gusto, náuseas, indigestión, diarrea, boca seca, dolor abdominal, vómitos.
Alergia: reacciones alérgicas generalizadas incluyendo hinchazón debajo de la piel que puede ocurrir en zonas tales como la cara y extremidades y puede obstruir las vías respiratorias pudiendo causar dificultades para tragar o respirar, urticaria, erupción localizada y generalizada, picor, reacción alérgica repentina y grave que pone en riesgo la vida.
Piel: erupción con aspecto blanco plateado (rash psoriasiforme) o empeoramiento de psoriasis, descamación de la piel.
Muscular: incremento de los signos y síntomas de miastenia gravis (trastorno muscular), sensaciones inusuales como hormigueo, debilidad muscular/cansancio, dolor muscular no causado por ejercicio.
Reproducción: disfunción sexual, deseo sexual disminuido.
Metabolismo: niveles bajos de azúcar en sangre.
Comunicación de efectos adversos
Si experimenta cualquier tipo de efecto adverso, consulte a su médico o farmacéutico, incluso si se trata de posibles efectos adversos que no aparecen en este prospecto. También puede comunicarlos directamente a través del sistema nacional de notificación incluido en el Anexo V. Mediante la comunicación de efectos adversos usted puede contribuir a proporcionar más información sobre la seguridad de este medicamento.
5. Conservación de DuoTrav
Mantener el producto fuera de la vista y del alcance de los niños.
No utilice DuoTrav colirio en solución después de la fecha de caducidad que aparece en el frasco y en el embalaje exterior después de “CAD”. La fecha de caducidad es el último día del mes que se indica.
No conservar a temperatura superior a 30°C.
Para evitar infecciones, debe desechar el frasco 4 semanas después de haberlo abierto por primera vez y utilizar un frasco nuevo. Anote la fecha de apertura en los espacios reservados de la etiqueta de cada frasco y caja.
Los medicamentos no se deben tirar por los desagües ni a la basura. Pregunte a su farmacéutico cómo deshacerse de los envases y de los medicamentos que no necesita. De esta forma ayudará a proteger el medio ambiente.
6. Contenido del envase e información adicional Composición de DuoTrav
Los principios activos son Travoprost y timolol. Cada ml de solución contiene 40 microgramos de travoprost y 5 mg de timolol (como maleato de timolol).
Los demás componentes son Polyquaternium-1, manitol (E421), propilenglicol (E1520), aceite de ricino hidrogenado y polioxietilenado 40, ácido bórico, cloruro de sodio, hidróxido de sodio o ácido clorhídrico (para ajustar el pH) y agua purificada.
Se añaden cantidades muy pequeñas de hidróxido de sodio o ácido clorhídrico para mantener los niveles de acidez (niveles de pH) normales.
Aspecto del producto y contenido del envase
DuoTrav es un líquido (una solución incolora y transparente) que se presenta en un frasco de plástico de 2,5 ml con un tapón de rosca.
Cada frasco se encuentra dentro de una bolsa.
Envases de 1, 3 o 6 frascos.
Es posible que no se comercialicen todas las presentaciones.
|
Titular de la autorización |
Fabricante |
Fabricante |
|
de comercialización | ||
|
Alcon Laboratories (UK) Ltd. |
S.A. Alcon-Couvreur N.V. |
Alcon Cusí, S.A., |
|
Frimley Business Park |
Rijksweg 14, |
Camil Fabra 58, |
|
Frimley |
B-2870 Puurs, |
08320 El Masnou, |
|
Camberley Surrey GU16 7SR Reino Unido. |
Bélgica. |
España. |
Puede solicitar más información respecto a este medicamento dirigiéndose al representante local del titular de la autorización de comercialización.
|
Belgie/Belgique/Belgien Luxembourg/Luxemburg Alcon NV @ + 32 (0)2 754 32 10 (Belgie/Belgique/Belgien) |
Latvija Alcon Pharmaceuticals Ltd ® + 371 67 321 121 |
|
E'Mrapna Ahkoh Etnrapna EOOfl ® + 359 2 950 15 65 |
Lietuva Alcon Pharmaceuticals Ltd atstovybé ® + 370 5 2 314 756 |
|
Ceská republika Alcon Pharmaceuticals (Czech Republic) s.r.o. ® + 420 225 775 111 |
Magyarország Alcon Hungária Gyógyszerkereskedelmi Kft ® + 36-1-463-9080 |
|
Danmark Alcon Nordic A/S ® + 45 3636 4300 |
Nederland Alcon Nederland BV ® + 31 (0) 183 654321 |
|
Deutschland Alcon Pharma GmbH ® + 49 (0)761 1304-0 |
Norge Alcon Nordic A/S ® + 45 3636 4300 |
|
ETAáSa/KÚTCpog A^kov Aagnopáxopig EXkác, AEBE ® + 30 210 68 78 300 (EMá5a) |
Osterreich Alcon Ophthalmika GmbH ® + 43 (0)1 596 69 70 |
|
Eesti Alcon Pharmaceuticals Ltd. Eesti filiaal ® + 372 6 313 214 |
Polska Alcon Polska Sp. z o.o. ® + 48 22 820 3450 |
|
España Alcon Cusí, S.A. ® + 34 93 497 7000 |
Portugal Alcon Portugal -Produtos e Equipamentos Oftalmológicos, Lda. ® + 351 214 400 300 |
|
France Laboratoires Alcon ® + 33 (0)1 47 10 47 10 |
Romania S.C. Alcon Romania S.R.L. ® + 40 21 203 93 24 |
|
Hrvatska Alcon Farmaceutika d.o.o. ® + 385 1 4611 988 |
Slovenija Alcon d.o.o. ® + 386 1 422 5280 |
Ireland
Malta
United Kingdom
Alcon Laboratories (UK) Ltd
® + 44 (0) 345 266 9363 (United Kingdom)
Slovenská republika Novartis Slovakia s.r.o. Alcon Division ® + 421 2 5441 0378
Ísland
Alcon Nordic A/S ® + 45 3636 4300
Suomi/Finland Alcon Nordic A/S ® + 45 3636 4300
Italia
Alcon Italia S.p.A. ® + 39 02 81 80 31
Sverige
Alcon Nordic A/S ® + 45 3636 4300
Fecha de la última revisión de este prospecto
La información detallada de este medicamento está disponible en la página Web de la Agencia Europea de Medicamentos: http://www.ema.europa.eu
31